对甲氧基苯基-2,3,4,6-四-O-乙酰基-α-D-吡喃甘露糖苷的合成
陈朗秋,伍桂龙,谢 蓉
(湘潭大学 化学学院 环境友好化学与应用省部共建教育部重点实验室,湖南 湘潭 411105)
在自然界中,酚类是一类分布很广泛的化合物,其中对甲氧基苯酚是糖苷偶联时的一种很有用的受体[1-4].对甲氧基苯基甘露糖苷广泛存在于天然化合物中,也是一种相当重要的中间体.一直以来均有关于对甲氧基苯基-2,3,4,6-四-O-乙酰基-α-D-吡喃甘露糖苷的研究[5-9].
虽然目前已经有关于对甲氧基苯基甘露糖苷合成的报道,但是开发立体选择性好、产率较高并且适用于甘露糖芳基酚苷的方法仍然十分必要.在化学合成法中,Koenigs-Knorr法是一种常用银盐和汞盐为催化剂的经典的立体选择性合成β-糖苷的反应[10],但是存在糖基供体卤代糖的稳定性差,不易保存,所用催化剂均为重金属盐,价格昂贵,对环境污染严重等问题.本文通过调研文献,参考其它糖苷的合成方法[10-15],采用五乙酰化糖为供体经过两步活化与酚类受体偶联,探索合成糖苷的方法的有效性.
1 实验部分
1.1 仪器与试剂
BRUKER-AVANCE-400型核磁共振仪 (瑞士Bruker公司);Bruker autoflexⅢTOF/TOF离子阱型电喷雾多级质谱仪(美国Bruker Daltonics公司),X-4数字显示显微熔点测定仪(河南巩义市英峪仪器厂).TLC分析使用青岛海洋化工厂生产的涂层为0.20~0.25mm的HF254型硅胶板,用UV或体积分数30%的硫酸甲醇溶液显色观察,柱色谱分离使用青岛海洋化工厂的100~200目硅胶.所用试剂均为市售分析纯或化学纯.
1.2 合成路线
如图1所示,以D-甘露糖(1)为原料,经全乙酰化得到1,2,3,4,6-五-O-乙酰基-D-甘露糖(2)经过一位脱保护得到2,3,4,6-四-O-乙酰基-D-甘露糖(3),化合物3经过碱催化得到2,3,4,6-四-O-乙酰基-D-吡喃甘露糖基三氯乙酰亚胺酯(4),活性高的化合物4与活性较低的对甲氧基苯酚偶联,立体选择性地得到了对甲氧基苯基-2,3,4,6-四-O-乙酰基-α-D-吡喃甘露糖苷(5).
1.3 实验方法
1.3.1 1,2,3,4,6-五-O-乙酰基-D-甘露糖(2)的合成
往250mL三颈圆底烧瓶中加入60mL吡啶和100mL乙酸酐,置于0℃冰水浴中冷却搅拌30min后,分批加入15.00g(0.083mol)D-甘露糖(1),保持瓶内温度低于20℃,继续搅拌12h,TLC监测(P/E 3∶1)检查反应完全,用二氯甲烷稀释,依次采用冰冷的饱和碳酸氢钠水溶液、饱和盐水洗涤,无水硫酸钠干燥,过滤,滤液浓缩至干,得到黄色糖浆29.10g,收率90%,直接用于下一步反应.
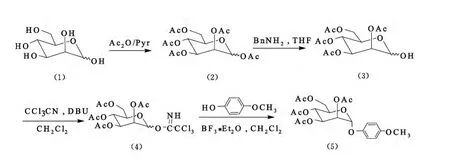
图1 对甲氧基苯基-2,3,4,6-四-O-乙酰基-α-D-吡喃甘露糖苷(5)的合成路线
1.3.2 2,3,4,6-四-O-乙酰基-D-甘露糖(3)的合成
往100mL圆底烧瓶中加入15.00g(38.5mmol)1,2,3,4,6-五-O-乙酰基-D-甘露糖(2)和40mL四氢呋喃,置于0℃冰水浴中冷却搅拌30min后,加入5mL(46mmol)苄胺,待反应1h后,转移至室温下继续反应12h,TLC监测(P/E 1∶1)反应完全.用二氯甲烷稀释,依次采用冰冷的饱和碳酸氢钠水溶液、饱和盐水洗涤,无水硫酸钠干燥,过滤,滤液浓缩后得到棕色浆状物10.68g,收率79.8%,直接用于化合物(4)的制备.
1.3.3 2,3,4,6-四-O-乙酰基-D-吡喃甘露糖基三氯乙酰亚胺酯(4)的合成
往100mL圆底烧瓶中加入7.50g(21.5mmol)黄色浆状物(3)和20mL CH2Cl2,搅拌溶解之后,依次加入3.20mL(25.1mmol)1,8-二氮杂二环[5.4.0]十一碳-7-烯(DBU)和13mL(129mmol)三氯乙腈,置于0℃冰浴中冷却搅拌3h后,TLC监测(P/E 2∶1)反应完成,减压抽滤,滤液浓缩,柱层析分离(P/E 3∶1),得到白色固体9.04g,收率85.4%,直接用于后续的偶联反应.
1.3.4 对甲氧基苯基-2,3,4,6-四-O-乙酰基-α-D-吡喃甘露糖苷(5)的合成
往100mL圆底烧瓶中加入8.00g(16.29mmol)黄色浆状物(4)、6.07g(48.88mmol)对甲氧基苯酚和50mL CH2Cl2,搅拌溶解之后,在冰浴条件下,滴加2.10mL(16.29mmol)三氟化硼乙醚溶液,置于0℃冰浴中冷却搅拌4h后,TLC监测(P/E 2∶1)反应完全,减压抽滤,滤液浓缩,柱层析分离(P/E 3∶1),得到白色固体5.69g,收率76.9%.105~107℃(文献[9]值101~102℃);[α]D+92.8°(c 2.0,CHCl3)(文献[9]值[α]D+95.9°(c 2,CHCl3);1H NMR (CDCl3)δ7.02(d,2H,J=8.7Hz,ArH),6.83(d,2H,J=8.7 Hz,ArH),5.55(dd,1H,J2,3=2.9Hz,J3,4=9.9Hz,H-3),5.44(s,1H,H-2),5.41(s,1H,H-1),5.36(t,1H,J4,5=10.0Hz,H-4),4.28(dd,1H,J5,6a=5.1Hz,J6a,6b=12.0Hz,H-6a),4.12~4.16(m,1H,H-5),4.09(d,1H,H-6b),3.78(s,3H,PhOCH3),2.20(s,3H,OAc),2.06(s,6H,2OAc),2.04(s,3H,OAc).MALDI-TOF MS(m/z):理论计算:C21H26O11:454.148[M];实测:477.225[M+Na]+,493.192 [M+K]+.
2 结果与讨论
D-甘露糖及相应的糖苷端基质子的偶合常数J1,2=3Jea=3Jee较小甚至接近于0,有时表现为一个变宽的单峰,不能依据J1,2确定其构型为1,2-顺式还是1,2-反式构型[16-17].
但是,比对所合成的α-糖苷(5)1H NMR数据可知,α-糖苷结构(5)的 H-1的化学位移值δ=5.41ppm(文献[6]:H-1的化学位移值δ=5.408),而且旋光和熔点数据与文献[9]基本一致.此外,在 MS谱中,对于α-糖苷(5)计算:C21H26O11:454.148[M];实测:477.225[M+Na]+,493.192[M+K]+,相应的氢谱和质谱见图2.

图2 对甲氧基苯基-2,3,4,6-四-O-乙酰基-α-D-吡喃甘露糖苷(5)的氢谱和质谱
3 结论
以D-甘露糖为原料,经全乙酰化得到1,2,3,4,6-五-O-乙酰基-D-甘露糖(2),经过一位脱保护得到化合物(3),化合物(3)经过有机碱DBU催化得到化合物(4),(4)作为活性高的供体与活性较低的受体对甲氧基苯酚偶联,立体选择性地获得了目标化合物对甲氧基苯基-2,3,4,6-四-O-乙酰基-α-D-吡喃甘露糖苷(5).方法有效,产率较高.
[1]Martin C E,Weishaupt M W,Seeberger P H.Progress toward developing a carbohydrate-conjugate vaccine against Clostridium difficile ribotype 027:synthesis of the cell-surface polysaccharide PS-I repeating unit[J].Chemical Communications,2011,47(37):10260-10262.
[2]Werz D B,Seeberger P H.Total synthesis of antigen Bacillus anthracis tetrasaccharide-creation of an anthrax vaccine candidate[J].Angewandte Chemie International Edition,2005,44(39):6315-6318.
[3]Yamanoi T,Fujioka A,Inazu T.New synthetic methods and reagents for cxomplex carbohydrates.IX.Aryl D-Glucopyranosides and 1-Aryl-1-deoxy-D-glucopyranoses from 2,3,4,6-Tetra-O-benzyl-.ALPHa.-D-glucopyranosyl dimethylphosphinothioate[J].Bulletin of the Chemical Society of Japan,1994,67(5):1488-1491.
[4]Jacobsson M,Malmberg J,Ellervik U.Aromatic O-glycosylation[J].Carbohydrate Research,2006,341(10):1266-1281.
[5]Tsuzuki Y,Tanaka K.Considerations on the nuclear magnetic resonance spectra of some anomeric Tetra-O-acetyl-D-glucopyranosides[J].Bulletin of the Chemical Society of Japan,1967,40(5):1208-1211.
[6]Mori M,Ito Y,Ogawa T.A highly stereoselective and practical synthesis of cyclomannohexaose,Cyclo{→ 4)-[α-D-Manp-(1→ 4)-]5-α-D-Manp-(1→},a manno isomer of cyclomaltohexaose[J].Carbohydrate Research,1989,192:131-146.
[7]Weingart R,Schmidt R R.Can preferentialβ-mannopyranoside formation with 4,6-O-benzylidene protected mannopyranosyl sulfoxides be reached with trichloroacetimidates[J].Tetrahedron Letters,2000,41(45):8753-8758.
[8]Yamanoi T,Yamazaki I.The catalytic synthesis of aryl O-glycosides using triaryloxyboranes[J].Tetrahedron Letters,2001,42(24):4009-4011.
[9]Vervoort A,De Bruyne C K.Synthesis of substituted phenylα-D-mannopyranosides[J].Carbohydrate Research,1970,12(2):277-280.
[10]Adasch V,Hoffmann B,Milius W,et al.Preparation of alkylα-andβ-D-glucopyranosides,thermotropic properties and X-ray analysis[J].Carbohydrate Research,1998,314(3):177-187.
[11]Bornaghi L F,Poulsen S A.Microwave-accelerated Fischer glycosylation[J].Tetrahedron Letters,2005,46(20):3485-3488.
[12]Nicolaou K C,Pfefferkorn J A,Roecker A J,et al.Natural product-like combinatorial libraries based on privileged structures.1.General principles and solid-phase synthesis of benzopyrans[J].Journal of the American Chemical Society,2000,122(41):9939-9953.
[13]卢高超,陈朗秋,刘灯峰,等.L-薄荷基-β-D-乳糖苷的简便合成[J].食品科学,2013,34(4):83-87.
[14]刘灯峰,陈朗秋,李宏伟,等.烷基-β-D-吡喃葡萄糖苷的合成及性能[J].应用化学,2013,30(10):1120-1126.
[15]易幸,史慎德,陈朗秋,等.保护的二糖半乳吡喃糖基(α1→2)葡萄吡喃糖苷的合成[J].光谱实验室,2011,28(5):2532-2535.
[16]陈朗秋,赖端,宋志伟,等.寡糖的立体选择性合成策略[J].有机化学,2006,26(5):627-642.
[17]蔡孟深,李中军.糖化学-基础、反应、合成、分离及结构[M].北京:化学工业出版社,2006:370-372.

