基于星点设计-效应面法优化盐酸曲美他嗪缓释微丸的制备及评价
叶星辰 陈燕忠*
(广东药学院药物研究所,广东 广州 510006)
基于星点设计-效应面法优化盐酸曲美他嗪缓释微丸的制备及评价
叶星辰陈燕忠*
(广东药学院药物研究所,广东 广州 510006)
目的制备盐酸曲美他嗪缓释微丸,并筛选最优处方。方法以体外释放度为考察指标,采用星点设计优化处方并验证。结果成功制备了盐酸曲美他嗪缓释微丸;得到缓释包衣的最优处方为:Eudragit RS100与Eudragit RL100的比例为8.15,包衣增重10.46%;验证实验证明最优处方工艺的重现性良好。结论采用星点设计-效应面法成功得到盐酸曲美他嗪缓释微丸的处方优化模型,实现了处方优化。
盐酸曲美他嗪;缓释;星点设计
曲美他嗪可选择性抑制3-酮酰基辅酶A硫解酶,在减少游离脂肪酸代谢的同时增加葡萄糖的氧化,从而改善心肌能量,是临床上心绞痛的一线治疗药物,具有保护心肌细胞的作用[1]。目前上市的剂型为法国施维雅公司生产的盐酸曲美他嗪片-万爽力[2-4]。
时辰病理学研究表明,清晨4~8时为心绞痛的发病高峰[5],而曲美他嗪的半衰期为6 h左右[6],因此考虑将其制成缓释制剂。本文采用星点设计-效应面法优选以Eudragit RS100和Eudragit RL100为缓释成膜材料的包衣处方工艺,制备盐酸曲美他嗪缓释微丸,使药物在体内缓慢释放,维持血药浓度在有效的范围之内,有效防止清晨心绞痛的发生,改善患者的顺应性。
1 仪器与材料
Aeromatic型流化床(NIRO,德国),ZR-4型智能溶出试验仪(天津大学无线电厂),高效液相色谱仪(Dionex Corp),BS224S型精密分析天平(Sartorius仪器有限公司),CP225D型精密分析天平(北京赛多利斯仪器系统有限公司),GZX-9246MBE型干燥箱(上海博讯实业有限公司医疗设备厂)。
盐酸曲美他嗪含药丸芯(自制),曲美他嗪对照品(含量99.8%),Eudragit(RS100、RL100,德固赛),聚乙二醇6000(PEG6000,卡乐康辅料公司),滑石粉(广州杰辅),其他试剂均为分析纯。
2 方法与结果
2.1分析方法的建立
2.1.1色谱条件。色谱柱:Diamonsil C18(250 mm×4.6 mm,5 μm);流动相:0.012 mmol/L庚烷磺酸钠溶液(加磷酸调节pH至3)∶甲醇∶乙腈=55∶36∶9;流速:1 mL/min;检测波长:230 nm;柱温:30 ℃;进样量:20 μL。
2.1.2标准曲线的建立:精密称取盐酸曲美他嗪对照品适量,加流动相溶解,配制成105.1 μg/mL的储备液。精密吸取储备液0.5,1.0,2.0,4.0,6.0 mL,分别置于10 mL容量瓶中,以流动相定容,用0.45 μm滤膜滤过,取续滤液。将制得的系列溶液分别进样测定,并以峰面积A对浓度做线性回归,得回归方程A=5722.3C-0.3971(r=0.9994),盐酸曲美他嗪在5.255~63.06 μg/mL范围内线性关系良好。
2.1.3精密度实验:吸取同一对照品溶液(42.04 μg/mL),按2.1.1项下的色谱条件连续进样5次。结果峰面积A的RSD为0.58%,表明仪器精密度良好。
2.1.4稳定性试验:取同一对照品溶液(42.04 μg/mL),分别于0、2、4、6、8、10、12、24 h各测定峰面积A一次,计算得峰面积的RSD为0.93%,表明所得样品在24 h内稳定。
2.2体外释放度方法的建立:采用转篮法进行测定。具体方法参考《中国药典》2010版第二部附录XD中释放度测定法第一法中之操作。前2 h的释放介质采用0.1 mol/L HCl溶液,水浴温度为(37±0.5) ℃,转速100 r/min。2 h后取样,并弃去HCl溶液;立即转入pH6.8磷酸盐(pH 6.8 PBS)缓冲溶液,分别于4、6、8、10、12、24 h各取样5 mL,同时补加等量同温pH6.8 PBS缓冲溶液;样品用0.45 μm微孔滤膜过滤,取续滤液稀释至适宜浓度,测定峰面积A,并计算累积释药率。
2.3曲美他嗪缓释微丸的制备
2.3.1包衣液的配制:取Eudragit RS100、Eudragit RL100及PEG 6000适量,缓慢加入75%乙醇中,搅拌至溶解,得溶液A。将滑石粉边搅拌边加入适量75%乙醇中,匀化5 min,得溶液B。将溶液B缓缓加入溶液A中,搅拌均匀,过80目筛,即得包衣液。
2.3.2缓释微丸的制备:将盐酸曲美他嗪含药丸芯置于流化床中,以底喷方式进行包衣。调整出风温度为25~35 ℃,喷雾压力为4 bar,喷液速率为1.5~2. 0 mL/min。包衣完成后继续流化干燥10 min,结束后置于烘箱中40 ℃熟化24 h。
2.4星点设计优化处方

图1 2 h累积释放率三维效应面图

图2 12 h累积释放率三维效应面图

图3 24 h累积释放率三维效应面
2.4.1实验设计:由单因素实验可知Eudragit RS100与Eudragit RL100的比例(X1)、包衣增重(X2)对曲美他嗪缓释微丸累积释放率的影响较为显著。因此选择以上2个条件作为考察因素,规定其取值范围分别为:X1:0.5~10,X2:5%~15%。选择曲美他嗪缓释微丸在2、12、24 h的累积释放率为考察指标(分别记为Q2h,Q12h,Q24h)。因素及水平表见表1,具体实验设计及结果见表2。

表1 因素水平表

表2 试验设计及各指标测定结果
2.4.2模型的拟合:采用Design-Expert软件分析表2中的数据,以考察指标Q2h、Q12h及Q24h为因变量分别对两因素进行多元线性(Linear)、二次多项式(Quadratic)和三次多项式(Cubic)模型拟合,考察指标和两个因素之间的关系,以置信度(P)和拟合优度(R2)作为模型的判定标准。结果表明:Q2h、Q12h及Q24h的最优拟合模型均为Cubic模型,拟合方程如下:
Q2h=24-11.86X1-10.02X2+1.15X1X2-1.87X12+2.01X22-1.65X12X2+6.88X1X22(R2=0.9997,P=0.0376)
Q12h=77.29-16.63X1-13.12X2-0.68X1X2-4.38X12-1.125*10-3X22-1.05X12X2+12.96X1X22(R2=0.9954,P=0.0028)
Q24h=89.82-7.89X1-8.45X2-0.60X1X2-0.78X12-0.68X22+1.83X12X2+6.51X1X22(R2=0.9579,P=0.0090)
根据拟合方程,采用Design-Expert软件分别绘制各指标与因素的三维响应面图,见图1~3。
2.4.3处方优化及预测:一般要求缓释制剂可在释放初期达到一定的药物浓度,而后缓慢释放,以维持体内血药浓度的稳定。规定微丸2 h的释放率为10%~30%,12 h的释放率为40%~60%,24 h的释放率为80%~100%。按以上要求,采用Design-Expert软件对响应面进行优化,并预测最优处方,结果如表3所示。
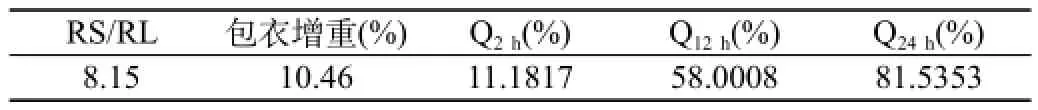
表3 优化结果
2.4.4工艺验证:按2.4.3中所得的最优处方制备曲美他嗪缓释微丸3批,以2、12、24 h的累积释放率为考察指标进行工艺验证,并计算预测值和实测值之间的偏差率,偏差率越小,说明该数学模型预测效果越好[7],结果见表4。

表4 预测值与实测值的偏差
由表4可知,各实测值与预测值间的偏差率均<5%,表明所建立的数学模型具有良好的预测性。
3 讨 论
本实验采用星点设计-效应面法对盐酸曲美他嗪缓释微丸的包衣处方进行了优化,并按照最佳处方进行工艺验证,比较了实测值与预测值之间的差异。结果表明,实测值与预测值的趋势基本一致,所建立的模型有良好的预测性,所选条件重现性良好。
[1]李玲珺,马鹏程,曹玉萍,等.盐酸曲美他嗪健康人中的药动学和生物等效性评价[J].中国药师,2009,12(2):156-159.
[2]周光荣.盐酸曲美他嗪治疗稳定型心绞痛临床疗效分析[J].中国现代药物应用,2010,4(18):20-21.
[3]Sellier P,Broustet JP.Assessment of Anti-Ischemic and Antianginal Effect at Trough Plasma Concentration and Safety of Trimetazidine MR 35mg in Patients with Stable Angina Pectoris:A Multicenter,Double-Blind,Placebo-Controlled Study[J].Am J Cardiovasc Drugs,2003,3(5): 361-369.
[4]陈义民.扩张型心肌病近期预后影响因素分析[J].安徽医药,2010,14(1): 84-85.
[5]何绍雄.时辰药理学与时辰治疗学[M].天津:天津科学技术出版社,1998: 99-101.
[6]冯琳,侯孝云.万爽力[J].中国新药杂志,2000,9(12): 864-865.
[7]Deependras S,Swarnlata S,Vinod KD,et al.Formulation optimization of gentamicin loaded Eudragit RS100 microspheres using factorial design study[J].Biol Pharm Bull,2008,31(4) :662-667.
Preparation and Evaluation of Trimetazidine Dihydrochioride Sustained-release Pellets by Central Composite Design and Response Surface Methodology
YE Xing-chen,CHEN Yan-zhong
(Institute of Medicine,Guangdong Pharmaceutical University,Guangzhou 510006,China)
Objective To prepare the sustained-release pellets of trimetazidine dihydrochioride and screen the optimal preparation. Methods The preparation factors of in vitro drug release behavior were studied through single-factor experiments. Central composition design was used to optimize the experiment design. The optimal preparation was verified by experiment. Results The trimetazidine dihydrochioride sustained-release pellets was successfully prepared. The optimal preparation was as follows: Eudragit RS100 and Eudragit RL100 are at the ratio of 4∶1;the coating level is 10.46%. The preparation technology was reproducible. Conclusion A reliable model is established using response surface methodology and implements the prescription optimization.
Trimetazidine dihydrochioride;Sustained-release;Central composite design
R9
B
1671-8194(2015)22-0004-02
E-mail:doctor.c@163.com

