TiB2晶须的自蔓延高温合成及其生长机理
王明远,李俊寿,武小娟,李 苏,赵 芳
(军械工程学院 先进材料研究所,石家庄 050003)
TiB2是B-Ti二元系统中唯一稳定的化合物。作为功能材料,TiB2由于具有良好的导电性能和红外性能,不仅可以制备大电流电极、导轨和电枢等功能部件,而且可以制备高性能的红外辐射涂层。作为结构陶瓷,TiB2由于具有高的硬度和耐磨性能,不仅可以直接用于制备陶瓷刀具、拉丝模、喷嘴和磨料,而且可以用于生产高性能的硬质合金和复相陶瓷。此外,棒状TiB2作为控制棒的组成材料有望用于高温核反应堆[1],用作接触性纳米加工的探针元件,用于扫描探针显微镜(SPM)等。在结构陶瓷中,棒状或晶须形态的TiB2既可以保持其良好的力学性能,也可以发挥其显著的增韧补强作用[2]。但是,近年来关于TiB2的研究多集中在单相和复相陶瓷的制备上[3],晶须形态的TiB2的合成和生长机理还未见报道。
本课题组曾以Mg、B2O3、TiO2为原料,采用燃烧合成法制备出高纯度的TiB2粉末[4],以Al+SnO+Cu2O为原料批量合成SnO2纳米纤维[5],本文的研究试图在Mg+B2O3+TiO2体系的基础上,通过加入不同量的Cu2O,研究其对TiB2晶体形态的影响,为合成晶须含量较高的TiB2粉末奠定基础。
1 实验
1.1 Mg-B2O3-TiO2体系的绝热燃烧温度计算
绝热燃烧温度Tad是判断SHS反应能否持续进行的主要参数。为计算绝热燃烧温度,需要假设绝热条件下反应完全进行,没有热损失,反应放出的所有能量全部用于生成物的加热。

若在T时反应开始,即把反应物都提前加热到T0,经充分混合后进行反应,就有:
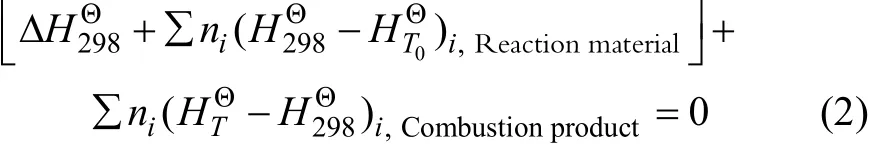
式中:T0是预热达到的温度,T即为待求的绝热燃烧温度,所需各物质的热力学参数由热力学手册[6]查出。根据文献[6]提供的热力学参数,对Mg+B2O3+TiO2反应体系进行热力学模拟仿真分析,得到了其绝热燃烧温度为3 009.25 K,远大于1 800 K的自蔓延高温反应经验维持判据,因此反应不需外界补充能量就能自发完成。
1.2 实验方法
本实验采用Mg-B2O3-TiO2反应体系,分别加入不同量的Cu2O作为添加剂,研究其对TiB2晶体形态的影响。Mg、B2O3、TiO2、Cu2O四种粉末主要发生以下2种化学反应:
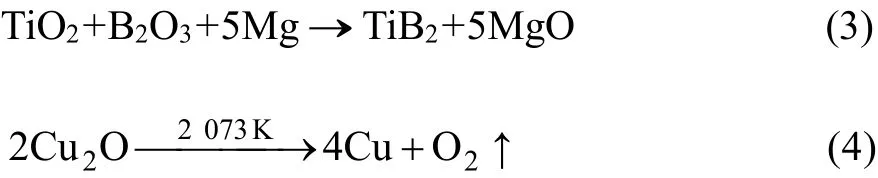
实验所用的原料如表1所列。
将上述Mg、B2O3、TiO2粉末按化学反应方程式(1)配料,分为4组,分别加入2%,4%,6%,8%的Cu2O粉末,均匀混合后,置于专用的反应模具中,适当压实,用钨丝引燃使其发生自蔓延高温合成反应。反应产物自然冷却到室温后,在行星球磨机中研磨 2 h,获得MgO+TiB2复相陶瓷粉末。在25%盐酸溶液中进行超声波辅助清洗 10~15 min,除去产物中的MgO,获得高纯度的TiB2粉体。通过对样品分别进行XRD分析与SEM分析,研究Cu2O添加剂对TiB2晶体形态的影响。

表1 本实验所用原料Tabal 1 Raw materials used in the present experiment
2 结果与讨论
2.1 XRD分析

图1 燃烧合成产物的XRD谱Fig.1 XRD patterns of combustion products
图1所示为燃烧反应产物的XRD图谱。其中A1,A2,A3,A4分别对应加入2%,4%,6%,8%Cu2O的燃烧反应产物。从图1(a)可以看出,4种试样燃烧反应产物都由MgO和TiB2两相组成,加入不同含量的Cu2O对燃烧产物的组分并没有明显的影响,但对产物形貌的影响比较明显。经XRD-K值法估算,产物中的MgO、TiB2的相对含量分别为87.46%、12.54%。在反应的产物中没有检测到Cu2O是因为Cu2O在1 800℃分解为金属Cu和O2,由于Cu含量少,熔点低(1 083℃),并且是重金属,密度远大于其他产物,在高温下聚集于模具底部。
图1(b)中B1、B2、B3、B4分别对应于A1,A2,A3,A4各燃烧产物酸洗后的XRD图谱。从图中可以看出4种试样均由单一的TiB2相组成,不存在MgO的衍射峰。
2.2 SEM分析
图2所示为燃烧反应产物的SEM形貌。图(a)、(b)、(c)、(d)分别对应添加2%,4%,6%,8%Cu2O的4种试样。在添加2%,4%,6%Cu2O的试样中,均发现有棒状的TiB2,但在添加8%Cu2O的试样中没有发现TiB2。
图2(a)中TiB2短棒的长度在0.5~1.5 μm,直径大多在100~200 nm以内,只有少量的棒状晶直径低于100 nm。多数棒状晶的顶端有球状的凸起。图2(b)中TiB2的长径比有了显著的增加。从图中可以看出,TiB2棒状晶在块状的TiB2和MgO晶体之间生长,长度为微米级,直径大多集中在50 nm以下,少量在50~100 nm之间。图2(c)中的棒状晶直径集中在100 nm,长度多在2 μm左右,有明显的断裂痕迹,因此棒状晶的长度应该有所延伸。图中棒状晶表面有大量细小的凸起,晶体表面不够光滑,这应该是晶体在生长过程中,粒状的TiB2和MgO晶体附着其上造成的。图2(d)中则形成了大量的块状晶及片状晶,晶粒尺寸大多集中在0.5~3.0 μm。并没有发现棒状晶。
2.3 棒状TiB2晶体生长的机理
从图2(a)中可以看到多数TiB2棒状晶的顶端有一个球状的凸起,这是气−液−固生长机制(V-L-S)区别于其它生长机制的重要特征[7]。因此,本文认为用此方法合成TiB2棒状晶的生长机理属于典型的V-L-S机制。上述化学反应方程式(1)反映了体系总的化学反应趋势,但实际上TiB2的合成是分两步完成的。首先Mg分别与B2O3和TiO2发生置换反应,还原出B原子和Ti原子;然后B原子和Ti原子发生化合反应,生成TiB2。相应的反应方程式如下:
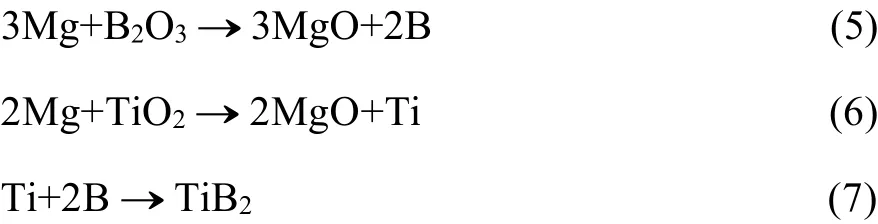

图2 不同Cu2O含量的燃烧合成产物的SEM图Fig.2 SEM images of combustion products with different Cu2O contents
Cu2O受热分解后生成金属Cu和O2,分解生成的O2在高温下膨胀,不断向外喷射,形成大量孔道[8],为TiB2晶须的生长提供一定的空间条件,自蔓延反应产生的高温也为TiB2晶体的形成提供了足够的能量条件。
图3为TiB2晶须生长机理的示意图。Mg与B2O3和TiO2的反应释放出大量的热,Cu2O在高温下分解成金属铜和氧气,大部分液态铜由于密度较大而流向合成模具的底部,少部分铜以液滴的形式落到已生成的TiB2晶体的水平面上后[9],才为TiB2的形核和生长提供条件。比较B、Cu、Ti的理化性能(如电负性、熔点、沸点等),Ti与Cu的原子亲和力远大于B与Cu,因而更容易进入铜液滴,形成Cu-Ti合金液滴[10];B原子与Ti原子的亲和力也很大,因而受到Cu-Ti合金液滴表面Ti原子的吸引随后进入合金液滴并生成TiB2;随着Ti原子和B原子的不断进入,当TiB2含量不断增加,达到过饱和状态时,TiB2便会沿着液(Cu-Ti)−固(TiB2)界面析出,成为TiB2晶核。由于TiB2的熔点远高于Cu,TiB2晶核很容易长大[11]。随着燃烧合成反应的进行,进入Cu-Ti合金液滴的B原子和Ti原子越来越多,TiB2晶体不断长大,最终生长成晶须形态。
事实上,利用V-L-S机制制备无机纳米线的研究表明[12],纳米线的直径由催化剂液滴的尺寸决定,催化剂液滴的尺寸越小,所制备出的纳米线直径越小。而液滴的尺寸又取决于液固界面和气固界面的表面能差。表面能差越大液滴直径越小。影响表面能差的因素除了液固材料本身的化学性质,还有温度、压力等[13]。
Cu2O作为催化剂并不是越多越好,Cu2O含量过低,其作用不明显;Cu2O含量过高,分解后生成的Cu容易聚到一起,以液体的形式流向底部。本研究表明,Cu2O的添加量控制在2%~6%时效果较好。
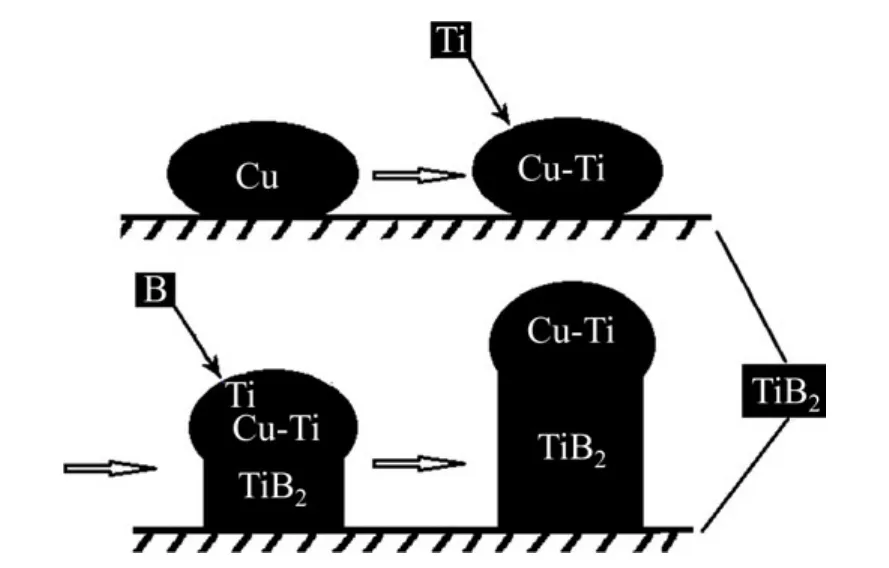
图3 TiB2的生长机理示意图Fig.3 The schematic of TiB2growing mechanism
图4所示为燃烧反应产物经酸洗后获得的TiB2晶须的SEM形貌,Cu2O添加量为4%。由图中可以看出,大量晶须形态TiB2集中有序地排列在一起,周围的MgO相及棒状晶顶端球状体消失。正是由于棒状晶顶端球状体内的杂质被清除,从而获得具有圆锥状端头的TiB2晶须。

图4 燃烧反应产物酸洗后的SEM图Fig.4 SEM images of combustion products after acid cleaning
3 结论
1)采用自蔓延高温合成法,以Mg、B2O3、TiO2粉末为原料,以Cu2O为添加剂可获得TiB2晶须,Cu2O的有效添加范围为2%~6%。加入4%的Cu2O可获得大量高长径比TiB2晶须。
2)TiB2晶须的生长机制属于V-L-S机制:首先Cu2O在高温下分解生成O2和Cu,O2向外喷射形成的孔道为TiB2晶须的生长提供空间条件,自蔓延反应产生的高温为其提供能量条件,熔融态的Cu作为催化剂,与Ti形成以反应生成的TiB2为衬底的合金液滴,然后通过不断吸收Ti原子和B原子,使TiB2形核并定向生长,最终形成TiB2晶须。
3)用25%盐酸在50℃下超声波辅助酸洗燃烧反应产物10~15 min,可以有效的去除杂质相,获得具有圆锥状端头的TiB2晶须。
[1] SUBRAMANIAN C,CH Ts,MURTHY R,et al.Synthesis and consolidation of titanium diboride[J].International Journal of Refractory Metals&Hard Materials,2007,25(4):345−350.
[2] 周 飞,夏长清,曾凡浩,等.原位合成TiB2对B4C/2014Al合金复合材料组织与力学性能的影响[J].粉末冶金材料科学与工程,2012,17(4):457−461.ZHOU Fei,XIA Chang-qing,ZENG Fan-hao,et al.In situ synthesis TiB2ofB4C/2014 Alalloy organization and mechanical properties of composite materials[J].Materials Science and Engineering of Powder Metallurgy,2012,17(4):457−461.
[3] LIJun-shou,CAIZong-ying,GUO Huan-sheng,etal.Characteristics of porous Al2O3-TiB2ceramics fabricated by the combustion synthesis[J].Journal of Alloys and Compounds,2009,479(1/2):803−806.
[4] LI Su,LI Junshou.Effect of Mg on the synthesis of TiB2powder by a self-propagating high-temperature synthesis technique[J].Applied Mechanics and Materials,2013,347−350:1144−1147.
[5] CAIZong-ying,LIJun-shou.Facile synthesisofsingle crystalline SnO2nanowires[J].Ceramics International,2013,39:377−382.
[6] 叶大伦,胡建华.实用无机物热力学数据手册[M].北京:冶金工业出版社,2002.YE Da-lun,HU Jian-hua.Practical Inorganic Thermodynamic Data Manual[M].Metallurgical industry press,Beijing,2002.
[7] BACA L,STELZERN.Adapting of sol-gel process for preparation of TiB2powder from low-cost precursors[J].Journal of the European Ceramic Society,2008,28:907.
[8] RABIEZADEH A,HADIAN A M,ATAIE A.Preparation of alumina/titanium diboride nano-composite powder by milling assisted sol-gel method[J].Int Journal of Refractory Metals and Hard Materials,2012,31:121.
[9] CHEN I W,ROSENFLANZ.A tough sialon ceramic based on α-Si2N4with a whisker-like microstructure[J].Nature,1997,389(6652):701−704.
[10] 罗 成,熊 翔,董仕节.TiB2和TiC复合熔敷棒的制备及电火花涂层特性[J].粉末冶金材料科学与工程.2010,15(1):54−58.LUO Chen,XIONG Xiang,DONG Shi-jie.The preparation of TiB2and TiC composite deposition and EDM coating properties[J].Materials Science and Engineering of Powder Metallurgy,2010,15(1):54−58.
[11]CALKA,OLESZAK.Synthesis of TiB2by electric discharge assisted mechanicalmilling [J].JournalofAlloys and Compounds,2007,440:346.
[12]RICCERI R,MATTEAZZI P.A fast and low-cost room temperature process for TiB2formation by mechanosynthesis[J].Materials Science and Engineering,2004,379:341.
[13]MATSUURA K,OBARAY,KOJIM K.Combustion synthesis of boride particle dispersed hard metal from elemental powders[J].Int Journal of Refractory Metals&Hard Materials,2009,27:376.

