甘草中甘草酸和甘草苷的提取工艺研究
魏 宁,郎伟君,2
(1.哈尔滨商业大学药学院,哈尔滨150076;2.哈尔滨乐泰药业有限公司,哈尔滨150025)
甘草为豆科植物甘草、胀果甘草、光果甘草的根及根茎,具有补脾益气、清热解毒、祛痰止咳、缓急止痛、调和诸药的功能[1].甘草的主要化学成分为三萜皂苷类和黄酮类,其中甘草酸、甘草苷分别是其重要的单体活性成分,具有很强的药理活性[2].
本文以甘草酸和甘草苷的提取率为指标,对提取溶剂的选择和最佳方法进行考察,旨在为甘草用于化妆品并实现工业化生产提供参考.
1 仪器与试药
高效液相色谱仪(日本岛津公司):SPDM20A型二极管阵列检测器、LC-10ATvP型泵、DGU-20A3型脱气器、CBM-20A型系统控制器、SIL-20A型自动进样器、LC solution色谱工作站、Diamonsil-C18色谱柱(5 μm,150 mm × 4.6 mm)(迪马公司).
甘草药材(哈药集团世一堂制药厂,经哈尔滨商业大学药学院张德连副教授鉴定为真品);甘草酸单铵盐对照品(批号:111089-201301)、甘草苷对照品(批号:111610-201301)均购自中国药品生物制品鉴定所;甲醇、乙腈、冰乙酸为色谱纯,水为双蒸水,无水乙醇为分析纯.
2 方法与结果
2.1 甘草酸和甘草苷的质量浓度测定
2.1.1 色谱条件
1)甘草酸
色谱柱:Diamonsil- C18柱(5 μm,150 mm ×4.6 mm);流动相:甲醇 -0.2 mol/L 醋酸铵溶液 -冰醋酸(67∶33∶1);检测波长:250 nm;流速:1 mL/min,进样量:10 μL.
2)甘草苷
色谱柱:Diamonsil- C18柱(5 μm,150 mm ×4.6 mm);流动相:乙腈 -0.5%冰醋酸(1∶4);检测波长:276 nm;流速:1.0 mL/min;进样量:20 μL.
2.1.2 对照品溶液的制备
1)甘草酸
精密称取甘草酸单铵盐对照品5 mg,置于5mL量瓶中,用流动相溶解并稀释至刻度,摇匀即得.
2)甘草苷
精密称取甘草苷对照品1.25 mg,置于5 mL量瓶中,加甲醇制成每1 mL含250 μg的溶液.
2.1.3 供试品溶液的制备
1)甘草酸
精密量取各提取液1 mL,置50 mL量瓶中,加流动相约20 mL,超声处理30 min,加流动相稀释至刻度,精密量取续滤液10 mL,置25 mL量瓶中,加流动相稀释至刻度,取续滤液,测定并计算;
2)甘草苷
精密量取各提取液1 mL,置具塞锥形瓶中,精密加入70%乙醇溶液10 mL,超声处理30 min,补足减失的重量,精密量取续滤液1 mL,置50 mL量瓶中,用20%乙腈稀释至刻度,取续滤液,测定并计算.
2.1.4 线性关系考察
1)甘草酸
精密吸取对照品溶液 0.25、0.50、0.75、1.00、1.50 mL,分别置于5 mL容量瓶中,流动相稀释,摇匀.分别精密吸取10 μL注入液相色谱仪进行分析.以甘草酸单铵盐对照品的进样质量浓度(C)对其峰面积积分值(A)进行线性回归,得回归方程:A=3811.1C+683.15(r=0.999 8),结果表明,甘草酸单铵盐对照品的进样质量浓度在50~300 μg/mL的范围内与其峰面积积分值呈良好线性关系.
2)甘草苷
精密吸取对照品溶液 0.25、0.50、0.75、1.00、1.50 mL,分别置于5 mL容量瓶中,甲醇稀释,摇匀.分别精密吸取20 μL注入液相色谱仪进行分析.以甘草苷对照品的进样质量浓度(C)对其峰面积积分值(A)进行线性回归,得回归方程:A=19 003C+10 174(r=0.999 7),结果表明,甘草苷对照品的进样质量浓度在6.25~37.5 μg/mL的范围内与其峰面积积分值呈良好线性关系.
2.2 提取工艺研究
2.2.1 不同提取溶剂的选择
根据文献报道[3]和2010年版《中国药典》(一部),结合实际生产的需要,对不同提取溶剂进行筛选.选取水和65%的乙醇作为提取溶剂,以甘草酸和甘草苷的提取率为评价指标进行比较,提取方法:1)水煎煮法:甘草粗粉50 g,用20倍量水煎煮3次,每次1.5 h,合并煎液,离心,倾取上清液,浓缩至50 mL,测定;2)乙醇回流提取法:甘草粗粉50 g,用6倍量65%的乙醇回流提取3次,每次1.5 h,合并提取液,回收乙醇至无醇味,浓缩至50 mL,测定.不同提取溶剂下甘草酸和甘草苷的提取率见表1.
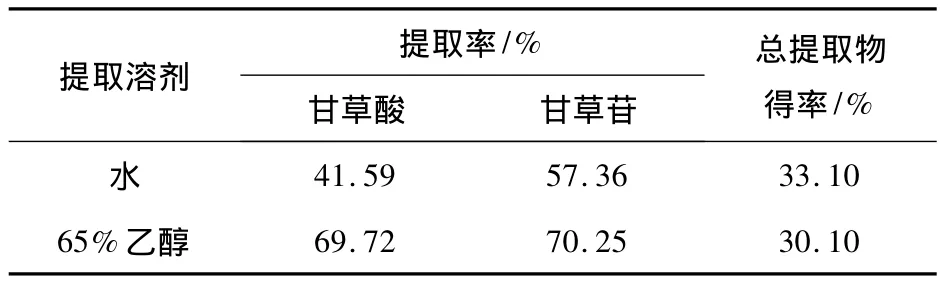
表1 不同提取溶剂下甘草酸和甘草苷的提取率
由表1可知,水煎煮法的总提取物得率比65%乙醇回流提取法的总提取物得率高一些,但65%乙醇回流提取法的甘草苷和甘草酸的提取率都比水煎煮法的高很多,综合结果优选65%的乙醇作为提取溶剂.
2.2.2 优化乙醇回流提取工艺
选用正交试验,优化乙醇回流提取条件.根据预实验选取乙醇体积分数(A)、溶媒用量(B)、提取时间(C)、提取次数(D)4个因素,每个因素选3个水平,采用L9(34)正交设计,以甘草酸和甘草苷的提取率综合值为指标进行考察,综合值=(甘草酸提取率+甘草苷提取率)/2.因素水平见表2;正交实验结果见表3;方差分析结果见表4.
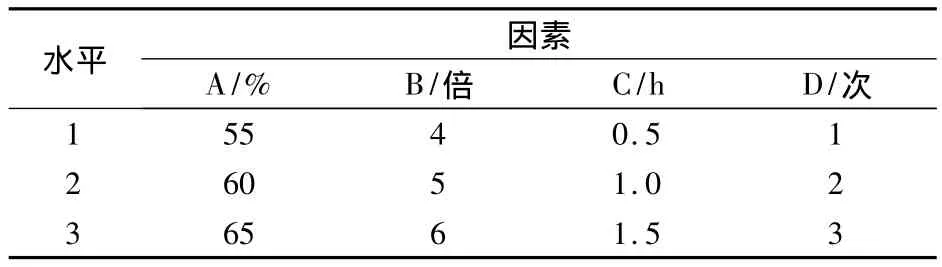
表2 甘草乙醇回流提取因素水平表

表3 正交实验方案与结果

表4 方差分析结果
由表3直观分析可知,各因素对提取效果的影响依次为D>C>B>A,优化水平是A2B3C3D3;由表4方差分析可知,提取次数(D)对甘草酸、甘草苷提取效果的影响有显著意义(P<0.05).以总提取物得率为考察指标时,直观分析表明各因素对提取效果的影响依次为D>C>B>A,优化水平是A2B3C3D3;方差分析表明,B、C、D三种因素对总提取物得率的影响均有显著意义(P<0.05);乙醇体积分数(A)对甘草酸、甘草苷的提取率,总提取物得率的影响均无显著意义.为降低大批量生产成本,决定选用 55%乙醇(A1),则最佳工艺为A1B3C3D3,即6倍量55%乙醇,回流提取3次,每次1.5 h.该结果与正交试验中综合值最高者的搭配A1B3C3D3一致.
2.2.3 验证试验
称取甘草50 g,按最佳工艺A1B3C3D3进行验证试验,测得甘草酸、甘草苷提取率分别为73.41%、74.18%,接近正交试验方案中的最高值,优化条件可行.
3 结语
有文献报道[4],甘草酸用氨水提取效果好.甘草苷易溶于有机溶剂,多用乙醇提取.通过查阅文献和预实验,并从甘草用于化妆品工业化生产和安全角度考虑,本试验综合优选乙醇作为提取溶剂,确定乙醇体积分数、溶媒用量、提取时间和提取次数为考察因素,通过验证放大实验表明,正交实验优选确定的最佳工艺水平是科学、可行的,有利于实际生产降低能源、节约时间,故确定甘草乙醇回流提取的最佳工艺为A1B3C3D3,即6倍量55%乙醇,回流提取3次,每次1.5 h.
[1]国家药典委员会.中国药典(一部)[M].北京:中国医药科技出版社,2010.80-81.
[2]张明发,沈雅琴,张艳霞.甘草及其有效成分的皮肤药理和临床应用[J].药物评价研究,2013,36(2):146-156.
[3]刘育辰,王文全,郭洪祝.甘草有效成分的提取纯化方法研究进展[J].中成药,2010,32(11):1953-1957.
[4]杜文彬,张 洪.甘草中甘草酸的提取工艺研究[J].安徽农业科技,2008,36(25):10935-10946.

