高乳清蛋白含量营养棒在储藏初期的小分子迁移及对其质地硬化的影响
陆乃彦,张 靓,张 轩,李艳芳,周 鹏,*
(1.江南大学食品科学与技术国家重点实验室,江苏无锡 214122;2.江南大学食品学院,江苏无锡 214122)
高乳清蛋白含量营养棒在储藏初期的小分子迁移及对其质地硬化的影响
陆乃彦1,2,张 靓1,张 轩1,李艳芳1,周 鹏1,2,*
(1.江南大学食品科学与技术国家重点实验室,江苏无锡 214122;2.江南大学食品学院,江苏无锡 214122)
高蛋白营养棒在储藏过程中的硬化问题,严重限制了此类食品的货架期。引起这类食品硬化的机制十分复杂。本研究采用乳清分离蛋白/水/甘油组成的简化模型体系,通过调整溶剂中水与甘油的比例,改变体系的储藏稳定性,并采用质构仪、激光共聚焦显微镜和低场核磁共振,研究小分子迁移对其储藏初期硬化的影响。结果表明,随着溶剂中甘油比例的逐渐增加,体系储藏初期硬度变化趋势从“基本不变”逐步转变为“迅速硬化”。在乳清蛋白的纯水体系中,蛋白颗粒完全溶解,体系均匀稳定而未发生显著的分子迁移,硬度几乎不变;随着溶剂中甘油比重的增加,体系内逐渐出现未完全水合的蛋白颗粒,小分子物质从体相向颗粒内部迁移,致使分子流动性显著降低,体系微结构发生改变从而导致质地不断硬化。由此推测,小分子迁移是高蛋白营养棒储藏初期迅速硬化的重要因素。
高蛋白食品,储藏初期,硬化,小分子迁移
高蛋白食品营养价值高、食用方便、口感好,被广泛应用于军事航天、应急救援及运动营养等领域。高蛋白营养棒是典型的高蛋白食品,主要成分包括蛋白质(乳清蛋白、酪蛋白和大豆蛋白等)、碳水化合物和其他小分子保湿/增塑剂(甘油、山梨醇等),具有广阔的开发前景。
在室温储藏过程中,高蛋白营养棒的颜色、风味和口感会发生不良变化,尤其是产品在储藏过程中发生硬化,大大限制了其应用[1]。引起硬化的机制十分复杂,包括蛋白质聚集[2-3]、美拉德反应[4-5]、糖结晶[6-7]、相分离[8]及水分迁移[9-10]等。有报道表明,高蛋白食品的硬化主要发生在储藏初期和中后期[8,11]。前期研究主要集中在储藏中后期的硬化机理,并且对水分造成的影响的研究报道相对较少。Zhou等发现,水分诱导的乳清蛋白自聚集会造成高蛋白食品的质地硬化[2,12]。还有研究者认为,高蛋白食品内部存在水分活度梯度,水分会在势能差的推动下,逐渐从高水分活度的糖浆混合物向低水分活度的蛋白颗粒方向迁移,从而导致水分的增塑能力降低而使质地硬化[6,11]。
前期研究发现,分别用等量的甘油或水与乳清蛋白混合后制成的样品均具有柔软的质地;但在短期的储藏后,两个体系的质构出现了明显差异,乳清蛋白的纯水体系依旧保持柔软,而其甘油体系的硬度则显著增加。本研究选取乳清分离蛋白,将其与水、甘油混合制成相应的简化模型体系;通过不断增加甘油在甘油-水溶液中的比例,采用激光共聚焦显微镜和低场核磁共振研究水及其他小分子迁移的变化情况,验证小分子迁移对其储藏初期硬化的影响。该研究旨在为今后提高高蛋白食品的整体品质以及贮藏稳定性提供有力的科学依据。
1 材料与方法
1.1 材料与仪器
乳清分离蛋白(WPI,90%) Fonterra公司(恒天然乳品集团);FITC荧光染料 Sigma-Aldrich 公司;甘油(分析纯) 国药集团;封口膜(Parafilm) Plechiney Plastic Packaging公司。
TCS SP5激光共聚焦显微镜 德国Zeiss公司;NMI20-Analyst核磁共振分析仪 上海纽迈电子科技股份有限公司;TA-XT-plus质构仪 英国Stable Micro Systems公司;SHP-250生化培养箱 上海森信实验仪器有限公司;高效十点磁力搅拌器 德国IKA公司;水分活度密闭容器(Plastic water activity sample cup) 美国Decagon公司。
1.2 实验方法
1.2.1 高蛋白食品模型体系的制备 如表1所示,称取6 g乳清蛋白与4.5 g甘油-水溶液混合(甘油质量分数分别为0%、33%、50%、67%、78%、83%和100%)混合并初步搅拌,随后用手揉搓均匀并成团,制成一系列的乳清蛋白简化模型体系(A~G),装进水分活度密闭容器中,并用封口膜密封,以防止水分丢失。将制好的样品在室温下平衡30 min,于25 ℃生化培养箱中贮藏,每个模型体系制备3个平行样品。
1.2.2 硬度的测定 用TA-XT-plus 质构仪检测贮藏时间分别为0、1、3 d时模型体系的硬度。本实验选取直径为2 mm的圆柱探头(P/2)进行穿刺(puncture)实验。测量参数为:下压速度1.0 mm/s,触发力5 g,下压程度50%。硬度以穿刺过程中测得的最大应力来表征。为了减小误差,测量点之间、测量点与容器壁之间的距离至少为1 cm,每个体系做三次平行。

表1 乳清蛋白简化模型体系的配方
1.2.3 微观结构的测定 用激光共聚焦显微镜(CLSM)检测模型体系在3 d内微观结构的变化。样品的染色方法参照Linaek等人的方法[13]并做微小改进。取0.5 g新鲜样品,滴加12 μL FITC/丙酮溶液(20 mmol/L),搅拌均匀后,取0.3 g转移至玻底培养皿中,盖上盖玻片,AB胶封边后,置于载物台上,设定激发波长为488 nm,发射波长为510 nm,20倍物镜下进行观察。电子照片使用Zen 2011图像采集软件分析处理。
1.2.4 横向弛豫时间T2的测定 用NMI20-Analyst 核磁共振分析仪检测贮藏时间为0、1、3 d时模型体系的横向弛豫时间(T2)来表征体系中小分子的流动性。将2 g样品放入直径为15 mm的核磁管中,置于射频线圈的中心位置,用硬脉冲序列(Hard Pluse FID)调节中心频率后,再进行多脉冲回波序列(CPMG)扫描实验,轮流采样,每个样品测3遍[14]。CPMG序列采用的参数:采样点数TD=94220,回波个数C0=2048,重复扫描次数NS=64,弛豫衰减时间D0=1 s。利用MultiExp InvAnalysis软件进行反演,得到T2的连续分布图。
1.2.5 统计学分析 相关数据使用SAS 8.0软件进行分析,方差分析使用一般线性模型分析。p<0.05表示结果差异有统计学意义。
2 结果与讨论
2.1 模型体系的硬度变化
甘油与水比例不同的乳清分离蛋白简化模型体系(A~G)在储藏初期的硬度变化如图1所示。
储藏0 d,样品的初始硬度随甘油在溶液中比重的增加,呈现出先增大后减小的变化趋势。乳清蛋白纯水体系(A)的初始硬度最小约为(0.39±0.01) N;随着体系中甘油含量的增加,模型体系的初始硬度也不断变大;当甘油在溶液中的比重达到78%时(E),其硬度达到最大值(19.22±1.04) N,此后样品的初始硬度随甘油含量的增加反而减小,纯甘油体系(G)的硬度仅为(0.99±0.04) N。储藏过程中,样品A~E均未出现硬化;样品F的硬度在1 d内增加66%,之后保持不变;纯甘油体系(G)则发生了显著的硬化,其硬度在储藏1 d后增加了40倍,随后缓慢增长。储藏过程中样品的最终硬度随体系中甘油含量的增加单调上升。
由此可见,样品的最终硬度与体系内的甘油含量成正相关,甘油含量越大,样品的最终硬度越大,推测其可能原因是:样品A~E之所以能保持硬度不变或仅发生微小的改变,是因为这些体系中的水分含量相对充足,体系中绝大部分的蛋白颗粒在制备过程中已经均较好地溶解及水合,因此制备后的体系较为均一稳定,所以在储藏过程中没有发生明显的分子迁移而保持柔软的质地;而样品F、G中甘油含量高而水分含量低,制备后的体系内存在大量未溶解及未较好水合的蛋白颗粒,体系处于非热力学稳定状态,因此在储藏过程中,甘油和部分水不断向蛋白颗粒内部迁移并与蛋白结合,造成体系的整体流动性降低,使样品发生硬化。为了验证上述推测,通过激光共聚焦荧光显微镜和低场核磁共振进一步观察了这些体系在储藏过程中微观结构以及小分子流动性的变化情况。

图1 储藏不同时间的乳清蛋白简化模型体系的硬度随甘油含量变化Fig.1 Relationship between hardness of simplified model systems and glycerol proportion in solvent during the storage
2.2 模型体系的微观结构变化
由新鲜的乳清蛋白简化模型体系的CLSM图(图2)可以发现,甘油与水的相对比重对样品的微观结构有着显著影响。

图2 新鲜的乳清蛋白简化模型体系的微观结构(10×20)Fig.2 Microstructure of fresh model systems made with whey protein(10×20)注:箭头a所指为蛋白碎片,箭头b所指为破碎的蛋白颗粒,箭头c所指为完整的蛋白颗粒。
以乳清蛋白为蛋白组成的高蛋白纯水模型体系(A)的微观比较均一,蛋白与水形成的连续相中分散着一些细小的蛋白碎片(a);随着模型体系中甘油含量增加和水分减少,样品中出现破碎的蛋白颗粒(图2B)和蛋白颗粒聚集体(图2C);随着甘油含量越多,体系中未溶解的蛋白颗粒就越多(E、F、G)。模型体系A~E中不存在或存在少量的蛋白整体颗粒,而模型体系F、G中存在大量未溶解的蛋白颗粒,与体系硬度变化趋势(图1)相一致。
根据图1和图2,选择A(纯水体系,初始硬度最小)、E(临界体系,初始硬度最大)和G(纯甘油体系,终硬度最大)三个体系进行储藏实验,并通过CLSM监测储藏过程中体系的微观结构变化。实验结果表明(图3),模型体系A、E的微观结构在储藏过程中均未发生明显改变,这与其硬度在储藏过程中基本不变相一致;而模型体系G中存在大量未溶解的蛋白颗粒,在储藏过程,蛋白颗粒吸收体系中的甘油及部分水并不断溶胀、变大,颗粒之间堆积更加紧密,导致其硬度在储藏过程中不断增大,直至达到平衡状态。

图3 乳清蛋白简化模型体系A、E和G的微观结构变化(10×20)Fig.3 Changes in microstructure of model system A,E and G made of whey protein(10×20)
2.3 模型体系中的小分子流动性的变化
采用低场NMR测得的横向弛豫时间(T2)可以反映样品内部氢质子所处的化学环境,T2值越大,则说明氢质子所受的束缚越小,自由度越大[15],进而表明样品内含有这部分氢质子的物质受到周围环境(大分子)的束缚越小,流动性越强。因此,通过监测乳清蛋白简化模型体系中最具代表的三个体系:A、E和G体系的横向弛豫时间(T2)随储藏时间的变化,来研究样品内小分子物质(水、甘油)所处的状态及其在储藏过程中的中的迁移运动和在体系内的重新分布。
在T2弛豫时间的连续分布图中,峰的个数代表了样品内小分子物质(水、甘油)主要存在的状态数;峰顶点和所对应的峰面积则分别代表该种状态下的小分子物质的弛豫时间常数(T2)以及对应的含量[16]。
2.3.1 乳清蛋白简化模型体系A(纯水体系) 模型体系A的T2变化图表明(图4),在乳清蛋白纯水体系中,水分子所处的状态比较单一,其中约96%的水分子处于束缚态(T22),而4%左右的水分子处于结合态(T21)。

图4 乳清蛋白纯水体系A的T2变化图Fig.4 Changes in T2 relaxation time of simplified model system A made of whey protein during the storage
食品内的水主要分为结合水和体相水两大类[17]。结合水是与体系中的亲水性大分子(如蛋白质)结合最为紧密的那部分水,且其横向弛豫时间T2通常在几到几百微秒之间[18];体相水则又可以分为截留水(被生物膜或凝胶内大分子网所截留)和自由水(宏观流动不受阻碍),且自由水的T2值一般在几十到几百毫秒之间[19-20]。结合模型体系A中两种水分子的弛豫时间常数(表2)以及各自在总水量中所占的百分比,模型体系A中主要存在结合水(T21)和截留水(T22)而没有流动性较强的自由水(T2>10 ms),体系内的水分子与蛋白大分子之间紧密结合。

表2 乳清蛋白简化模型体系A、E和G的T2弛豫时间常数
注:
注:T2弛豫时间常数为峰顶点对应横向弛豫时间,A、E和G分别表示模型体系中的甘油占溶剂总量的0%、78%和100%。
储藏过程中,不同储藏时间(0、1、3 d)的T2弛豫曲线几乎完全重合,且弛豫时间常数也没有明显变化(表2,p>0.05),表明A体系处于平衡状态,性质比较稳定,在储藏过程中没有发生水分子的迁移或重新分布,这与其微观结构变化(图3)和质构变化(图1)相吻合。
2.3.2 乳清蛋白简化模型体系E(临界体系) 模型体系E的T2图表明(图5),在乳清蛋白的甘油-水临界体系中(甘油占溶剂的78%),小分子物质存在两种状态:受到蛋白束缚、流动性较弱的T21(1.81~9.11 ms),这部分小分子物质约占总量的77%;相对自由、流动性较强的T22(9.47~16.88 ms),这部分小分子物质约占总量的23%。在储藏过程中,模型体系E的T2弛豫时间轻微减小(图5,表2,p<0.05),表明该体系的分子流动性有所降低,这是因为模型体系E中存在着少量未溶解的蛋白颗粒(图3),储藏过程中这些未溶解的蛋白颗粒吸收体系中的小分子(水/甘油)并与之紧密结合,使其流动性有所降低,这与该体系的硬度有微弱增长(图1)相符合。
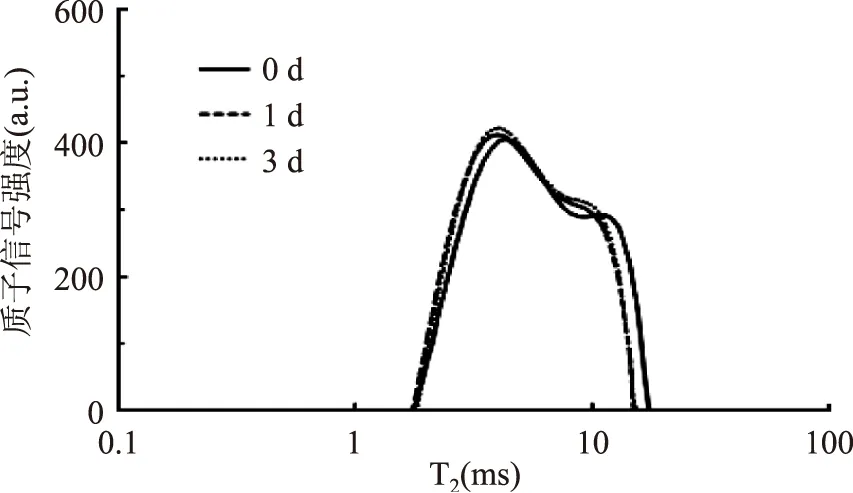
图5 乳清蛋白简化模型体系E的T2变化图Fig.5 Changes in T2 relaxation time of simplified model system E made of whey protein during the storage
2.3.3 乳清蛋白简化模型体系G(纯甘油体系) 模型体系G的T2变化图表明(图6),在乳清蛋白的纯甘油体系中,甘油分子存在两种状态:受到蛋白束缚、流动性较低的T21,以及存在于蛋白颗粒空隙间流动性较强的T22。由图中初始状态的实线(0 d)可以看出,绝大部分的甘油分子都处于高流动态(T22),这部分具有高流动性的甘油分子在体系中充当着塑化剂,而使样品具有较小的初始硬度。由图6中虚线(1 d和3 d)可知,甘油分子在储藏过程中发生了显著的迁移与重新分布:储藏1 d后,弛豫曲线中高弛豫部分的峰(T22)消失,低弛豫部分的峰(T21)骤然增大并左移(表2,p<0.05),表明体系内处于高流动态的甘油分子全部转化为低流动态,整体分子流动性显著减小,体系更加接近于固体,这与模型体系G在储藏1 d后硬度显著增大相吻合;随后弛豫时间常数T21变化速度明显降低(3 d),与其硬度变化趋势一致(图1)。结合CLSM图像(图3),推测模型体系G中存在大量未溶解的蛋白颗粒,储藏过程中颗粒空隙间流动性较强的甘油分子向颗粒内部迁移,将蛋白颗粒湿润溶胀,同时甘油因为与蛋白结合也失去塑化能力,导致样品发生硬化。

图6 乳清蛋白纯甘油体系G的T2变化图Fig.6 Changes in T2 relaxation time of simplified model system G made of whey protein during the storage
综上所述,模型体系A~E比较均一、稳定,体系中不存在或存在极少量的蛋白颗粒,储藏过程中无明显分子迁移而保持硬度基本不变;模型体系F、G中存在大量未溶解的蛋白颗粒,储藏过程中体系中流动性较强的小分子物质向蛋白颗粒内部迁移将其润湿、溶胀而使蛋白颗粒间堆积的越发紧密,致使样品硬化。具有高流动性的甘油和水分子在体系中充当着塑化剂的作用,但当其与蛋白紧密结合致使流动性降低后,便逐渐会失去其塑化能力,致使体系进一步硬化。由此可见,小分子迁移是高蛋白食品在储藏初期发生硬化的重要原因之一,当样品的结构均一、体系稳定而在储藏过程中没有发生明显的分子迁移时(乳清蛋白纯水体系),体系就能保持柔软的质地;而当体系中含有较多未溶解的蛋白颗粒(乳清蛋白甘油体系),小分子物质会从体相向颗粒内部迁移,致使分子流动性显著降低,体系微结构发生改变从而导致质地不断硬化。
3 结论
本实验建立了乳清蛋白/甘油/水组成的简化模型体系,并通过不断增加甘油在甘油-水溶液中的比例(0%~100%),逐渐改变乳清蛋白体系在储藏过程中的稳定状态,使其从“硬度不变”转变为“不断硬化”。NMR的实验结果表明体系内的小分子迁移造成了体系微结构的改变及整体流动性的降低,是模型体系从硬度不变(样品A~E)转变为不断的硬化(样品F、G)的主要原因,进而验证了关于分子迁移是导致体系初期硬化的重要因素的相关假设。而且体系内分子迁移程度越大,体系硬化程度则越显著。
[1]Hogan S A,Chaurin V,O’Kennedy BT,et al. Influence of dairy proteins on textural changes in high-protein bars[J]. International Dairy Journal,2012,26(1):58-65.
[2]Zhou P,Labuza T P. Effect of water content on glass transition and protein aggregation of whey powders during short-term storage[J]. Food Biophysics,2007,2(2-3):108-116.
[3]Zhou P,Liu X M,Labuza T P. Moisture-induced aggregation of whey proteins in a protein/buffer mode system[J]. Journal of Agricultural and Food Chemistry,2008,56(6):2048-2054.
[4]Zhou P,Guo M F,Liu D S,et al. Maillard-reaction-induced modification and aggregation of proteins and hardening of texture in protein bar model systems[J]. Journal of Food Science,2013,78(3):C437-C444.
[5]Imtiaz S R,Kuhn-Sherlock B,Campbell M. Effect of dairy protein blends on texture of high protein bars[J]. Journal of Texture Studies,2012,43(4):275-286.
[6]Loveday S M,Hindmarsh J P,Creamer L K,et al. Physicochemical changes in intermediate-moisture protein bars made with whey protein or calcium caseinate[J]. Food Research International,2010,43(5):1321-1328.
[7]Li T C,Zhou P,Labuza T P. Effects of sucrose crystallization and moisture migration on the structural changes of a coated intermediate moisture food[J]. Frontiers of Chemical Engineering in China,2009,3(4):346-350.
[8]McMahon D J,Adams S L,McManus W R. Hardening of high-protein nutrition bars and sugar/polyol-protein phase separation[J]. Journal of Food Science,2009,74(6):E312-E321.
[9]Labuza T P,Hyman C R. Moisture migration and control in multi-domain foods[J]. Trends in Food Science and Technology,1998,9(2):47-55.
[10]Liu W R,Langer R,Klibanov A M. Moisture-induced aggregation of lyophilized proteins in the solid state[J]. Biotechnology and Bioengineering,1991,37(2):177-184.
[11]Loveday S M,Hindmarsh J P,Creamer L K,et al. Physicochemical changes in model protein bar during storage[J]. Food Research International,2009,42(7):798-806.
[12]Zhou P,Liu X M,Labuza T P. Effects of moisture-induced whey protein aggregation on protein conformation,the state of water molecules,and the microstructure and texture of high-protein-containing matrix[J]. Journal of Agricultural and Food Chemistry,2008,56(12):4534-4540.
[13]Linaek H M,Broe M L,Hoier E,et al. Improving the yield of mozzarella cheese by phospholipase treatment of milk[J]. Journal of Dairy Science,2009,89(11):4114-4125.
[14]邵小龙,李云飞.用低场核磁共振研究漂烫对甜玉米水分分布和状态影响[J]. 农业工程学报,2009,25(10):302-306.
[15]Doona C J,Baik M Y. Molecular mobility in model dough systems studied by time-domain nuclear magnetic resonance spectroscopy[J]. Journal of Cereal Science,2007,45(3):257-262.
[16]Li J,Kang J,Wang L,et al. Effect of water migration between arabinoxylans and gluten on baking quality of whole wheat bread detected by magnetic resonance imaging(MRI)[J]. Journal of Agricultural and Food Chemistry,2012,60(26):6507-6514.
[17]谢笔钧. 食品化学[M]. 北京:科学出版社,2004:36-41.
[18]Midori K,Andrew R L,Sonoko A,et al. Quantitative NMR imaging study of the cooking of Japonica and Indica rice[J]. Food Research International,2007,40(8):l020-1029.
[19]Reinders J E A,Van As H,Schaafsma T J,et al. Water balance in Cucumis plants,measured by nuclear magnetic resonance[J]. Journal of Experimental Botany,1988,39(9):1199-1210.
[20]Tollner E W,Hung,Y C. Low resolution pulse magnetic resonance for measuring moisture in selected grains and kernels[J]. Journal of Agricultural Engineering Research,1992,53(3):195-208.
Migration of small molecules and its effect on texture hardening in high-protein nutritious bars made of WPI during early storage
LU Nai-yan1,2,ZHANG Liang1,ZHANG Xuan1,LI Yan-fang1,ZHOU Peng1,2,*
(1.State Key Laboratory of Food Science and Technology,Jiangnan University,Wuxi 214122,China;2.School of Food Science and Technology,Jiangnan University,Wuxi 214122,China)
High-protein nutritious bars are suffering from texture hardening,which limits their shelf life. The mechanisms for the hardening of high-protein nutritious bars are rather complicated. In this research,protein bar model systems were prepared with WPI,water,and glycerol. By adjusting the proportion of water and glycerol in the solvent fraction,a series of models with different storage stability were obtained. Texture analyzer,confocal laser scanning microscope,and low-field nuclear magnetic resonance were used to investigate the relationship between migration of small molecules and texture hardening of the systems in the early stage of storage. It was suggested that the changes in texture of the model system converted from “keeping constant” to “hardening rapidly” as the proportion of glycerol in solvent increased. WPI-water system formed a uniform structure without undissolved protein particles. Migration of small molecules or change of microstructure was not observed and the system kept soft during the early stage of storage. However,as the proportion of glycerol was increased,undissolved protein particles could be observed and the small molecules such as glycerol and water migrated into the particles during the storage,which caused texture hardening. In conclusion,the migration of small molecules was a key factor for the rapid hardening of high-protein nutrition bars in the early stage of storage.
high-protein foods;early stage of storage;hardening;migration of small molecules
2014-12-15
陆乃彦(1985-),男,博士,副教授,研究方向:食品科学,E-mail:lunaiyan@jiangnan.edu.cn。
*通讯作者:周鹏(1975-),男,博士,教授,研究方向:食品科学,E-mail:zhoupeng@jiangnan.edu.cn。
国家自然科学基金(31471697,31071492);新世纪优秀人才支持计划(NCET-11-0666);教育部科学技术研究项目(113032A)。
TS252.5
A
1002-0306(2015)15-0049-05
10.13386/j.issn1002-0306.2015.15.001

