载铜活性炭的制备及其吸附甲苯性能研究
黄艳芳,刘志军,刘金红
(南通职业大学 化学与生物工程学院,南通 226007)
VOCs污染已引起各界政府和社会公众的广泛关注,有效治理VOCs环境污染刻不容缓。目前,制理VOCs污染的方法主要有销毁法和回收法[1]。其中销毁法是将VOCs转换为CO2、H2O或者其他易处理的物质,这种方法不仅导致某些昂贵的VOCs无法回收,造成资源浪费,并且还会带来二次污染(如燃烧法处理VOCs过程中有可能产生比初始气体更有害的污染物二噁英、乙醛、呋喃等;等离子体处理过程产生的CO等)。因此,回收法无论从环保还是从经济角度来看,都是值得提倡的VOCs治理技术。VOCs回收方法主要有吸收、吸附、冷凝、膜分离等。其中吸附分离回收被认为是一种极具发展潜力的VOCs治理技术。
活性炭因其特殊的孔道结构,在环境污染治理中越来越广泛的被用于气体的吸附脱除。为了进一步优化活性炭的吸附性能,研究者从活性炭的制备和改性两方面入手,取得了一系列成果。其中,基于络合作用的新型负载型吸附剂的研究越来越引起了学者的兴趣[2-4]。李德伏等[5]采用三种金属溶液(Cu (NO3)2水溶液、CuCl2加 HCl和 La(NO3)2水溶液)对活性炭进行改性,并研究其对乙烯的吸附性能。梅华等[6]研究了CuCl改性活性炭对乙烯、乙烷的分离性能。
以上研究的理论依据为乙烯中的π键与亚铜离子之间存在络合作用。这种π络合吸附作用力强于物理吸附作用力。因此在某些场合,例如高温下,当物理吸附作用力很弱时,π络合吸附依然可以发挥作用,从而增强吸附剂的吸附能力。但是,π络合吸附作用力又弱于化学吸附作用力,故又可以很方便的实现吸附剂的再生。甲苯中的苯环同样存在π键,理论上也可与亚铜离子形成络合键,基于此制备了负载氯化亚铜的载铜活性炭吸附剂,并对其吸附甲苯性能进行了研究。
1 实验部分
1.1 实验药品与仪器
药品:二水氯化铜,分析纯;活性炭,木质,20~40目;盐酸,w=36.5%;氮气,φ=99.9%)。
仪器:自制动态吸附装置;气相色谱仪,SP-6890,山东瑞虹化工仪器有限公司。
1.2 载铜吸附剂的制备
将一定量的氯化铜溶解于一定体积1mol/L的HCl溶液中,将活性炭等体积浸渍其中。室温下放置一定时间后150℃空气中干燥备用。将活性炭装填于吸附柱中,氮气保护下高温焙烧,使Cu(II)转化成Cu(I),得到 1g 活性炭分别负载 0、0.1、0.2、0.3、0.4、0.5、0.6g的 CuCl的吸附剂, 分别记为 AC0、AC1、AC2、AC3、AC4、AC5、AC6。 冷却后进行甲苯的吸附实验。
1.3 甲苯吸附性能评价
采用自制的小型固定床实验装置进行模拟工业的柱动态吸附,如图1所示。吸附柱尺寸为φ18mm×400mm。甲苯气源由氮气流经置于高压装置中的液相甲苯获得,吸附压力0.2MPa。通过气相色谱仪对吸附尾气进行分析检测,确定甲苯的穿透时间和饱和吸附时间,甲苯的饱和吸附量由重量法测定。

图1 动态吸附实验流程图
1.4 吸附剂的表征
吸附剂的BET比表面积在美国Micromeritics公司生产的ASAP2010型自动吸附仪上测定。
XRD在德国Bruker公司的D8 ADVACE型X射线衍射仪上进行,实验条件为:CuKα射线源(衍射狭缝从左到右均为1mm),镍单色器(0.6mm);扫描范围2θ为10~70°;工作电压和电流分别为40kV和30mA。
TPR在美国Quantachrome公司生产的chembet-3000装置上进行。采用双气路,氩氢混合气中φ(H2)=5%,气体流速为20mL/min,升温速率为10℃/min。
2 结果与讨论
2.1 CuCl2在活性炭表面的还原
因为CuCl在水中的溶解度很小,且在空气中易被氧化为CuCl2,故在吸附剂的制备中,需先将CuCl2负载于活性炭表面,然后通过高温还原的方法,将Cu(II)转变为Cu(I)。活性组分的还原通常会在H2、CO等还原性气体氛围中进行,但由于活性炭表面性质的特殊性,其表面官能团可与Cu(II)作用完成自还原过程,因此以活性炭为载体时,活性组分的还原可在惰性气体氮气中进行,这是活性炭材料作为载体的一大优势[7]。本研究还原过程采用了惰性气体氮气,经还原后,样品中出现了CuCl晶相(见图3),从实验角度验证了上述观点。
为了进一步确定Cu(II)转化为Cu(I)的温度,将制备的CuCl2-AC样品进行了H2-TPR分析,结果如图2所示。从图中可以看出,CuCl纯品的谱图只在400℃附近存在氢消耗峰,对应Cu(I)向 Cu(0)的转变。CuCl2-AC与AC0相比,出现了两个明显的氢消耗峰,分别在270℃和400℃附近。400℃的峰同样对应着 Cu(I)向Cu(0)的转化,270℃的峰即为 Cu(II)向Cu(I)的转变峰。由此可见,还原温度应设定在270℃左右。还原温度低于270℃,无法将Cu(II)还原成Cu(I),而温度过高,则可能出现Cu(II)的过度还原。本研究采用的还原温度为300℃。

图2 样品的H2-TPR曲线
2.2 CuCl分散阈值的测定
根据单层分散理论,大部分盐类或其氧化物在一定条件下都能在载体上自发的单层分散,并且每个分散体系都存在一个相对固定的最大分散量,即分散阈值。为了确定CuCl在活性炭表面的最佳负载量,通过XRD测定了CuCl的分散状况。图3从下至上依次为未经负载的活性炭AC0、负载量为0.4g/gAC、0.5g/gAC、0.6g/gAC的吸附剂样品。 AC0及负载量为0.4g/gAC的样品中,均无CuCl的特征峰出现,表明当负载量为0.4g/gAC时,CuCl在载体表面单层分散。当负载量为0.5g/gAC时,XRD谱图中出现了微弱的CuCl特征峰 (2θ=28.5°处), 表明CuCl在活性炭表面的分散达到阈值点。当负载量增加至0.6g/gAC时,CuCl的特征峰进一步增强(2θ角为28.5°和47.5°处),此时CuCl在活性炭表面已不再呈现单层分布,而以某种晶体形式存在。由此确定了CuCl在活性炭表面的分散阈值为0.5g/gAC,即0.454mg/m2(活性炭的比表面积为1100m2/g)。

图3 不同负载量的CuCl/AC的XRD谱图
2.3 载铜活性炭吸附甲苯性能研究
2.3.1 温度对载铜活性炭吸附甲苯性能的影响
制备了负载量分别为 0.1、0.2、0.3、0.4、0.5g/gAC的吸附剂,测定其在20℃和100℃的甲苯饱和吸附量,如图4所示。20℃时,跟未经负载的活性炭相比,载铜活性炭的饱和吸附量具有不同程度的降低,且随着负载量的增加,饱和吸附剂的吸附量越来越小。而100℃时,载铜活性炭的吸附量明显大于未经负载的活性炭,随着负载量的增加,饱和吸附量先呈现明显的上升趋势,达到最高点后,又略有降低。这是因为在载铜活性炭表面同时发生物理吸附和络合吸附。低温下,物理吸附占主导地位,而负载的CuCl反而占据了部分吸附表面,阻挡了部分孔道,从而造成载铜吸附剂的饱和吸附量小于未经负载的活性炭,随着负载量的增加,CuCl占据的吸附表面越多,饱和吸附量就越低。而高温下,物理吸附作用大大削弱,络合吸附占据了主导地位,故载铜吸附剂的饱和吸附量明显大于未经负载的活性炭,此时活性炭的表面的Cu(I)越多,络合吸附作用越强,所以随着负载量的增加,饱和吸附量有所增加。极值点的出现说明,负载量并不是越多越好。原因可能是负载量过大反而影响Cu(I)在的活性炭表面的均匀分布或一定程度上阻碍了甲苯在活性炭表面的扩散。

图4 载铜活性炭吸附甲苯性能(20℃、100℃)
2.3.2 负载量对载铜活性炭吸附性能的影响
测定了40~200℃下不同负载量的活性炭吸附剂对甲苯的饱和吸附量,结果如图5所示。从图5中可以看出,随着温度的升高,饱和吸附量呈现下降趋势,符合高温不利于吸附的普遍规律。载铜活性炭的饱和吸附量均大于未经负载的活性炭,其中AC3饱和吸附量最大,由此确定最佳负载量为m(CuCl)/m(AC)=0.3,该值小于分散阈值m(CuCl)/m(AC)=0.5。这与载铜吸附剂吸附乙烯的规律不同,文献[8]报道,对于载铜活性炭吸附乙烯体系,最佳负载量基本与分散阈值一致。这可能是因为,甲苯的分子大于乙烯,造成甲苯在吸附剂中的扩散要比乙烯困难。而过多的CuCl负载,不可避免要占据一定的孔道(见表1),反而阻碍了甲苯的扩散。因此对于载铜活性炭吸附甲苯的体系,最佳负载量要小于分散阈值。

图5 不同负载量吸附剂的吸附甲苯性能
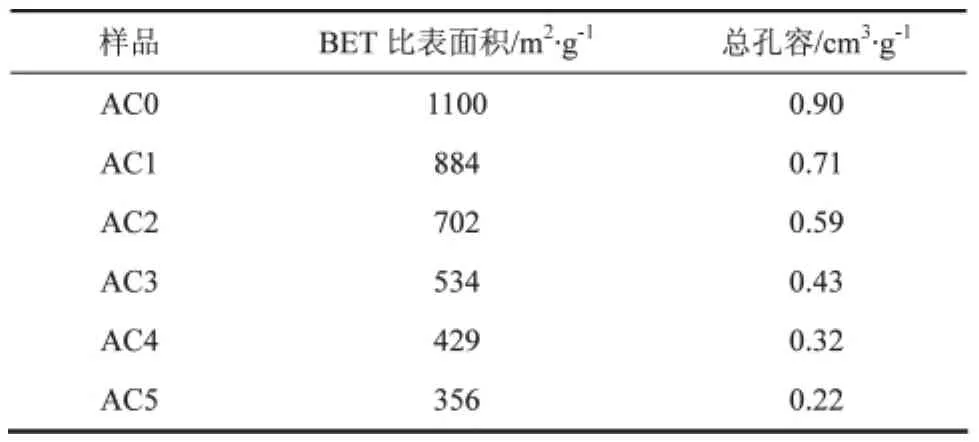
表1 不同负载量吸附剂的比表面积和孔容
3 结论
(1)在氮气保护下,通过与活性炭表面官能团作用可实现Cu(II)到Cu(I)的自还原转化,转化温度为270℃左右。
(2)通过XRD确定了CuCl在活性炭表面的分散阈值为m(CuCl)/m(AC)=0.5,即0.454mg/m2。
(3)低温下,载铜活性炭对甲苯的饱和吸附量小于未经负载的活性炭;高温时,正好相反。
(4)在40~200℃范围内,载铜活性炭对甲苯的饱和吸附量均大于未经负载的活性炭,最佳负载量为m(CuCl)/m(AC)=0.3。
[1]Khan F I,Ghoshal A K.Removal of volatile organic compounds from polluted air[J].J Loss Prevent Proc,2000,13:527-545.
[2]Takahashi A,Yang F H,Yang R T.Aromatics/aliphatics separation by adsorption:New sorbents for selective aromatics adsorption by π-complexation [J].Ind Eng Chem Res,2000,39:3856-3867.
[3]张广林,赵新强,王延吉.CuCl2负载量对CuCl2-La(NO3)3/AC吸附分离乙烯/乙烷中乙烯的影响 [J].天然气化工(C1化学与化工),2008,33(6):27-30.
[4]Huang H Y,Yang R T,Chen N.Anion effects on the adsorption of acetylene by nickel halides[J].Langmuir,1999,15:7647-7652.
[5]李德伏,曾海,王金渠,等.活性炭的改性及对乙烯的吸附性[J].石油化工,2001,30(9):677-680.
[6]梅华,胡成刚,刘晓勤,等.活性炭表面氧化改性对负载铜(I):吸附剂及其乙烯吸附性能的影响[J].新型炭材料,2002,17(4):33-37.
[7]Takahashi A,Yang R T,Munson C L,et al.Cu(I)-Y-zeolite as a superior adsorbent for ciene/olefin separation[J].Langmuir,2001,17:8405-8413.
[8]岳军,刘晓勤,姚虎卿.CuCl负载型吸附剂的深度脱硫性能研究[J].高校化学工程学报,2006,20(6):1001-1004.

