pH值及焙烧气氛对Cu-Zn-Al甲醇合成催化剂结构和性能的影响
闫 杏 ,吕晓东 ,王 霞 ,栾春晖 ,樊金串 ,3*,黄 伟
(1.太原理工大学 化学化工学院,山西 太原 030024;2.太原理工大学 煤科学与技术教育部和山西省重点实验室,山西 太原 030024;3.中国科学院山西煤炭化学研究所 煤转化国家重点实验室,山西 太原 030001)
甲醇是一种重要的基础有机化工产品和潜力巨大的清洁可替代燃料[1]。Cu-Zn-Al催化剂由于具有较好的催化活性,较长的使用寿命,高的抗毒性以及相对较低的反应温度和压力,被用于工业甲醇合成,其研究一直是人们感兴趣的课题[2]。目前,研究主要集中于催化剂的原料配比[3]、制备方法[4]以及催化剂改性[5]等方面,认为铜组分的分散性、CuZn组分间的相互作用是影响催化剂反应活性和稳定性的重要因素。工业上甲醇合成催化剂一般采用沉淀法制备[6],在固定床反应器上进行反应;由于甲醇合成是一个放热反应,为了避免催化剂过热失活,通常都控制合成气的转化率在一个较低的水平。浆态床反应器由于具有传热快,易于控制反应温度等优点被用于甲醇合成的研究之中。Zhai等[7]将工业甲醇合成铜基催化剂用于浆态床反应,发现催化剂存在失活现象,认为活性组分铜颗粒的烧结长大是导致催化剂在不同的反应时间失活速率不同的主要原因。黄伟等[8]针对浆态床反应器的特点提出了一种新的催化剂制备方法——完全液相法,它和传统方法的最大差异是催化剂在液相中形成,而传统法则是在气相中焙烧得到。研究表明,完全液相法本身能赋予催化剂特有的性质,它不仅仅限于浆态床反应,也应该能用于固定床反应中。Luan等[9]将完全液相法制备的催化剂用于固定床反应,发现催化剂的反应活性较差,其原因是催化剂表面覆盖了一层碳膜所致。为此,本文首先以氨水作为pH调节剂,采用完全液相法制备了系列Cu-Zn-Al催化剂,并将其分别在N2和空气气氛下进行焙烧处理,考察了铜盐溶液的pH值及焙烧气氛对催化剂结构和性能的影响。
1 实验部分
1.1 催化剂制备
将硝酸铝溶解在蒸馏水中,加氨水调pH≥9.2,使其完全形成勃姆石沉淀,将所得沉淀离心洗涤至pH=7;然后向沉淀中加入一定量蒸馏水 (n(H2O)/n(Al)=100),并在45℃下搅拌沉淀至分散均匀,之后加入一定量浓硝酸(n(H+)/n(Al)=0.27),升温至95℃回流搅拌30min制得透明稳定的铝溶胶。
将一定量Cu(NO3)2·3H2O(AR)溶于蒸馏水中(此时pH=3),缓慢滴加氨水调节pH至7和9,然后将一定量的Zn(NO3)2·6H2O(AR)乙醇溶液缓慢滴加至80℃的铝溶胶中,再将上述铜盐溶液加入其中,在80℃下回流搅拌4h,室温下老化3d获得催化剂前驱体。将前驱体与一定量的聚乙二醇-200混合,在230℃下恒温搅拌7h,制得Cu-Zn-Al浆状催化剂,经离心分离、水洗、醇洗后在40℃下烘干备用。催化剂投料比n(Cu)/n(Zn)/n(Al)=2/1/0.8,铜盐溶液pH=3、7、9 对应的催化剂分别记为 CA1,CA2和 CA3。
将上述催化剂分别在空气和N2气氛中于300℃焙烧3h,对应催化剂分别为CAi-N2、CAi-Air,所得样品用于各种表征。
1.2 催化剂表征
样品的XRD表征采用日本岛津的XRD-6000型衍射仪,Cu-Ka辐射源,Ni为滤片,管电压40kV,电流 100mA, 扫描范围 2θ=10°~80°, 扫描速率为4°/min,物相识别用粉末衍射标准卡片(JCPDS)对照读取。N2吸附测定采用美国康塔公司生产的Quanta Chrome QDS-30物理吸附仪,用BET方程计算催化剂的比表面积,总的孔容由BJH模型确定。X射线光电子能谱 (XPS)分析采用VG公司ESCALAB250型X射线光电子能谱仪,以单色化的Al-Ka 为辐射源(hv=1486.6eV),基础真空 7.0×10-8Pa。样品测试时,通过能为30eV,步长0.1eV;采用污染碳C1s(Eb=284.6 eV)对样品进行荷电校正,使用sheirly法扣除背景;根据各元素特征峰的峰面积和灵敏度因子求算催化剂表面的元素组成。NH3-TPD是在TP-5000型(天津先权仪器厂)装置上进行。催化剂用量为100mg,首先以 φ(H2)=5%的 H2/N2混合气为还原气,流速为30mL/min,在280℃下还原0.5h,He气吹扫0.5h,然后降温至50℃进行脉冲吹扫,最后以10℃/min的速率从50℃升温至810℃,质谱检测NH3脱附量。
1.3 催化剂活性评价
催化剂的活性测试在加压连续流动的固定床不锈钢反应器中进行。将催化剂压片造粒(40~60目)后装入内径为8mm的固定床反应管中,催化剂的用量为 2mL。以 φ(H2)=20%的 H2/N2混合气、0.5℃/min 升温至250℃常压还原4h,降温后切换为合成气进行反应。合成气n(H2)/n(CO)=2,气体总流量为100mL/min,反应温度250℃,反应压力为4MPa。反应后气体经冷凝器冷凝后气液两相分离,液相产物每24h收集一次,在上海华爱GC9560气相色谱仪上分析气体和液体产物的组成。用TCD(TDX-01)检测H2、CO和CO2,用FID(Plot-Q柱)检测甲醇、二甲醚和烃等物质,利用外标法定量分析各组分的含量。
2 结果与讨论
2.1 催化剂XRD表征
图1为未焙烧催化剂的XRD谱图,可以看到,采用完全液相法制备的催化剂中只有Cu和ZnO的衍射峰,而没有看到氧化态的铜物种,这是由于聚乙二醇具有一定的还原能力,在热处理过程中将其还原为单质Cu。随pH值的增大,Cu的衍射峰强度逐渐减弱,而ZnO的衍射峰逐渐增强,即Cu晶粒尺寸逐渐减小,而ZnO晶粒由小变大。主要原因是随着pH的增大,氨水加入量的增加,在体系中形成的Cu(NH3)42+的浓度也随之增大,催化剂形成过程中,Cu2+缓慢释放被聚乙二醇还原所致。

图1 未焙烧催化剂的XRD谱图
图2是在N2和空气气氛中焙烧后催化剂的XRD谱图。与未焙烧催化剂相比,在N2气氛中焙烧后,催化剂的物相没有发生变化,仍然为Cu和ZnO;Cu晶粒尺寸均减小,且随着pH值的增加,Cu晶粒先增大后减小,pH为9时Cu的分散性最好,见表1。在空气中焙烧后,催化剂的物相主要为CuO和ZnO,它们的部分特征峰出现了重叠,说明在催化剂焙烧过程中,Cu被氧化的同时,Cu2+和Zn2+之间发生了相互同晶取代反应,促进了Cu-Zn间的协同作用,使得CuO和ZnO的衍射峰宽化[10]。
反应后,所有催化剂的物相均是Cu和ZnO,见图3。Cu晶粒大小随pH的变化规律一致,与焙烧气氛无关。总体来看,空气中焙烧的催化剂中的铜晶粒略小于相应N2气氛下焙烧的催化剂,因为在还原和甲醇合成反应时,空气气氛下形成的ZnO可以有效阻止因局部过热导致的铜晶粒尺寸的长大,起到助催化作用[11]。
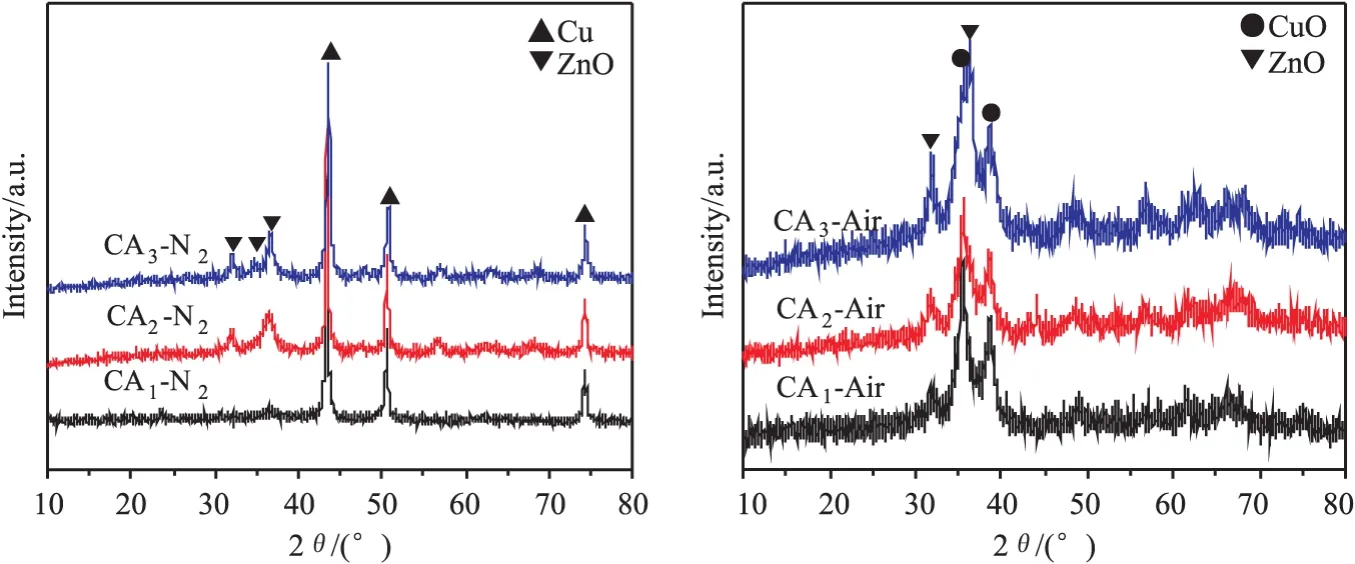
图2 焙烧后催化剂的XRD谱图

图3 反应后催化剂的XRD谱图

表1 不同催化剂中Cu的晶粒大小 单位:nm
2.2 催化剂N2吸附表征
表2为催化剂的织构性质。可以看出,焙烧后,随pH值的增加,催化剂的比表面积缓慢增大,比孔容和平均孔径先减小后增大,变化规律与焙烧气氛无关。两种气氛下焙烧后催化剂的比表面积相差不大,但催化剂的平均孔径和孔容有较大差异,总体来看,空气中焙烧有利于催化剂孔容和平均孔径增大,这主要是由于在焙烧过程中催化剂表面残留的有机碳物种被氧化逸出所致。
反应后,催化剂的比孔容和孔径都增大,但增幅不一;而比表面积的变化规律与焙烧气氛密切相关。N2气氛焙烧的催化剂在反应后比表面积均有不同程度的增加,孔容和孔径略有增大;而空气中焙烧的催化剂在反应后比表面积均减小,这可能与空气气氛焙烧的催化剂在还原过程中金属氧化物的氧与氢反应生成水而逸出、较小的孔结构被破坏和合并从而使得大孔数目增多、孔径增大有关。

表2 Cu-Zn-Al催化剂的织构性质
2.3 催剂XPS表征
图4为焙烧后催化剂的Cu2p-XPS谱图。由图4可以看出,空气中焙烧的催化剂,Cu2p3/2的结合能位于933.2eV附近,在940eV~945eV之间存在一个明显的伴峰,说明催化剂表面上的铜物种以Cu2+的形式存在;N2气氛下焙烧的催化剂,在940eV~945eV之间没有伴峰出现,表明催化剂中的铜物种主要以Cu0或Cu+形式存在[12-14];CA2-N2催化剂表面的Cu2p3/2结合能相对于其余两个催化剂明显升高约0.6eV,表明在pH=7时,催化剂表面Cu物种所处环境有一定的特殊性。一般认为,CO分子中C端呈部分负电性,金属原子的电子结合能越高,其吸附呈部分负电性的C端的能力就越强,就越容易形成化学吸附,从而活化C-O键进行加氢反应[5],有利于提高催化剂的反应性能。

图4 焙烧后催化剂的Cu2p-XPS谱图
表3为焙烧后催化剂的表面元素组成。可以看到,在空气中焙烧后催化剂表面碳含量明显较低,Cu、Zn、Al含量较高,这是由于在有氧气氛下,催化剂中残留的有机碳物种大量被氧化消除;而N2气氛下焙烧的催化剂表面仍然存在一些碳物种在焙烧温度下无法分解逸出,导致活性组分在催化剂表面的含量较低。催化剂在制备时的投料比为n(Cu)/n(Zn)/n(Al)=2/1/0.8,而所有催化剂样品表面的Cu/Zn和Cu/Al比均小于投料比,说明催化剂中Zn和Al存在不同程度的表面富集现象,这是由于ZnO和Al的晶格能大于Cu物种的晶格能所致[15]。除了晶格能的影响,催化剂所处的化学环境也是影响表面元素富集的主要原因。空气中焙烧后,催化剂表面的Cu/Zn比和Cu/Al比明显高于N2气氛中焙烧的催化剂,且随pH增大,表面Cu/Zn比增大;N2气氛中焙烧后催化剂表面的Cu/Zn比与pH没有一定的顺变关系,pH=7时催化剂表面具有较高的Cu/Zn比。从表3还可以看到,pH=7的催化剂CA2经焙烧后,催化剂表面的铜含量最高,表明在催化剂制备时用氨水调节铜盐溶液的pH可以提高催化剂表面的铜含量。

表3 焙烧后催化剂的表面元素组成
2.4 催化剂NH3-TPD表征
图5为焙烧后催化剂的NH3-TPD谱图。可以看到,所有催化剂均出现了两个主要的NH3脱附峰,分别对应弱酸位和中强酸位。N2气氛焙烧的催化剂,随着pH的增加,酸强度变化不大,但弱酸和中强酸酸量呈现先减小后增加的趋势。在空气中焙烧的催化剂,随着pH的增加,中强酸的强度先增加后减弱,而其酸量逐渐增大。相对来看,空气中焙烧的催化剂的弱酸和中强酸酸量均较少。文献报道[16],催化剂表面较强碱性和较弱酸性有利于活性组分与载体间的相互作用,有利于CO的吸附。
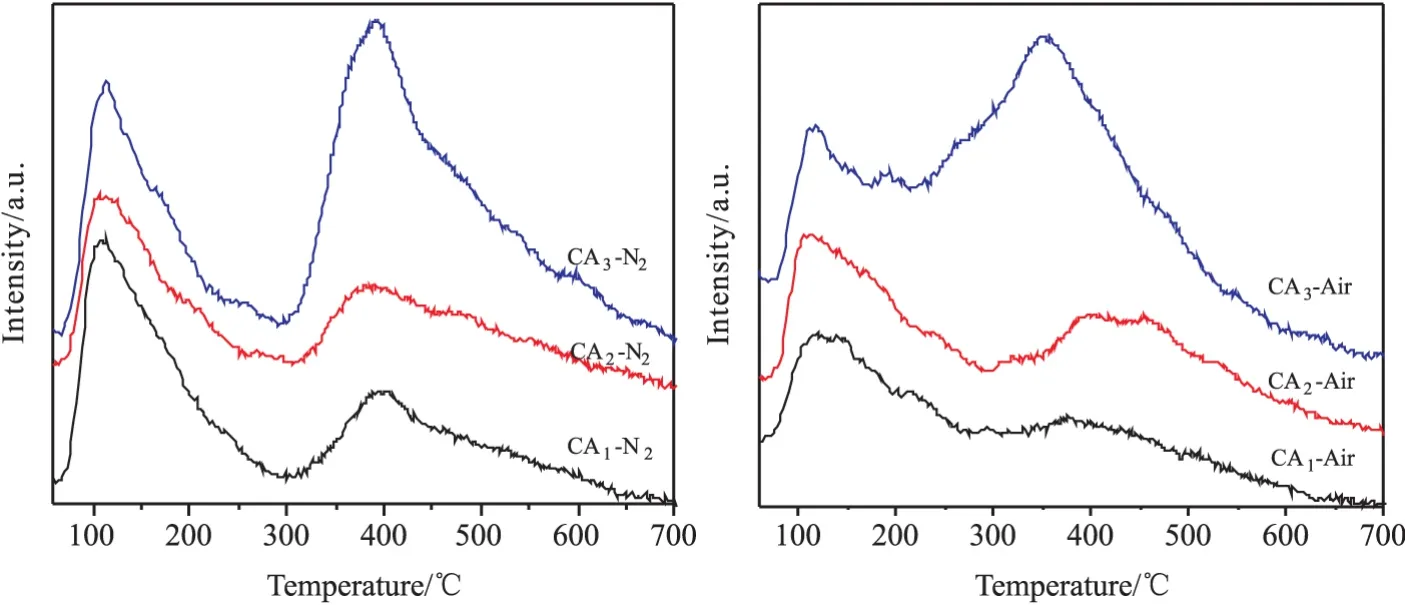
图5 焙烧后催化剂的NH3-TPD谱图
2.5 催化剂反应性能
图6是不同催化剂上CO转化率随反应时间的变化曲线,可以看到,虽然N2气氛焙烧的催化剂反应活性低,但是其稳定性较好;而空气中焙烧的催化剂CO转化率达到最大值之后活性均略有降低,这可能与反应后催化剂比表面积减小有关。

图6 不同催化剂上CO转化率随反应时间的变化
表4为不同催化剂上的CO加氢反应性能,可以看出,在空气中焙烧后的催化剂上CO转化率显著高于在N2气氛焙烧的催化剂,且对甲醇的选择性整体较高,这与催化剂表面的碳含量较低而Cu含量较高有关。一般认为,具有高比表面积、高的铜物种分散度、以及高的表面铜含量的催化剂有利于催化反应活性的提高[4-5],但是,结合上述表征结果发现,pH=9的CA3催化剂铜物种的分散性和比表面积是最大的,它的反应活性却是最低的;相反,pH=7的CA2催化剂的反应活性最高。因此认为,催化剂具有较低的表面碳含量、较高的表面铜含量以及较少的表面酸量更有利于CO加氢反应活性的提高,这与文献报道一致[16,17]。
反应产物中除甲醇外,还有少量烃、DME和CO2以及C2+醇生成。通常认为,弱酸位有利于甲醇脱水生成二甲醚,中强酸位和强酸位有利于甲醇脱水生成烃[18]。N2气氛焙烧的催化剂由于其弱酸位和中强酸位量较高,所以其对烃、DME和CO2的选择性较高。

表4 不同催化剂上的CO加氢反应性能
3 结论
采用完全液相法制备的Cu-Zn-Al催化剂,随铜盐溶液pH值的增加,Cu的分散性逐渐增大,但焙烧后Cu的分散性无规律可循。催化剂在空气气氛下焙烧,可以有效促进Cu-Zn组分间的相互作用,抑制铜晶粒尺寸的长大,增加催化剂中的大孔数目,大幅度降低催化剂表面的碳含量提高表面铜含量,从而显著提高了催化剂的催化性能。催化剂在N2气氛中焙烧后表面仍残留一定量的碳物种,因而对催化活性的提高幅度不大。铜盐调节至pH=7及空气气氛焙烧可以提高催化剂表面的表面铜含量,降低表面酸量,从而对催化剂的CO加氢性能更有利。
[1]Phan K X,Bakht iary-Davijany H,Myrstad R,et al.Preparation and performance of Cu-based monoliths for methanol synthesis[J].Appl Catal A,2011,405:1-7.
[2]Wang F,Liu Y W,Gan Y H,et al.Study on the modification of Cu-based catalysts with cupric silicate for methanol synthesis from synthesis gas[J]. Fuel Process Technol,2013,110:190-196.
[3]李忠,郑华艳,谢克昌.浆态床合成甲醇CuO/ZnO/Al2O3催化剂的表面性质[J].催化学报,2008,29(5):431-435.
[4]林胜达,唐浩东,吕兆坡,等.沉淀方法对铜基甲醇合成催化剂前驱体及其性能的影响 [J].催化学报,2010,31(10):1257-1262.
[5]郝爱香,于杨,陈海波,等.表面助剂改性对Cu/ZnO/Al2O3甲醇合成催化剂性能的影响 [J].物理化学学报,2013,29(9):2047-2055.
[6]孙焕红,李霞.甲醇合成催化剂的研究概况分析[J].产业与科技论坛,2014,13(18):50-52.
[7]Zhai X F,Shamoto J,Xie H J,et al.Study on the deactivation phenomena of Cu-based catalyst for methanol synthesis in slurry phase[J].Fuel,2008,87:430-434
[8]黄伟,高志华,郝立峰,等.浆态床用催化剂及制备方法[P].CN:1314491C,2004.
[9]Luan C H,Zhang A R,Wang X D,et al.Catalytic activity of liquid phase prepared Cu-Zn-Al catalyst for CO hydrogenation in a fixed bed reactor[J].Indian J Chem Sect A,2012,51A:1663-1668.
[10]房德仁,刘中明,黎晓琼,等.沉淀pH值对CuO/ZnO/Al2O3系催化剂前体性质的影响[J].石油化工,2004,33(7):622-626.
[11]李忠,郭启海,张小兵,等.前驱体物相转变对浆态床合成甲醇催化剂活性的影响 [J].高等学校化学学报,2009,30(11):2215-2221.
[12]Chapelle A,Pasquet I,Presmanes L,et al.Structural and gas-sensing properties of CuO-CuxFe3-xO4nanostructured thin films[J].Sens Actuators B,2011,153:117-124.
[13]Yu J G,Hai Y,Jaroniec M.Photocatalytic hydrogen production over CuO-modified titania[J].J Colloid Interface Sci,2011,357:223-228.
[14]Zuo Z J,Wang L,Liu Y J,et al.The effect of CuO-ZnOAl2O3catalyst structure on the ethanol synthesis from syngas[J].Catal Commun,2013,34:69-72.
[15]李志红,黄伟,左志军,等.用XPS研究不同方法制备的CuZnAl一步法二甲醚合成催化剂 [J].催化学报,2009,30(2):171-177.
[16]马中义,杨成,周玮,等.载体表面性质对Cu/ZrO2催化剂CO加氢反应行为的影响 [J].燃料化学学报,2009,37(2):217-221.
[17]范辉,李忠,郑华艳,等.微波辐射对浆态床合成甲醇CuO/ZnO/Al2O3催化剂前驱体晶相转变的影响 [J].无机化学学报,2011,27(3):509-518.
[18]高志华,贾钦,程凯,等.添加聚乙二醇对CuZnAl浆状催化剂结构和性能的影响 [J].化学学报,2012,70(3):325-330.

