温度/pH 双敏型羧甲基壳聚糖/海藻酸钠凝胶微球的制备
王娟,张保华,崔晓翠,孔祥平
(青岛农业大学 化学与药学院,山东青岛 266109)
聚合物微球是被广泛研究和应用的一类药物载体[1]。由于能对外界环境(如温度、pH、电、光、磁场、特定生物分子等)微小的变化或刺激产生显著应答,环境敏感型凝胶微球作为控制释放载体材料受到人们的广泛关注[2-3]。温度和pH 是两个重要的环境因素,具备温度/pH 双敏型凝胶微球控释材料对实现药物的有效控释至关重要。羧甲基壳聚糖同时含有—NH2和—COOH[4],在溶液中表现出两性聚电解质性质,存在一特定等电点,表现出明显的pH 敏感性,适于用作pH 敏感型控释载体材料。海藻酸钠易与一些2 价阳离子形成凝胶,其温和的溶胶凝胶过程、良好的生物相容性使其适于作为释放或包埋药物、蛋白及细胞的微胶囊[5]。羧甲基壳聚糖/海藻酸钠作为载体的控释剂已有报道[6-7],但关于羧甲基壳聚糖/海藻酸钠凝胶微球的性能研究较少,限制了其应用。本文以羧甲基壳聚糖和海藻酸钠为原料,氯化钙和戊二醛混合溶液为交联剂,制备温度/pH 双敏型凝胶微球,为其用于药物控释载体提供依据。
1 实验部分
1.1 试剂与仪器
羧甲基壳聚糖(自制,其取代度为0.99,脱乙酰度为88%[4];黏均分子量[8]为3.8 ×105);海藻酸钠(黏度1.05 ~1.15 Pa·s)、戊二醛(≥50%)、氯化钙、氢氧化钠、盐酸均为分析纯;标准缓冲溶液(pH =4.00,6.86,9.18)。
98-1 型磁力搅拌器;AR2140 型电子分析天平;FD-1C-55 型真空干燥箱;HH-S 数显恒温水浴锅;Sartorius PB-10 型pH 计;注射器(带7#针头)。
1.2 实验方法
1.2.1 凝胶微球的制备 将羧甲基壳聚糖和海藻酸钠按一定比例混合,配成2%的羧甲基壳聚糖/海藻酸钠混合溶液。分别取一定量的氯化钙和戊二醛,配成5%的氯化钙/戊二醛混合交联剂。在磁力搅拌器不断搅拌下,用10 mL 注射器(7#针头)将羧甲基壳聚糖/海藻酸钠混合溶液逐滴滴加到氯化钙/戊二醛混合交联液中,保鲜膜封口,30 ℃恒温水浴交联1 h(温度影响实验除外),去除交联液,用去离子水洗涤数次,60 ℃下干燥12 h,得凝胶微球。
采用称量法测定凝胶微球的溶胀度[9]。准确称取50 个干燥凝胶微球的质量,记为m0,将凝胶微球置于去离子水中浸泡至溶胀平衡,取出,用滤纸吸干表面多余水分,称量,记为m,溶胀度SR=(m- m0)/m0,平行测定3 次,取平均值。
将10 个凝胶微球并成一排,用直尺量出溶胀前后的长度,计算出溶胀前后单个凝胶微球的粒径,平行测定3 次,取平均值。
1.2.2 凝胶微球的pH、温度敏感性 将干燥的凝胶微球分别置于不同pH 溶液中,通过测定微球的溶胀度考察微球的pH 敏感性。采用类似的方法研究凝胶微球的温度敏感性。
2 结果与讨论
2.1 凝胶微球的制备条件优化
2.1.1 氯化钙和戊二醛的配比 固定羧甲基壳聚糖和海藻酸钠的配比为1∶1(质量比,下同),交联温度30 ℃,氯化钙与戊二醛混合交联液的pH 为6.8,改变氯化钙和戊二醛的配比制备凝胶微球,结果见表1。可以看出,随着氯化钙量的减少,凝胶微球的溶胀度先升高后降低,在氯化钙和戊二醛的配比为1∶1 时,溶胀度最高,此时微球的粒径最小,因此优选氯化钙与戊二醛的配比为1∶1。
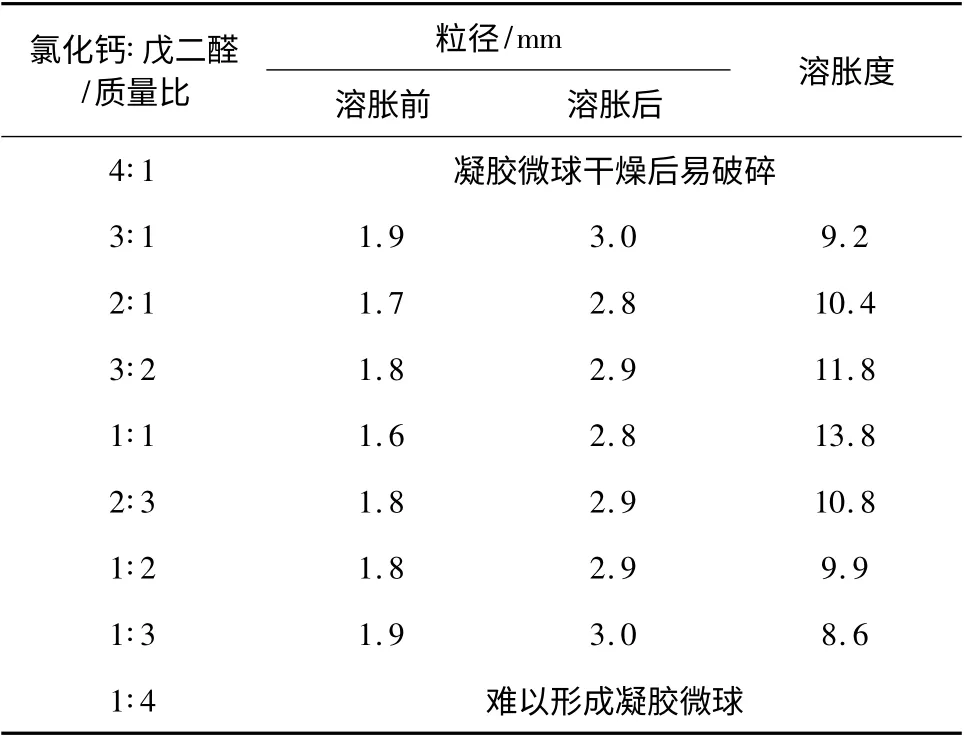
表1 氯化钙和戊二醛的配比对制备凝胶微球的影响Table 1 Effect of the ratio of calcium chloride and glutaraldehyde on the preparation of hydrogel microsphere
2.1.2 羧甲基壳聚糖和海藻酸钠的配比 固定氯化钙与戊二醛的配比为1∶1,交联液的pH 为6.8,交联温度30 ℃,改变羧甲基壳聚糖和海藻酸钠的配比制备凝胶微球,结果见表2。可以看出,随着氯化钙量的减少,凝胶微球的粒径基本保持不变,溶胀度先升高后降低,在羧甲基壳聚糖和海藻酸钠的配比为1∶1时达到最大值14.4,优选羧甲基壳聚糖和海藻酸钠的配比为1∶1。

表2 羧甲基壳聚糖和海藻酸钠的配比对制备凝胶微球的影响Table 2 Effect of the ratio of carboxymethyl chitosan and sodium alginate on the preparation of hydrogel microsphere
2.1.3 pH 的影响 固定交联温度30 ℃,调节2∶1配比的氯化钙与戊二醛混合交联液的pH 分别为1.2,2.0,3.0,4.0,5.0,6.0,6.8,7.4,8.0,9.0,10.0,分别将1∶1 配比的羧甲基壳聚糖/海藻酸钠混合液逐滴滴加到上述混合交联液中,考察pH 对制备凝胶微球的影响,结果见表3。当pH 为1.2 时,难以形成微球,原因可能是海藻酸钠经质子催化快速水解所致。由表3 可知,溶胀度开始随pH 的升高而升高,当pH>6 时,溶胀度基本保持不变。另外,凝胶微球的粒径随pH 的升高而增大,当pH≥8 时,微球粒径较大,综合考虑微球的溶胀度和粒径,优选pH 为6.8 ~7.4。
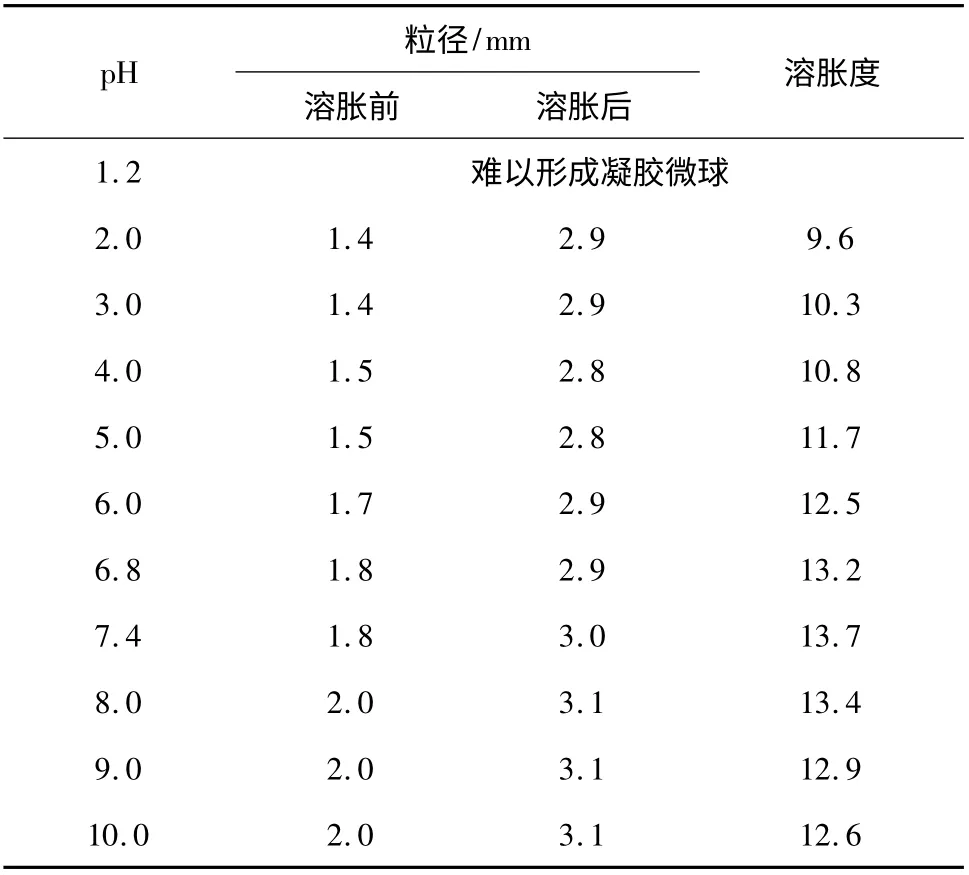
表3 pH 对制备凝胶微球的影响Table 3 Effect of pH on the preparation of hydrogel microsphere
2.1.4 温度的影响 固定羧甲基壳聚糖和海藻酸钠的配比为1∶1,氯化钙与戊二醛的配比为1∶1,交联液的pH 为5.0,改变恒温水浴交联的温度,考察温度对制备凝胶微球的影响,结果见图1。可以看出,溶胀度开始随温度的升高而升高,在温度为35 ~45 ℃时,溶胀度较高,在温度为40 ℃时,溶胀度最大,达12.9,随后溶胀度随温度的升高而降低。另外,随着温度的升高微球硬度也是先增加后降低,在温度为40 ℃时硬度最好,因此优选温度为40 ℃。
综上,当2%的羧甲基壳聚糖/海藻酸钠混合液和5%的戊二醛/氯化钙混合交联剂的质量配比均为1∶1,交联剂的pH 为6.8 ~7.4,交联温度为40 ℃时,成球性好,凝胶微球硬度高,溶胀度最大。
2.2 凝胶微球的pH、温度敏感性
2.2.1 凝胶微球的pH 敏感性 凝胶微球在不同pH溶液中的溶胀度见图2。
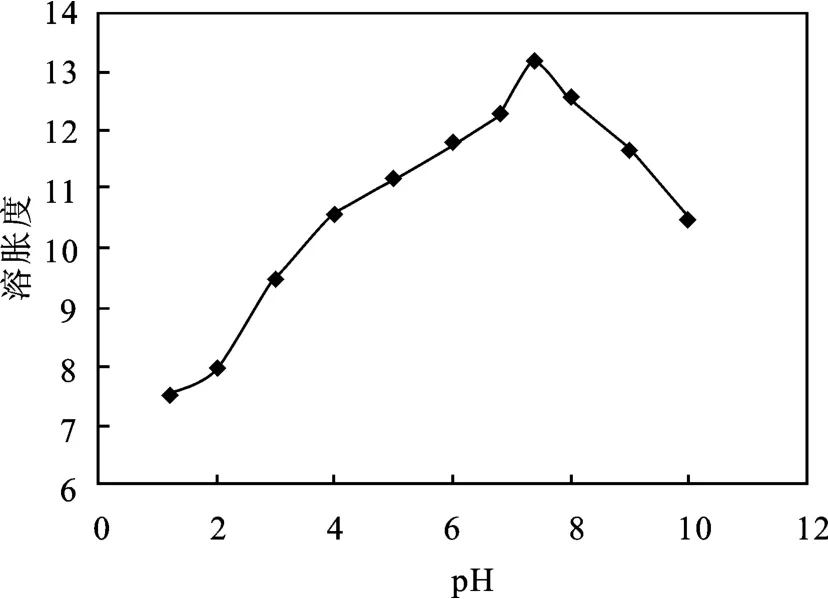
图2 不同pH 溶液对凝胶微球溶胀度的影响Fig.2 Effect of pH on the swelling ratio of hydrogel microsphere
由图2 可知,随着pH 的升高,微球的溶胀度先升高后降低,在pH 为6.8 ~8.0 时溶胀度较大,表现出明显的pH 敏感性。微球在pH 为1.2(胃液环境pH)的酸性环境中溶胀度较小,为7.5,而在pH 为7.4(结肠环境pH)的弱碱性环境中溶胀度最大,达到13.2,表明凝胶微球在胃液环境中具有较好的稳定性,而在结肠位置则具有很好的靶向溶胀选择性,因此有望作为结肠靶向给药的药物载体[10]。
2.2.2 凝胶微球的温度敏感性 凝胶微球在不同恒温水浴温度下的溶胀度见图3。
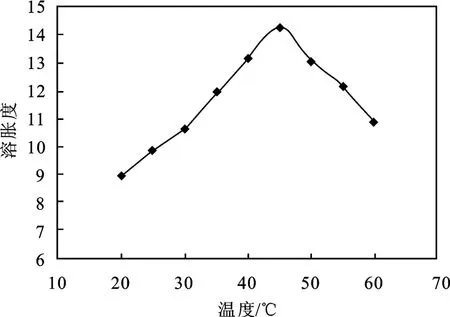
图3 温度对凝胶微球溶胀度的影响Fig.3 Effect of temperature on the swelling ratio of hydrogel microsphere
由图3 可知,随着温度的升高,微球的溶胀度先升高后降低,在温度为45 ℃时溶胀度最大,达到14.3,表现出明显的温度敏感性。当温度低于45 ℃时,溶胀度随温度的升高而升高,原因可能是随着温度的升高,水凝胶网络水合作用增强(水合作用通常为吸热反应)。当温度高于45 ℃时,网络结构中的疏水基团逐渐占据了主导因素,较高的温度促使分子之间的氢键作用遭到破坏,疏水基团聚集,排出一定量的水分子,使溶胀度下降[11]。另外,当温度在35 ~40 ℃时,微球的溶胀度较高(12.0 ~13.2),说明凝胶微球适用于作为温度控释药物的载体。
3 结论
(1)羧甲基壳聚糖/海藻酸钠凝胶微球的适宜制备条件:2%的羧甲基壳聚糖/海藻酸钠混合溶液和5%的戊二醛/氯化钙混合交联剂的质量配比均为1∶1,交联剂的pH 为6.8 ~7.4,交联温度为40 ℃。
(2)凝胶微球的溶胀度随pH 和温度的升高均表现出先升高后降低的趋势,具有明显的pH 和温度敏感性,适用于作为药物控释载体材料。
[1] 赵丽,丁建勋,肖春生,等.聚(L-谷氨酸)微球的制备及其口服药物控释研究[J].化学学报,2015,73:60-65.
[2] Rudzinski W E,Dave A M,Vaishnav U H,et al.Hydrogels as controlled release devices in agriculture[J]. Designed Monomers and Polymers,2002,5(1):39-65.
[3] 赵玉强,张志斌,刘宁,等.智能水凝胶的应用[J].现代化工,2007,27(3):66-69.
[4] Kong X P.Simultaneous determination of degree of deacetylation,degree of substitution and distribution fraction of —COONa in carboxymethyl chitosan by potentiometric titration[J].Carbohydrate Polymers,2012,88(1):336-341.
[5] 李芝,武伟红,刘敏,等.啶虫脒/羧甲基壳聚糖-海藻酸钠凝胶球的制备与控制释放性能研究[J]. 河北农业大学学报,2010,33(3):107-110.
[6] Li X Y,Weng Y H,Kong X Y,et al.A covalently crosslinked polysaccharide hydrogel for potential applications in drug delivery and tissue engineering[J]. Journal of Materials Science-Materials in Medicine,2012,23:2857-2865.
[7] Li X Y,Kong X Y,Zhang Z L,et al.Cytotoxicity and biocompatibility evaluation of N,O-carboxymethyl chitosan/oxidized alginate hydrogel for drug delivery application[J]. International Journal of Biological Macromolecules,2012,50:1299-1305.
[8] Kong X P,Wang J,Wang C J,et al.Basicity,water solubility and intrinsic viscosity of carboxymethyl chitosan as a biofunctional material[J].Advanced Materials Research,2012,531:507-510.
[9] 孙立苹,杜予民,陈凌云,等. 羧甲基壳聚糖水凝胶制备及其在药物控释中的应用[J]. 高分子学报,2004,2:191-195.
[10]张驰宇,贺高红,焉晓明,等.pH 敏感型海藻酸钙多孔凝胶微球的制备及溶胀性能的研究[J]. 功能材料,2010,41(12):2153-2156.
[11]于跃芹,许洋,李延顺.壳聚糖交联温敏性水凝胶的制备与性能[J]. 高分子材料科学与工程,2009,25(7):133-135,139.

