HPLC 法在测定番泻总苷胶囊中番泻苷A B含量中的应用
张 苗,顾 燕
(1.江苏省中医院,江苏南京210029;2.江苏睿博医药有限公司,江苏南京211112)
HPLC 法在测定番泻总苷胶囊中番泻苷A B含量中的应用
张 苗1,顾 燕2
(1.江苏省中医院,江苏南京210029;2.江苏睿博医药有限公司,江苏南京211112)
目的 建立番泻总苷胶囊中番泻苷A、B含量的测定方法。方法 采用高效液相色谱(HPLC)法,以八烷基硅烷键合硅胶柱、乙腈-0.1%三氟乙酸水溶液为流动相梯度洗脱,检测波长340nm。结果 番泻苷A在0.2104~1.0520μg、番泻苷B在0.225 0~1.125 0 μg呈良好的线性关系,平均回收率分别为99.51%(RSD=1.30%)和99.07%(RSD=0.69%)。结论 该方法简单快捷、结果可靠,可作为番泻总苷胶囊质量控制的方法。
番泻叶(中药); 胶囊; 番泻甙/分析; 色谱法,高压液相
番泻叶为豆科植物狭叶番泻或尖叶番泻的干燥小叶,具有泻热行滞、通便、利水之功效。用于热结积滞、便秘腹痛、水肿胀满[1]。番泻叶的应用历史悠久,现已成为全世界范围内应用最广的导泻剂;药理试验表明,番泻叶导泻作用的活性成分主要为蒽醌类的番泻苷,因而控制番泻苷的含量可以确保制剂的药效[2-3]。番泻总苷胶囊为番泻叶经过提取加工而成的富含番泻苷活性成分的制剂,本文拟通过试验确立番泻苷A、B含量的测定方法。
1 材料与方法
1.1 仪器与试剂 Agilent 1100高效液相色谱仪(HPLC仪),DAD检测器,番泻苷A(含量大于或等于97.0%,SIGMA公司,批号:112607015204229),番泻苷B(含量大于或等于96.5%,SIGMA公司,批号:110156210605370)等。乙腈为色谱纯,三氟乙酸为化学纯。
1.2 方法
1.2.1 色谱条件与系统适用性试验 以八烷基硅烷键合硅胶为填充剂;0.1%三氟乙酸水溶液-乙腈系统按表1梯度洗脱。检测波长340 nm;流速1 mL/min;柱温25℃。理论塔板数按番泻苷B峰计算应不低于4 000,番泻苷A、B及与其他组分的分离度应不低于1.5。
1.2.2 对照品、供试品及阴性溶液的制备
1.2.2.1 对照品溶液的制备 精密称取番泻苷A对照品适量,以30%乙醇制成50 μg/mL的溶液;同法制备番泻苷B对照品溶液,质量浓度为70 μg/mL。
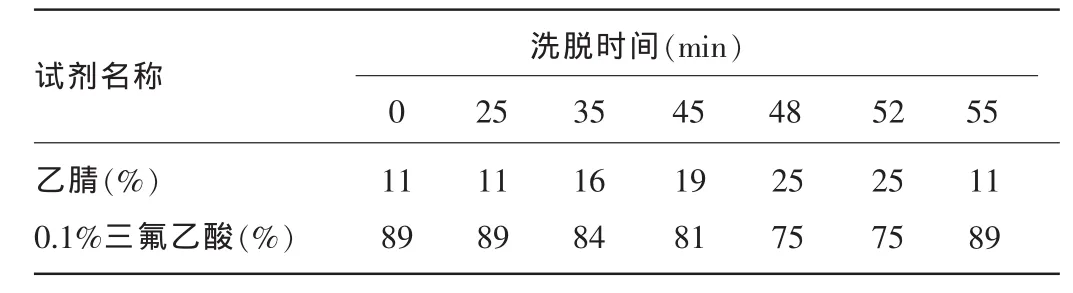
表1 梯度洗脱表
1.2.2.2 供试品溶液的制备 取胶囊10粒,倾倒出内容物,混合均匀,取内容物0.02 g,精密称定,置25 mL容量瓶中,加入30%乙醇20 mL,超声处理30 min,放冷,加30%乙醇至刻度,混匀,滤过,取续滤液,即为供试品溶液。
1.2.2.3 阴性对照液 称取辅料0.015 g(按处方比例),精密称定,置25 mL容量瓶中,与供试品溶液同法制取,作为阴性对照溶液。
1.2.3 测定法 分别精密吸取上述溶液各10 μL,注入HPLC仪,测定,即得。
1.3 方法学验证
1.3.1 专属性试验 取阴性对照液、对照品溶液及供试品溶液各10 μL,分别注入HPLC仪,测定,考察方法的专属性。
1.3.2 线性关系考察 (1)精密称取番泻苷A对照品10.52 mg于100 mL容量瓶中,以30%乙醇溶解定容至刻度,作为番泻苷A储备溶液;分别精密移取该溶液2、4、6、8、10 mL,置10 mL容量瓶中,30%乙醇溶解定容至刻度,摇匀,制成不同质量浓度的一系列溶液,各进样10 μL,2针,考察线性关系。(2)精密称取番泻苷B对照品11.25 mg,同法制得对照品番泻苷B储备溶液。与番泻苷A储备液同法稀释,制成不同质量浓度的一系列溶液,各进样10 μL,2针,考察线性关系。
1.3.3 精密度试验 按照1.2.2.2项方法制备供试品溶液,连续进样6次,分别以番泻苷A、B峰面积计算RSD。
1.3.4 稳定性试验 按1.2.2.2项方法制备供试品溶液,在第0、2、4、6、8、10、12 h各进样10 μL,计算峰面积的RSD,考察溶液稳定性。
1.3.5 重现性试验 按1.2.2.2项方法测定,平行测定6次,考察重现性。
1.3.6 加样回收率试验 精密称取已知含量样品(番泻苷A 2.87%,番泻苷B 10.02%)0.01 g,平行9份,精密称定,置25 mL容量瓶中,另取质量浓度为76.05 μg/mL的番泻苷A溶液、质量浓度为99.85 μg/mL番泻苷B溶液,分别按样品含量的80%、100%、120%精密加入番泻苷A、B对照品溶液,用30%乙醇溶解并定容至刻度,每个质量浓度等级3份,按1.2项方法测定,计算番泻苷A、B的回收率。
1.3.7 样品测定 取3批样品 (批号:131201、131202、131203),按含量测定方法进行检测,计算番泻苷A、B的含量。
2 结 果
2.1 专属性试验 专属性试验结果表明,阴性制剂在番泻苷A、B的保留时间处无干扰。见图1~4。
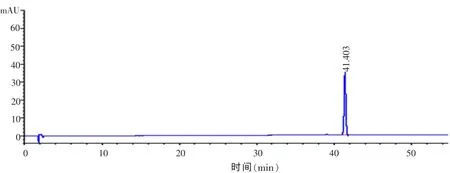
图1 番泻苷A对照品溶液
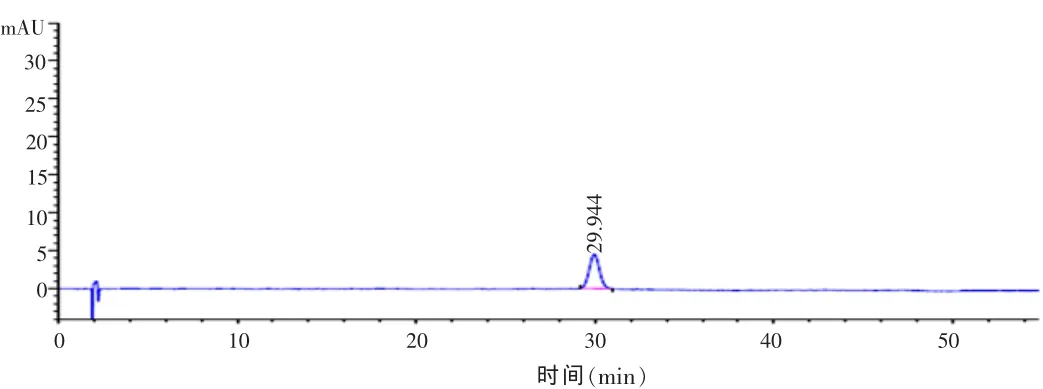
图2 番泻苷B对照品溶液
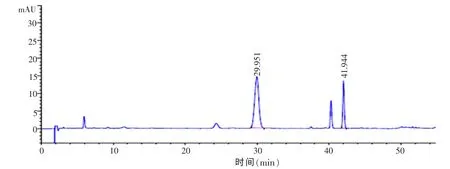
图3 番泻总苷胶囊供试品
图4 番泻总苷胶囊阴性制剂
2.2 线性关系考察 线性关系考察结果发现,番泻苷A在0.210 4~1.052 0 μg、番泻苷B在0.225 0~1.125 0 μg呈良好的线性关系。见表2、3。
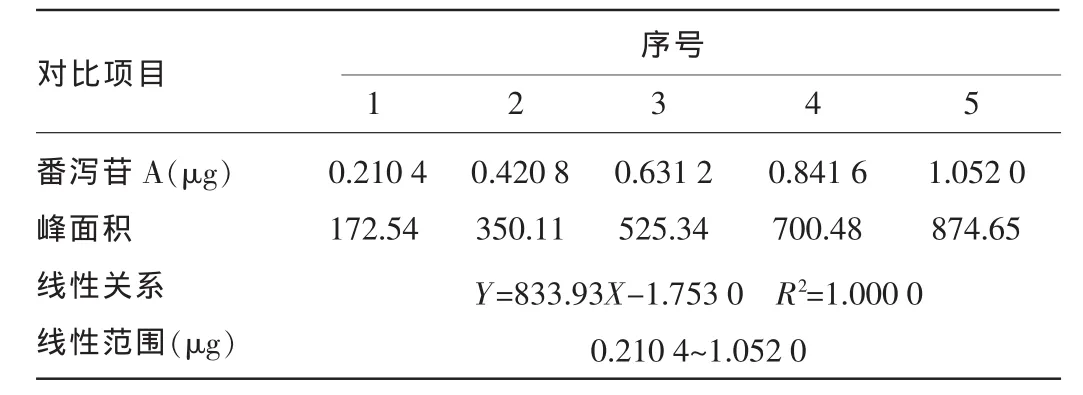
表2 番泻苷A线性关系测定结果
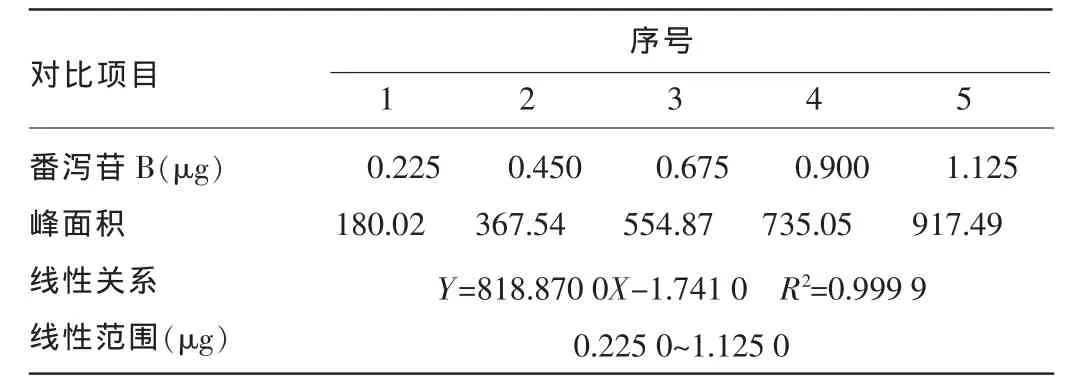
表3 番泻苷B线性关系测定结果
2.3 精密度试验 连续进样6针,结果番泻苷A峰面积的RSD为0.24%,番泻苷B峰面积的RSD为0.14%,表明本方法精密度良好。见表4。
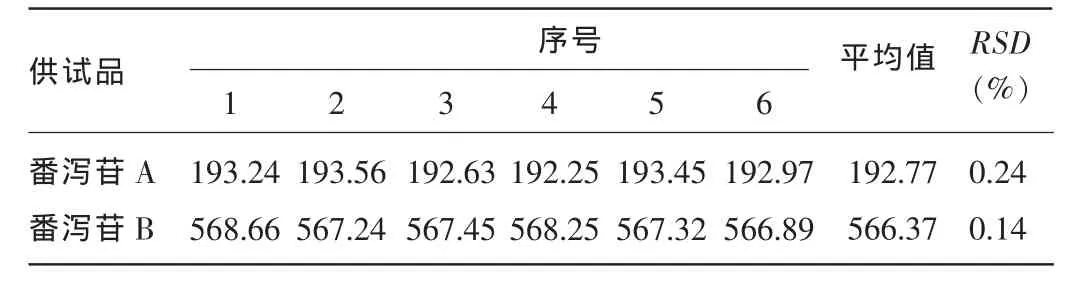
表4 精密度试验结果
2.4 稳定性试验 12 h内番泻苷A、B的峰面积RSD分别为0.22%、0.16%,表明供试品溶液在12 h内稳定。见表5。
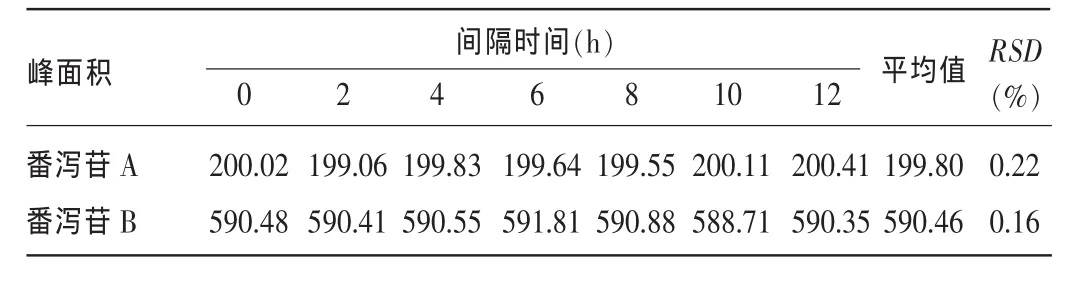
表5 稳定性试验结果
2.5 重现性试验 平行测定6次,结果番泻苷A平均含量为2.87%,RSD为1.01%;番泻苷B平均含量为10.02%,RSD为1.02%,表明该含量测定方法重现性良好。见表6。
2.6 加样回收试验 番泻苷A回收率为97.9%~101.9%,平均回收率为99.51%,RSD为1.30%;番泻苷B回收率为98.1%~100.3%,平均回收率为99.07%,RSD为0.69%。表明该含量测定方法的回收率较好。见表7、8。
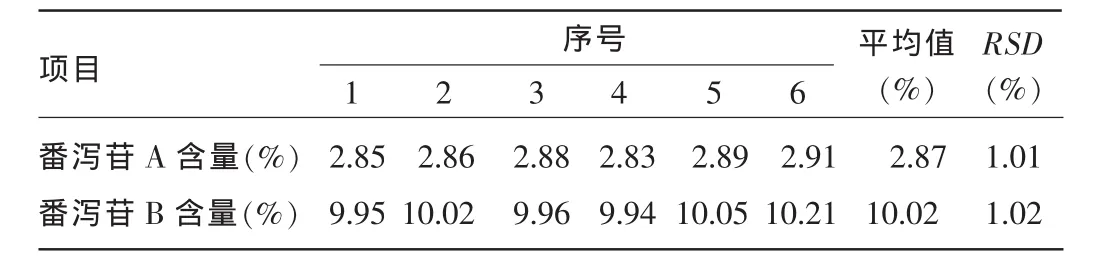
表6 重复性试验结果
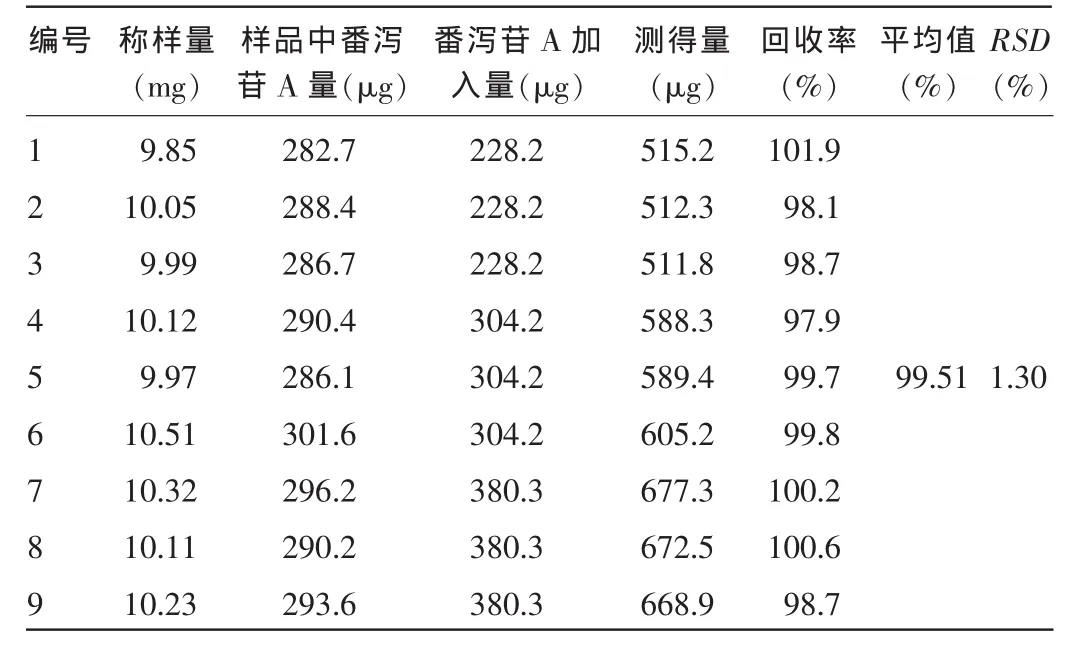
表7 番泻苷A回收率试验结果
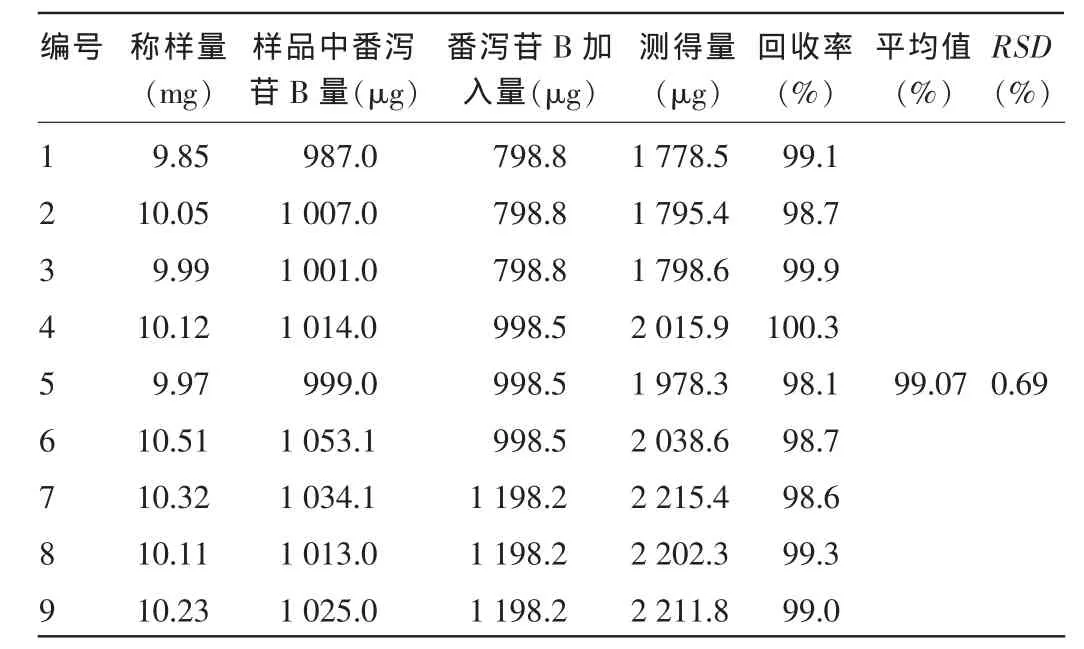
表8 番泻苷B回收率试验结果
2.7 样品含量测定 3批样品的番泻苷A含量均在2.50%以上,番泻苷B含量在9.50%以上,可作为制定质量标准的参考。见表9。
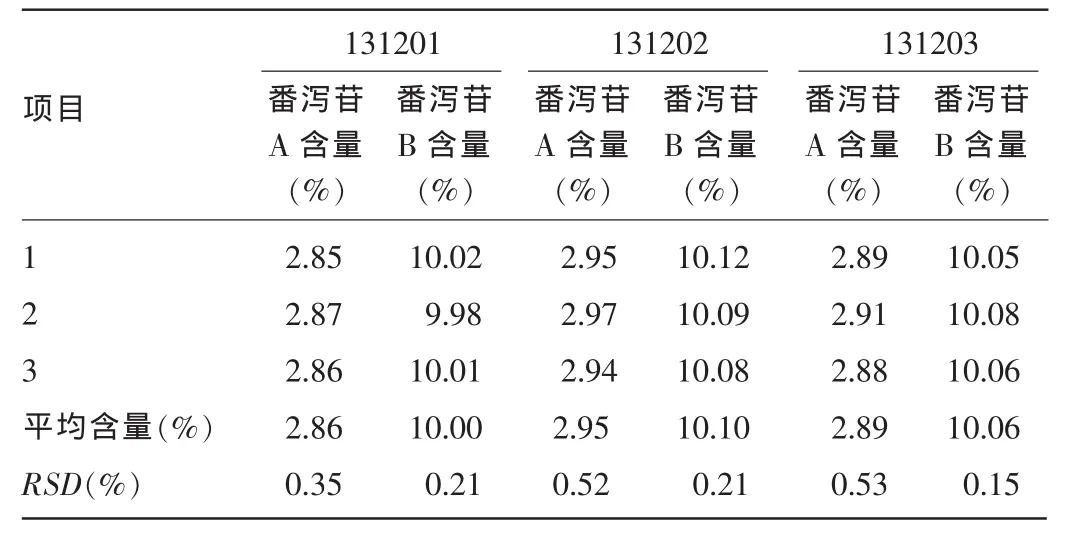
表9 制剂中番泻苷A、B含量测定结果
3 讨 论
番泻叶含蒽醌及其衍生物、多糖及挥发油等成分,主要药理作用的活性成分为蒽醌类。番泻苷A、B、C、D、G(番泻苷A的手型异构体)等蒽醌类成分在体内通过不同途径转变成大黄酸蒽酮而发挥作用[4]。通过控制番泻苷A、B的含量可确保番泻总苷胶囊的临床作用。
番泻苷胶囊为番泻叶提取物加辅料制备而成,番泻苷提取物中番泻苷A、B的含量超过50%,也是制剂中的主要成分,因而选择番泻苷A、B的总含量作为控制指标。
有文献报道,番泻苷含量测定可采用比色法[5]、电泳法[6]、紫外分光光度法[7]、HPLC法[8-10]等,其中HPLC法为近年来常用的方法。该法采用乙腈(5 mmol/L)四庚基溴乙胺的醋酸-醋酸钠缓冲液(35∶65,pH 5.0)混合溶液作为流动相,但配置麻烦。何伟等[11]采用乙腈-0.1%三氟乙酸水溶液梯度的方法测定了番泻叶提取物中的番泻苷A、B含量;邬秋萍等[12]采用乙腈-1%冰醋酸溶液梯度的方法测定番泻叶中5种主要化学成分的含量。本研究选择乙腈-0.1%三氟乙酸作为流动相,并摸索到样品的处理方法及梯度程序。
有研究采用30%乙醇溶解番泻苷B,番泻苷A及样品均用40%乙醇作为稀释液。为方便操作,尝试采用30%乙醇溶解番泻苷A及制剂,并与40%的乙醇进行比较,未见明显差异,故稀释液均采用30%乙醇。
番泻苷易被光、热、强酸等破坏,因而在样品处理过程中对温度进行了控制,结果发现,在25℃既能使有效成分充分提取,又不会遭到破坏。本研究采用的方法稳定、结果可靠,可作为制剂质量控制的方法。
[1]国家药典委员会.中华人民共和国药典2010年版(一部)[M].北京:中国医药科技出版社,2010:326-328.
[2]田莉,刘圣,陈象清,等.番泻叶导泻作用的药理学研究概况[J].基层中药杂志,2004,14(1):53-55.
[3]高晔,朱艳华,贺微.番泻叶的药用研究进展[J].中医药学刊,2006,24(11):2145-2146.
[4]杨建平,刘晓燕,曾正.番泻叶的临床药理作用以及化学成分的研究进展[J].药物与人,2014,27(A3):22.
[5]裴晓丽,杜康平,张小山,等.比色法测定益寿通口服液番泻甙B含量[J].中医药研究,1997,13(4):14.
[6]石上梅,张庆生,王宝琴.高效毛细管电泳法测定番泻叶中番泻苷A的含量[J].药物分析杂志,2002,22(1):25-26.
[7]杨素玲,杜文孝,刘新华,等.紫外分光光度法测定通便灵胶囊番泻苷B的含量[J].现代中医药,2004,24(1):65-66.
[8]郑志华,祝晨蔯.HPLC测定大黄提取工艺产物番泻苷A的含量[J].中药材,2004,27(12):950-951.
[9]吕曙华,吕归宝.HPLC法测定番泻叶中番泻苷A及番泻苷B的含量[J].中国药品标准,2002,3(5):48-50.
[10]何伟,张朝波,严军,等.HPLC法测定番泻叶中番泻苷A、番泻苷B的含量[J].海峡药学,2008,20(9):48-51.
[11]何伟,张现涛,严军,等.HPLC测定番泻总苷提取物中番泻苷A、番泻苷B的含量[J].中成药,2008,30(8):1182-1184.
[12]邬秋萍,王祝举,唐力英,等.HPLC测定番泻叶中5种主要化学成分的含量[J].中国中药杂志,2008,33(4):363-365.
Application of HPLC method for determination of sennoside A and B contents in Senna Total Glycosides Capsules
Zhang Miao1,Gu Yan2
(1.Jiangsu Provincial Hospital of Traditional Chinese Medicine,Nanjing,Jiangsu 210029,China;2.Jiansu Ruibo Pharmaceutical Co.,Ltd.,Nanjing,Jiangsu 211112,China)
Objective To establish a method for the determination of sennoside A and B contents in Senna Total Glycosides Capsule.Methods The high performance liquid chromatography(HPLC)method was adopted,the gradient elution was performed with octadecyl silane bonded silica gel column,the mobile phase of acetonitrile-0.1%trifluoroacetic acid aqueous solution and the detection wavelength of 340 nm.Results Sennoside A in the range of 0.210 4-1.052 0 μg and sennoside B in the range of 0.225 0-1.125 0 μg had good linear relationship.The average recovery rates were 99.51%(RSD=1.30%)for sennoside A and 99.07%(RSD=0.69%)for sennoside B.Conclusion The established method is simple,quick and reliable,which can be used as a quality control method for Senna Total Glycosides Capsules.
Cassiae angustifolia(TCD); Capsules; Sennoside/analysis; Chromatography,high pressure liquid
10.3969/j.issn.1009-5519.2015.21.011
A
1009-5519(2015)21-3235-03
2015-07-15)
张苗(1987-),女,江苏徐州人,主要从事药品调配工作;E-mail:zm.1987.86@163.com。

