焙烧态类水滑石/HZSM-5双功能催化剂的制备及催化CO2加氢合成二甲醚
常琴琴, 赵 博, 杨 萌, 刘 艳, 刘恩周, 樊 君
(西北大学 化工学院, 陕西 西安 710069)
焙烧态类水滑石/HZSM-5双功能催化剂的制备及催化CO2加氢合成二甲醚
常琴琴, 赵 博, 杨 萌, 刘 艳, 刘恩周, 樊 君
(西北大学 化工学院, 陕西 西安 710069)
采用并流共沉淀法制备了不同ZrO2含量的CuO-ZnO-Al2O3-ZrO2类水滑石前体,焙烧后与HZSM-5分子筛物理混合得到CuO-ZnO-Al2O3-ZrO2/HZSM-5双功能催化剂,采用XRD、N2物理吸附、H2-TPR等技术对催化剂的物相、结构特征及还原性进行了表征,考察了催化剂对CO2加氢直接合成二甲醚(DME)反应的催化性能。实验结果表明,所有前体试样均具有结晶相为Cu3Zn3Al2(OH)16·4H2O的水滑石结构,ZrO2的加入改善了催化剂的还原性和活性,DME合成速率主要取决于甲醇的合成速率。在533 K、3.0 MPa、n(H2):n(CO2)=3:1、GHSV=2 400 h-1的反应条件下,当n(ZrO2):n(Al2O3+ZrO2)=0.10时,催化剂的反应性能最佳,CO2转化率达25.87%,DME选择性达48.15%;反应30 h后,催化剂仍表现出较高的活性及稳定性。
类水滑石前体;HZSM-5分子筛;双功能催化剂;锆助剂;二氧化碳加氢;二甲醚
carbon dioxide hydrogenation; dimethyl ether
随着化学工业的发展,CO2排放量增加导致全球气候变暖问题日益严重[1]。目前,采用CO2加氢制二甲醚(DME)被认为是CO2转化利用最具前景的途径之一。DME不仅是重要的有机化工原料,也是很有前途的清洁燃料。因此CO2加氢直接合成DME兼有能源、化工和环保等多重意义[2]。
近年来,有关CO2直接加氢合成DME的报道主要集中在合成甲醇CuO-ZnO-Al2O3催化剂的研究方面[3-6]。前体的结构影响催化剂的比表面积、平均晶粒和活性等,因此通过改变制备条件来改变前体的结构,可提高催化剂的活性。Busca等[7]报道了类水滑石前体焙烧后得到的Co-Zn-Al和Co-Ni-Zn-Al催化剂具有较好的分散性和乙醇重整活性。Venugopal等[8-9]通过共沉淀法制备了以类水滑石为前体的Cu-Zn-Al催化剂,并成功应用于甲醇合成反应中。类水滑石的化学通式为[M(Ⅱ)1-xM(Ⅲ)x(OH)2-][An-]x/n·mH2O,其中,M(Ⅱ)和M(Ⅲ)分别为二价和三价金属离子,An-为层间阴离子。类水滑石在673~773 K下焙烧后得到的复合金属氧化物具有层间阴离子可交换性、热稳定性、组分可调控性、大比表面积和较强碱性等优点[2,10-11]。为进一步改善CuO-ZnO-Al2O3催化剂的性能,还可尝试添加其他助剂。
本工作采用并流共沉淀法制备了一系列不同ZrO2含量的CuO-ZnO-Al2O3-ZrO2类水滑石前体,焙烧后与HZSM-5分子筛[12]物理混合得到CuO-ZnO-Al2O3-ZrO2/HZSM-5双功能催化剂,并应用于CO2加氢直接合成DME反应。探讨了ZrO2含量对催化剂的结构和物理化学性质的影响及其与催化性能之间的关系。
1 实验部分
1.1 催化剂的制备
将Cu(NO3)2·3H2O,Zn(NO3)2·6H2O,Al(NO3)3·9H2O,ZrO(NO3)4·2H2O按一定比例配成一定浓度的混合盐溶液,并将NaOH和Na2CO3配成混合碱溶液;在333 K、搅拌条件下,将混合盐溶液和混合碱溶液同时滴加到沉淀槽中,pH=10±0.5;沉淀结束后继续搅拌老化15 h,洗涤、过滤,于353 K下干燥12 h,773 K下焙烧4 h,得到不同ZrO2含量的甲醇合成催化剂CuO-ZnO-Al2O3-ZrO2[13],记作HTlc-x(x=n(ZrO2):n(Al2O3+ZrO2),x=0, 0.05, 0.10, 0.30, 0.50)。将HTlc-x与HZSM-5分子筛(硅铝比为25)按质量比2:1充分混合,研磨压片、破碎至60~80目,所得催化剂记作HTlc-x/HZ。
1.2 催化剂的表征
催化剂的物相结构采用Shimadzu公司XRD-6000型X射线粉末衍射仪分析,CuKα辐射,管电压40 kV,管电流40 mA。比表面积和孔分布采用Quantachrome公司NOVA2000e型多点氮吸附仪测量,测试前试样在473 K下真空处理4 h。H2-TPR测试在自组装程序升温化学吸附装置上进行,通入H2,待基线平稳后,以10 K/min的速率从323 K升至673 K进行测试。
1.3 催化剂活性的评价
催化剂活性的评价在管式固定床反应装置上进行,催化剂用量1.0 g。反应前催化剂在纯H2气氛中于603 K下还原3 h,降至反应温度,切换为原料气升压进行反应。反应物和产物采用FULI公司9790Ⅱ型气相色谱仪进行在线分析,TCD检测,Porapak-Q填充柱。根据反应尾气中各组分的含量,以碳原子数计算CO2转化率及DME选择性。
2 结果与讨论
2.1 催化剂的晶相结构
HTlc-x试样的XRD谱图见图1。从图1可见,所有HTlc-x试样在2θ=11.780°,23.713°,34.728°,39.365°,61.569°处均出现结晶相为Cu3Zn3Al2(OH)16·4H2O的水滑石结构的特征衍射峰(ICDD:37-0629),未发现其他结晶相的衍射峰。随ZrO2含量的增加,水滑石的特征衍射峰强度不断减弱,结晶度下降。表明水滑石前体层与层之间的作用力逐渐减弱,且随Al含量的减小,形成了大量的无定形物质。
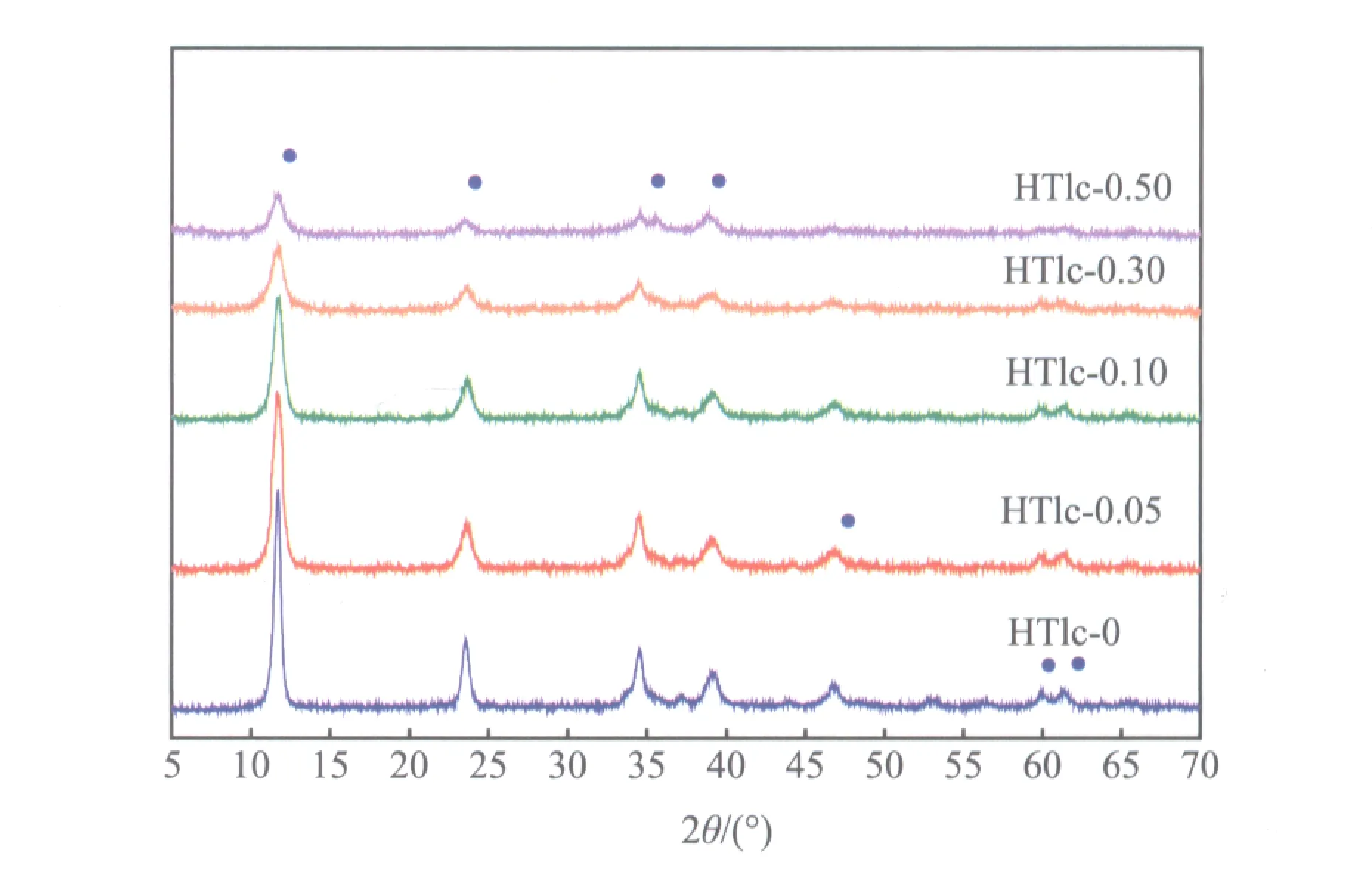
图1 HTLc-x试样的XRD谱图
焙烧后HTlc-x试样和HTlc-x/HZ试样的XRD谱图见图2。

图2 焙烧后HTlc-x试样(a)和HTlc-x/HZ试样(b)的XRD谱图
由图2a可看出,焙烧后试样的类水滑石结构被破坏,生成金属氧化物。由图2b可看出,所有HTlc-x/HZ试样均在2θ=8.000°,8.901°,23.141°,23.960°,24.439°处出现HZSM-5分子筛的特征衍射峰(ICDD:37-0359);在2θ=35.561°,38.857°处出现较强的CuO特征衍射峰(ICDD:65-2309),且随Zr4+含量的增加,CuO的特征衍射峰先变宽后变窄,说明适宜含量ZrO2的加入提高了CuO的分散性;在2θ=31.771°,34.419°,36.225°处出现较弱的ZnO的特征衍射峰(ICDD:65-5973),且2θ=35.561°处CuO的特征衍射峰与2θ=36.255°处ZnO的特征衍射峰相互重叠,表明CuO较好地分散于ZnO晶格中,形成Cu-Zn固溶体,协同作用较好。当x=0~0.30时,HTlc-x/HZ试样的XRD谱图中均未出现ZrO2的特征衍射峰,而主要出现CuO和ZnO的特征衍射峰,说明ZrO2极有可能是以无定形或微晶状态存在,较好地分散在HTlc-x中;当x=0.50时,即HTlc-0.50/HZ试样,在2θ=31.781°,50.358°处出现单斜晶相ZrO2的特征衍射峰(ICDD:49-1642),且CuO的特征衍射峰最窄,这表明加入过量的ZrO2使CuO的结晶度增大、分散性变差、颗粒聚集,这可能造成催化剂的活性下降。
2.2 催化剂的比表面积
HTlc-x/HZ试样的物性数据见表1。从表1可看出,当x逐渐增大时,试样的比表面积、孔体积和平均孔径均呈先增大后减小的趋势,当x=0.10时达到最大值。
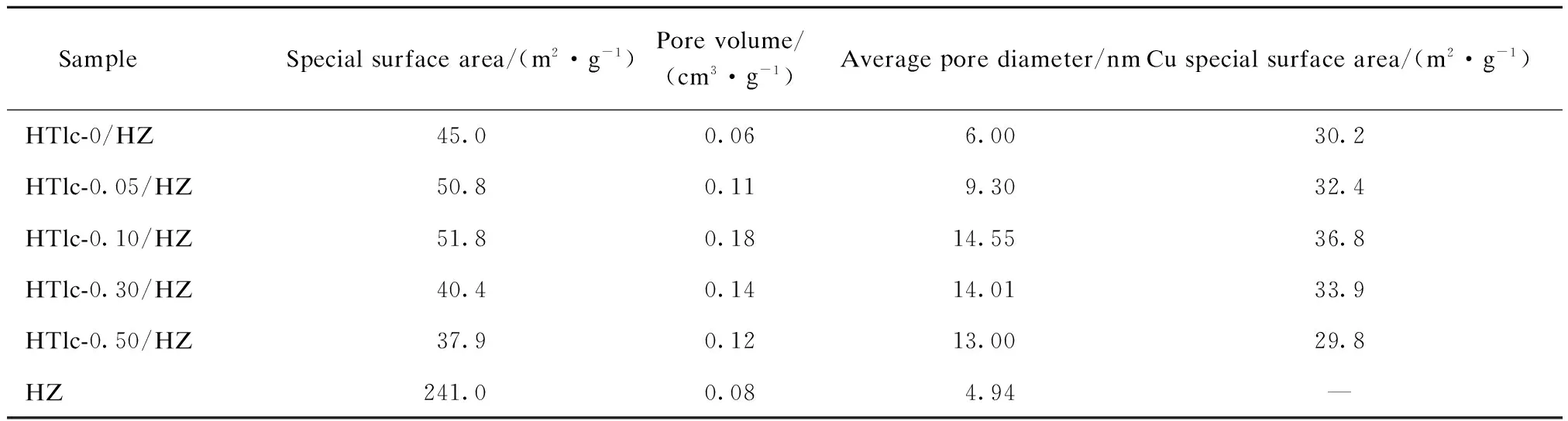
表1 HTlc-x/HZ试样的物性数据
2.3 催化剂的还原性
HTlc-x/HZ试样的H2-TPR曲线见图3。由图3可见,所有试样均在473~573 K之间出现一个主要的低温还原峰,可归属为CuO—Cu或CuO—Cu2O—Cu的还原峰[14]。当x从0增至0.10时,试样的还原峰逐渐向低温方向偏移,HTlc-0.10/HZ试样的还原峰温度最低,为473 K。这主要是由于随ZrO2含量的增加,CuO与ZnO之间的相互作用力增强,抑制了Cu晶粒的增长,更多的Cu物种暴露在催化剂表面,分散度提高,促进了催化剂的还原[15-16]。HTlc-0.30/HZ和HTlc-0.50/HZ试样分别出现了一个主峰和一个微弱的肩峰,可分别归属为高度分散的CuO和体相CuO的还原峰,且HTlc-0.50/HZ试样的还原峰温度远高于其他试样的还原峰温度,这表明引入过量的ZrO2减弱了CuO的还原性。而适量ZrO2的引入,可促进CuO与ZnO之间的协同作用,降低催化剂的还原温度,提高Cu物种的分散度,从而提高催化剂的活性。
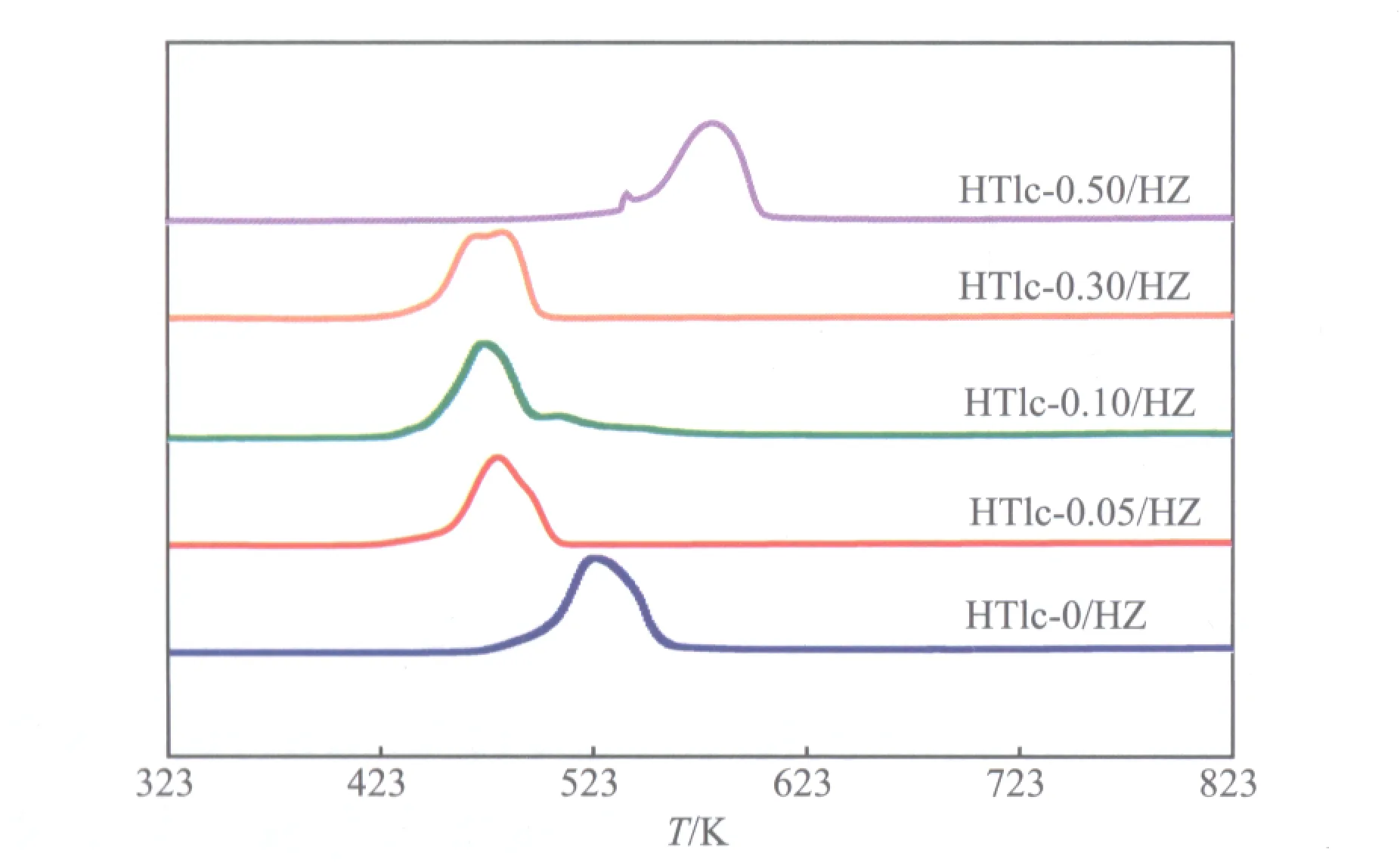
图3 HTlc-x/HZ试样的H2-TPR曲线
2.4 催化剂的活性
CO2加氢合成DME主要包含3个反应:CO2加氢合成甲醇、逆水汽变换和甲醇脱水反应[3,17]。
CO2+3H2→CH3OH +H2O
(1)
CO2+H2→CO +H2O
(2)
2CH3OH→CH3OCH3+H2O
(3)
甲醇和DME是目标产物,而CO和H2O是主要副产物。逆水汽变换反应为吸热反应,反应温度越高越有利于CO2的转化;而CO2加氢合成甲醇和甲醇脱水反应为放热反应,高温时受热力学的控制反应受到抑制。
HTlc-x/HZ催化剂上CO2加氢合成DME反应的转化率和选择性与反应温度的关系见图4。由图4可看出,CO2转化率随反应温度的升高先逐渐增大后趋于平缓;DME选择性随反应温度的升高先增大后减小,在533 K时达到最大值。这主要是由于在低温下CO2转化为甲醇的反应主要受动力学控制,高温下受到热力学的限制以及积碳的形成[18-19]、Cu晶粒的烧结和增长以及大量水的生成,导致合成甲醇催化剂失活[20]。
从图4还可看出,不同ZrO2含量的HTlc-x/HZ催化剂上,CO2转化率和DME选择性随反应温度的变化趋势一致。其中,HTlc-0.10/HZ催化剂的活性最高,当反应温度为533 K时,CO2转化率为25.87%,DME选择性为48.15%。这是因为HTlc-0.10/HZ催化剂的比表面积大、分散度好,从而具有良好的活性。添加ZrO2能促进Cu比表面积的增大,稳定Cu粒子,从而提高催化剂的活性[2,21];但催化剂活性的提高与ZrO2的加入量并不成正比,ZrO2含量过高将导致活性组分的分散性变差,一种组分覆盖另一种组分[22]。根据催化剂的表征结果可知,大的Cu比表面积、低的还原峰温度、高的Cu物种分散性有利于CO2加氢合成DME反应。
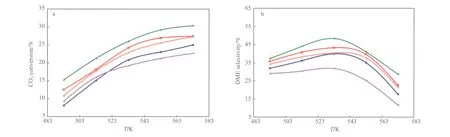
图4 HTlc-x/HZ催化剂上CO2转化率(a)和DME选择性(b)与反应温度的关系
2.5 热力学和动力学分析
HTlc-0.30/HZ催化剂上反应温度对CO2加氢合成DME反应的热力学与动力学的影响见图5。其中,β为实验平衡常数(根据转化率和选择性数据计算所得)与标准平衡常数(见表2)[23-24]之比。由图5可见,低于533 K时,随反应温度的升高,β1和β3均增大,表明低温下甲醇合成反应和逆水汽变换反应均为动力学控制;其中,β1的增幅远大于β3,表明低温下甲醇合成反应比逆水汽变换反应更有利于进行。但随反应温度的进一步升高,β1和β3的增幅相近,说明反应速率不仅受到动力学的控制还受到热力学的控制。此外,随反应温度的变化,β2变化不大,表明甲醇在酸性组分HZSM-5分子筛上可快速脱水使反应有效达到平衡[25],因此合成DME的速率主要取决于甲醇合成步骤,这与其他研究者的结论[26-27]一致。基于以上实验结果,HTlc-x/HZ催化剂在533 K时的活性最高。
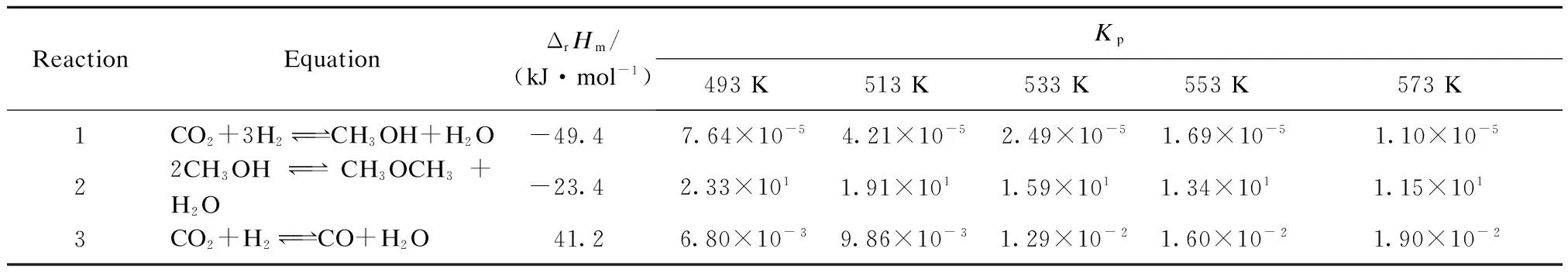
表2 HTlc-0.30/HZ催化剂上CO2加氢合成DME的主要反应热力学数据
ΔrHm:molar enthalpy of reaction;Kp:standard equilibrium constant.
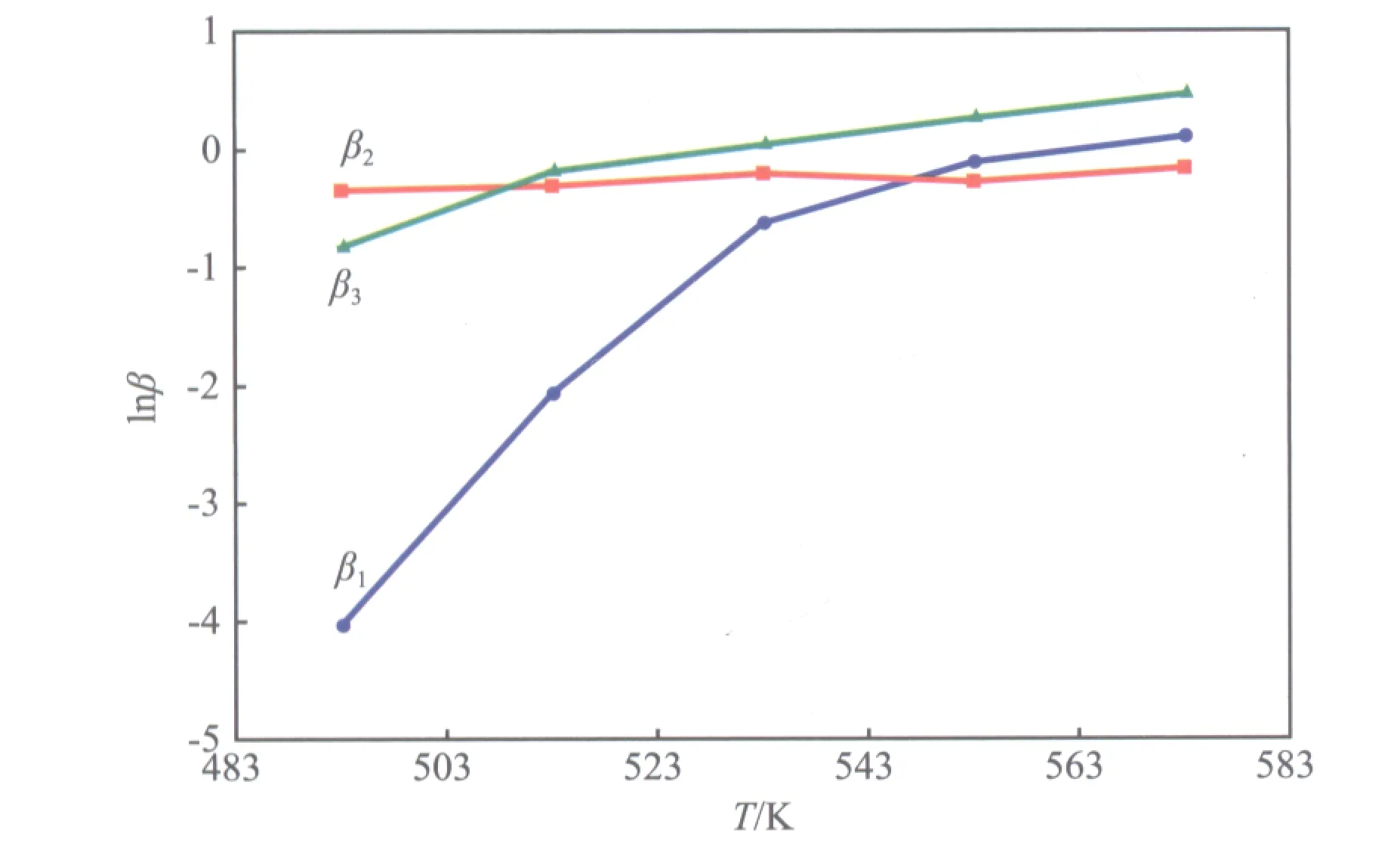
图5 HTlc-0.30/HZ催化剂上反应温度对CO2加氢合成DME反应的热力学与动力学的影响
2.6 催化剂的稳定性
选取HTlc-0.10/HZ催化剂进行稳定性实验,实验结果见图6。
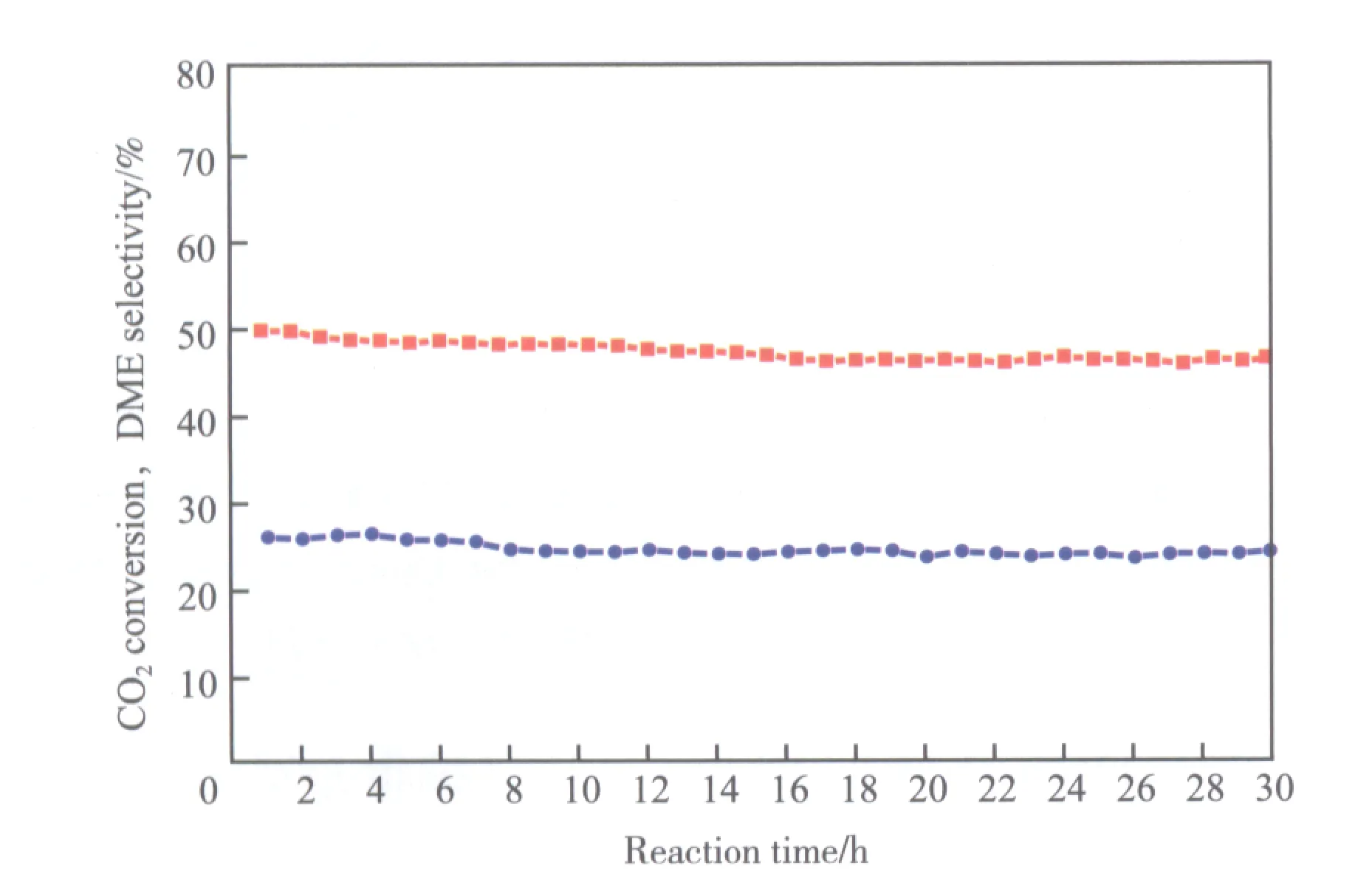
图6 HTlc-0.10/HZ催化剂的稳定性
由图6可看出,在反应30 h内CO2转化率和DME选择性几乎没有变化,催化剂表现出高的活性及稳定性。这表明在反应过程中催化剂表面不发生或很少发生积碳的形成和烧结,不会消弱CuO,ZnO,Al2O3间的相互作用[28]。这是由于类水滑石的结构及适量的ZrO2稳定了低价态反应活性中心,从而提高了催化剂的稳定性。
3 结论
1)采用并流共沉淀法制备出不同ZrO2含量的CuO-ZnO-Al2O3-ZrO2类水滑石前体,经773 K焙烧后与HZSM-5分子筛物理混合得到HTlc-x/HZ双功能催化剂,该催化剂对CO2加氢合成DME反应具有较好的催化性能。
2) 加入适量ZrO2可增大HTlc-x/HZSM-5催化剂的比表面积,并能增强CuO与ZnO的协同作用,提高CuO的分散性,降低CuO的还原温度,从而改善催化剂对CO2加氢合成DME反应的催化性能。
3)热力学和动力学分析结果表明,DME合成速率主要取决于甲醇的合成速率,反应温度为533 K时,HTlc-x/HZSM-5催化剂的活性最高。
4) 不同ZrO2含量的催化剂上,CO2转化率和DME选择性随反应温度的变化趋势一致。在533 K、3.0 MPa、n(H2):n(CO2)=3:1、GHSV=2 400 h-1的反应条件下,HTlc-0.10/HZ催化剂的活性最高,CO2转化率为25.87%,DME选择性为48.15%。
[1] 高健, 苗成霞, 汪靖伦, 等. 二氧化碳资源化利用的研究进展[J]. 石油化工, 2010, 39(5): 465-475.
[2] Flores J H, Peixoto D P B, Appel L G, et al. The Influence of Different Methanol Synthesis Catalysts on Direct Synthesis of DME from Syngas[J].CatalToday, 2011, 172(1): 218-225.
[3] Bonura G, Cordaro M, Spadaro L, et al. Hybrid Cu-ZnO-ZrO2/H-ZSM- 5 System for the Direct Synthesis of DME by CO2Hydrogenation[J].ApplCatal,B, 2013, 140/141(8/9):16-24.
[4] Arcoumanis C, Bae C, Crookes R, et al. The Potential of Dime- thyl Ether(DME) as an Alternative Fuel for Compression-Ignition Engines: A Review[J].Fuel, 2008, 87(7):1014-1030.
[5] Jia Guangxin, Tan Yisheng, Han Yizhou. A Comparative Study on the Thermodynamics of Dimethyl Ether Synthesis from CO Hydrogenation and CO2Hydrogenation[J].IndEngChemRes, 2006, 45(3):1152-1159.
[6] Khoshbin R, Haghighi M, Asgari N. Direct Synthesis of Dimethyl Ether on the Admixed Nanocatalysts of CuO-ZnO-Al2O3and HNO3-Modified Clinoptilolite at High Pressures: Surface Properties and Catalytic Performance[J].MaterResBull, 2013, 48(2): 767-777.
[7] Busca G, Costantino U, Montanari T, et al. Nickel Versus Cobalt Catalysts for Hydrogen Production by Ethanol Steam Reforming: Ni-Co-Zn-Al Catalysts from Hydrotalcite-Like Precursors[J].IntJHydrogenEnergy, 2010, 35(11): 5356-5366.
[8] Venugopal A, Palgunadi J, Deog J K, et al. Dimethyl Ether Synthesis on the Admixed Catalysts of Cu-Zn-Al-M(M=Ga, La, Y, Zr) and γ-Al2O3: The Role of Modifier[J].JMolCatalA:Chem, 2009, 302(1/2): 20-27.
[9] Gao Peng, Li Feng, Zhan Haijuan, et al. Influence of Zr on the Performance of Cu/Zn/Al/Zr Catalysts via Hydrotalcite-Like Precursors for CO2Hydrogenation to Methanol[J].JCatal, 2013, 298(2): 51-60.
[10] 徐盼.类水滑石的制备及其对水中硝酸盐的去除研究[D]. 广州:华南理工大学,2013.
[11] Behrens M, Kasatkin I, Kuhl S, et al. Phase-Pure Cu, Zn, Al Hydrotalcite-Like Materials as Precursors for Copper Rich Cu/ZnO/Al2O3Catalysts[J].ChemMater, 2010, 22(2):386-397.[12] 黎汉生, 徐航, 吴芹,等. 用于甲醇脱水制二甲醚的固体酸催化剂的研究进展[J]. 石油化工, 2010, 39(9): 1052-1058.[13] 高鹏, 李枫, 赵宁, 等. 以类水滑石为前驱体的Cu/Zn/Al/(Zr)/(Y)催化剂制备及其催化CO2加氢合成甲醇的性能[J]. 物理化学学报, 2014, 30(6): 1155-1162.
[14] Li Congming, Yuan Xingdong, Fujimoto K. Development of Highly Stable Catalyst for Methanol Synthesis from Carbon Dioxide[J].ApplCatal,A, 2014, 469(1): 306-311.
[15] Liu Ruiwen, Qin Zuzeng, Ji Hongbing, et al. Synthesis of Dimethyl Ether from CO2and H2Using a Cu-Fe-Zr/HZSM-5 Catalyst System[J].IndEngChemRes, 2013, 52(47):
16648-16655.
[16]Guo Xiaoming, Mao Dongsen, Lu Guanzhong, et al. Glycine-Nitrate Combustion Synthesis of CuO-ZnO-ZrO2Catalysts for Methanol Synthesis from CO2Hydrogenation[J].JCatal, 2010, 271(2):178-185.
[17] Ma Xianggang, Ge Qingjie, Ma Junguo, et al. Synthesis of LPG via DME from Syngas in Two-Stage Reaction System[J].FuelProcessTechnol, 2013, 109(5): 1-6.
[18] Mao Dongsen, Xia Jianchao, Zhang Bin, et al. Highly Efficient Synthesis of Dimethyl Ether from Syngas over the Admixed Catalyst of CuO-ZnO-Al2O3and Antimony Oxide Modified HZSM-5 Zeolite[J].EnergConversManage, 2010, 51(6): 1134-1139.
[19] Zhu Yingying, Wang Shurong, Ge Xiaolan, et al. Experimental Study of Improved Two Step Synthesis for DME Production[J].FuelProcessTechnol, 2010, 91(4): 424-429.
[20] Naika S P, Ryub T, Bui V, et al. Synthesis of DME from CO2/H2Gas Mixture[J].ChemEngJ, 2011, 167(1): 362-368.
[21] Sun Kunpeng, Lu Weiwei, Qiu Fengyan, et al. Direct Synthesis of DME over Bifunctional Catalyst: Surface Properties and Catalytic Performance[J].ApplCatal,A, 2003, 252(2): 243-249.
[22] Zhang Qiang, Zuo Yizan, Han Minghan, et al. Long Carbon Nanotubes Intercrossed Cu/Zn/Al/Zr Catalyst for CO/CO2Hydrogenation to Methanol/Dimethyl Ether[J].CatalToday, 2010, 150(1/2): 55-60.
[23] Arena F, Barbera K, Italiano G, et al. Synthesis, Characterization and Activity Pattern of Cu-ZnO/ZrO2Catalysts in the Hydrogenation of Carbon Dioxide to Methanol[J].JCatal, 2007, 249(2): 185-194.
[24] Arena F, Truno G, Alongi E, et al. Modelling the Activity-Stability Pattern of Ni/MgO Catalysts in the Pre-Reforming ofN-Hexane[J].ApplCatal,A, 2004, 266(2): 155-162.
[25] García-Trenco A, Valencia S, Martínez A. The Impact of Zeolite Pore Structure on the Catalytic Behavior of CuZnAl/Zeolite Hybrid Catalysts for the Direct DME Synthesis[J].ApplCatal,A, 2013, 468(19): 102-111.
[26] García-Trenco A, Martínez A. The Influence of Zeolite Surface-Aluminum Species on the Deactivationof CuZnAl/Zeolite Hybrid Catalysts for the Direct DME Synthesis[J].CatalToday, 2013, 227(8): 145-154.
[27] Bae J W, Kang S H, Lee Y J, et al. Synthesis of DME from Syngas on the Bifunctional Cu-ZnO-Al2O3/Zr-Modified Ferrierite: Effect of Zr Content[J].ApplCatal,B, 2009, 90(3/4): 426-435.
[28] Allahyari S, Haghighi M, Ebadi A, et al. Ultrasound Assisted Co-Precipitation of Nanostructured CuO-ZnO-Al2O3over HZSM-5: Effect of Precursor and Irradiation Power on Nanocatalyst Properties and Catalytic Performance for Direct Syngas to DME[J].UltrasonSonochem, 2014, 21 (2): 663-673.
(编辑 安 静)
Synthesis of Dimethyl Ether from CO2/H2on Bifunctional Calcined Hydrotalcite-Like Precursors/HZSM-5 Catalysts
ChangQinqin,ZhaoBo,YangMeng,LiuYan,LiuEnzhou,FanJun
(School of Chemical Engineering, Northwest University, Xi'an Shaanxi 710069, China)
A series of CuO-ZnO-Al2O3-ZrO2hydrotalcite-like precursors with different ZrO2content were prepared through co-precipitation and then were calcinated. The products were physically mixed with HZSM-5 to prepared catalysts for the synthesis of dimethyl ether(DME) by the hydrogenation of CO2. The catalysts were characterized by means of XRD, N2physisorption and H2-TPR. The results showed that the catalysts exhibited hydrotalcite-like structure with Cu3Zn3Al2(OH)16·4H2O phase. The addition of ZrO2improved the reducibility and activity of the catalysts. The experimental results indicated that the DME synthesis rate depended on the methanol synthesis rate. The catalyst withn(ZrO2):n(Al2O3+ZrO2) 0.10 showed the highest conversion of CO2(25.87%) and the selectivity to DME(48.15%) under the optimal reaction conditions of 533 K, 3.0 MPa,n(H2):n(CO2) 3:1 and GHSV 2 400 h-1. In addition, the catalyst still showed the high catalytic activity and the good stability after running 30 h.
hydrotalcite-like precursor; HZSM-5 zeolite; bifunctional catalysts; zirconium promoter;
2014-10-08;[修改稿日期] 2014-12-16。
常琴琴(1989—),女,陕西省榆林市人,硕士生。联系人:樊君,电话 029-88305252,电邮fanjun@nwu.edu.cn。
国家自然科学基金项目(21476183)。
1000-8144(2015)04-0441-06
TQ 032.4
A

