双杂原子Cr-Co-β沸石的合成及其苯乙烯氧化性能
吴 娟,甘丽文,何红运,何 震
(1. 湖南师范大学 化学化工学院, 湖南 长沙 410081;2. 中南大学 化学化工学院,湖南 长沙410083)
双杂原子Cr-Co-β沸石的合成及其苯乙烯氧化性能
吴 娟1,甘丽文1,何红运1,何 震2
(1. 湖南师范大学 化学化工学院, 湖南 长沙 410081;2. 中南大学 化学化工学院,湖南 长沙410083)
采用水热法在SiO2-Cr2O3-CoO-(TEA)2O-H2O-NH4F体系中((TEA)2O:氧化四乙基铵)合成了具有良好结晶的双杂原子Cr-Co-β沸石,通过XRD,FTIR,UV-Vis,TG-DTG,SEM等技术对试样的结构进行了表征。以H2O2为氧化剂氧化苯乙烯为探针反应,考察了Cr-Co-β沸石的催化活性,研究了溶剂种类、金属配比、H2O2与苯乙烯的摩尔比、催化剂用量、反应时间和反应温度等对反应的影响。实验结果表明,以丙酮为溶剂,以n(Si):n(Cr+Co)=20的Cr-Co-β沸石为催化剂,在催化剂用量60 mg、苯乙烯用量17 mmol、H2O2与苯乙烯的摩尔比3、反应温度70 ℃、反应时间7 h的条件下,苯乙烯转化率为88.4%,苯甲醛选择性为85.3%,环氧苯乙烷选择性为10.7%,苯甲醛收率为75.4%。
双杂原子铬-钴-β沸石;水热合成;催化氧化;苯乙烯
β沸石分子筛具有良好的热稳定性、疏水性和耐酸性,己在石油炼制及精细化工等领域得到广泛应用[1-7]。在传统沸石分子筛骨架上引入Ti,Cr,Fe,Mo,V,Co,Mn,Ni,Cu等过渡金属(统称为杂原子)[5-12],可增加沸石表面的吸附性能,使其具备常规金属氧化物所没有的催化氧化还原功能。特别是在同一沸石中引入两种不同的杂原子,利用两种不同杂原子分别占据沸石骨架的不同位置,可改变沸石孔道的性能和提高活性组分的比例,提高催化剂的活性和对目标产物的选择性,满足某些特定催化反应的需要。
苯甲醛是工业上重要的芳香醛之一,可作为生产多种精细化工品的中间体,广泛应用于香料、食品、染料、医药和农药等[8]行业,市场需求量很大。近年开发出以H2O2为氧化剂的催化氧化苯乙烯制备苯甲醛的环境友好新工艺,但其中所用沸石分子筛催化剂的活性以及苯甲醛的选择性有待提高[13]。
本工作将Cr和Co两种杂原子同时引入到β沸石骨架中,采用水热法在SiO2-Cr2O3-CoO- (TEA)2O-H2O-NH4F((TEA)2O:氧化四乙基铵)体系中合成了双杂原子Cr-Co-β沸石,研究了Cr-Co-β沸石对苯乙烯氧化反应的催化性能。
1 实验部分
1.1 试剂
四乙基氢氧化铵(TEAOH):工业级,含量35%(w),湖南建长石化股份有限公司;白炭黑:工业级,SiO2含量99.9%(w),沈阳化工股份有限公司;Cr(NO3)3·9H2O:AR,成都格雷西亚化学技术有限公司;CoCl2·6H2O:AR,北京化学试剂三厂;苯乙烯:CP,国药集团化学试剂有限公司;丙酮、甲苯、N,N-二甲基甲酰胺(DMF)、乙腈:AR,国药集团化学试剂有限公司;NH4F:CP,上海中西化工厂;30%(w)H2O2水溶液:AR,湖南师大化学实业发展公司;去离子水。
1.2 Cr-Co-β沸石的合成
依次将计量的Cr(NO3)3·9H2O、CoCl2·6H2O、去离子水和TEAOH加入烧杯中,搅拌2 h后加入白炭黑,继续搅拌2 h后加入NH4F,再强力搅拌4 h;把所得均匀溶胶转入带聚四氟乙烯衬里的不锈钢高压釜中,在140 ℃下晶化12 d;取出反应釜,冷却后用高速离心机分离结晶产物,充分洗涤至接近中性,再将产物用1 mol/L的NH4Cl溶液浸泡2 h,搅拌,静置澄清后倾去上层清液,搅拌后过滤,将产物于100 ℃下干燥4 h,得到双杂原子Cr-Co-β沸石试样,用于结构表征;将该试样于550 ℃下焙烧4 h,用于催化性能测试。
1.3 Cr-Co-β沸石的表征
XRD表征在丹东奥龙射线仪器集团有限公司Y-2000型X射线衍射仪上进行,管电压30 kV,管电流20 mA,CuKα射线,=0.154 18 nm,扫描范围2θ=4°~40°,扫描速率0.25 (°)/min。FTIR表征采用Nicolet公司AVATAR370型傅里叶变换红外光谱仪,KBr压片。UV-Vis表征采用Hitachi公司U-3310型紫外可见分光光度计,参比物为硫酸钡。TG-DTG分析采用耐驰仪器制造有限公司STA409PC型热分析仪,O2气氛。SEM表征采用日本电子公司JSM-6700F型场发射扫描电子显微镜,工作电压5 kV。
1.4 Cr-Co-β沸石催化苯乙烯氧化反应
苯乙烯氧化反应在配有电磁搅拌、恒温水浴和回流冷却装置的圆底烧瓶中进行。将一定量的催化剂、苯乙烯、H2O2水溶液和溶剂依次加入到烧瓶内,在设定温度下反应一定时间。产物离心分离后取清液在上海海欣色谱仪器有限公司GC-920型气相色谱仪上进行分析,分析条件:毛细管色谱柱ATXE-60(0.32 mm×0.5 μm×30 m),柱温120 ℃,汽化室温度200 ℃,FID温度240 ℃,进样量0.4 μL,分流比1:50,N2载气流量40 mL/min。
2 结果与讨论
2.1 原料配比对Cr-Co-β沸石合成的影响
2.2 Cr-Co-β沸石的表征结果
2.2.1 XRD表征结果
图1是Cr-Co-β沸石试样的XRD谱图。由图1可看出,在2θ=21.42°,22.46°,25.35°,26.90°,29.64°处出现了β沸石(300),(302),(304),(008),(306)晶面的特征衍射峰[16],说明合成的试样确实是β沸石相。

图1 Cr-Co-β沸石试样的XRD谱图
2.2.2 FTIR表征结果
图2为Cr-Co-β沸石试样的FTIR谱图。

图2 Cr-Co-β沸石试样的FTIR谱图
据文献[13]报道,β沸石的FTIR谱图中在525,575 cm-1附近出现两个特征峰,分别归属于骨架中双四元环和五元环的振动。本实验合成的Cr-Co-β沸石由于Cr和Co对Si或Al的同晶取代,使T—O键的平均键长增大,折合质量增大,导致这两个特征峰向低波数方向移至521,562 cm-1附近;同时在970 cm-1附近出现吸收峰(见图2)。970 cm-1附近的吸收峰归属于沸石骨架上与杂原子键合的SiO4单元的伸缩振动,可作为杂原子是否进入沸石骨架的旁证[5]。这说明本实验合成的Cr-Co-β沸石试样中,Cr和Co原子进入了沸石骨架。
2.2.3 UV-Vis表征结果
图3为CoCl2、Cr(NO3)3和Cr-Co-β沸石试样的UV-Vis谱图。由图3可以看出,CoCl2和Cr(NO3)3试样的吸收峰与Cr-Co-β沸石试样明显不同,因O 2p轨道电子易向骨架杂原子的空d轨道发生p-d跃迁,使得Cr-Co-β沸石试样在219, 318 nm处出现β沸石的特征峰[16];但CoCl2试样在457, 540 nm处和Cr(NO3)3试样在286 nm处的强吸收峰在Cr-Co-β沸石试样的UV-Vis谱图中均未出现,说明Cr-Co-β沸石试样中不存在非骨架的Cr和Co,即证明Cr和Co原子进入了沸石骨架。
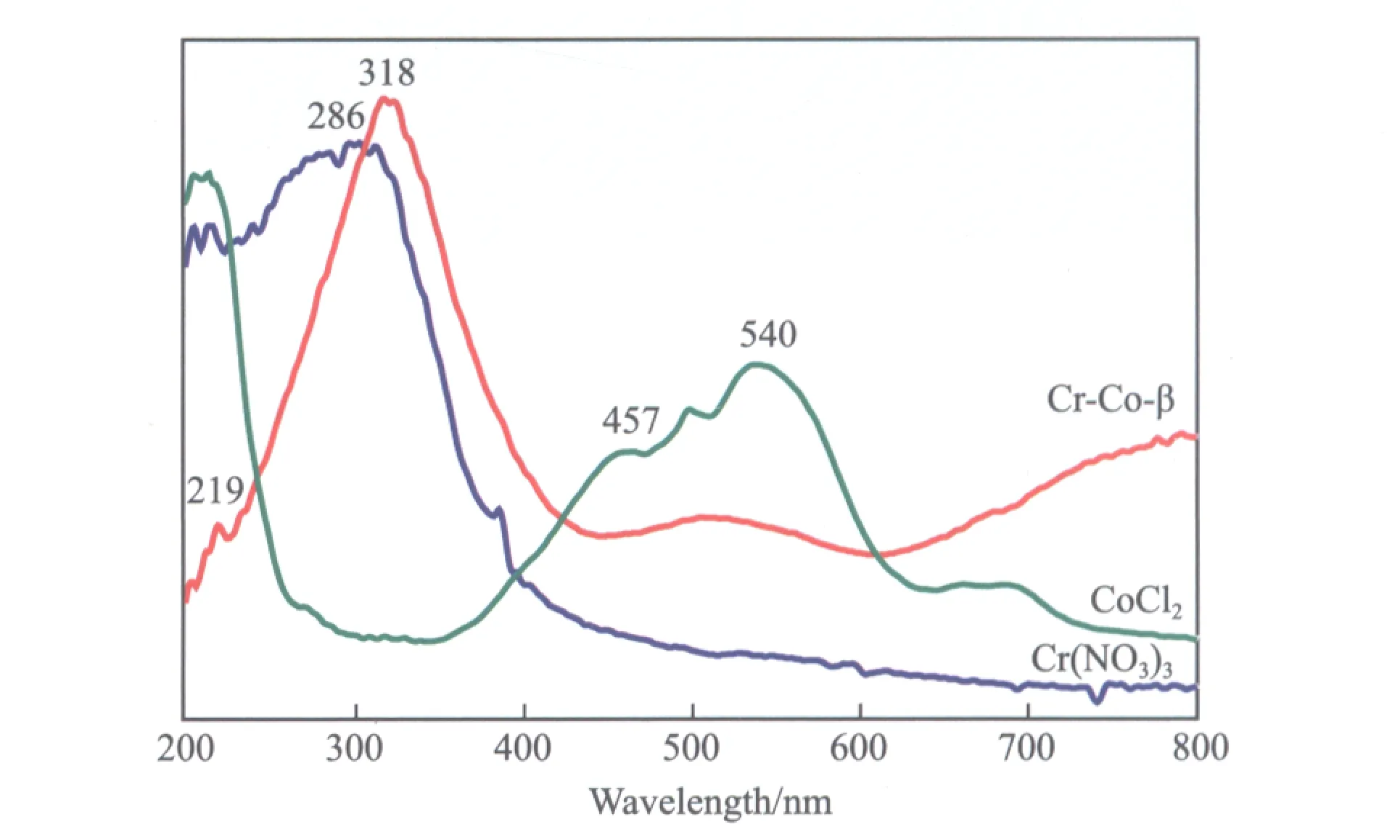
图3 CoCl2、Cr(NO3)3和Cr-Co-β沸石试样的UV-Vis谱图
2.2.4 TG-DTG表征结果
图4为Cr-Co-β沸石试样在O2气氛下的TG-DTG曲线。
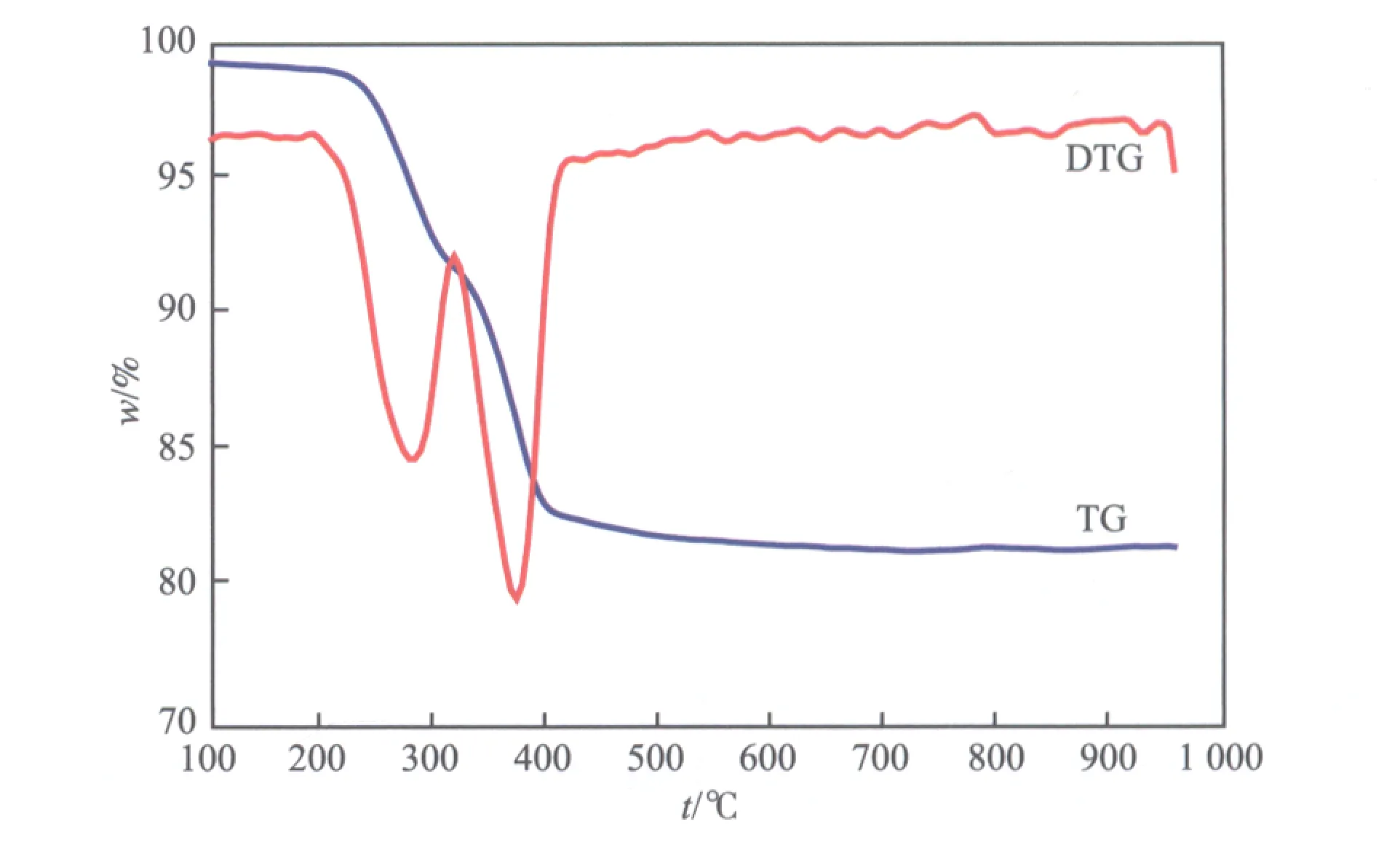
图4 Cr-Co-β沸石试样在O2气氛下的TG-DTG曲线
由图4可看出,在195~320 ℃和320~420 ℃之间有两个明显的失重阶段,第一阶段失重7.25%,对应于吸附在沸石孔道内的模板剂脱附并发生氧化分解;第二阶段失重9.21%,对应于平衡骨架负电荷的TEA+的氧化分解;加热至800 ℃时,没有再出现失重现象,表明Cr-Co-β沸石骨架具有良好的热稳定性。
2.2.5 SEM表征结果
图5是Cr-Co-β沸石试样的SEM照片。

图5 Cr-Co-β沸石试样的SEM照片
由图5可看出,所合成的Cr-Co-β沸石试样结晶良好,晶粒表面干净,粒度较大,形状规则,不存在其他胶态物质。
2.3 Cr-Co-β沸石催化苯乙烯氧化反应的结果
2.3.1n(Si):n(Cr+Co)的影响
不同n(Si):n(Cr+Co)的Cr-Co-β沸石催化苯乙烯氧化反应的结果见表1。由表1可看出,随Cr-Co-β沸石中杂原子含量的增加,苯乙烯转化率和苯甲醛选择性均先增加后降低,当n(Si):n(Cr+Co)=20时,苯乙烯转化率和苯甲醛选择性均最高,而后随杂原子含量的增加,苯乙烯转化率和苯甲醛选择性均逐渐减小,而环氧苯乙烷选择性略有增大。这可能是由于随杂原子含量的增加,进入沸石骨架的Cr和Co原子量增加,活性中心增多,催化活性提高;但Cr和Co原子量过多时,可能有部分Cr和Co离子包裹在沸石孔道内,或以非骨架氧化物的形式混杂于沸石中,沸石孔道被堵塞,部分沸石表面被无催化活性的氧化物覆盖,从而影响催化剂的活性。因此,适宜的n(Si):n(Cr+Co)=20。
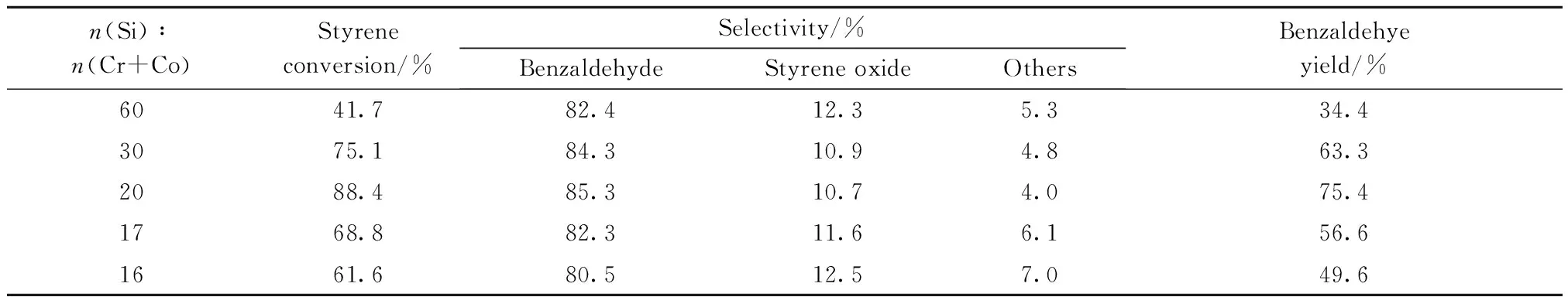
表1 不同n(Si):n(Cr+Co)的Cr-Co-β沸石催化苯乙烯氧化反应的结果
Reaction conditions:catalyst 60 mg,styrene 17 mmol,n(H2O2):n(styrene)=3,70 ℃,7 h,acetone 12 mL.
2.3.2 溶剂种类的影响
分别以甲苯、DMF、乙腈和丙酮为溶剂,以n(Si):n(Cr+Co)=20的Cr-Co-β沸石为催化剂,考察了溶剂种类对苯乙烯氧化反应的影响,实验结果见表2。由表2可看出,当溶剂为甲苯时,苯乙烯转化率很低,而以DMF、乙腈和丙酮为溶剂时,苯乙烯转化率均在88%以上。这可能是由于催化剂活性与溶剂的极性有关,极性较强的DMF、乙腈和丙酮能使苯乙烯与H2O2更易互相
溶解,所以苯乙烯转化率相对更高。其中,苯乙烯在乙腈中的转化率最高,可能是由于乙腈与H2O2反应生成过亚氨酸从而促进氧化反应更好地进行[17]。但在乙腈中产物苯甲醛和环氧苯乙烷的选择性较在DMF和丙酮中的低,这是由于乙腈的极性大于DMF和丙酮,极性的增大使得产物与H2O2进一步接触出现过度氧化。所以,从毒理学、环境角度和实验结果综合考虑,选择丙酮为溶剂最佳。

表2 溶剂种类对苯乙烯氧化反应的影响
Reaction conditions:catalyst(Cr-Co-β zeolite withn(Si):n(Cr+Co)=20, the same below) 60 mg,styrene 17 mmol,n(H2O2):n(styrene)=3,70 ℃,7 h,solvent 12 mL.
2.3.3 反应条件的影响
以n(Si):n(Cr+Co)=20的Cr-Co-β沸石为催化剂,考察了催化剂用量、H2O2与苯乙烯的摩尔比、反应时间和反应温度对苯乙烯氧化反应的影响,实验结果见图6。
由图6(a)可看出,随H2O2用量的增大,苯乙烯转化率和苯甲醛选择性均增加,环氧苯乙烷选择性降低;但当H2O2与苯乙烯的摩尔比大于3时,虽然苯乙烯的转化率继续增加,但苯甲醛的选择性和收率降低,这可能是由于H2O2用量过多时易使产物深度氧化。因此H2O2与苯乙烯的最佳摩尔比为3。

图6 反应条件对苯乙烯氧化反应的影响
由图6(b)可看出,随催化剂用量的增大,苯乙烯转化率和苯甲醛选择性均呈现先增加后下降的趋势。这一方面是由于过量的催化剂会加速H2O2的无效分解,另一方面催化剂用量增加会导致反应物吸附在催化剂颗粒间的可能性增大[18],进而降低了反应机会。所以催化剂用量为60 mg较适宜。
由图6(c)可看出,延长反应时间可使苯乙烯转化率增大,但超过最佳反应时间后,产物苯甲醛深度氧化,导致其选择性降低;而苯甲醛收率先增大后减小,在7 h时苯甲醛收率最大。因此适宜的反应时间为7 h。
由图6(d)可看出,苯乙烯转化率和苯甲醛收率在50~70 ℃之间随反应温度的升高而增大,反应温度超过70 ℃时,苯甲醛选择性降低,而环氧苯乙烷选择性基本不变,这可能是由于反应温度的升高会使苯甲醛发生深度氧化。同时,反应温度超过70 ℃后苯乙烯转化率反而下降,可能是由于反应温度过高时H2O2分解过快而得不到有效利用。综合考虑,选择70 ℃为最佳反应温度。
2.3.4 催化剂的稳定性
以n(Si):n(Cr+Co)=20的Cr-Co-β沸石为催化剂,考察了催化剂使用次数对苯乙烯氧化反应的影响,实验结果见表3。
由表3可看出,随催化剂使用次数的增加,苯乙烯转化率略有降低,但产物苯甲醛和环氧苯乙烷的选择性降低较明显。其原因可能是随催化剂使用次数的增加,其他副产物生成量增多。但催化剂重复使用4次后苯乙烯转化率仍保持在87%以上,说明催化剂的稳定性良好。

表3 催化剂使用次数对苯乙烯氧化反应的影响
Reaction conditions:catalyst 60 mg,styrene 17 mmol,n(H2O2):n(styrene)=3,70 ℃,7 h,acetone 12 mL.
3 结论
1) 在初始原料配比为n(SiO2):n(Cr2O3):n(CoO):n((TEA)2O):n(H2O):n(NH4F) = 60:(0.25~1.25):(0.25~2.50):18:700:30的反应体系中,在140 ℃下晶化12 d可制备出具有良好结晶的双杂原子Cr-Co-β沸石。
2) 以丙酮为溶剂、n(Si):n(Cr+Co)=20的Cr-Co-β沸石为催化剂,在催化剂用量60 mg、苯乙烯用量17 mmol、H2O2与苯乙烯的摩尔比3、反应温度70 ℃、反应时间7 h的条件下,苯乙烯转化率、苯甲醛和环氧苯乙烷的选择性、苯甲醛收率分别为88.4%,85.3%,10.7%,75.4%。
[1] Zhang Xingguang, Liu Ping, Wu Yajing, et al. Synthesis and Catalytic Performance of the Framework-Substituted Manganese β Zeolite[J].CatalLett,2010 , 137(3/4) : 210-215.
[2] Corma A , Domine M E , Nemeth L. Al-Free Sn-Beta Zeolite as a Catalyst for the Selective Reduction of Carbonyl Compounds(Meerwein-Ponndorf-Verley Reaction)[J].JAmChemSoc,2002 , 124(13) : 3194-3195.
[3] 何红运, 李艳凤,何震,等. 全硅β沸石的合成、表征及在苯酚羟基化反应中的催化性能[J]. 应用化学,2007 , 24(7) : 790-794.
[4] Lu Xionghui, Zhou Dezhi, Xia Qinghua , et al. Catalytic Epoxidation of Alkenes with 30%H2O2over Mn2+-Exchanged Zeolites[J] .JMolCatalA:Chem, 2010, 322(1): 73-79.
[5] 张敏,高丙莹,何红运. 新型V-Ni-β沸石的合成、表征及催化性能[J]. 无机化学,2012, 28 (11) : 2355-2362.
[6] Vander W J C , Lin P , Rigutto M S. Catalytic Properties of Aluminium-Free Zeolite Ti-Beta[J].StudSurfSciCatal,1997,105(11):1093-1100.
[7] Corma A, Domine M E, Valencia S. Water Resistant Solid Lewis Acid Catalysts: Meerwein-Ponndoif-Verley and Oppenauer Reactionscatalyzed by Tin-Beta Zeolite[J].JCatal,2003, 215(2):294-304.
[8] 中国化工产品大全编委会. 中国化工产品大全[M]. 北京:化学工业出版社,2002: 47-55.
[9] 何红运, 何驰剑,许青,等. Cr-β沸石的合成及催化性能研究[J] .无机化学,2005 , 21(3): 320-324.
[10] 何红运,丁红,庞文琴. 高硅无铝Mo-Beta沸石的合成与结构表征[J]. 无机化学,2002, 18(4): 367-372.
[11] Lin Kaifeng,Pescarmona P P, Houthoofd K, et al. Direct Roomtemperature Synthesis of Methyl-Functionalized Ti-MCM-41 Nanoparticles and Their Catalytic Performance in Epoxidation[J].JCatal,2009 , 263(1): 75-82.
[12] 陈君华,伏再辉,尹笃林,等. 中孔Cu-HMS分子筛的合成[J]. 石油化工,2000, 29(11): 756-759.
[13] 张旭,张利雄,徐南平. 苯乙烯氧化合成环氧苯乙烷和苯甲醛催化剂的研究进展[J]. 石油化工,2009, 38(2): 215-220.
[14] Pereze P J, Martens J A, Rosinski E J. Hydrothermal Crystalliztion of Zeolite Beta[J].ApplCataL, 1987, 31(7) : 35-64.
[15] 祁晓岚,刘希尧,林炳雄,等. 四乙基溴化铵-氟化铵复合模板剂合成β沸石:Ⅰ.合成热力学相区[J]. 催化学报,2000, 21(1): 75-78.
[16] 何红运,庞文琴. Co-β沸石的合成与结构表征[J]. 应用化学,2002,19(6): 588-590.
[17] Hulea V, Moreau P. The Solvent Effect in the Sulfoxidation of Thioethers by Hydrogen Peroxide Using Ti-Containing Zeolites as Catalysts[J].JMolCatalA:Chem, 1996, 113(3): 499-505.
[18] Maurya M R, Chandrakar A K, Chand S. Zeolite-Y Encapsulated Metal Complexes of Oxovanadium(Ⅵ), Copper(Ⅱ) and Nickel(Ⅱ) as Catalyst for the Oxidation of Styrene, Cyclohexane and Methyl Phenyl Sulfide[J].JMolCatalA:Chem, 2007, 274(1/2): 192-201.
(编辑 安 静)
Synthesis and Catalytic Performance for Styrene Oxidation of Heteroatomic Cr-Co-β Zeolites
WuJuan1,GanLiwen1,HeHongyun1,HeZhen2
(1. College of Chemistry and Chemical Engineering, Hunan Normal University, Changsha Hunan 410081, China;2. College of Chemistry and Chemical Engineering, Central South University, Changsha Hunan 410083, China)
Well-crystallized heteroatomic Cr-Co-β zeolites were hydrothermally synthesized in a SiO2-Cr2O3-CoO-(TEA)2O-H2O-NH4F system((TEA)2O: tetraethyl ammonium oxide) and were characterized by means of XRD, FTIR, UV-Vis, TG-DTG and SEM. The oxidation of styrene to styrene oxide on the Cr-Co-β zeolite catalysts was investigated with 30%(w)H2O2as oxidant. The effects of solvents,n(Si):n(Cr+Co) in the catalysts, molar ratio of H2O2to styrene, catalyst dosage, reaction time and reaction temperature on the oxidation were explored. The results indicated that under the conditions of acetoneas solvent , 60 mg Cr-Co-β zeolite catalyst withn(Si):n(Cr+Co) 20, styrene 17 mmol, mole ratio of H2O2to styrene 3, reaction temperature 70 ℃ and reaction time 7 h, the conversion of styrene, the yield of benzaldehyde, the selectivity to benzaldehyde and the selectivity to styrene oxide were 88.4%, 75.4%, 85.3% and 10.7%, respectively.
heteroatomic chromium-cobalt-β zeolite; hydrothermal synthesis; catalytic oxidation; styrene
2014-09-27;[修改稿日期]2014-12-26。
吴娟(1990—),女,江西省吉安市人,硕士生,电话15707490043,电邮wujuan19900714@126. com。联系人:何红运,电话 0731-88872530,电邮 hhy1956@163.com。
湖南省自然科学基金项目 (08JJ3026)。
1000-8144(2015)04-0447-06
TQ 426.82
A

