舒血宁注射液与环磷腺苷葡胺注射液的配伍稳定性研究
张晨华
(浙江省台州市第一人民医院 药剂科,浙江 台州 318020)
舒血宁注射液与环磷腺苷葡胺注射液的配伍稳定性研究
张晨华Δ
(浙江省台州市第一人民医院 药剂科,浙江 台州 318020)
目的 研究舒血宁注射液与环磷腺苷葡胺注射液的配伍稳定性。方法 采用正交试验设计优选舒血宁注射液与环磷腺苷葡胺注射液的配伍方案,以舒血宁注射液中主要成分银杏总黄酮(以槲皮素、山奈素及异鼠李素为对照品)和银杏内酯(以银杏内酯A、B、C为对照品)的含量及环磷腺苷葡胺注射液中主成分环磷腺苷(以环磷腺苷为对照品)的含量为主要考察指标绘制标准曲线,选择温度(A)、光照(B)、放置时间(C)、溶媒种类(D)4 个影响因素,同时考察配伍前后各溶液中不溶性微粒和pH值的变化情况。结果 正交试验优选方案为A2B1C1D1(25 ℃、避光、放置1 h、5%葡萄糖为溶媒),方差分析结果表明对于舒血宁注射液中的槲皮素、山奈素而言,温度(A)、光照(B)和放置时间(C)3个因素均对其含量有显著影响(P<0.05),而溶媒(D)对它们的含量无显著性影响;温度(A)、光照(B)、放置时间(C)和溶媒(D)对配伍液中的其他5种成分均具有显著性影响(P<0.05)。在0、1、4、6 h,配伍液(A2B1C1D1)的外观、pH值无明显变化,随着放置时间的延长,不溶性微粒数符合中国药典的相关规定。结论 舒血宁注射液与环磷腺苷葡胺注射液在一定的条件下配伍稳定性较好,临床上可以配伍使用。
舒血宁注射液;环磷腺苷葡胺注射液;配伍稳定性;正交实验;优选
舒血宁注射液是由银杏叶提取物制备而成的中药注射剂,其活性成分主要包含银杏叶总黄酮及总内酯等,具有扩张血管,改善微循环的作用,临床上用于治疗缺血性心脑血管疾病、冠心病、心绞痛、脑栓塞、脑血管痉挛[1]。环磷腺苷葡胺注射液的主要成分为环磷腺苷,其具有正性肌力作用,能增加心肌收缩力,改善心脏泵血功能;且具有扩张血管的作用,可降低心肌耗氧量,改善心肌细胞代谢,保护缺血、缺氧的心肌。两药在临床上常配伍使用治疗心脑血管疾病。之前关于两药配伍稳定性的研究[2-3],仅仅限于检测时间和溶媒对配伍液稳定性的影响,且所用检测方法专属性不强。
本实验选择温度、光照、放置时间、溶媒种类4 个影响因素,采用L9(34)正交试验表对舒血宁注射液与环磷腺苷葡胺注射液的配伍方案进行了优选,用HPLC法对舒血宁注射液中主要成分银杏总黄酮和银杏内酯的含量及环磷腺苷葡胺注射液中主成分环磷腺苷的含量进行了测定,同时考察了配伍前后各溶液中不溶性微粒及pH值的变化情况,为临床用药安全提供了较为全面、合理的数据支持。
1 材料与方法
1.1 材料
1.1.1 仪器:LC20A高效液相色谱仪(岛津公司);色谱柱:Dikxna Cl8(4.6 mm×250 mm, 5 μm);AB135S型电子天平(梅特勒-托利多);PB-10型酸度计(德国赛多利斯集团);2501型紫外可见分光光度计(岛津公司);GWS-20型智能微粒检测仪(江苏苏净集团);SC-15型电热恒温水槽( 上海比朗仪器制造有限公司);SW-CJ-1FD单人单面净化工作台(上海苏净实业有限公司)。
1.1.2 试剂:舒血宁注射液(通化谷红制药有限公司,规格:5 mL/支,批号:150307/2,150511/1,150615/2);环磷腺苷葡胺注射液(徐州莱恩药业有限公司, 规格:2 mL:30 mg,批号:150521,150615,150711);槲皮素对照品(中国药品生物制品检定研究院,批号:100081-200406,含量:98%);山奈素对照品(中国药品生物制品检定研究院,批号:110861-200606,含量:98%);异鼠李素对照品(中国药品生物制品检定研究院,批号:110860-200608);银杏萜类内酯A、B、C对照品(中国药品生物制品检定研究院,批号:110862 - 200305,110863 - 200204,110864 - 200203 );环磷腺苷对照品(中国药品生物制品检定研究院,批号:140709-201003);0.9%氯化钠注射液(四川科伦药业股份有限公司);5%葡萄糖注射液[华裕(无锡)制药有限公司];5%葡萄糖氯化钠注射液[华仁药业(日照)有限公司];甲醇为色谱纯,水为超纯水,其他试剂为分析纯。
1.2 配伍液的配制 按参考文献[2]上的配伍比例,取舒血宁注射液2 mL与环磷腺苷葡胺注射液1 mL,混合于25 mL容量瓶中,分别用0.9%氯化钠注射液、5%葡萄糖注射液、5%葡萄糖氯化钠注射液溶解并稀释至刻度,摇匀,根据正交试验表安排试验,每个试验做3份,共制备27个样品溶液。
1.3 含量测定
1.3.1 舒血宁中银杏总黄酮与银杏总内酯:
① 色谱条件[4]:银杏总黄酮:流动相:甲醇-0.4%磷酸溶液(47︰53),流速:0.8 mL/min,DAD检测器,检测波长:360 nm,柱温:45 ℃,进样量:20 μL;
银杏内酯:流动相:四氢呋喃-甲醇-水(10︰20 ︰75),流速:0.5 mL/min,蒸发光散射检测器,以空气为载气,流速3 L/min,漂移管温度:105 ℃,柱温:30 ℃。
② 溶液的配制: 对照品溶液:银杏总黄酮:精密称取槲皮素、山奈素及异鼠李素对照品适量,加甲醇制成每1 mL含槲皮素、山奈素及异鼠李素0.05 mg的黄酮苷元对照品混合溶液,即得;银杏内酯:精密称取银杏内酯A、B、C对照品适量,加丙酮制成每1 mL分别含银杏内酯A、B、C1、0.5、0.5 mg的对照品混合溶液,即得。
供试品溶液:银杏总黄酮:取1.2项下各条件的配伍液(25 mL),加甲醇-12 moL/min盐酸(7︰1)混合溶液15 mL,68 ℃水浴加热3 h,冷却,滤过,取续滤液即得;银杏内酯:取1.2项下各条件的配伍液,每个实验取3份(共75 mL),加稀盐酸调节pH值至2.0,然后用乙酸乙酯提取4次(80、40、40、40 mL),合并乙酸乙酯液,用5%的醋酸钠溶液80 mL洗涤,分离出乙酸乙酯层,醋酸钠溶液再用乙酸乙酯40 mL洗涤,合并乙酸乙酯液及洗涤液,用水洗涤2次,每次80 mL,分离乙酸乙酯液,蒸干,残渣加丙酮适量溶解,并转移至2 mL量瓶中,加丙酮稀释至刻度,摇匀,用0.45 μm滤膜过滤,取续滤液即得;
③ 标准曲线的绘制:银杏总黄酮:精密量取1.3.1项下②中的黄酮苷元对照品混合溶液1、3、5、8、10 mL加甲醇至10 mL量瓶,即得每1 mL含槲皮素、山奈素及异鼠李素分别为5、15、25、40、50 μg的对照品混合溶液;按1.3.1项下①银杏总黄酮的色谱条件进样分析,以峰面积A为纵坐标,对照品浓度C(μg/mL)为横坐标,进行线性回归。
银杏内酯:精密量取1.3.1项下②中银杏内酯对照品混合溶液2、6、10、16、20 μL,按1.3.1项下①银杏内酯项下的色谱条件进样分析,以进样量(μg)的自然对数为横坐标(X),峰面积的自然对数(Y)为纵坐标,绘制标准曲线。
1.3.2 环磷腺苷葡胺注射液中主成分环磷腺苷:
① 色谱条件[5]:流动相:0.05 mol/L磷酸二氢钾溶液-乙腈(94︰6),流速:,1.0 mL/min,DAD检测器,检测波长:259 nm,柱温:25 ℃,进样量:20 μL;
② 溶液的配制:对照品溶液:精密称取减压干燥至恒重的环磷腺苷对照品适量,加甲醇制成每1 mL含环磷腺苷0.15 mg的溶液,即得;
供试品溶液:取1.2项下各条件的配伍液2.5 mL,加流动相稀释至10 mL,滤过,取续滤液即得;
③ 标准曲线的绘制:称取减压干燥至恒重的环磷腺苷对照品适量,加甲醇制成每1 mL含环磷腺苷5 mg的溶液,精密吸取上述溶液1、3、5、8、10 mL加流动相至100 mL量瓶,即得每1 mL含环磷腺苷0.05、0.15、0.25、0.40、0.50 mg的对照品混合溶液;按1.3.2项下①的色谱条件进样分析,以峰面积Y为纵坐标,对照品浓度X(μg/min)为横坐标,进行线性回归。
1.3.3 配伍液中药物含量测定:按照1.3.1项下①和1.3.2项下①色谱条件和正交试验设计表,取1.3.1项下②和1.3.2项下②各对照品溶液和供试品溶液,分别进样检测,每个样品测定3次,取均值。
1.4 正交试验
1.4.1 因素水平:以舒血宁注射液中的有效成分银杏总黄酮(槲皮素、山奈素、异鼠李素)和银杏内酯(银杏内酯A、B、C)与环磷腺苷葡胺注射液溶液中的有效成分(环磷腺苷)的含量为主要检测指标,采用L9(34)正交试验表,选择温度、光照[6]、放置时间、溶媒种类4个影响因素,每个因素分为3个考察水平(见表1),进行正交试验分析。
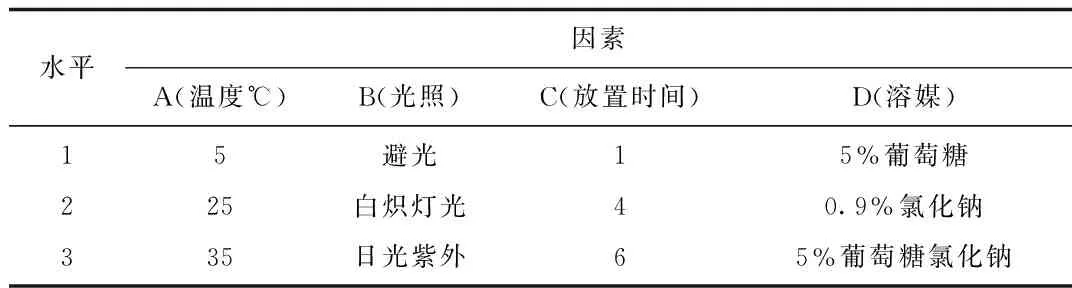
表1 因素水平表Tab.1 Factor and level of orthogonal design
1.4.2 验证试验:按照正交试验结果优选的配伍方案配制3份配伍溶液,分别测定配伍液中银杏总黄酮、银杏内酯和环磷腺苷的含量(以未配伍时各注射液主成分的含量为100%计),每份配伍液重复检测3次(n=3)。
1.4.3 配伍液外观观察:取洁净的20 mL具塞纳氏比色管,加入15 mL用5%的葡萄糖注射液稀释的配伍液,尽量避光,于0、1、4、6 h观察其外观变化,以未配伍的2种注射液作为参照。
1.4.4 pH测定:取上述配伍液于0、1、4、6 h测定pH值,避光,每个样本连测3次,取平均值。
1.4.5 不溶性微粒:药典规定100 mL以下的静脉注射液含≥10 μm的微粒不得过6000粒,含≥25 μm的微粒不得过600粒)[7]。取配伍液及未配伍的舒血宁注射液、环磷腺苷葡胺注射液及5%的葡萄糖注射液于0、1、4、6 h按中国药典微粒检测法中的光阻法检查微粒[8]。
2 结果
2.1 标准曲线
2.1.1 舒血宁中银杏总黄酮与银杏总内酯:
① 银杏总黄酮:槲皮素、山奈素及异鼠李素的线性方程分别为Y=812118X+2325.1(r=0.9995,n=5)、Y=415572X+3182.7(r=0.9997,n=5)、Y=115892X+2741.7(r=0.9998,n=5)。
② 银杏内酯:得到银杏内酯A、B、C的线性方程分别为Y=571576X+1427.2(r=0.9996,n=5)、Y=319513X+2683.4(r=0.9994,n=5)、Y=608337X+1683.3(r=0.9995,n=5)。
以上结果表明,槲皮素、山奈素及异鼠李素在5~50 μg/ mL的浓度范围内线性关系良好;银杏内酯A、B、C分别在2~20 μg、1~10 μg及1~10 μg的质量范围内相关性良好。
2.1.2 环磷腺苷葡胺注射液中主成分环磷腺苷:环磷腺苷的线性方程为Y=273415X+3157.2 (r=0.9996,n=5)。
2.2 正交试验结果 正交试验结果见表2,直观表见表3。结果表明影响各成分含量的因素主要是放置时间,其次是温度或光照,溶媒的影响较小。有文献报道,舒血宁注射液最好与5%葡萄糖溶液配伍[7],得出优选的配伍使用方案为A2B1C1D,即在25 ℃下,以5%的葡萄糖注射液为溶媒(在1h内滴注完毕,尽量避光,最终确定正交试验优选方案为A2B1C1D1。
表4方差分析结果显示,对于舒血宁注射液中的槲皮素、山奈素而言,温度(A)、光照(B)和放置时间(C)3个因素均对其含量有显著性影响(P<0.05),而溶媒(D)对它们的含量无显著性影响;温度(A)、光照(B)、放置时间(C)和溶媒(D)对配伍液中的其他5种成分均具有显著性影响(P<0.05)。

表2 正交试验结果(n=3)Tab.2 Results of the orthogonal test(n=3)

表3 直观分析表Tab.3 Intuitive analysis table
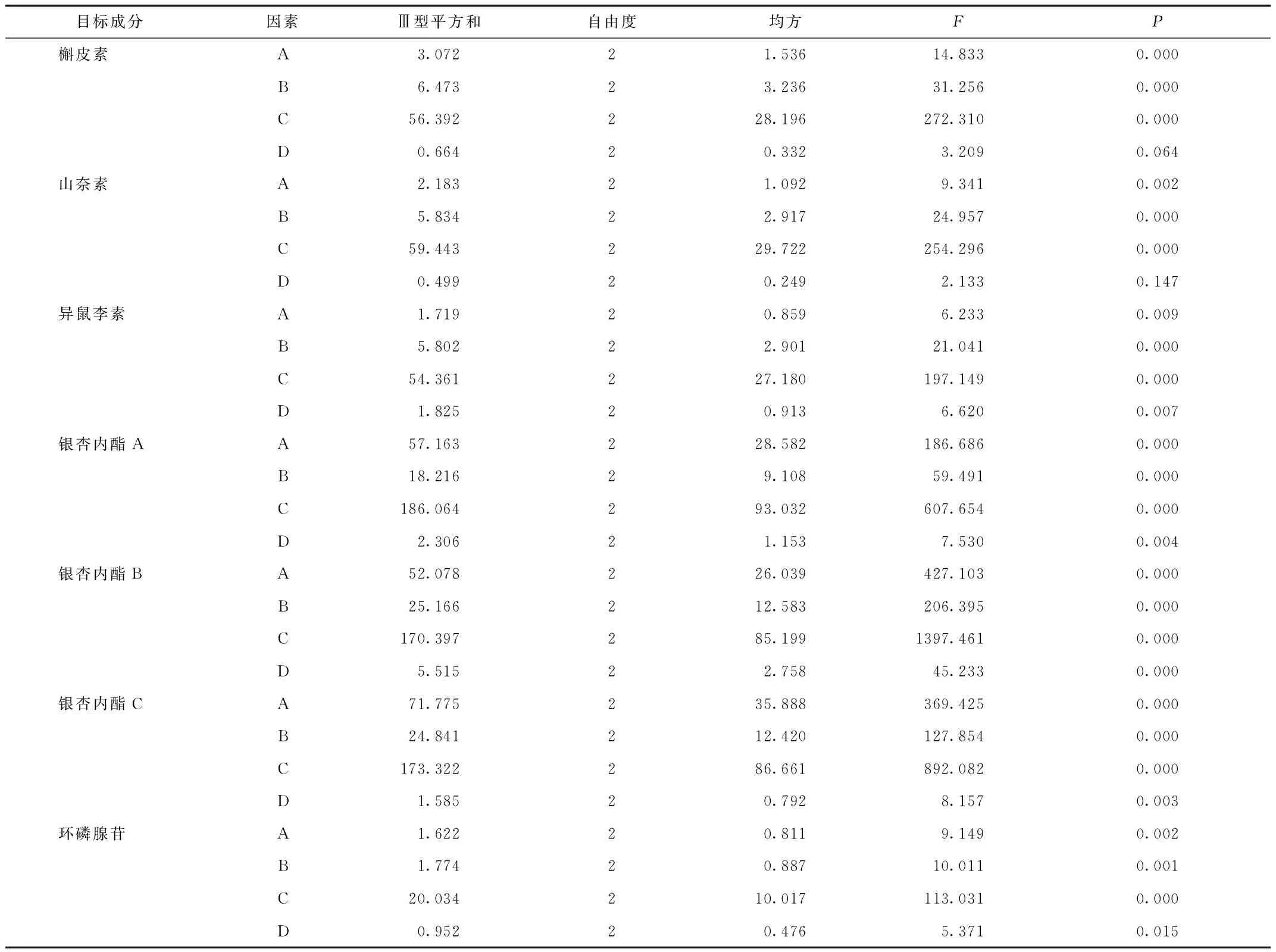
表4 方差分析表Tab.4 Variance analysis table
2.3 验证试验结果 取舒血宁注射液与环磷腺苷葡胺注射液按正交试验优选结果(A2B1C1D1),得到配伍液中各成分的含量(以未配伍时各注射液主成分的含量为100%计)。结果表明,配伍方案重复性良好,配伍溶液质量稳定。见表5。
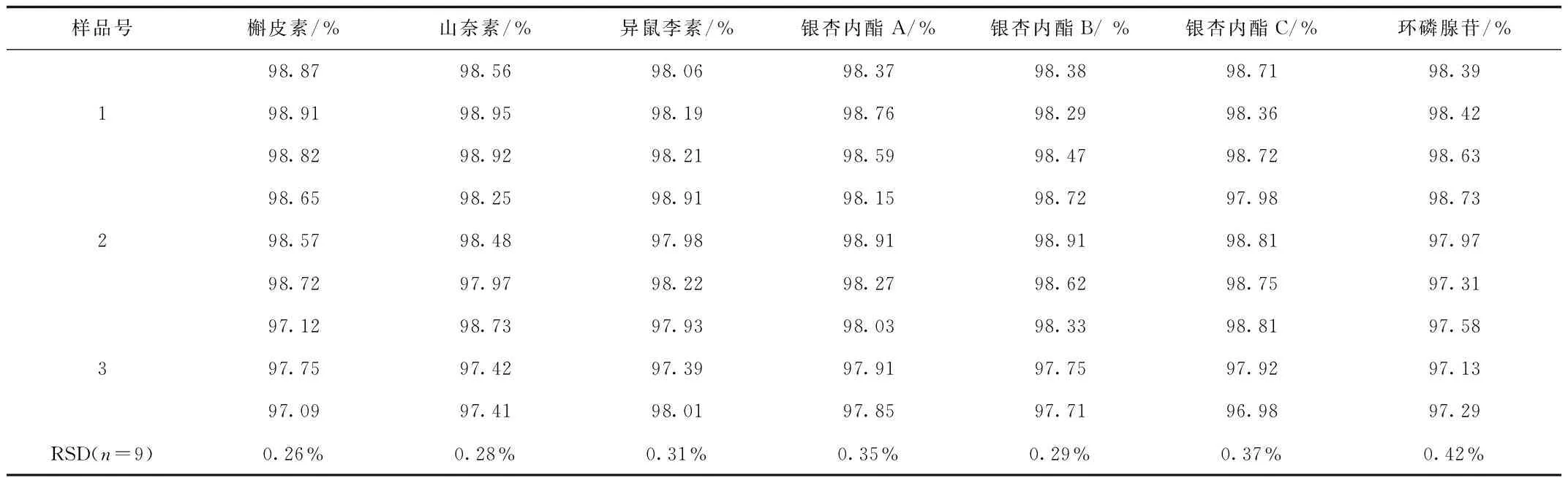
表5 验证实验结果(n=3)Tab.5 The test results (n=3)
2.4 配伍液外观观察 配伍液(A2B1C1D1)于0、1、4、6 h的外观变化与未配伍的2种注射液相比无明显变化。
2.5 pH测定 配伍液(A2B1C1D1)于0、1、4、6h测的pH值结果表明,配伍液的pH值在配伍后0 h有一定的变化,后趋于平稳,结果见表6。
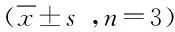
表6 配伍前后溶液pH值的变化Tab.
2.6 不溶性微粒 2药于0、1、4、6 h在5%的葡萄糖注射液中配伍后,随着放置时间的延长,配伍液微粒数有较明显的增加,但仍在《中国药典》规定的范围内。见表7。

表7 2药配伍不同时刻的不溶性微粒数±s, n=3)Tab.7 Insoluble particles of compatibility solution at different ±s,n=3)
3 讨论
3.1 本实验采用正交法优选了舒血宁注射液与环磷腺苷葡胺注射液在临床常用输液中的配伍方案,得出的优选方案为:取舒血宁注射液2 mL与环磷腺苷葡胺注射液1 mL溶解于25 mL的5%葡萄糖注射液中,于1 h内滴注完毕,且应注意尽量避光。 使用正交分析法优选药物的配伍方案可避免一般方法的盲目性,其试验点分布均匀,具有简单可靠的特点。配合直观分析与方差分析,可以提供更加详尽的数据支持。
3.2 之前关于舒血宁注射液与环磷腺苷葡胺注射液配伍稳定性的研究,对于配伍液主成分的考察仅仅为配伍液紫外光谱的变化,专属性较差;本研究采用HPLC法考察了配伍液中7个主要成分在不同时间及不同条件下的变化情况,为临床配伍方案提供了更为详尽可靠的实验数据。
3.3 舒血宁注射液与环磷腺苷葡胺注射液均是临床上用来治疗心脑血管疾病的药物,其稀释液一方面应考虑配伍后的稳定性,其次还应从临床用药方面靠, 尽量避免使用盐类,否则会加重心脏负担。
[1] 于法忠,刘爱香.输血宁注射液治疗冠心病心绞痛疗效观察[J].现代中西医结合杂志,2004,13(4):480-481.
[2] 何心,李雪峰,石春伟.舒血宁注射液与环磷腺苷葡胺注射液的配伍稳定性考察[J].中国药房,2008,19(5):354-356.
[3] 张蓬华,肖淼生,张静,等.舒血宁与五种注射液配伍后的稳定性考察[J].中国药师,2009,12(2):259-260.
[4] 欧琴,张芦燕,钱一鑫,等.HPLC法测定舒血宁注射剂黄酮和内酯的含量[J].贵州大学学报:自然科学版,2010,27(5):34-37.
[5] 任玉军,张海燕.高效液相色谱法测定环磷腺苷葡胺注射液含量的方法研究[J].河北医药,2009,31(13):1660-1661.
[6] 李秀梅,黄罗生,富志军.光照条件对红花黄色素稳定性的影响[J].海峡药学,2011,23(5):64-66.
[7] 国家药典委员会.中华人民共和国药典:二部[S].2010年版.北京:中国医药科技出版社,2010:附录:99-101.
[8] 张蓬华,肖淼生,张静,等.舒血宁与五种注射液配伍后的稳定性考察[J].中国药师,2009,12(2):259-260.
(编校:王俨俨)
Compatible stability of Shuxuening injection and meglumine adenosine cyclophosphate injection
ZHANG Chen-huaΔ
(Department of Pharmacy, The First People’s Hospital in Zhejiang Taizhou, Taizhou 318020, China)
ObjectiveTo study the compatibility stability of Shuxuening injection and meglumine adenosine cyclophosphate injection.MethodsThe compatibility program of Shuxuening injection and meglumine adenosine cyclophosphate injection was optimized by orthogonal experimental design, with the main components total flavone of Ginkgo biloba (quercetin, kaempferide and isorhamnetin as control substance) and Ginkgo lactone (ginkgolide A, B and C as control substance) of Shuxuening injection, the principal components adenosine cyclophosphate (denosine cyclophosphate as control substance) of meglumine adenosine cyclophosphate injection as the main index to draw calibration curve, select temperature (A), illumination (B),storage time (C) and solvent (D) as factor, the change of insoluble particles and pH in solution was studied also.ResultsThe optimal compatibility conditions of orthogonal experimental design was A2B1C1D1(25 ℃, lucifugal, storage time of 1 h,5% glucose solution), ANOVA results showed that temperature (A), illumination (B) and storage time (C) have significant effects on quercetin and kaempferide contents in Shuxuening injection (P<0.05), however, solvent (D) has no significant effect on them.The temperature (A), illumination (B),storage time (C) and solvent (D) have significant effects on the other five substances (P<0.05).At 0, 1, 4, 6 h, the appearance and pH value of compatible solution (A2B1C1D1)were not significantly changed and the number of insoluble particles in accordance with the relevant provisions of the Chinese Pharmacopoeia with storage time increasing.ConclusionThe compatible stability of Shuxuening injection and meglumine adenosine cyclophosphate injection is good under certain conditions, and could use compatibility in clinical therapy.
Shuxuening injection; meglumine adenosine cyclophosphate injection; compatibility stability; orthogonal experiment; optimize
张晨华,男,通讯作者,大专,副主任药师,研究方向:临床药学及医院药学,E-mail: 3326764232@qq.com。
R969.3
A
1005-1678(2015)09-0164-06

