以三苯基膦为保护剂制备纳米金溶胶
邵霞,索掌怀
以三苯基膦为保护剂制备纳米金溶胶
邵霞,索掌怀
(烟台大学化学化工学院,山东烟台264005)
以三苯基膦(PPh3)为保护剂,采用水相化学还原法制备了纳米金溶胶.利用紫外可见分光光度计和透射电子显微镜对纳米金颗粒的尺寸及形貌进行表征.讨论了还原剂种类与用量、保护剂用量与加入方式、金粒子浓度、溶液pH值等因素对纳米金颗粒粒径、形貌和分散性的影响.结果表明:采用硼氢化钠为还原剂时,PPh3与金质量比为0.02∶1,溶液pH值为7,制得纳米金粒子平均粒径为4~5 nm.采用柠檬酸钠为还原剂时,PPh3与金质量比为0.04∶1,柠檬酸钠与金质量比为10∶1,溶液pH=3~4,制得金粒子平均粒径为13~15 nm.采用草酸为还原剂时,PPh3与金质量比为0.08∶1,草酸与金质量比为3∶1,金前驱液pH值为6,制得金粒子平均粒径为23~25 nm.加入保护剂后,粒子的分散性增强,形状不规则粒子增多.
纳米金溶胶;三苯基膦;硼氢化钠;柠檬酸钠;草酸
纳米金溶胶具有独特的物理、化学性质,使其在催化、光电、信息存储、诊断医疗、生化分析、微生物检测等方面备受关注[1-6].表面结构的控制与功能化一直是纳米材料研究的关键.在金溶胶中引入表面分子与修饰基团不仅可以控制金核的尺寸、形状、分散性,而且可使其表面进一步功能化[3].目前,在纳米金表面引入配体一是在粒子合成时直接加入表面活性剂[7];二是先合成表面修饰剂稳定的纳米金粒子,再通过表面的配体取代反应引入特定基团[8].但这2种方法都存在一定的局限性.寻找一种易于进一步表面功能化的纳米金粒子的合成策略能够大大促进纳米金的应用.纳米金颗粒可与氨基发生非共价的静电吸附,或与巯基形成强的Au-S共价键[9],像硫醇、四烷基胺等[10-11]修饰金纳米粒子、控制其颗粒大小的方法已有文献报道.由于这些分子不容易再被其他配体所取代,从而使其应用在一定程度上受到了限制.
三苯基膦(PPh3)是常见的含磷化合物,应用于医药工业、有机合成、分析等领域,还可作为染料工艺的增光剂、高分子聚合剂,彩色胶卷显像的抗氧剂及聚环氧化的稳定剂等.PPh3中的P原子易于与金属形成配合物,如Pd(PPh3)4被广泛应用于钯催化偶联反应中的催化剂,Rh(PPh3)3Cl为烯烃催化加氢催化剂(即Wilkinson's催化剂).Schwerdtfeger等[12]报道,P原子易于与Au配位结合.PPh3中的Ph基团也很容易被别的官能团修饰或取代[13].Hutchison等[8]报道,以Au55(PPh3)12Cl6为反应物,通过配体交换法,可以生成直径约为1.7 nm的巯基稳定的纳米金颗粒.通过这种配体交换法,不仅易于在金纳米晶体的周围生成不同尺寸、功能和物理性质的配位体外壳,同时还能保持金颗粒的大小不发生改变,这为制备含有不同官能团的配体修饰的纳米金粒子开拓了一种新的方法.
本实验以PPh3为稳定剂,采用水相还原法制备了纳米金溶胶,研究了还原剂种类、还原剂用量、保护剂用量、加入方式、金粒子浓度、pH值等因素对纳米金颗粒粒径、形貌、和分散性的影响,获得了尺寸、形貌等比较规则的纳米金颗粒.
1 实验部分
1.1 试剂与仪器
氯金酸(HAuCl4·H2O分析纯,上海稀有金属研究所),三苯基膦(PPh3化学纯,国药集团化学试剂有限公司),硼氢化钠(NaBH4化学纯,含量≥96.0%,国药集团化学试剂有限公司),柠檬酸钠(Na3C6H5O7分析纯,天津市瑞金特化学品有限公司),草酸(H2C2O4分析纯,天津市巴斯夫化工有限公司).
PHS-29A型精密酸度计,85-2型恒温磁力搅拌器,TU-1901型紫外-可见分光光度计,JEOL JEM-1400型透射电子显微镜
1.2 纳米金溶胶的制备及表征
1.2.1 纳米金溶胶的制备硼氢化钠为还原剂时:取1 mL 5 mmol/L的氯金酸溶液于50 mL水中,用0.1 mol/L NaOH调节pH值为7.0,逐滴加入新鲜配置的1 mg/mL NaBH4至溶液变为酒红色,加入0.2 mg/mL PPh3溶液,继续搅拌0.5 h以上.
柠檬酸钠为还原剂时:取1 mL 5 mmol/L的氯金酸溶液于50 mL水中,加热至沸腾,加入0.2 mg/ mL PPh3溶液,加入10 mg/mL柠檬酸钠溶液,搅拌0.5 h后凉至室温.
草酸为还原剂时:取1 mL 5 mmol/L的氯金酸溶液于50 mL水中,用0.1 mol/L NaOH调节pH值为6.0,加入1 mg/mL草酸溶液,加热至沸腾,继续加入0.2 mg/mL PPh3溶液,搅拌0.5 h后凉至室温.
为使最终制备的纳米金溶胶具有最好的稳定性,需进行制备条件优化实验.优化实验中各试剂用量,请参照下文中的实验结果与讨论.
1.2.2 纳米金溶胶的表征利用TU-1901型紫外-可见分光光度计测定金溶胶的紫外-可见光谱.利用JEOL JEM-1400型透射电子显微镜观察胶体金纳米粒子的尺寸和形貌.将制备得到的纳米金溶胶滴在镀有碳膜的铜网上,干燥后,放入透射电镜样品台摄取TEM图像.
2 结果与讨论
2.1 PPh3保护剂加入方式的影响
在讨论保护剂用量对于生成纳米金颗粒的影响之前,先对保护剂的加入方式予以讨论.在实验中采用了先加保护剂后加还原剂、先加还原剂后加保护剂以及二者一起加入的3种加入方式.本实验发现:以硼氢化钠和草酸为还原剂时,先加还原剂后加保护剂效果要好;以柠檬酸钠为还原剂时,则是先加保护剂后加还原剂效果更优.由于P原子易于与Au配位结合,如果先加入保护剂,PPh3会迅速与金粒子结合,此时再加入还原剂将金粒子还原形成更小的颗粒,不利于金颗粒的稳定;而以柠檬酸钠为还原剂时,由于柠檬酸钠本身具有较强的保护剂作用,在还原金颗粒的同时能进一步保持金粒子的稳定性.
2.2 PPh3保护剂用量的影响
金属颗粒的最大吸收峰位置随着颗粒尺寸的减小而蓝移,这是因为纳米颗粒的量子尺寸效应,使得被占据和未被占据分子轨道能级之间的能隙随颗粒直径的减小而增大,导致光吸收带向短波方向移动.通常,较窄的半峰宽对应的纳米金粒子粒径分布也较窄.谱峰的最大吸收峰位置可以粗略的表征粒子的粒径,波长越大,粒径越大,峰强度则表示了金粒子的浓度[2].
图1为3种还原剂下加入不同PPh3用量制备的金溶胶紫外吸收谱图.图2反映了所得金溶胶的最大吸收波长与PPh3/Au质量比的关系.可以看出,随PPh3加入量的增加,金溶胶的最大吸收峰发生红移,半峰宽增加,说明生成的金颗粒的粒径增加,粒径分布范围变宽.采用不同还原剂还原金溶液,所得金溶胶的最大吸收峰的形状与位置均发生变化,其中以硼氢化钠还原制备的金溶胶变化明显,而以柠檬酸钠及草酸还原制备的金溶胶变化较小.
由于PPh3中的P原子能和Au原子配位结合,使得金粒子在溶胶中得到稳定并分散.随着PPh3量的增加,与金纳米粒子表面结合的PPh3中的苯基使金纳米粒子表面趋向于疏水状态,从而导致纳米金粒子发生不同程度的聚集.因此随着PPh3量的增加,金粒子粒径变大,且粒径分布变宽.
2.3 还原剂用量的影响
还原剂用量对金溶胶的最大吸收峰也有明显的影响.从图3可以看出,柠檬酸钠还原的金溶胶在520 nm附近出现纳米金的表面等离子体共振吸收峰.随柠檬酸钠用量的增加,此吸收峰发生红移,且半峰宽变大,说明生成的金颗粒粒径不断变大,且粒径分布变宽.因为柠檬酸钠不仅起到还原剂的作用,同时起到保护剂的作用[14].柠檬酸钠加入量过多,柠檬酸根在金晶核表面已经吸附饱和,过多钠离子的存在会中和金颗粒表面的负电荷,降低颗粒间的静电排斥力,导致溶胶的团聚,从而使得颗粒变大,因此柠檬酸钠的添加量不宜过高.

图2 3种还原剂下金溶胶最大吸收波长与PPh3/Au质量比的关系Fig.2 Maximum absorption wavelength of gold colloids as afunction of PPh3/Au mass ratios at three reducing agents

图3 不同还原剂与金质量比制备的金溶胶紫外吸收谱Fig.3 UV-Vis spectra of gold colloids as a function of reducing agents/Au mass ratios
采用草酸作还原剂时,金溶胶吸收峰随草酸用量的增加先蓝移后红移(图4).这是因为草酸对纳米金溶胶也具有一定稳定作用[15],刚开始加入的草酸量过少不足以将金颗粒完全还原,因此随着草酸用量的增加金溶胶吸收峰发生蓝移.当草酸与金质量比为3∶1时达到最小值(530 nm),且半峰宽没有明显变化,说明此时生成的金颗粒粒径最小.而随着草酸加入量的过多,其原理和柠檬酸钠相同,添加量过多会使金颗粒变大.
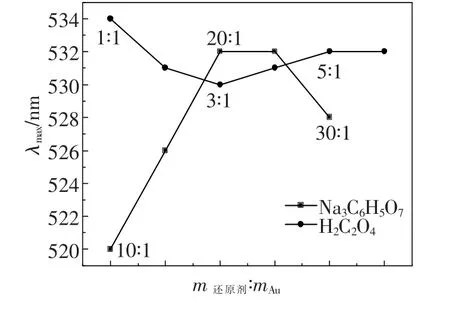
图4 金溶胶最大吸收波长与还原剂用量的关系Fig.4 Maximum absorption wavelength of gold colloids as a function of reducing agent amount.
2.4 金溶液pH值的影响
金前驱液的pH值也会影响金溶胶的紫外吸收.图5是在不同pH值下,以硼氢化钠和草酸为还原剂时制备的金溶胶的紫外吸收光谱.图5所示,对不同pH值下制备的金溶胶,其最大吸收峰位置(525 nm)都没有发生明显的变化,但峰形变化显著.以硼氢化钠为还原剂时,在金前驱液pH=7.0时所得金溶胶的紫外吸收峰峰形较好,金的粒径分布最为均一;以草酸为还原剂时,则是pH=6.0的峰形较好.在更高pH值下以及草酸为还原剂pH= 5.0时,发现在600 nm以上也出现吸收峰,表明溶液中有更大的金粒子存在.这是因为在金前驱体溶液中,金物种以[Au(OH)xCl4-x]-存在形式,其中x与溶液pH值有关[16-17].而金物种的存在形式不仅会影响金物种与还原剂的作用,也会影响所得金粒子的尺寸大小与分布[18].

图5 不同pH值下制备的金溶胶的紫外吸收光谱Fig.5 UV-Vis spectra of gold nanoparticles reduced under different pH values of gold solution
实验还发现,当以柠檬酸钠为还原剂时,只有pH值为3~4的金前驱体溶液能生成相对稳定的金溶胶,而在其他pH值下,加入还原剂后立即生成黑色沉淀,表明得到的金粒子不稳定,容易聚沉.
2.5 金溶液浓度的影响
除了金溶液的pH值外,金溶液的浓度也会影响所得金溶胶的紫外吸收峰.正如图6所示,随着氯金酸浓度的增大,使用3种还原剂所得金溶胶的最大吸收峰位置都没有发生变化,但硼氢化钠和草酸制备的金溶胶的峰形对称性较差,且在600 nm以上出现吸收峰.说明所得金溶胶中金粒子的尺寸大小均一性逐渐变差,而以柠檬酸钠为还原剂制备的金粒子具有相对均匀的粒径尺寸.
由于金粒子具有亲金的性质,在溶液中易形成键能几乎与氢键相等的Au—Au键[9],使得溶液中金粒子容易发生聚集.而保护剂的加入,可以有效地避免金粒子的聚集,增强金溶胶的稳定性.文献中报道,柠檬酸钠本身具有保护剂的作用[14],因此在加入等量的保护剂、还原剂的条件下,增大氯金酸浓度,柠檬酸钠还原的金溶胶粒子具有更好的均一性.而草酸虽然也有保护剂的作用,但相对于柠檬酸钠,其保护作用较弱[15],硼氢化钠本身并没有保护剂的作用,因此二者的均一性随着金粒子的浓度增加而变差.
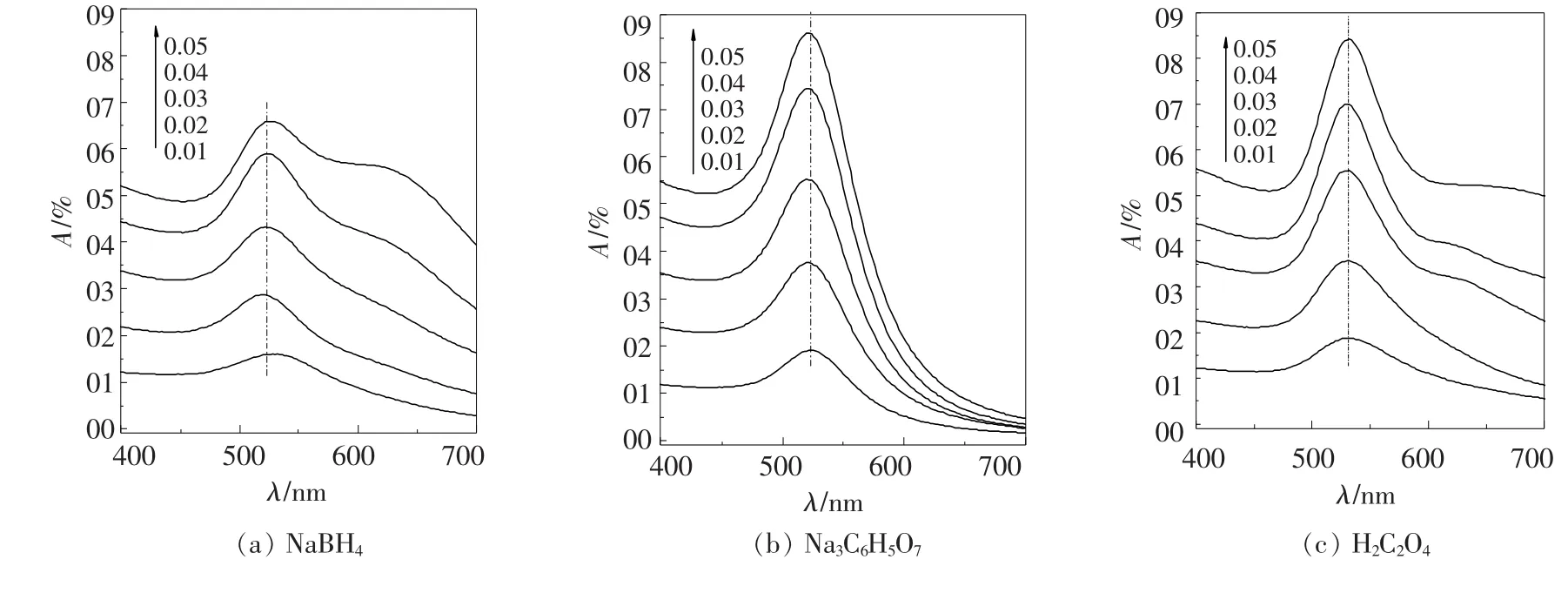
图6 金前期躯体溶液浓度对金溶胶紫外吸收光谱的影响Fig.6 UV-Vis spectra of gold nanoparticles as different concentration of Au solution
2.6 金粒子的TEM照片及粒子大小分布
在优化的制备条件下,采用3种不同还原剂制备了纳米金溶胶,其紫外吸收光谱示于图7.相对于柠檬酸钠还原制备的纳米金溶胶的吸收峰峰位,硼氢化钠还原制备的发生蓝移,而草酸还原制备的红移十分明显,由此可推断3种还原剂制备的纳米金颗粒粒径:NaBH4<Na3C6H5O7<H2C2O4.
透射电镜实验进一步证明了这一结论.图8为3种还原剂在加保护剂PPh3及不加保护剂时制得的纳米金颗粒TEM照片及其粒子大小分布.从图8所得,以NaBH4、Na3C6H5O7、H2C2O4为还原剂制备的纳米金颗粒平均粒径分别为4~5 nm、13~15 nm、23~25 nm,说明3种还原剂的还原能力为NaBH4>Na3C6H5O7>H2C2O4.虽然NaBH4还原产生的金粒子尺寸小,但也有一定程度的聚集,600 nm以上出现的吸收峰也说明有较大的粒子存在; H2C2O4还原制备的金粒子也以团簇形式分散,但其聚集程度不及NaBH4;而Na3C6H5O7还原制备的金粒子则以单分子形式分散在溶胶中.这是由于柠檬酸钠和草酸本身对金粒子具有一定的保护和分散作用,因此金粒子分散性要明显优于硼氢化钠还原制备的金粒子.加入一定量PPh3保护剂后,金粒子的分散性明显得到提高.

图73 种还原剂制备的金溶胶紫外吸收谱图Fig.7 UV-Vis spectra of gold nanoparticles prepared using three different reducing agents
从金粒子形貌上看,以NaBH4,Na3C6H5O7为还原剂制备的金粒子呈圆球形.而以H2C2O4为还原剂制备的金粒子大部分呈圆球形,但也存在三角形、六边形等,而加入PPh3后,三角形、六边形金粒子明显增多,这为制备不同形貌的纳米金粒子提供了一条新思路.
3 结论
本研究以三苯基膦为保护剂,硼氢化钠、柠檬酸钠、草酸为还原剂制备纳米金溶胶,优化其制备条件.实验发现,最优条件下3种还原剂制备金颗粒的平均粒径为:硼氢化钠4~5 nm,柠檬酸钠13~15 nm,草酸23~25 nm,说明其还原能力:NaBH4>Na3C6H5O7>H2C2O4.加入保护剂三苯基膦后,金颗粒的分散性都有不同程度的提高.柠檬酸钠和草酸由于本身带有保护剂作用还原制备的金溶胶分散性明显优于硼氢化钠,H2C2O4还原制备的金粒子以团簇形式分散,而Na3C6H5O7还原制备的金粒子则以单分子形式分散在溶胶中.3种还原剂制备的金粒子大部分呈圆球形,当草酸为还原剂时,出现三角形、六边形等形状,加入PPh3后,三角形、六边形金粒子明显增多.

图8 在3种还原剂及PPh3保护剂存在下制备的纳米金颗粒TEM照片及粒径分布图Fig.8 TEM photographs and particle distribution of gold nanoparticles prepared at different reducing agent and PPh3protective agent
[1]Liu Bin,Wang Xiaoman,Zhao Yanwei,et al.Polymer shell as a protective layer for the sandwiched gold nanoparticles and their recyclable catalytic property[J].Journal of Colloid and Interface Science,2013,395:91-98.
[2]Daniel M C,Astruc D.Gold nanoparticles:assembly,supramolecular chemistry,quantum-size-related properties,and applications toward biology,catalysis,and nanotechnology[J].Chemical Reviews,2004,104(1):293-346.
[3]Alexandridis P.Gold nanoparticle synthesis,morphologycontrol,and stabilization facilitated by functional polymers[J].Chemical Engineering&Technology,2011,34(1):15-28.
[4]Yu Yu-ying,Chang Ser-sing,Lee Chien-liang,et al.Gold nanorods:electrochemical synthesis and optical properties[J].The Journal of Physical Chemistry B,1997,101(34): 6661-6664.
[5]Pannerec-Varna M,Ratajczak P,Bousquet G,et al.In vivo uptake and cellular distribution of gold nanoshells in a preclinical model of xenografted human renal cancer[J].Gold Bulletin,2013,46(4):257-265.
[6]Tsai T H,Thiagarajan S,Chen Shenming,et al.Ionic liquid assisted synthesis of nano Pd—Au particles and application for the detection of epinephrine,dopamine and uric acid[J].Thin Solid Films,2012,520(7):3054-3059.
[7]Brust M,Walker M,Bethell D,et al.Synthesis of thiolderivatised gold nanoparticles in a two-phase liquid-liquid system[J].Chemical Communications,1994(7):801-802.
[8]Brown L O,Hutchison J E.Convenient preparation of stable,narrow-dispersity,gold nanocrystals by ligand exchange reactions[J].Journal of the American Chemical Society,1997,119(50):12384-12385.
[9]Caracelli I,Zukerman-Schpector J,Tiekink E R T.Supra-molecular synthons based on gold…π(arene)interactions[J].Gold Bulletin,2013,46(2):81-89.
[10]Makosch M,Bumbálek V,Sá J,et al.Alternative preparation of size-controlled thiol-capped gold colloids[J].Gold Bulletin,2013,46(3):161-164.
[11]Dumur F,Guerlin A,Dumas E,et al.Controlled spontaneous generation of gold nanoparticles assisted by dual reducing and capping agents[J].Gold Bulletin,2011,44(2):119 -137.
[12]Schwerdtfeger P.Gold goes nano—from small clusters to low-dimensional assemblies[J].Angewandte Chemie International Edition,2003,42(17):1892-1895.
[13]Lu Yadong,Wang Yanhua,Jin Zilin.Rh nanoparticles stabilized by PEG-substituted triphenyl-phosphine:A highly active and recyclable catalyst for aqueous biphasic hydrogenation of benzene[J].Chinese Chemical Letters,2010,21(9):1067-1070.
[14]Zhou Jingfang,Ralston J,Sedev R,et al.Functionalized gold nanoparticles:synthesis,structure and colloid stability[J].Journal of Colloid and Interface Science,2009,331(2): 251-262.
[15]兰新哲,金志浩.PVP保护还原法制备纳米金溶胶[J].稀有金属材料与工程,2003,32(1):50-53.
[16]Lee S J,Gavriilidis A.Supported Au catalysts for lowtemperature CO oxidation prepared by impregnation[J].Journal of catalysis,2002,206(2):305-313.
[17]Moreau F,Bond G C,Taylor A O.Gold on titania catalysts for the oxidation of carbon monoxide:control of pH during preparation with various gold contents[J].Journal of Catalysis,2005,231(1):105-114.
[18]金明善,原慧卿,荆济荣,等.纳米金粒子与R-藻红蛋白的相互作用[J].高等学校化学学报,2009(6): 1183-1188.
Preparation of Nanogold Colloid Using Triphenylphosphine as Protective Agent
SHAO Xia,SUO Zhang-huai
(School of Chemistry and Chemical Engineering,Yantai University,Yantai,264005,China)
Nanogold colloid is synthesized by chemical reduction using triphenylphosphine(PPh3)solution as protective agent.UV-Vis spectroscopy and transmission electron microscopy(TEM)are used to characterize the prepared Au nanoparticles.Some factors such as the type and the amount of reducing agent,the adding way and the amount of protective agent,the concentration and pH value of Au solution,which affects the particle size,morphology and dispersion of Au nanoparticles,are discussed.The results show that the optimized processing parameters for preparing gold nanoparticles using NaBH4with an average diameter from 4 to 5 nm are:mPPh3∶mAu=0.02∶1,pH= 7.The optimal conditions obtained for making gold nanoparticles using Na3C6H5O7with particle size from 13 to 15 nm are:mPPh3∶mAu=0.04∶1,mNa3C6H5O7∶mAu=10∶1,pH=3-4.The size of Au nanoparticles prepared with H2C2O4is within the range of 23~25 nm.The optimal conditions are mPPh3∶mAu=0.08∶1,mH2C2O4∶mAu=3∶1,pH =6.After adding a certain amount of PPh3,colloidal gold nanoparticles show higher dispersion and more irregular shapes.
nanogold colloid;triphenylphosphine;sodium borohydride;sodium citrate;oxalic acid
O643
A
(责任编辑 周雪莹)
1004-8820(2015)03-0173-06
10.13951/j.cnki.37-1213/n.2015.03.005
2014-12-10
国家自然科学基金资助项目(21273193);山东省自然科学基金资助项目(ZR2011BM024).作者简介:邵霞(1989-),女,山东青岛人,硕士研究生.
索掌怀(zhsuo@ytu.edu.cn),教授,博士,主要从事纳米贵金属催化剂的制备与应用研究.

