长期抗病毒治疗对慢性乙型肝炎疗效的Meta分析
唐亚宁,吴 波,唐 文,2,赵 艳,杨梅媚,2
(1.成都市妇女儿童中心医院,四川 成都 610091;2.成都市第五人民医院,四川 成都 611130)
长期抗病毒治疗对慢性乙型肝炎疗效的Meta分析
唐亚宁1,吴 波1,唐 文1,2,赵 艳1,杨梅媚1,2
(1.成都市妇女儿童中心医院,四川 成都 610091;2.成都市第五人民医院,四川 成都 611130)
目的:系统评价长期抗病毒治疗[干扰素和核苷(酸)类药物]对防止慢性乙型肝炎(慢乙肝)进展到肝癌和死亡的疗效。方法:检索PubMed、Cochrane图书馆、Web of Science、EMbase、CBM-disc和CNKI等数据库中关于抗病毒治疗治疗慢乙肝的随机对照研究(RCT)。截止时间设定为2014年11月。评价指标包括肝癌和死亡率。结果:纳入16篇RCT,共1 814名慢乙肝患者。Meta分析结果表明,抗病毒治疗可以降低肝癌发生率(OR=0.57,95%CI=0.35~0.92)和死亡发生率(OR=0.52,95%CI=0.34~0.80)。亚组分析结果表明核苷(酸)类药物比干扰素的效果更明显。各个Meta分析中不存在显著的异质性和发表偏倚。结论:长期抗病毒治疗对降低肝癌发生率和死亡率有显著疗效,核苷(酸)类药物效果可能比干扰素的效果更好。
抗病毒治疗;乙型肝炎;肝癌;死亡;Meta分析
全世界大约有20亿人感染了乙型肝炎病毒。乙型肝炎病毒可能导致肝癌、肝硬变和肝功能衰竭,每年大约有60万人死于肝炎[1]。在引发死亡的癌症中,肝癌在男性中排第5位,女性中排第6位[2-3]。虽然疫苗确实能减少乙型肝炎的发病率[4-5],但是由于慢性乙型肝炎(慢乙肝)患者发病率高,乙型肝炎病毒引起的肝癌、肝硬变所导致的死亡率却在上升[6]。目前,推荐的抗病毒治疗方法有干扰素和核苷(酸)类药物[7],其目的就是防止慢乙肝患者进展到肝癌及死亡[8]。但是,既往临床研究和Meta分析对这两种治疗方式疗效的结论并不一致[9-10]。有Meta分析认为抗病毒治疗能降低肝病相关的死亡率[11],而有的随机对照试验则认为其对防止肝癌和死亡的发生并无显著效果[12-13]。本研究利用Meta定量分析已有的随机对照试验,客观评价抗病毒治疗方式对防止慢乙肝患者走向肝癌和死亡的疗效,为临床提供理论依据。
1 资料与方法
1.1 文献检索 通过计算机检索PubMed、Cochrane图书馆、EMbase和Web of Science等外文数据库和中国知识基础设施工程(China national knowledge infrastructure,CNKI)、中国生物医学文献数据库(China biomedical literature database,CBM)等中文数据库,截止时间设为2014年11月。文献检索中,英文检索词为hepatitis B或者hepatitis B virus或者HBV与antiviral therapy或者interferon或者nucleos(t)ide analogues的组合,中文检索词为乙型肝炎或者乙型肝炎病毒与抗病毒治疗或者干扰素或者核苷(酸)类的组合。为了避免遗漏相关文献,对会议摘要和纳入文献的参考文献进行检查。
1.2 纳入与排除标准 该研究主要分析抗病毒治疗[干扰素或者核苷(酸)类药物]对慢乙肝疗效的随机对照试验(Randomized controlled trial,RCT),因此实验组患者必须是接受干扰素或者核苷(酸)类药物治疗,对照组患者接受常规治疗,同时对照组患者属于未接受任何抗病毒治疗的患者。只纳入RCT是为了使得到的结论更可靠,所以符合以下条件之一的文献将会被排除:(1)使用同一数据的重复文献;(2)病例报道和系统评价;(3)回顾性研究。另外,由于有些文献在纳入患者时并没有对患者进行超声波检测,可能疏忽有些患者已经存在小范围肝癌的事实,故选择12个月作为截止时间点,随访未达12个月的文献也将会被排除。同时12个月也将作为长期治疗的截止时间点。
1.3 文献质量评价 采用Cochrane协作网推荐的评估方法对初步纳入的文献质量及方法学进行评估[14]。评价内容主要包括涉及实验内部真实性的指标,如所用的是否随机、是否使用盲法(单盲或双盲)、是否说明失访或退出的人数及理由、2组患者的基线资料是否匹配等。有2项及2项以上存在高风险的初步纳入文献也将被排除。纳入文献的质量评价由2位研究者独立完成,并相互验证,达成一致后决定文献最终的纳入排除。
1.4 数据提取 2名评价者根据纳入排除标准,独立筛选所有候选文献,评估纳入文献的质量并提取数据。筛选提取过程中产生的任何争议,与第3方讨论解决。对于不能直接提取所需数据的文献,将通过邮件与文献作者联系取得,或查看引用该文献的文献中是否提及所需数据。数据的提取包括:每组总人数,纳入患者的人口学资料和临床资料,主要评价指标肝癌人数,次要评价指标死亡人数,患者治疗后是否患肝癌的诊断使用推荐标准[15]。
1.5 数据分析 数据统计分析采用RevMan 5.1软件。使用该软件中的I2和Q检验进行异质性检验,如果I2<50%且P>0.10,则认为无异质性,选用固定效应模型,否则选用随机效应模型。如果存在异质性且无法判断异质性的来源,则不进行Meta分析,采用描述性分析。风险比率(odds ratio,OR)和95%置信区间(confidence interval, CI)作为计数数据的模型效应参数。采用倒漏斗图对潜在的发表偏移进行评估。
2 结 果
2.1 文献筛选 最初检索到2 134篇文献,其中中文468篇、外文1 666篇。依据纳入排除标准,根据文章标题排除1 228篇文献,根据摘要排除634篇,根据全文排除256篇文献,最后只有16篇RCT被初步纳入[16-29,12-13],其中8篇中文、8篇英文。所有步骤由2位研究者独立完成,筛选提取过程中产生的争议,与第3方讨论解决。
2.2 纳入文献的特征 详见表1(其中I为干预组,C为对照组。下同)。纳入的16篇RCT文献随访时间从1~11年,其中6篇使用干扰素治疗,10篇使用核苷(酸)类药物治疗。
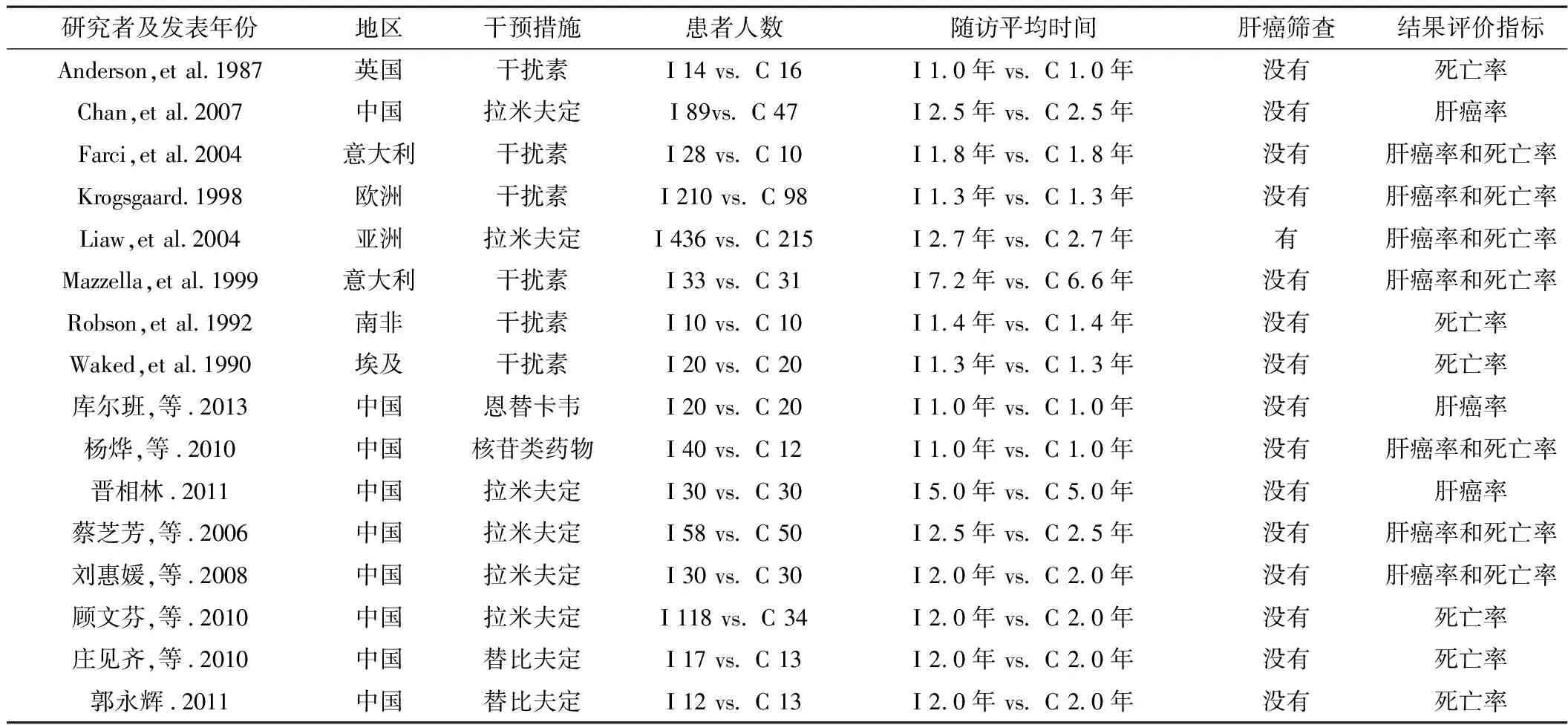
表1 纳入文献的特征资料
2.3 纳入患者的基线资料 详见表2。纳入文献共有1 814例慢乙肝患者,其中接受抗病毒治疗1 165例,接受常规治疗方式的有649例。纳入文献中患者男性比例45%~100%;患者年龄19~67岁;纳入时已有肝硬变的患者比例0%~100%。初步纳入的16篇RCT文献都使用了随机分组,且没有存在2项或2项以上高风险的文献,因此最终纳入Meta分析的RCT文献有16篇。
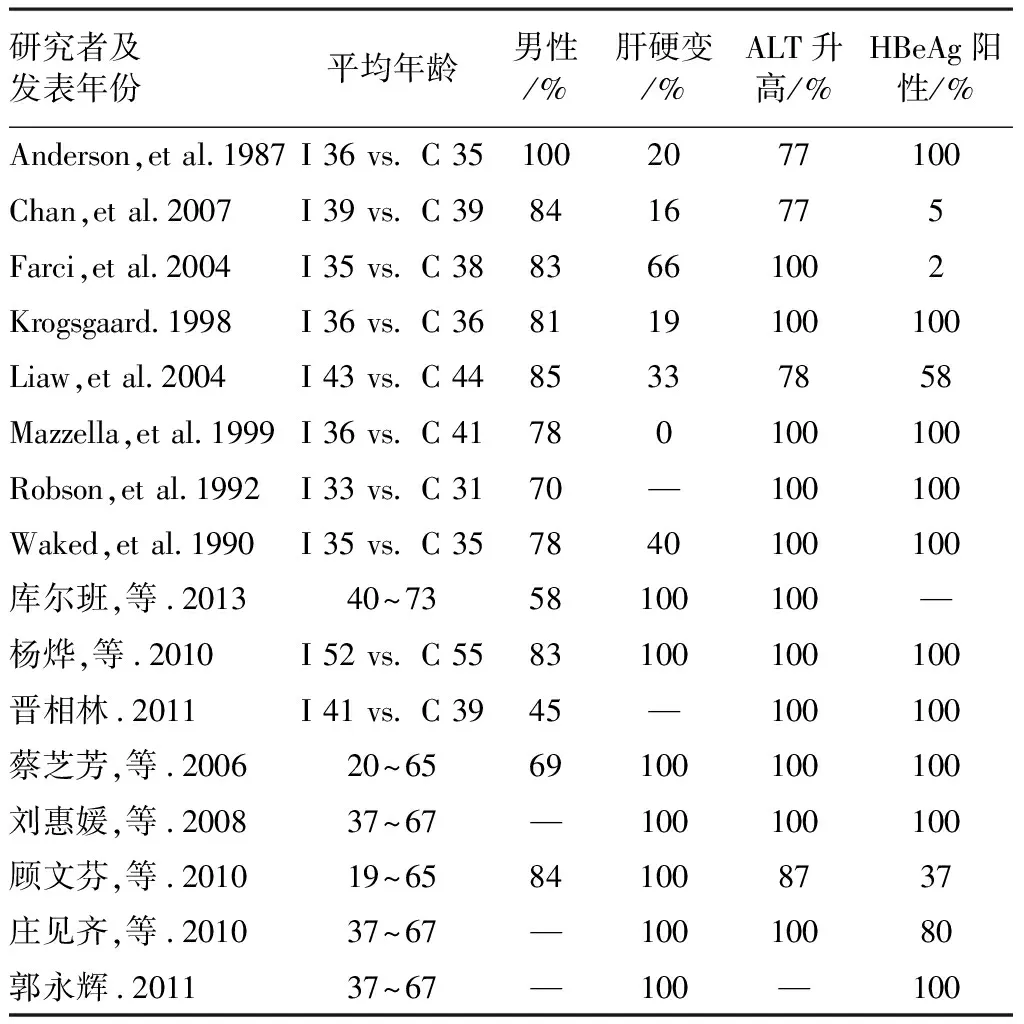
表2 纳入患者的基线资料
2.4 肝癌率的Meta分析 肝癌率的Meta分析包括10篇RCT文献,共1 517名慢乙肝患者,其中治疗组的974名患者中有41名确诊为肝癌,对照组的543名患者中有39名确诊为肝癌。固定效应模型得到的OR值为0.57 (95%CI=0.35~0.92),这表明在防止肝癌发生率方面,抗病毒治疗的有效率显著性高于常规治疗方式。经检验,各个研究之间无异质性存在(I2=0%,P=0.93)。同时,倒漏斗图基本对称,说明结果没有明显的发表偏倚,表明该Meta分析的结果未受到发表偏倚的影响。
2.5 死亡率的Meta分析 包括13篇RCT文献,共1 578名慢乙肝患者。其中,治疗组的1 026名患者中有47名最终死亡,对照组的552名患者中有48名最终死亡。固定效应模型得到的OR值为0.52 (95%CI=0.34~0.80),表明在防止死亡率方面,抗病毒治疗的有效率显著性高于常规治疗方式。经检验,各个研究之间无异质性存在(I2=2%,P=0.43)。同时,倒漏斗图基本对称,说明结果没有明显的发表偏倚,表明该Meta分析的结果未受到发表偏倚的影响。
2.6 亚组分析 推荐的抗病毒治疗方法有干扰素和核苷(酸)类药物2种。亚组分析结果显示,干扰素组的肝癌和死亡发生率方面较常规治疗组低,但无显著性差异,OR值分别为0.49(95%CI=0.13~1.38)和0.75(95%CI=0.34~1.67);核苷(酸)类组的肝癌和死亡发生率方面较常规治疗组低,且有显著性差异,OR值分别为0.58(95%CI=0.35~0.97)和0.44(95%CI=0.26~0.74)。
3 讨 论
慢乙肝严重危害人的身体健康,给个人及家庭乃至社会造成沉重的经济负担。在中国大约有2亿人感染了乙型肝炎病毒,其中约15%~20%发展成慢乙肝。慢乙肝反复发作,肝纤维逐渐增生,如不能及时有效地治疗,最终可能会导致患者患上肝癌甚至死亡。
目前,有效的抗乙肝病毒的药物非常有限,推荐的抗病毒治疗方法主要是干扰素和核苷(酸)类药物。干扰素治疗可以减少血清中的乙肝病毒脱氧核糖核酸,并改善患者的临床及肝功能。干扰素并不直接抑制或杀死病毒,而是通过产生抗病毒蛋白来抑制病毒的复制,同时提高机体的免疫功能。临床应用中须注意干扰素的疗效与疗程成正比关系,一般疗程为1年,但在某些特殊情况下,延长治疗时间能获得更满意的疗效。核苷(酸)类药物已经渐渐成为慢性乙肝的首要治疗措施,主要有拉米夫定、阿德福韦、恩替卡韦、替比夫定和替诺福韦。长期接受核苷(酸)类药物治疗可持续抑制乙肝病毒的复制,能够有效防止慢性乙肝进展到肝癌和相关的死亡,从而改善患者的生活质量,延长患者的生存时间。
干扰素不良反应的几种常见类型及处理方法有:流感样不良反应可服用解热镇痛药;中性粒细胞和血小板减少可选择降低干扰素剂量,待恢复后增加至原剂量;食欲下降、乏力、体质量减轻及脱发无须特殊处理;精神异常可选择抗抑郁药,若严重则停用干扰素;皮肤反应须注意观察,若较严重甚至全身皮疹则须立即停药。核苷(酸)类药物抗病毒治疗时须关注发生乳酸酸中毒的潜在风险,同时耐药是影响这类药物疗效的重要障碍。临床实践中,主要通过检测HBV复制水平、肝脏生化指标以及随访等方式监测耐药性。另外,了解患者的既往治疗情况、选择强效及高耐药基因屏障的药物作为初始用药、避免单药随意序贯等方式都能有效防止耐药性的发生[30]。
必须指出,该研究也存在局限性:(1)未分析抗病毒治疗的短期疗效;(2)尚不清楚结果是否适用于青少年患者;(3)纳入文献数量有限,无法确定最佳的治疗时间;(4)相关文献较少,没有分析不同核苷(酸)类药物对防止肝癌及死亡发生的疗效。
综上所述,长期抗病毒治疗可以降低慢乙肝进展到肝癌和死亡的概率,核苷(酸)类药物效果可能比干扰素的效果更好。该研究结果有助于临床医师为慢乙肝患者制定优化的治疗方案,提高患者的生活质量和生存时间,值得临床推广。
[1]WHO. Position paper:Hepatitis B[Z], 2009.
[2] EL-SERAGHB.Hepatocellular carcinoma[J].N Engl J Med,2011,365:1118-1127.
[3]EL-SERAG HB. Epidemiology of viral hepatitis and hepatocellular carcinoma[J]. Gastroenterology, 2012, 142(6): 1264-1273.e1.
[4]NI YH, CHANG MH, WU Jia-feng, et al. Minimization of hepatitis B infection by a 25-year Universal vaccination program[J]. J Hepatol, 2012, 57(4): 730-735.
[5]OTT JJ, STEVENS GA, GROEGER J, et al. Global epidemiology of hepatitis B virus infection: New estimates of age-specific HBsAg seroprevalence and endemicity[J]. Vaccine, 2012, 30(12): 2212-2219.
[6]KN LN, XING J, KLEVENS RM, et al. The increasing burden of mortality from viral hepatitis in the United States between 1999 and 2007[J]. Ann Intern Med, 2012, 156(4): U33-271.
[7]PAPATHEODORIDIS G, BUTI M, CORNBERG MA, et al. EASL clinical practice guidelines: management of chronic hepatitis B virus infection[J]. J Hepatol, 2012, 57(1): 167-185.
[8]LOK AS. Does antiviral therapy for hepatitis B and C prevent hepatocellular carcinoma?[J]. J Gastroenterol Hepatol, 2011, 26(2): 221-227.
[9]SHEN Ying-chun, HSU C, CHENG CC, et al. A critical evaluation of the preventive effect of antiviral therapy on the development of hepatocellular carcinoma in patients with chronic hepatitis C or B: A novel approach by using Meta-Regression[J]. Oncology, 2012, 82(5): 275-289.
[10]SINGAL AK,FONTANA RJ. Meta-analysis: oral anti-viral agents in adults with decompensated hepatitis B virus cirrhosis[J]. Aliment Pharmacol Ther, 2012, 35(6): 674-689.
[11]WONG G, YIU K, WONG V, et al. Meta-analysis: reduction in hepatic events following interferon-alfa therapy of chronic hepatitis B[J]. Aliment Pharmacol Ther, 2010, 32(9): 1059-1068.
[12]LIAW YF, SUNG JJ, CHOW WC, et al.Lamivudine for patients with chronic hepatitis B and advanced liver disease[J]. N Engl J Med, 2004, 351(15): 1521-1531.
[13]KROGSGAARD K. The long-term effect of treatment with interferon-alpha 2a in chronic hepatitis B. The Long-Term Follow-up Investigator Group. The European Study Group on Viral Hepatitis (EUROHEP). Executive Team on Anti-Viral Treatment [J]. J Viral Hepat, 1998, 5:389-397.
[14]HIGGINS J, ALTMAN D. Chapter 8: assessing risk of bias in included studies: the Cochrane Collaboration, Cochrane Handbook for Systematic Reviews of Interventions [M]. John Wiley & Sons, Ltd, Chichester, UK, 2011:22-36.
[15]European Assoc Study Liver. European Org Res treatmentCanc.EASL-EORTC clinical practice guidelines:management of hepatocellular carcinoma[J]. Eur J Cancer, 2012, 48(5): 599-641.
[16]ANDERSON MG, HARRISON TJ, ALEXANDER G, et al.Randomised controlled trial of lymphoblastoid interferon for chronic active hepatitis B[J]. J Hepatol, 1986, 3(Supplement 2): S225-S227.
[17]CHAN HL, WANGHao, NIU Jun-qi, et al. Two-year lamivudine treatment for hepatitis B e antigen-negative chronic hepatitis B: a double-blind, placebo-controlled trial[J]. Antivir Ther, 2007, 12(3): 345-353.
[18]FARCI P, ROSKAMS T, CHESSA L, et al. Long-term benefit of interferon a therapy of chronic hepatitis D: Regression of advanced hepatic fibrosis[J]. Gastroenterology, 2004, 126(7): 1740-1749.
[19]MAZZELLA G, SARACCO G, FESTI D, et al. Long-term results with interferon therapy in chronic type B hepatitis: A prospective randomized trial[J]. American Journal of Gastroenterology, 1999, 94(8): 2246-2250.
[20]ROBSON SC, BRICE E, Van RENSBURG C, et al. Safety and efficacy of interferon alpha-2b following prednisone withdrawal in the treatment of chronic viral hepatitis B. A case-controlled, randomised study [J]. S Afr Med J, 1992, 82:317-320.
[21]WAKED I, AMIN M, ELFATTAH SA, et al. EXPERIENCE WITH INTERFERON IN CHRONIC HEPATITIS-B INEGYPT[J]. Journal of Chemotherapy, 1990, 2(5): 310-318.
[22]依娜瓦提克孜·库尔班,吾加巴特.恩替卡韦治疗失代偿性乙肝肝硬变20例疗效观察[J].医学信息,2013,26(4):438-439.
[23]郭永辉.替比夫定治疗失代偿期乙肝肝硬变2年随访观察[J].中国医学创新,2011,8(24):56-57.
[24]杨烨,陈景寿,欧晓娟,等.核苷(酸)类似物治疗失代偿期乙肝肝硬变的随访研究[J].首都医科大学学报,2010,31(5):573-577.
[25]晋相林.拉米夫定对乙肝肿瘤标志物的临床研究[J].河南职工医学院学报,2011,23(6):694-695.
[26]蔡芝芳,尚凤梅,赵文学,等.拉米夫定治疗失代偿期乙肝肝硬变的临床研究[J].西安交通大学学报:医学版,2006,27(6):575-577.
[27]刘惠媛,石裕明.拉米夫定治疗失代偿期乙肝肝硬变的临床研究[J].胃肠病学和肝病学杂志,2008,17(3):240-242.
[28]顾文芬,陈春华,吴剑.拉米夫定治疗乙肝肝硬变失代偿期临床分析[J].华西医学,2010,25(12):2244-2245.
[29]庄见齐,林秀辉,李涛,等.替比夫定治疗失代偿期乙肝肝硬变30例临床观察[J].河北医学,2010,16(1):50-52.
[30]庄辉.核苷(酸)类药物治疗慢性乙型肝炎耐药及其管理专家共识解读[J].医学研究杂志,2013,42(9):1-2.
Long-term Effect of Interferon and Nucleotide Analogues on Treating Chronic Hepatitis B:A Meta-Analysis of Randomized Controlled Trials
TANG Yaning1, WU Bo1, TANG Wen1,2, ZHAO Yan1, YANG Meimei1,2
(1.Chengdu Women’s & Children’s Center Hospital,Sichuan Chengdu 610091,China;
2.Chengdu Fifth People’s Hospital,Sichuan Chengdu 611130,China)
Objective:To evaluate the long-term effect of antiviral therapy with nucleotide analogues and interferon for prevention of hepatocellular carcinoma(HCC) and mortality in chronic hepatitis B through meta-analysis.Methods:A comprehensive literature search(including PubMed,CCTR,Web of Science,Embase,CBM-disc,and CNKI) was conducted dating until Augest 2014.Two researchers independently reviewed studies and abstracted data according to inclusion/exclusion criteria. HCC incidence and mortality were the outcome measures.Results:Data were obtained from 16 RCTs with 1 814 patients.The analysis found antiviral therapy could significantly decease the risk of HCC (OR=0.57,95%CI=0.35~0.92) and the risk of mortality(OR=0.52,95%CI=0.34~0.80).Significant heterogeneity and potential publication bias did not exist.Conclusion:The long-term treatment of antiviral therapy on chronic hepatitis B can significantly decreased the risk of HCC and mortality and was worthy of clinical popularization.
antiviral therapy;hepatitis B;hepatocellular carcinoma;mortality
唐亚宁,1547075061@qq.com
R512.6+2
A
10.11851/j.issn.1673-1557.2015.03.007
http://www.cnki.net/kcms/detail/51.1688.R.20150507.1718.015.html
2015-01-08)

