158例青霉素皮试阴性致过敏反应的文献分析
黄毅婷,阳丽梅,黄旭慧*
[1.福建省立金山医院(福建省立医院南院)药学部,福州 350028;2.福建省立医院药学部,福州 350001]
·综 述·
158例青霉素皮试阴性致过敏反应的文献分析
黄毅婷1,阳丽梅2,黄旭慧1*
[1.福建省立金山医院(福建省立医院南院)药学部,福州 350028;2.福建省立医院药学部,福州 350001]
目的:了解青霉素皮试阴性致过敏反应的相关因素,为临床安全、合理使用青霉素类药物提供参考。方法:检索中国知网(CNKI)、中文科技期刊数据库(维普,VIP)、中国生物医学期刊引文数据库和万方数据-数字化期刊群中报道的青霉素皮试阴性后所致过敏反应,对病人年龄、性别、原患疾病、过敏史、给药途径、合并用药情况、临床表现等信息进行分析。结果:在158例青霉素皮试阴性致过敏反应中,女性的构成比高于男性;21~40岁年龄段构成比高于其他年龄段;静脉滴注给药为最常见给药途径;临床表现以皮肤及其附件损害为主,严重者出现过敏性休克。结论:皮试阴性的病人使用青霉素治疗也应严密监护,以保障用药安全。
青霉素;皮肤试验;药物副反应报告系统;综述
[Pharm Care Res,2015,15(4):294-298]
青霉素属于β-内酰胺类抗生素,具有高效、低毒、疗效确切、价格低廉的特点,临床应用广泛,但其过敏反应发生率高达0.7%~10%[1],居各类药物之首,且危害极大。皮试是预防发生严重过敏反应的常规手段,在使用各种剂型的青霉素前都需做皮试。但青霉素皮试阴性的病人仍有可能发生过敏反应,皮试假阴性是对安全用药很大的威胁,因此了解青霉素皮试阴性致过敏反应的相关因素具有十分重要的意义。对青霉素皮试假阴性的文献大多为个案报道,仅少数文献汇总多个病例进行分析,但样本量仍较少。作者对青霉素皮试阴性致过敏反应的相关文献进行较为全面的系统分析,以期为临床安全、合理使用青霉素提供参考。
1 资料和方法
1.1 资料来源 以“青霉素”、“皮试阴性”、“假阴性”、“过敏反应”为关键词,检索中国知网(CNKI)1981-2014年、中文科技期刊数据库(维普)1994-2014年、中国生物医学期刊引文数据库(CMCI)1989-2014年、万方数据-数字化期刊群1981-2014年的文献,排除其他药品不良反应(adverse drug reactions,,ADRs),剔除综述及重复报道,最终获得有分析价值的文献109篇,共158例ADRs。摘录病人的年龄、性别、原患疾病、过敏史、给药途径、合并用药情况、静脉滴注溶媒及溶媒量、临床表现、ADRs发生时间、转归等信息,进行分析。
1.2 文献资料的质量评价 本研究所纳入文献资料的信息相对齐全,但仍有部分信息缺失,可能对研究结果有一定的影响。其中11例ADRs对原患疾病记录不详,31例ADRs对青霉素静脉给药的溶媒和/或溶媒量记录不全,绝大多病人所用的青霉素皮试液信息不详。
2 结 果
2.1 病人的年龄和性别分布 在158例过敏反应中,涉及男性57例(36.1%),女性101例(63.9%),年龄最小7个月[2],最大73岁[3]。病人的性别和年龄分布情况见表1。

表1 青霉素过敏反应病人的性别与年龄分布Table 1 Distribution of age and gender in patients with penicillin allergy
2.2 原患疾病和既往过敏史 158例过敏反应病人的原患疾病分布情况见表2。2例病人对磺胺药和解热镇痛药过敏,30例无青霉素过敏史(其中2例有家族青霉素过敏史),126例病人的过敏史不详。
2.3 青霉素皮试液浓度 158例过敏反应中,对青霉素皮试液信息介绍大多不详。青霉素皮试液浓度为50U/ml有4例,20U/ml有2例,10U/ml有1例,用青霉素常规皮试液有5例,氨苄青霉素皮试液1例,其他病人所用皮试液信息不详。
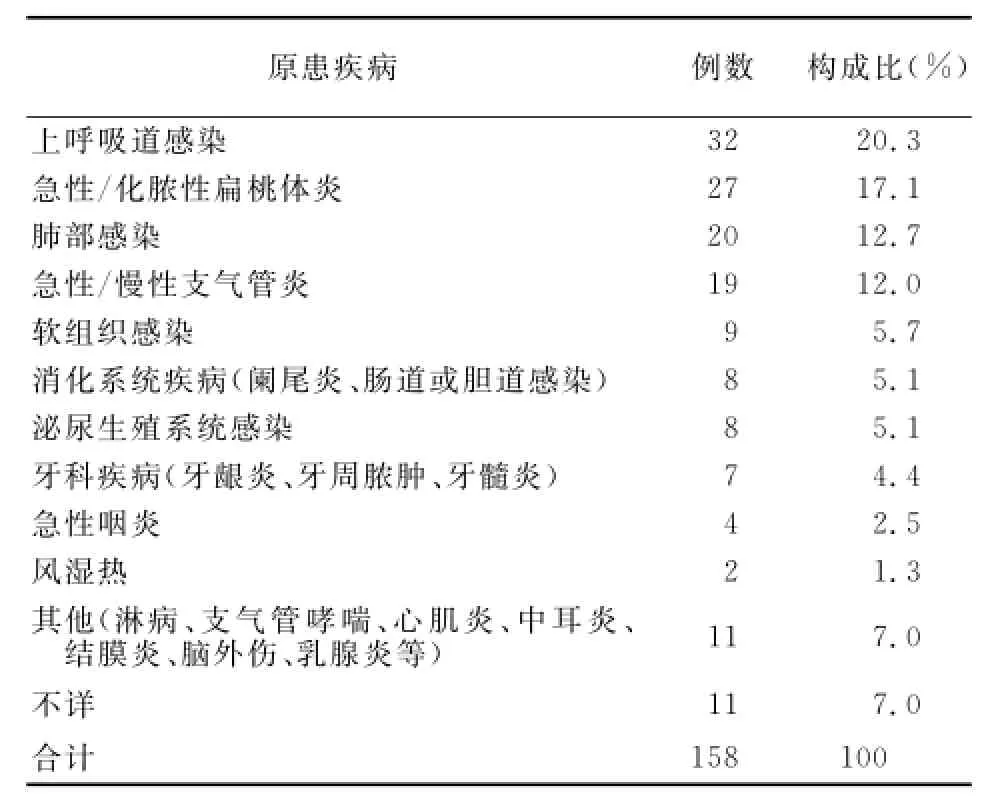
表2 青霉素过敏反应病人的原患疾病分布Table 2 Distribution of primary diseases in patients with penicillin allergy
2.4 给药途径、合并用药情况和静脉输液溶媒 158例过敏反应中,静脉滴注给药114例(72.2%),肌内注射36例(22.8%),静脉滴注及肌内注射联合给药5例(3.2%),口服给药2例(1.3%),静脉推注1例(0.6%)。静脉滴注给药的溶媒及溶媒量统计结果见表3。158例过敏反应中有19例记录合并用药情况,合用抗菌药物(甲硝唑、头孢菌素、红霉素、哌拉西林钠)5例,合用复方制剂感冒药(酚麻美敏、氯芬黄敏、氨咖黄敏、酚咖伪麻)3例,合用利巴韦林注射液3例,合用地塞米松注射液2例,合用双黄连注射液+对乙酰氨基酚+阿莫西林,地塞米松+复方制剂感冒药,维生素C+维生素B,消炎利胆片,咽喉消炎丸,氨茶碱+盐酸氨溴索各1例。
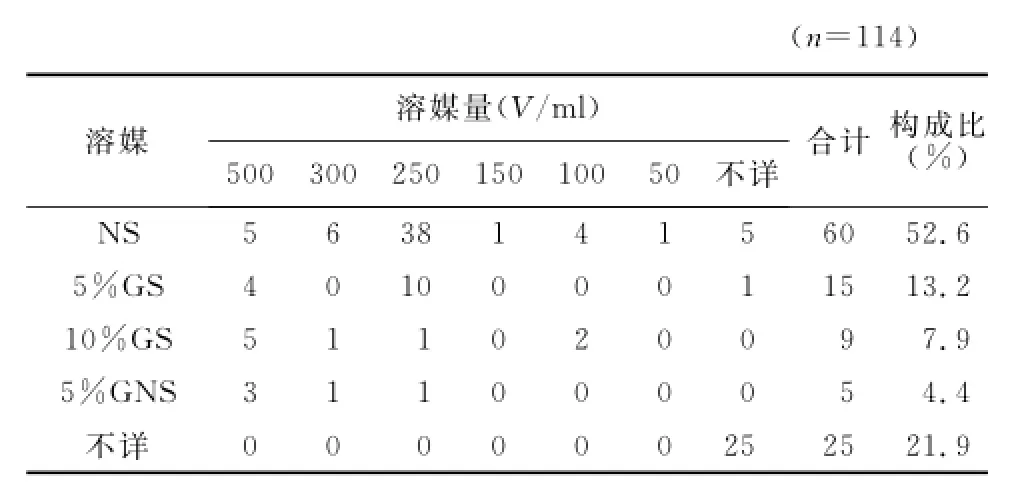
表3 青霉素静脉输液的溶媒及溶媒量Table 3 Solvents and their volumes of the intravenous administration of penicillin injection
2.5 过敏反应累及系统器官与临床表现 参考薛丽平等[4]对青霉素过敏反应的分类方法及WHO不良反应术语,将158例ADRs按临床表现和累及的器官系统进行分类,见表4。青霉素的过敏反应包括速发型、延缓型、血清病型及其他过敏反应,过敏性休克是最常见、最严重的速发型过敏反应。
2.6 过敏反应发生时间 158例过敏反应发生最快的为用药后即刻发生[5],最迟为用药2周后才发生[6]。用药后1~5min内发生55例(34.8%),6~10min内发生15例(9.5%),11~30min内发生33例(20.9%),31min~1h内发生11例(7.0%),1h~1d内发生6例(3.8%),2~5d内发生29例(19.4%),≥6d内发生9例(5.7%)。
2.7 过敏反应的转归 158例过敏反应病人发生死亡4例,其中3例病人出现过敏性休克[7-9],积极抢救后无效死亡。1例病人伴有高血压和肾小动脉硬化症,在此基础上青霉素过敏造成间质性肾炎、皮疹和剥脱性皮炎,最终导致尿毒症而死亡。其余病例均经立即停药、对症处理而恢复。
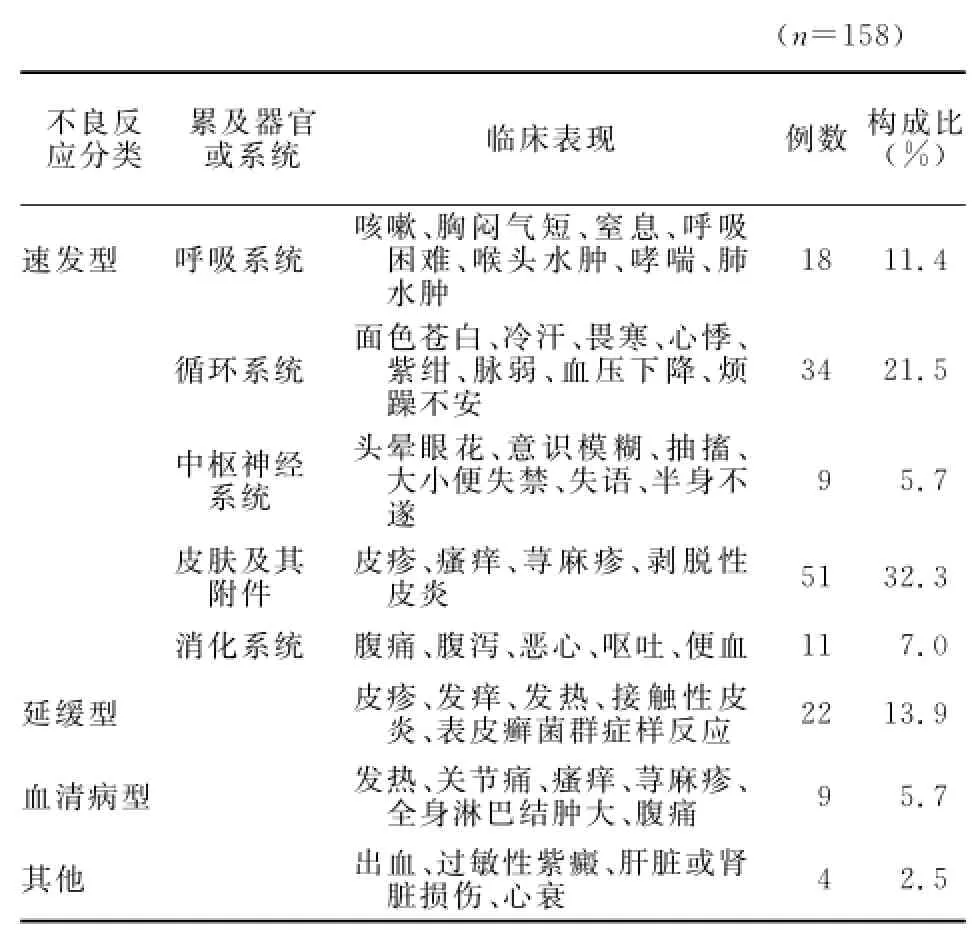
表4 青霉素过敏反应的临床表现Table 4 Clinical manifestations of penicillin allergies
3 讨 论
3.1 青霉素过敏反应的机制 青霉素过敏反应的过敏原是其制剂中的高分子杂质[10],这些杂质具有过敏反应的决定簇,与蛋白质、多肽结合形成大分子化合物,引发过敏性反应。过敏反应的决定簇包括大抗原决定簇、小抗原决定簇和侧链抗原决定簇[1]。这些决定簇均可刺激产生IgE,使机体处于致敏状态,当机体再次接触同一抗原时,IgE与之结合,最终导致平滑肌收缩、毛细血管扩张及通透性增强,产生皮肤、呼吸系统、循环系统、消化系统等过敏症状。
3.2 青霉素过敏反应相关因素分析
3.2.1 性别和年龄与过敏反应的关系 过敏反应在各年龄段病人均有发生,中青年(21~40岁)病人占比最大(43.6%)。从理论上来说,老年人过敏反应发生率应高于中青年,但由于老年人患有多种疾病,过敏反应常被原发疾病掩盖,诊断较困难,往往病情严重时才被发现,也延误了治疗时机。从性别分布来看,女性构成比高于男性,这与美国的一项流行病学调查结果相符合[11]。分析原因可能是女性生理状况不同于男性,对药物敏感度高,耐受性差。此外,妊娠期妇女发生的过敏反应有7例,这与妊娠期可选择的抗菌药物少,青霉素因安全性好、不增加致畸危险从而使用机会较多有关[12]。
3.2.2 原患疾病和过敏史与过敏反应的关系 原患疾病为上呼吸道感染、急性/化脓性扁桃体炎、肺部感染的病例数较多,支气管哮喘病人最好避免选用青霉素,因为青霉素可能诱发或加重支气管哮喘症状[13,14]。158例过敏反应中,有对磺胺药、解热镇痛药过敏及有家族青霉素过敏史病人,提示医师开具医嘱前必须详细询问病人的药物过敏史,对过敏体质病人使用青霉素尤需谨慎小心。
3.2.3 皮试液与过敏反应的关系 我国青霉素皮试液大多将青霉素G钠用0.9%氯化钠注射液配成适当浓度的溶液,或者直接购买厂家生产的青霉素皮试液。由于青霉素皮试液不规范导致皮试假阴性的原因有:(1)皮试液浓度过低,《中华人民共和国药典 临床用药须知》规定,青霉素皮试液浓度应为500U/ml[15],而本研究纳入的158例过敏反应中有7例病人所用皮试液浓度<500U/ml,其他大部分病人所用皮试液浓度不详。(2)皮试液剂量不足,《中华人民共和国药典 临床用药须知》规定青霉素皮试剂量为0.1ml,但在临床也存在不严格按照要求执行的情况。皮试液剂量不足会导致局部反应不明显,从而出现假阴性现象。(3)不同青霉素制剂因生产厂家、批号以及储存条件不同,其中青霉噻唑结合物、青霉烯酸、青霉吡唑酸、青霉胺等高分子杂质的种类和含量也可能不同,这些高分子杂质作为过敏原导致过敏反应的可能性也不尽相同。因此,采用统一的青霉素G钠作为皮试剂是否妥当,迄今为止仍存在争议。
3.2.4 给药途径及溶媒与过敏反应的关系 从给药途径来看,多数发生ADRs的病人为静脉滴注给药,这是由于静脉滴注为青霉素最主要的给药途径。葡萄糖注射液(GS)pH值偏低可造成青霉素水解,不仅使药品效价降低,而且使青霉噻唑酸和青霉烯酸的含量增高,从而增大发生过敏反应的可能性[16]。本次文献汇总发现,发生过敏反应的病人以5%GS、10%GS和5%葡萄糖氯化钠注射液(GNS)为溶媒的仍占一定比例,另有21.9%病人所用溶媒不详,这也是青霉素皮试阴性致过敏反应的原因之一。NS较5%GS、10%GS、5%GNS更为稳定,故静脉滴注时应选择NS作为青霉素的溶媒,过敏反应的发生率较小。另外,随着溶媒量的增加,滴注时间相对延长,导致溶解后的青霉素放置时间延长,稳定性及效价均降低,故建议溶媒量以100~200ml为佳。
3.2.5 合并用药与过敏反应的关系 地塞米松和感冒药中的抗组胺成分,如马来酸氯苯那敏、苯海拉明能抑制免疫反应,对过敏反应起掩盖作用,皮试前使用这些药物可能导致假阴性,一旦撤药需高度警惕过敏反应的发生[17]。临床医师在开具医嘱时应认真询问病人的用药史,对近日内使用糖皮质激素和抗组胺药者,建议不要使用青霉素皮试,以免出现假阴性现象。
3.3 研究的缺陷 本次研究所纳入ADRs信息均来源于文献资料,原文献对于过敏反应因果关系的评价大多不明确,其中评定ADRs肯定与青霉素有关的仅74例。19例合并用药病人发生的过敏反应,文献作者根据ADRs发生的可能性对其他联用药物进行排除者为7例,其他案例仅罗列联用药物,未对其他药物导致ADRs的可能性进行排除。这也提醒广大医务工作者在进行个案报道时应尽可能提供详细的病人信息,尤其是合并用药情况、ADRs发生时间、转归等,对ADRs进行因果关系评定,从而为后续研究提供更有价值的参考。
3.4 预防措施 临床医师、药师应对青霉素过敏反应有全面了解,严格按药品说明书指导合理用药。在使用青霉素时应遵循如下原则:(1)详细询问病人的疾病史和过敏史,对过敏体质和体弱者慎用,对儿童、高龄老人、肾功能不全及过敏体质者应严格按用药指征规范用药。(2)规范操作青霉素皮试,使用规定浓度和剂量的皮试液,皮试后观察30min,无任何不适方可用药。(3)静脉滴注建议选择NS为溶媒,溶液量控制在100~200ml。(4)认真询问病人的用药史,近期使用糖皮质激素和抗组胺药者,需考虑药物对过敏反应的掩盖作用。(5)对青霉素皮试阴性的病人仍要警惕过敏反应,尤其是过敏性休克的发生,静脉给药必须在院内完成。用药后如发现ADRs,立即采取抢救措施,避免延误救治时机。
[1]乔海灵,赵永星,马统勋.青霉素类抗生素过敏反应机制及诊断的新近研究进展[J].国外医药抗生素分册,2002,23(5):197-205.
Qiao HaiLing,Zhao YongXing,Ma TongXun.New advances in mechanisms and diagnosis of penicillin allergy[J].World Notes Antibiot,2002,23(5):197-205.In Chinese.
[2]张利露.青霉素引起胃肠道过敏症状一例[J].中华护理杂志,1997,32(2):98.
Zhang LiLu.One case of penicillin-induced gastrointestinal allergy[J].Chin J Nurs,1997,32(2):98.In Chinese.
[3]曹美莲,王 静.青霉素皮试阴性用药发生过敏反应的护理[J].泰山卫生,2002,26(2):54-55.
Cao MeiLian,Wang Jing.Nursing of allergy cases with negative response to penicillin skin test[J].Taishan Health J,2002,26(2):54-55.In Chinese.
[4]薛丽平,宋永林.青霉素过敏性不良反应的临床用药研究[J].中国现代药物应用,2013,7(13):129-130.
Xue LiPing,Song YongLin.Research on clinical medication in penicillin allergy[J].Chin J Mod Drug Appl,2013,7(13):129-130.In Chinese.
[5]李 颖.皮试假阴性与青霉素过敏性休克5例[J].哈尔滨医药,2004,24(6):57-58.
Li Ying.False negative response to penicillin skin test and 5 cases of penicillin-induced anaphylactic shock[J].Harbin Med J,2004,24(6):57-58.In Chinese.
[6]李柳新.5例氨苄青霉素迟发过敏反应的临床体会[J].中国现代药物应用,2009,3(5):141.
Li LiuXin.Clinical experience of nursing 5patients with delayed allergy to benzathine penicillin[J].Chin J Mod Drug Appl,2009,3(5):141.In Chinese.
[7]严金玲.青霉素钠皮试假阴性致死1例[J].中国医院药学杂志,1998,18(3):131.
Yan JinLing.One case of penicillin-induced death with false negative response to penicillin skin test[J].Chin J Hosp Pharm,1998,18(3):131.In Chinese.
[8]贾晓青,孙铭钏,葛振民.青霉素皮试阴性静脉滴注青霉素过敏致死1例[J].新医学,2004,35(2):109.
Jia XiaoQing,Sun MingChuan,Ge ZhenMin.One case of death induced by intravenous drip of penicillin with false negative response to penicillin skin test[J].New Med,2004,35(2):109.In Chinese.
[9]邓世雄,孙云林.皮试“阴性”的青霉素过敏性休克死亡的法医学鉴定1例[J].法医学杂志,1996,12(2):110.
Deng ShiXiong,Sun YunLin.Medicolegal expertise of one case of death induced by anaphylactic shock with negative response to penicillin skin test[J].J Forensic Med,1996,12(2):110.In Chinese.
[10]Stewart G T.Allergy to penicillin and related antibiotics:antigenic and immunochemical mechanism[J].Ann Rev Pharmacol,1973,13:309-324.
[11]Park M A,Matesic D,Markus P J,et al. Female sex as a risk factor for penicillin allergy[J]. Ann Allergy Asthma Immunol,2007,99(1):54-58.
[12]苗 丽,邓万俊.妊娠及哺乳期应用抗生素的研究现状[J].国外医药抗生素分册,2008,29(6):248-254.
Miao Li,Deng WanJun.Research progress of antibiotic use during pregnancy and lactation[J].World Notes Antibiot,2008,29(6):248-254.In Chinese with English abstract.
[13]王久惠,游 舟.青霉素诱发急性重症哮喘2例[J].内科急危重症杂志,2002,8(2):109.
Wang JiuHui,You Zhou.Two cases of acute severe asthma induced by penicillin[J].J Intern Intens Med,2002,8(2):109.In Chinese.
[14]程保青,孔凡敏,于正军.青霉素诱发支气管哮喘急性发作1例[J].临床合理用药,2013,6(9):56.
Cheng BaoQing,Kong FanMin,Yu ZhengJun.One case of acute bronchial asthma induced by penicillin[J].Chin J Clin Ration Drug Use,2013,6(9):56.In Chinese.
[15]国家药典委员会.中华人民共和国药典 临床用药须知(化学药和生物制品卷)[M].2010年版.北京:中国医药科技出版社,2010:628.
State Pharmacopoeia Committee.Pharmacopoeia of the People’s Republic of China.Guidelines for clinical medication.Volume ofchemical and biological products[M].2010ed.Beijing:Chinese Medical Science Press,2010:628.In Chinese.
[16]来文立,杨春友,王永军,等.试论青霉素溶剂的选择与合理用药[J].药学实践杂志,1996,14(4):216-217.
Lai WenLi,Yang ChunYou,Wang YongJun,et al. Discussion on the choice of solvent and rational use of penicillin[J]. J Pharm Pract,1996,14(4):216-217. In Chinese.
[17]于宝东,李 毅,刘 琳.伴随用药对青霉素类药物皮试结果的影响[J].儿科药学杂志,2014,20(4):58-60.
Yu BaoDong,Li Yi,Liu Lin.Effect of concomitant drugs to penicillin skin testing[J].J Pediatr Pharm,2014,20(4):58-60.In Chinese with English abstract.
Literature analysis of 158 allergic reaction cases with negative response to penicillin skin test
HUANG YiTing1,YANG LiMei2,HUANG XuHui1*
[1.Department of Pharmacy,Fujian Provincial Jinshan Hospital(South Branch of Fujian Provincial Hospital),Fuzhou 350028,China;2.Department of Pharmacy,Fujian Provincial Hospital,Fuzhou 350001,China]
Objective:To investigate relevant factors of allergic reactions in patients with negative response to penicillin skin test,so as to provide reference for safe and rational use of penicillins clinically.Methods:Literature about allergic reactions with negative responses to penicillin skin test was retrieved in China Knowledge Resource Integrated Database(CNKI),Chinese Science and Technology Journal Database(VIP),Chinese Medical Citation Index(CMCI)and Wanfang-Data-Digitalization. Adverse drug reactions(ADRs)cases were analyzed in the aspects of patients’age,gender,primary diseases,allergic history,routes of medication,combined medication,clinical manifestations,etc.Results:In the 158ADRs cases,the incidence of allergic reactions was higher in female than that in male. Patients at the age stage of 21-40years had a higher incidence. The main route of administration was intravenous drip. The principal clinical manifestations of allergic reactions were lesions of skin and its appendix. Anaphylactic shock occurred in severe cases.Conclusion:Patients with negative response to skin test should also be closely monitored to ensure safety when they were administered with penicillins.
penicillin;skin tests;adverse drug reaction reporting system;review
R978.11,R994.11 [
] A [
] 1671-2838(2015)04-0294-05
10.5428/pcar20150417
2014-08-01
] 2015-06-30
黄毅婷(女),硕士,药师.
E-mail:huangyiting1204@163.com
黄旭慧,E-mail:huangys1024@163.com
[
[本文编辑] 兰芬

