GC-MS测定利夫康洗液中蛇床子素的含量
陈琴华,朱 军,黄麟杰,余 飞
·药学研究·
GC-MS测定利夫康洗液中蛇床子素的含量
陈琴华,朱 军*,黄麟杰,余 飞
目的 建立快速、灵敏的气相-质谱联用法,测定利夫康洗液中蛇床子素的含量。方法 色谱条件:DB-5MS (30 m×0.32 mm,0.25 μm)石英毛细管色谱柱;程序升温条件为140 ℃保持2 min,以10 ℃/min升至280 ℃,保持6 min;进样口和接口温度为280 ℃。样品水浴蒸干,乙酸乙酯溶解,应用气相-质谱联用法进行测定。结果 蛇床子素在1.0~50 μg/mL线性关系良好,r=0.999 1,精密度为2.01%,平均回收率为97.26%,检测限为1.0 ng/mL。结论 本方法简便、快速,灵敏度高,结果准确可靠,可以用于利夫康洗液中蛇床子素的含量测定。
利夫康洗液;蛇床子素;气相色谱-质谱
0 引言
利夫康洗液由苦参、黄柏、蛇床子、白鲜皮、黄连、地肤子、花椒、赤芍、板蓝根、何首乌、土茯苓等11味中药组成,具有清热燥湿、杀虫止痒的功效,常用于真菌性、滴虫性阴道炎以及湿疹、接触性皮炎和体股癣[1]。蛇床子为主要构成中药,具有温肾助阳、祛风、燥湿、杀虫之功效,主要用于治疗滴虫性阴道炎、银屑病等[2-4]。蛇床子素是蛇床子中主要有效成分之一,是从蛇床子中提取的主要香豆素类化合物,现代药理试验研究证明,其具有抗滴虫、抗心律失常、性激素样和抗炎等作用[5-7]。目前对蛇床子素的测定主要有分光光度法[8]、荧光法[9]、薄层扫描法[10]和HPLC法[11-12]。由于蛇床子素具有一定的挥发性,气相色谱也可用来定量测定蛇床子素[13]。随着质谱的发展,气相色谱-质谱联用(GC-MS)在中药挥发性成分定量测定的应用越来越广泛[14-15],为了控制该洗液的质量,笔者采用GC-MS法测定利夫康洗液的主要有效成分-蛇床子素,为其质量评价提供科学依据。
1 仪器与试药
GCMS-QP2010型气相-质谱联用仪(日本岛津),工作站GCMSsolution 2.10,DB-5 (30 m×0.32 mm,0.25 μm)毛细管气相色谱柱(安捷伦);KQ-100DB型数控超声波清洗器(苏州江东精密仪器有限公司);HP-01溶剂过滤器(杭州赛析科技有限公司);日本岛津AEU-210电子天平;TG16G离心仪。
蛇床子素对照品(中国药品生物制品检定所,批号:110822-200406,20 mg,供含量测定);利夫康洗液(西安太极药业有限公司,批号:131108);高纯氦气(昆山普克莱斯实用气体有限公司,纯度≥99.999%);乙酸乙酯(分析纯,西安化学试剂厂)。
2 方法与结果
2.1 色谱条件 DB-5 (30 m×0.32 mm,0.25 μm)毛细管气相色谱柱为分析柱;以高纯氦气为载气,流速2.0 mL/min;进样口温度:280 ℃,程序升温:起始温度140 ℃,保持2 min,以10 ℃/min速率升温至280 ℃,保持6 min;进样量为1 μL,接口温度280 ℃,EI源温度200 ℃,电子轰击能量为70 eV,采集延时2.5 min;进样方式不分流进样,m/z为244(蛇床子素)。
2.2 溶液的配制 对照品溶液:取蛇床子素对照品约10 mg,精密称定,置10 mL量瓶中,用甲醇溶解并定容,作为蛇床子素对照品储备液。精密吸取适量,用甲醇稀释得50 μg/mL的工作溶液。供试品溶液:精密吸取利夫康洗液20 mL,置水浴(95 ℃)中挥干,加10 mL乙酸乙酯,完全溶解后用0.45 μm微孔滤膜滤过,得供试品溶液。阴性对照品溶液:按照利夫康洗液的处方组成,称取独缺蛇床子的阴性样品适量,100 mL甲醇超声提取,置水浴(95 ℃)中挥干,加入适量乙醚完全溶解后,用0.45 μm 微孔滤膜滤过,即得阴性对照溶液。
2.3 专属性试验 精密吸取对照品溶液、供试品溶液和阴性对照溶液适量,分别注入气相色谱-质谱联用仪,按“2.1”项下色谱条件进样分析。供试品溶液色谱图中,在与对照品溶液相应的位置上有一相同的色谱峰,而阴性对照品溶液在此保留时间无吸收峰,表明阴性对照对测定无干扰。色谱图见图1。从图1可见,利夫康洗液的其他成分在该色谱条件下不影响蛇床子素的测定,因此,其专属性较强,可以用于利夫康洗液中蛇床子素的测定。
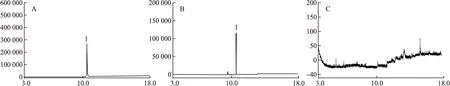
图1 离子监测色谱图
2.4 线性关系考察 取一定量的蛇床子素对照品溶液,配置一系列浓度的对照品溶液,其浓度分别为1.0、1、5、10、20、50 μg/mL,按“2.1”项下分析条件进样1 μL,以蛇床子素的峰面积为纵坐标(Y)、蛇床子素对照品浓度为横坐标(X)进行线性回归,得回归方程,记录色谱图。回归方程:Y=4 652 X-6 002,r=0.999 0。结果表明,蛇床子素在1.0~50 μg/mL范围内呈良好的线性关系,S/N=3时,测得蛇床子素的检测限为1.0 ng/mL。
2.5 精密度、重复性和稳定性试验 取20 μg/mL蛇床子素对照品溶液,连续进样5次,计算蛇床子素对照品峰面积的RSD为1.76%,表明该方法精密度良好。
取同一批样品(批号:130408),共5份,按“2.2”项下供试品溶液的制备方法制备供试品溶液,进样测定,计算利夫康洗液中蛇床子素的含量。结果平均含量为10.2 μg/mL,RSD为2.12 %,表明该方法重复性良好。
取同一批样品(批号:130408),按“2.2”项下供试品溶液的制备方法制备供试品溶液,分别于0、1、2、4、6、8 h进样测定,记录峰面积,计算蛇床子素对照品峰面积RSD为2.01 %。说明蛇床子在利夫康洗液溶液中12 h 内稳定。
2.6 加样回收率试验 精密量取10 mL已知含量的利夫康洗液 (含蛇床子素10.2 μg/mL) 5份,分别加入蛇床子素对照品(40 μg/mL) 0.5 mL,混匀,按“2.2”项下供试品溶液的制备方法制备样品,并按“2.1”项下色谱条件进样,按外标法,以峰面积计算回收率,其平均回收率为97.26%,RSD为2.01%。见表1。
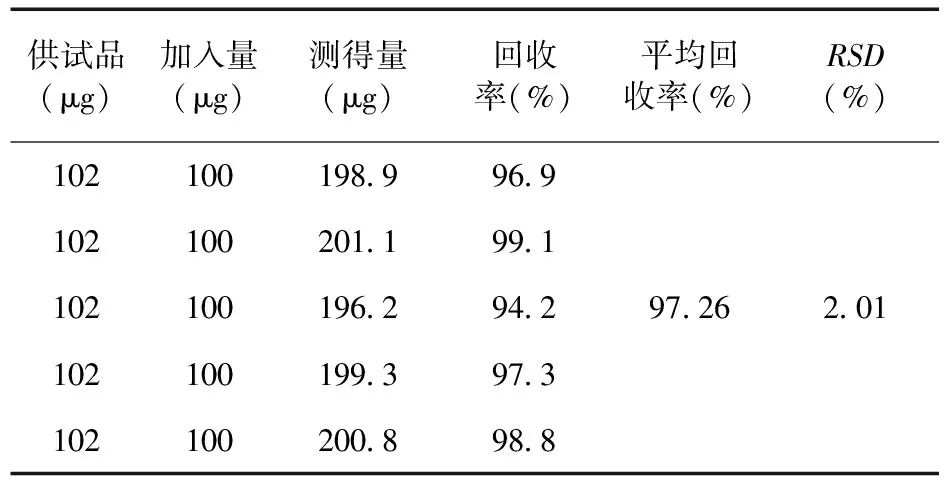
表1 蛇床子素加样回收率
2.7 样品的测定 取利夫康洗液适量,按“2.2”项下供试品溶液的制备方法制备3份,按“2.1”项下色谱条件进样分析。用GC-MS-SIM法测定蛇床子素的含量。在利夫康洗液中,蛇床子素的含量分别为10.1、10.2、10.4 μg/mL,平均含量为10.23 μg/mL。
3 讨论
中药质量评价和控制是制约中药现代化发展的关键[16]。中药成分复杂,而中成药又多为中药复方组成,其组分虽然较多,但每一组分的含量较低,灵敏度低的分析方法难以达到要求。因此,可应用GC-MS的高灵敏度与高分离效能进行成药的分析[17]。
本研究首次采用GC-MS选择离子监测法测定利夫康洗液中蛇床子素的含量,从色谱图可以看出,该方法专一性强,相关系数和回收率均达到了含量测定的要求,而且检测限低(1.0 ng/mL),是可以用来测定蛇床子素的较好的方法。
在供试品处理中,选用溶剂时,曾考虑应用乙酸乙酯和乙醚,但是乙醚容易挥发,重复性较差,因此选择乙酸乙酯。在处理样品时,将样品直接在水浴上蒸干,然后采用乙酸乙酯溶解,上清液进样分析,这样可以避免使用过多的有机溶剂来萃取利夫康洗液中的蛇床子素。
[1] 李鹏,陈琴华,朱军,等.高效液相色谱法测定利夫康洗液中蛇床子素的含量[J].医药导报,2011,30(6):785-786.
[2] 张建武,陈诗渝,林静,等.蛇床子提取液对离体蟾蜍坐骨神经动作电位的影响[J].四川生理科学杂志,2014,36(2):58-59.
[3] 陈宝进,颜娜芬.中药蛇床子临床应用概述[J].亚太传统医药,2014,10(10):51-52.
[4] 马远.蛇床子的成分、药理及临床应用研究[J].中国药物经济学,2014,9(2):234-235.
[5] 苏晓乾,杨建宏.蛇床子素提取工艺优化研究[J].天津药学,2009,21(6):3-4.
[6] 闫俊,宣伟东,卞俊.蛇床子素的研究进展[J].中国药业,2012,21(11):110-112.
[7] 罗玉鸿,高植明,梁逊莹,等.蛇床子素的止痒作用[J].中国药房,2014,25(19):1750-1753.
[8] 杨秀成.分光光度法测定中药蛇床子中总香豆素的研究[J].中国医疗前沿,2010,5(9):71-72.
[9] 赵韶华,韩桂茹,许红辉,等.荧光扫描法测定八子补肾胶囊中蛇床子素含量[J].中成药,2005,27(7):783-785.
[10]郑立卿,张丹参,薛贵平,等.薄层扫描法测定蛇床子提取液中蛇床子素的含量[J].河北北方学院学报(医学版),2008,9(2):8-10.
[11]苑振亭,程丽萍,郇瑜.高效液相色谱法测定复方蛇床子搽剂中蛇床子素的含量[J].中国药物与临床,2014,14(4):480-481.
[12]王巨存,谢宪斌,冯鑫,等.RP-HPLC法同时测定壮骨止痛颗粒中淫羊藿苷、延胡索乙素和蛇床子素的含量[J].药物分析杂志,2014,34(3):418-422.
[13]张晓霞,周卯星,张高勇,等.气相色谱法测定蛇床子提取物中蛇床子素的含量[J].时珍国医国药,2006,16(8):1384-1385.
[14]陈琴华,李鹏,朱军.气-质联用法测定鱼腥草注射液中甲基正壬酮的含量[J].中国医院药学杂志,2011,31(21):1768-1770.
[15]陈琴华,熊琳,李鹏,等.气相色谱-质谱法测定白芷中异欧前胡素的含量[J].医药导报,2014,33(4):487-489.
[16]张铁军.中药质量认识与质量评价[J].中草药,2011,42 (1):1-9.
[17]陈琴华,李鹏,彭林,等.气相色谱-质谱联用法在体内药物分析中的应用[J].中国医院药学杂志,2010,30(3):239-241.
Quantitative determination of osthole in lifukang lotion by GC-MS
CHEN Qin-hua,ZHU Jun*,HUANG Lin-jie,YU Fei
(Institute of Pharmaceutical Analysis and Drug Screening,Hubei University of Medicine,Shiyan 442008,China)
Objective To develop a rapid and sensitive GC-MS method for the determination of osthole in lifukang lotion.Methods GC-MS conditions: DB-5MS capillary column (30 m×0.32 mm×0.25 μm); column temperature program: 140 ℃ held 2 min,and then programmed to 280 ℃ at 10 ℃/min for 6 min; interface and inlet temperature: 280 ℃.The sample was evaporated and dissolved by acetic ether.Quantitative determination of analysis was performed by GC-MS.Results The linear range of osthole was 1.0~50 μg/mL (r=0.999 1).The recovery rate was 97.26%,RSDwas 2.01%,and the limit of quantitation was 1.0 ng/mL.Conclusion The method is convenient and rapid,with good sensibility and accuracy,it can be used to determine the content of osthole in lifukang lotion.
Lifukang lotion; Osthole; GC-MS
2014-07-02
湖北医药学院附属东风医院药物分析与筛选研究所,湖北 十堰 442008
十堰市科技局项目(2013st033、14Y55);湖北省卫生和计划生育委员会计划项目(2013Z-B04);湖北省2011协同创新中心基金(4)
10.14053/j.cnki.ppcr.201504015
*通信作者

