关于初中化学反应中“量”的初探
向贵玉

结合人教版初中化学教材,采用个案研究、对比研究和文献研究的方法,突破初中化学计算中物质的量在反应中的影响因素!
初中化学物质质量化学计算化学计算是九年级化学的重要组成部分,在中考中占有重要地位,也是学生必须具备的一种重要能力和可持续性学习的重要环节。义务教育化学课程标准明确要求:能利用相对原子质量、化学式进行物质组成的简单计算,能正确书写简单的化学方程式,并能进行简单的计算,这就要求学生必须掌握三种简单的计算:根据化学式的计算、有关溶质质量分数的计算、根据化学方程式的计算。
凭本人长年在教学一线工作对学生的了解,对于才接触化学启蒙教育的学生来说,化学计算是一大难点,对质量守恒定律没有从理论上深层次的理解。有些同学对盐酸和氢氧化钠溶液反应后溶液的组成感到很困惑;对多种物质同时反应时的先后顺序拿捏不准;对二氧化碳与澄清石灰水的反应分析不透彻!特别是物质的质量在化学反应中的决定因素没有理解透。据此本人想通过几个浅显的例子,对同学们在此方面知识短板进行弥补,希望能起到抛砖引玉的作用!
物质在发生化学反应时,由于物质的质量不同,可能会导致生成物的质量不同;反应的现象不同;生成物不同。
一、初学者对反应物的质量的误解:生成物的质量错误
在教学中我们经常会碰到初学者犯这样的错误:根据质量守恒定律,10g硫在20g氧气中燃烧会产生30g二氧化硫。
分析:质量守恒定律是指参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。出现这样错误的原因是,学生理解质量守恒,就是各物质的质量机械相加。一是没有搞清楚化学反应各物质是按一定的质量关系反应的,在S+O2点燃SO2的反应中,反应物是按32g硫和32g氧气反应的,也就是按1∶1的质量关系来反应的;二是没有理解质量守恒定律中的“参加化学反应的各物质的质量”,此题中10g硫与20g氧气反应时,硫能反应完,而氧气只能反应10g还有10g氧气是没有参加反应的。所以生成的二氧化硫的质量应该是20g。
二、反应物的量不同:反应现象不同
1.将带火星的木条放在空气中,木条不能复燃;而把带火星的木条放在氧气中,木条会立即复燃!其实带火星的木条放在空气中和放在氧气中都是木条与氧气的反应,出现不同的现象是由于空气中氧气的浓度比较低。
2.如硫在空气中燃烧,发出微弱的淡蓝色火焰;在氧气中燃烧则发出明亮的蓝紫色火焰。这是由于氧气的量不同而引起的,因为空气中氧气的体积分数只占21%。虽然反应现象不同,但生成物是相同的:S+O2点燃SO2。
3.如在CaCl2和HCL的溶液中滴加Na2CO3溶液,如果Na2CO3溶液滴加的少,我们就只能看到有气泡产生:2HCl+Na2CO3=2NaCl+CO2↑+H2O.如果Na2CO3溶液足量,我们就会先看到产生气泡,后看到白色沉淀:CaCl2+Na2CO3=2NaCl+CaCO3↓是由于Na2CO3溶液先和HCL反应,盐酸反应完了Na2CO3溶液才和CaCl2反应出现碳酸钙的白色沉淀。
在CaCl2和HCL的混合溶液中滴加Na2CO3溶液,其反应可用以下图像反映碳酸钙沉淀的质量:
三、反应物的量不同:生成物可能不同
如碳在氧气中燃烧,当氧气充足时,生成物是CO2,C+O2点燃CO2根据化学方程式的意义或化学式中元素的质量关系都可以得出碳和氧气的质量比为3∶8;当氧气不充足时,生成物是CO,2C+O2点燃2CO同理可知碳和氧气的比为3∶4.在此要特别说明的是,当C:O2的质量比在3∶4与3∶8之间时生成物就为CO和CO2了。由于CO有剧毒,所以冬天用煤取暖时要防止空气不流通,氧气不足而产生CO造成煤气中毒。
四、反应物的量不同:生成物不同,现象不同,生成物的量也不同
在人教版初中化学教材上册P118用澄清的石灰水检验二氧化碳时,就是比较典型的。
我们用具体的数据来探讨这个问题:
向含有7.4gCa(OH)2的石灰水中不断的通入CO2气体。
1.随着CO2量的变化,生成物不同:当石灰水与CO2开始反应到石灰水刚反应完时,生成物是CaCO3,Ca(OH)2+CO2=CaCO3↓+H2O
继续通入CO2,就开始产生Ca(HCO3)2了,CaCO3+ CO2+ H2O=Ca(HCO3)2
2.随着CO2量的变化,反应时现象不同:
石灰水由澄清→浑浊→澄清;
3.随着CO2量的变化,生成物的质量不断的变化:
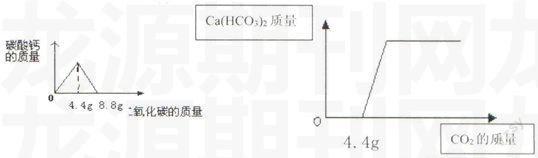
当CO2的质量由0g→4.4g→8.8g时,沉淀CaCO3的质量变化是:0g→10g→0g
当CO2的质量由0g→4.4g→8.8g时,Ca(HCO3)2的质量由0g→0g→16.2g。
也可用以下两个图像直观反映:
有了上面的分析和图像,此时就不难看出要得到5g的沉淀,二氧化碳的质量就应该是数值:2.2g或6.6g,这在初中化学里是很特殊的!所以我们用澄清的石灰水来检验二氧化碳时,要把握好二氧化碳的质量,不能使二氧化碳气体的质量过量,否则最后就观察不到澄清石灰水变浑浊的现象。
在人教版九年级化学教材下册P60实验10-8中:把一定量的氢氧化钠溶液置于烧杯中,逐滴加入稀盐酸时,反应后溶液的成分都是与反应物盐酸和氢氧化钠的量有关的!我们不考虑烧杯中的水时,烧杯中的物质就是这样变化的:当盐酸为0时,溶液的成分是NaOH;滴加盐酸与氢氧化钠反应,但氢氧化钠没反应完时溶液的成分是NaOH和NaCl;继续滴加盐酸,与氢氧化钠恰好完全反应时,溶液的成分是NaCl;继续滴加盐酸过量,溶液的成分就是NaCl和HCl了;溶液酸碱性的变化是:碱性→中性→酸性。我们为了很容易的判断HCl和NaOH恰好完全反应,所以在滴加稀盐酸前,在NaOH溶液中滴入酚酞溶液,溶液由红色恰好变成无色时,盐酸和氢氧化钠溶液恰好中和。现在探究起来思路就清楚了!
因此,我们在学习化学反应时一定要注意反应物的量在化学反应中的影响,不能用静态的观点,而要用动态的观点来思考问题,解决问题,化学反应中现象的变化实际上是物质的变化所引起的!物质的变化又与物质的质量息息相关。其理论依据就是化学方程式所反映的各物质的质量关系和质量守恒定律。
参考文献:
[1]化学课程标准(2012年版).
[2]新课标人教社九年级化学教材.
[3]吕渭源.创造教育与课堂教学改革(讲义).

