左束支传导阻滞与心脏再同步化治疗
蔡思宇 吴祥
●古树新枝
左束支传导阻滞与心脏再同步化治疗
蔡思宇 吴祥
左束支传导阻滞(LBBB)的发现已有100余年的历史,由于左、右心室活动失同步,引起左心室扩张,尤其是延迟激动区域心室质量增加,而出现心力衰竭后LBBB对心室失同步的影响更明显。研究显示LBBB是心力衰竭患者死亡的独立危险因子,与全因死亡率和猝死相关[1]。但目前有关LBBB对心脏电-机械效应的影响、对心肌缺血和血流动力学的影响仍不完全清楚。在过去数十年里,心脏再同步化治疗(CRT)已成为左心室射血分数(LVEF)降低伴QRS波群增宽的症状性心力衰竭患者一个重要的非药物治疗手段,但在临床实践中仍有约30%的患者对CRT无应答,LBBB患者的应答率显著高于右束支传导阻滞(RBBB)或不定型室内阻滞者[2],而超声心动图在预测对机械失同步的反应方面并无优势[3],这重新激发起人们对LBBB研究的兴趣。
1 LBBB的发现历史
1909年,Eppinger与Rothberger[4]在动物实验中,将硝酸银注入犬的心脏破坏一部分心肌后记录到心电图改变。他们惊奇地发现,与破坏大块心室游离壁相比,室间隔区域小部分心肌损伤后却出现显著心电图改变。这是对心脏传导系统最早的认识,他们猜测心电图改变系对室间隔区域束支损伤所致,并在此后数年中证实了以上结论。
这些研究者在犬实验中使用食道-直肠导联,发现切断左束支导致垂直导联QRS波群向上,而切断右束支引起QRS波群向下(图1)。由于人的Ⅱ、Ⅲ接近犬实验中使用的食道-直肠导联,他们推断人的ⅠQRS主波直立、Ⅱ、Ⅲ倒置也提示RBBB。Lewis发表了可能是LBBB的第1份心电图,与Eppinger相似,他将该图诊断为RBBB(图2)。根据早期的犬实验结果推断人的心电图,导致此后长达20余年的时间里人们一直把LBBB与RBBB图形完全颠倒。
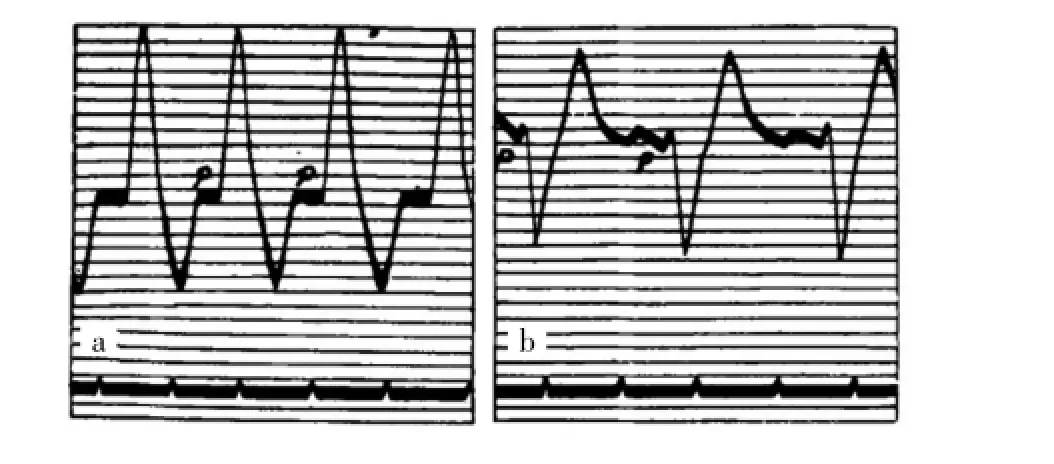
图1 A.Eppinger与Rothberger发表的第1份心电记录,分别显示切断左束支(a)和右束支(b)后的改变。

图2 可能是最早发表的LBBB心电图,由于Ⅲ主波向下,Lewis根据早期动物实验结果,错误地推断为右束支损伤。
1929年,Barker等[5]在对1例30岁化脓性心包炎患者行心包造口术中,在心室不同部位放置电极记录心电图,发现人类来自左、右心室的期前收缩QRS形态与以往报道的犬的研究完全相反。他们认为,一直被当作RBBB的心电图图形实际是LBBB。与当年Lewis在实验中钳夹右束支时,同时损伤了部分左束支,以及与水平位的人类心脏相比,犬的心脏悬挂于脊柱,位置垂直有关。
2 左束支的解剖与血供
左束支是希氏束的延续,起始于无冠窦与右冠窦之间的区域,呈6~10mm直径扁带状结构,向下、前方走行。其主干在主动脉环下穿过室间隔膜部后呈扇形分支走行于室间隔左侧心内膜下,下行约1.5cm后在室间隔中上1/3交界处依次发出分支,先分出的纤维形成左后分支,向后下行至后乳头肌,支配下壁和后壁心肌;其次分出的形成左前分支,通过左心室流出道,抵达前乳头肌底部,支配左心室前侧壁心肌;60%的心脏还有支配室间隔中下部的间隔支。左、右束支的分支纤维进一步形成浦肯野纤维网,直接或经过渡细胞与普通心肌细胞相连。
由于左束支主干和左前分支的血供来自于左前降支的间隔支和右冠状动脉的房室结动脉,左后分支由左旋支、右冠状动脉的房室结动脉和后降支双重供血,而且在室间隔内,左前降支的间隔支与后降支的间隔支之间存在广泛吻合,受损机会较少,病变比较广泛时才易受损,故一旦发生完全性LBBB,多提示有器质性心脏病,心肌受损范围较广。
虽然最初LBBB的心电图表现来自动物实验中切断左束支后的记录,但LBBB不一定是左束支传导系统完全断裂,可因暂时的心肌缺血或炎症、水肿使传导纤维不应期延长,或传导速度减慢,左束支传导时间较右束支相对延长,从而发生LBBB。与正常情况下左、右束支同时激动两侧心室肌不同,如左侧传导时间较右侧延长40ms以上,左侧心肌即由右侧激动通过室间隔心肌来兴奋,产生宽大的QRS波群,表现为完全性LBBB;但如两侧束支传导延迟程度相同,则两侧心室激动仍然同步,心电图上QRS波群正常。
3 LBBB对左心室电和机械同步性的影响
3.1 LBBB时心室除极异常正常心脏的激动由窦房结发出,经房室结、希氏束顺传,心室除极从室间隔左侧中1/3处开始,方向自左向右,经左、右束支及浦肯野纤维迅速扩展至左、右心室,使左、右心室产生几乎同步的机械收缩效应。LBBB时,心室激动顺序发生改变,左心室除极不再通过左束支及浦肯野纤维,心室除极始于室间隔右侧下部,首先跨室间隔右向左除极,到达左侧室间隔心内膜突破点后,经左心室心肌自右前向左后方心室壁除极,而激动在心肌中的传导速度远较正常传导系统慢,导致整个心室除极过程显著延长,左、右心室之间及左心室各节段的同步电机械耦联效应丧失。
3.2 LBBB时左心室激动扩布形式三维电解剖接触及非接触标测技术均显示心力衰竭伴LBBB患者左心室心内膜突破点(breakthrough)和激动顺序存在异质性(heterogeneous)。Auricchio等[6]发现约1/3LBBB患者跨间隔传导时间正常,左心室心内膜激动时间轻微延长或接近正常,QRS波群增宽主要是心肌内传导延缓的结果。有些患者左心室突破点位于前壁或基底部间隔,跨间隔激动可能通过间隔支传导;而另一些患者突破点在中间隔或间隔近心尖部,激动自右向左经室间隔心肌传导。Vassallo等[7]对18例LBBB患者进行心内膜标测,12例仅有1处左心室心内膜突破点,其中9例位于左侧室间隔的中1/3,3例位于室间隔近心尖部。6例同时有两处突破点,其中5例均有1处位于室间隔中1/3。12例单个突破点患者的左心室最迟激动部位,7例在游离壁下基底部或侧壁,3例在前上游离壁,2例在游离壁后基底部。不仅激动顺序呈高度异质性,而且突破后左心室心内膜激动时间也存在异质性。
LBBB患者的左心室激动扩布方式有两种类型:从间隔到侧壁的均匀扩布(Ⅰ型)和U型激动形式(Ⅱ型)。Auricchio等[6]对伴LBBB的心力衰竭患者进行三维电解剖标测时,发现激动从室间隔开始,在左心室最早突破点处向上、下扩布,由于在室间隔与左心室侧壁心外膜之间存在一条从心底部到心尖部的阻滞线,激动绕过心尖,通过下壁到达侧壁和后壁,整个左心室激动径路呈U型。而且此阻滞线是功能性的,部位和长度不固定,与左心室突破点的位置和时间有关。Auricchio的研究中,Ⅱ型者占96%,其他研究显示发生率约60%~65%。不同左心室激动类型与CRT应答率有关,Ⅰ型者低而Ⅱ型者高。3.3LBBB与心肌缺血间歇性LBBB患者的胸痛或胸部不适症状常与LBBB同步出现,而且呈频率依赖性,运动时易发。胸痛呈局限性而无放射,伴心悸,冠状动脉造影一般正常。由于胸部不适与LBBB同时出现而无前驱的缺血性ST段改变,推测以上症状与LBBB时心室活动异常有关,不一定是心肌缺血的结果。此外,近80%的LBBB伴左前降支造影正常者,核素心肌运动负荷显像提示室间隔区域灌注缺损和再分布,达靶心率者缺损更明显。目前认为运动试验中出现此类局限于室间隔区域的灌注缺损为假阳性。犬的起搏试验提示LBBB时心肌灌注缺损是室间隔收缩不同步导致血流受限的结果[8]。
3.4 LBBB与心力衰竭传统被认为是电生理异常的LBBB,也因其显著的血流动力学效应而日益受到关注[9]。组织多普勒超声心动图发现LBBB患者左心室侧壁收缩较室间隔明显延迟,导致左心室内收缩不同步,进而导致左心室收缩功能降低、二尖瓣反流增加。此外,LBBB患者左心室各节段的等容收缩时间亦存在明显不同。LBBB不仅导致左心室收缩不同步,由于左心室激动延迟,右心室激动及收缩先于左心室,左、右心室之间也存在不同步,这种不同步可以导致室间隔运动异常。超声心动图研究已证明收缩期室间隔呈矛盾运动或无运动者每搏输出量、左心室充盈量及LVEF均降低。Ozdemir等[10]针对单纯LBBB患者的研究显示,与正常传导组相比,LBBB患者等容收缩期延长,左心室收缩起始延迟,射血期缩短,左心室收缩末内径增加,LVEF降低;等容舒张期延长,快速充盈减速时间及舒张期缩短,导致左心室舒张末压升高,提示单纯LBBB亦可损害左心室舒张和(或)收缩功能。LVEF降低和左心室舒张末压升高均与室间隔运动异常有关。合并器质性心脏病时,LBBB对心功能的影响更显著。扩张型心肌病伴慢性LBBB时,LBBB常伴随进行性左心室扩张和二尖瓣反流,但LBBB与左心室扩张之间的因果、先后关系尚不清楚。从间歇性LBBB患者中可以观察LBBB引起的急性血流动力学效应,合并严重扩张型心肌病时,LBBB常导致心功能急速和显著减退,表现为动脉血压突然下降、收缩射血期延迟出现和结束、舒张期缩短、每搏量降低、心率加快和肺水肿[11]。
4 LBBB与CRT
CRT已成为有症状心力衰竭合并LVEF降低的LBBB患者一种重要的治疗方法。CRT主要通过双心室起搏同步室间隔与左心室侧壁收缩、恢复心室电激动同步性,从而提高心脏泵血功能,已被大量临床试验证实能够有效改善心力衰竭症状,逆转心室重塑,并且显著降低患者的住院率和死亡率。
最初的CRT试验仅入选QRS时间延长(>120ms)的患者,对心室阻滞的类型未作具体规定。由于只有LBBB患者在室间隔与左心室侧壁的激动之间存在明显不同步,仅后者有可能被CRT纠正,而其他原因引起的QRS时间延长(如RBBB、左心室扩张或肥厚、左心室壁内传导延迟、分支阻滞)时,左心室激动仍可快速传导至左心室浦肯野系统,在室间隔与左心室侧壁间很少发生激动延迟。其次,即使是LBBB,大多数CRT研究中并未描述其定义或诊断标准,心电图结果也仅来自计算机自动诊断而未经心电图中心实验室复核,因此多个临床试验显示大约30%的患者CRT后无血流动力学改善(无应答)[2]。
研究者曾将大部分精力集中于在超声心动图参数中寻找能预测CRT治疗有效的指标,但收效甚微,近期研究重点重新转移到体表心电图。PROSPECT研究[3]显示LBBB是唯一能预测6个月后心室容量和临床反应的指标,与终点事件的相关性优于任何超声心动图指标。
一项来自随机对照研究的荟萃分析评估了不同类型传导障碍时,CRT对临床事件的影响。总计4个随机试验、5 356例基线时LBBB患者入选,结果显示CRT显著降低LBBB患者终点事件(RR=0.64,P=0.00001),非LBBB患者无获益(RR=0.97,P=0.75)[12]。MADIT-CRT[13]入选心功能NYHAⅠ/Ⅱ级、QRS≥130ms的心力衰竭患者,与ICD组相比,CRT-D治疗使LBBB组心力衰竭事件或死亡率降低53%(HR0.47,P<0.001),但非LBBB组心力衰竭事件或死亡增加24%(P=0.26),非特异左心室传导延迟者预后较RBBB组更差。延长随访研究进一步证明CRT显著增加非LBBB患者心力衰竭事件或死亡率。最近,14 946例接受CRT治疗的Medicare患者的数据[14]显示,与LBBB患者相比,非LBBB者早期和晚期死亡率均显著增加,QRS时间≥150ms对预后的预测价值局限于LBBB患者。以上研究提示,仅仅要求QRS时间>120ms是不够的,只有完全性LBBB患者能从CRT获益,而非特异左心室传导延迟或RBBB难以获益,甚至可能有害。
2012年ESC心力衰竭诊治指南首先提出LBBB对于CRT的重要性,此后无论是ESC、ACCF/AHA/HRS,还是中华医学会指南中有关CRT的Ⅰ类适应证,除了QRS波群增宽,均要求为LBBB(表1)。
5 LBBB心电图标准的演变
正常情况下心室除极时,首先是室间隔从左向右除极,参与QRS波群起始部形成。Ⅰ、aVL、V5、V6出现小而窄的Q波(间隔Q波),V1、V2出现小r波。LBBB时,激动从右心室沿室间隔向左心室激动,正常室间隔自左向右的起始激动消失,QRS波群早期间隔部向右前方的向量消失,且左心室除极顺序改变,导致QRS波群延长、形态改变。除了QRS时间≥120ms,心电图主要表现为V1呈QS或rS型,Ⅰ、V6Q波消失、呈单向R波(图3),这也是目前使用最广泛的完全性LBBB心电图标准(习用标准),目前见于部分教材和多数专业医学网站。
1985年世界卫生组织-国际心脏病联合会(WHO-ISFC)[15]提出了典型LBBB的诊断标准:(1)QRS时间≥120ms;(2)Ⅰ、aVL、V5、V6R波增宽、有切迹或粗钝,偶尔V5、V6呈RS型;(3)Ⅰ、V5、V6Q波消失;(4)V5、V6至R波峰顶时间延长至>60ms。R波增宽、切迹或粗钝伴达峰时间延长反映了LBBB时激动从右心室向左心室游离壁传导所需时间延长。Ⅰ、V5、V6Q波消失反映了正常间隔激动消失。2009年AHA/ACCF/HRS推荐的心电图标准化和解析建议采用了WHO-ISFC的标准[16],某些心电图教材也引用,但该标准未被普遍接受或采用。

表1 2012年前、后不同指南中有关CRT的Ⅰ类适应证
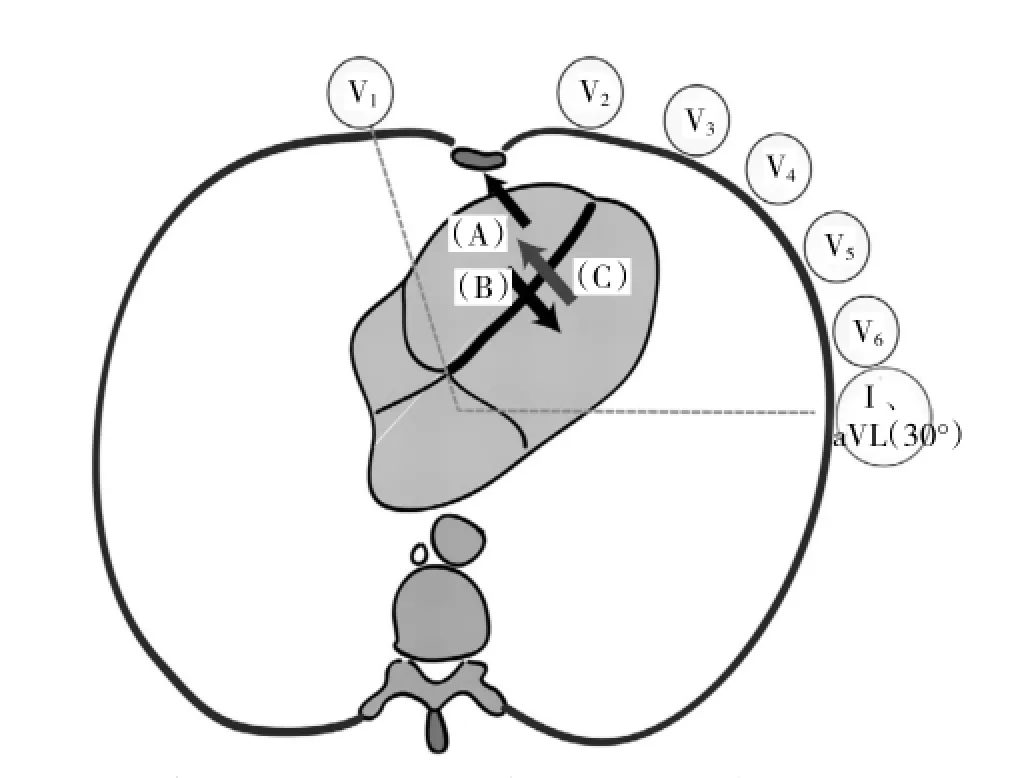
图3 V1靠近并几乎与室间隔垂直,V6、Ⅰ、aVL位置接近,V6较Ⅰ、aVL低。正常情况下,右心室游离壁自心内膜向心外膜除极方向(A)与室间隔除极向量(C)相同,V1呈rS型(r波≥1mm)。完全性LBBB时室间隔除极方向变为自右向左(B),与右心室游离壁除极向量综合后,V1呈QS型或rS型(r波<1mm)。
临床上对完全性LBBB的心电图诊断标准一直存在争议。CRT对伴LBBB的心力衰竭患者的显著疗效使之重新得到关注。Grant等[17]认为,LBBB的习用标准中QRS时间延长40ms来源于动物实验模型,用于诊断人类LBBB时并不完全正确,在人类QRS波群延长常达70~80ms。LBBB时,室间隔激动由右心室向左心室扩布,激动穿越间隔由右心室心内膜到左心室心内膜至少需要40ms,传导至左心室侧后壁心内膜需要额外50ms,最后还至少需要50ms才能激动左心室侧后游离壁心外膜,因此总的QRS时间应该≥140ms。而Auricchio等[6]对习用标准定义的LBBB患者进行心内膜标测后发现,近1/3患者左心室心内膜激动起始时间较右心室并无明显延迟,两者差值<20ms,其余2/3患者差值>40ms。由此推断,右心室激动跨间隔传导时间<20ms的LBBB并非真正的LBBB。据估计,此类患者占近1/3,系左心室肥厚合并左前分支阻滞所致。根据以上发现,2011年Strauss等[18]对完全性LBBB的习用标准提出质疑,建议更严格的诊断标准,为CRT识别合适的心力衰竭患者。严格的LBBB标准包括:QRS时间≥140ms(男性)或130ms(女性),V1或V2呈QS或rS形,V1~V2、V5~V6、Ⅰ和aVL中有两个以上导联的QRS波群中部有切迹或粗钝。不同性别QRS时间阈值不同,与女性心室小、基线QRS时间较男性短[分别为女性(87.1±8.7)ms、男性(92.7±9.3)ms]有关。
无论是WHO-ISFC标准,还是严格的LBBB标准,与习用心电图标准相比,除了QRS时间阈值要求更严,形态学上Ⅰ、V5、V6R波不仅要增宽,还要有切迹或粗钝。LBBB时QRS波群中部切迹/粗钝见于Ⅰ、aVL、V5、V6的R波和V1、V2的S波。WHOISFC标准要求V5、V6切迹第2部分的R波峰值时间≥60ms,而严格标准要求切迹位于QRS波群起始40ms后,因为QRS波群起始40ms以内的切迹可能是梗死或瘢痕所致。切迹起始代表电除极波阵穿过室间隔在左心室心内膜突破的时间点,切迹结束发生于除极波阵到达左心室侧壁心外膜时。由于激动波阵穿过室间隔至少需要40ms,因此切迹必须起始于QRS波群的前半部分,终止于QRS总时间的前2/3。一些研究中使用的是LBBB的习用标准,对切迹没有要求,推测入选了此类患者可部分解释对CRT治疗无应答。至于WHO标准中Ⅰ、V5、V6Q波消失,对无合并症的LBBB患者是正确的,但在前间隔心肌梗死时,完全性LBBB时以上导联也可出现Q波。

图4 3种代表性心电图[20]。A.真正LBBB,QRS时间142ms,Ⅰ、aVL、V5明显QRS波群中部切迹,V6QRS波群中部粗钝;B.非真正LBBB,QRS时间140ms,Ⅰ、aVL、V5、V6无QRS波群中部切迹或粗钝;C.非特异性室内阻滞,QRS时间156ms,Ⅰ、aVL、V5~V6明显Q波,QRS形态呈非特异性,不同于LBBB与RBBB。
已有小样本研究支持使用Strauss的严格诊断标准预测CRT获益、筛选合适患者。Mascioli等[19]共入选111例符合LBBB习用诊断标准并接受CRT的心力衰竭患者,其中61例为真正LBBB(符合Strauss严格诊断标准),50例为假性LBBB(符合习用LBBB标准,但不符合严格标准),术后平均随访(816±517)d,主要研究终点为全因死亡及心力衰竭住院率。结果显示,假性LBBB组的主要终点事件发生率显著高于真正LBBB组(38%vs 16.4%,P =0.016),多变量分析显示,假性LBBB者心力衰竭住院或死亡增加4倍(HR3.98,P=0.005)。在CRT应答率方面,真正LBBB组的应答率也同样高于假性LBBB组(65.6%vs 30%,P<0.001),多变量分析显示,真正LBBB是唯一与LVEF增加显著相关的变量(HR4.57,P=0.002)。国内郭继鸿等[20]也进行了类似前瞻性研究,将58例心力衰竭患者分成真正LBBB(习用标准并QRS时间≥130ms、QRS波群中部切迹/粗钝≥2个)、非真正LBBB(LBBB但QRS波群切迹<2个)和非特异性室内阻滞(图4)。6个月随访时,LVEF平均增加值依次为(16.0±11.6)%、(8.1±11.2)%和(3.3±7.8)%,NYHA心功能分级变化依次为-1.2±0.6、-0.8±0.6和-0.5±0.6,差异均有统计学意义。所有真正LBBB组患者均对CRT有应答,部分为超级应答者。
LBBB因其在CRT应答方面的特殊地位而重新受到重视,已成为各国CRT指南中Ⅰ类适应证的必需条件。最近,从CRT获益的角度,Strauss等提出LBBB的严格心电图标准,除了QRS时间≥140ms(男性)或130ms(女性)、V1或V2呈QS或rS型,最重要的是要求V1、V2、V5、V6、Ⅰ和aVL中有2个以上导联的QRS波群中部有切迹或粗钝,临床研究也证实按此标准诊断的真正LBBB患者终点事件发生率显著低于假性LBBB患者,为提高CRT应答率、选择合适患者提供了新的线索。
[1]Schneider J F,Thomas H E Jr,Sorlie P,et al.Comparative features of newly acquired left and right bundle branch block in the general population∶the Framingham study[J].Am J Cardiol,1981,47(4)∶931-940.
[2]Bax J J,Abraham T,Barold S S,et al.Cardiac resynchronization therapy∶Part 1——issues before device implantation[J].J Am Coll Cardiol,2005,46(12)∶2153-2167.
[3]Hsing J M,Selzman K A,Leclercq C,et al.Paced left ventricular QRS widthandECGparameterspredictoutcomesaftercardiac resynchronization therapy∶PROSPECT-ECG substudy[J].Circ ArrhythmElectrophysiol,2011,4(6)∶851-857.
[4]Eppinger H,Rothberger J.Uber die folgen der durchschneidung der tawaraschenschenkeldesreizleitungssystems[J].KlinMed, 1910,70∶1-20.
[5]Barker P S,Macleod A G,Alexander J.The excitatory process observed in theexposed human heart[J].AmHeartJ,1930,5∶720-742.
[6]Auricchio A,Fantoni C,Regoli F,et al.Characterization of left ventricular activationinpatientswithheartfailure andleft bundle-branch block[J].Circulation,2004,109(9)∶1133-1139.
[7]Vassallo J A,Cassidy D M,Marchlinski F E,et al.Endocardial activationofleftbundlebranchblock[J].Circulation,1984,69(5)∶914-923. [8]Vernooy K,Verbeek X A,Peschar M,et al.Left bundle branch block induces ventricular remodelling and functional septal hypoperfusion [J].EurHeartJ,2005,26(1)∶91-98.
[9]Littmann L,Symanski J D.Hemodynamic implications of left bundle branch block[J].JElectrocardiol,2000,33 Suppl∶115-121.
[10]Ozdemir K,Altunkeser B B,Dani ,G,et al.Effect of the isolated left bundle branch block on systolic and diastolic functions of left ventricle[J].JAmSocEchocardiogr,2001,14(11)∶1075-1079.
[11]Takeshita A,Basta L L,Kioschos J M.Effect of intermittent left bundle branch block on left ventricular performance[J].Am J Med, 1974,56(2)∶251-255.
[12]Sipahi I,Chou J C,Hyden M,et al.Effect of QRS morphology on clinical event reduction with cardiac resynchronization therapy∶metaanalysis of randomized controlled trials[J].Am Heart J,2012,163(2)∶260-267.
[13]Zareba W,Klein H,Cygankiewicz I,et al.Effectiveness of cardiac resynchronization therapy by QRS morphology in the multicenter automatic defibrillator implantation trial-cardiac resynchronization therapy(MADIT-CRT)[J].Circulation,2011,123(10)∶1061-1072.
[14]Bilchick K C,Kamath S,DiMarco J P,et al.Bundle-branch block morphology and other predictors of outcome after cardiac resynchronization therapy in Medicare patients[J].Circulation,2010,122(20)∶2022-2030.
[15]Willems J L,Robles D M E,Bernard R,et al.Criteria for intraventricular conduction disturbances and pre-excitation.World Health Organizational/International Society and Federation for Cardiology Task ForceAd Hoc[J].JAmCollCardiol,1985,5(6)∶1261-1275.
[16]Surawicz B,Childers R,Deal B J,et al.AHA/ACCF/HRS recommendations for the standardization andinterpretationofthe electrocardiogram∶partⅢ∶intraventricular conduction disturbances∶ascientificstatementfrom theAmericanHeartAssociation Electrocardiographyand Arrhythmias Committee,Council on Clinical Cardiology;the American College of Cardiology Foundation;and the Heart Rhythm Society.Endorsed by the International Society for Computerized Electrocardiology[J].J Am Coll Cardiol,2009,53(11)∶976-981.
[17]Grant R P,Dodge H T.Mechanisms of QRS complex prolongation in man left ventricular conduction disturbances[J].Am J Med,1956,20(6)∶834-852.
[18]Strauss D G,Selvester R H,Wagner G S.Defining left bundle branch block in the era of cardiac resynchronization therapy[J].Am J Cardiol, 2011,107(6)∶927-934.
[19]Mascioli G,Padeletti L,Sassone B,et al.Electrocardiographic criteria of true left bundle branch block∶a simple sign to predict a better clinical and instrumental response to CRT[J].Pacing Clin Electrophy siol,2012,35(8)∶927-934.
[20]Yun Tian,Ping Zhang,Xuebin Li,et al.True complete left bundle branch block morphology strongly predicts good response to cardiac resynchronization therapy[J].Europace,2013,15(10)∶1499-1506.
2015-07-13)
(本文编辑:杨丽)
310009浙江大学医学院附属第二医院心脏中心