整平剂对酸性电镀硬铜的影响
肖宁,邓志江,滕艳娜,潘金杰,张宜初,雍兴跃*
(北京化工大学化学工程学院,北京 100029)
目前,在凹印制版行业,制做版辊一般采用铁辊为基体,通过预镀镍 + 酸性镀铜 + 镀硬铬的组合工艺。其中,电子雕刻(文字或图案)在镀铜层上完成,为了保证雕刻质量,除了要求镀层结晶细致、表面平整之外,还要求镀铜层的硬度能维持在180 ~ 220 HV 之间。硬度太低,难以保证雕刻精度;硬度太高,又会导致雕针过度磨损,甚至发生打针或断针现象,从而缩短了雕针的使用寿命,增加了制版成本[1]。
为了使镀铜层的表面微观形貌及硬度能满足电子雕刻的要求,一般会在酸性镀铜液中添加适当的整平剂(或称硬度调节剂),常见的整平剂有2-巯基苯并咪唑(M)[2-3]、乙撑硫脲(N)[4-5]、四氢噻唑硫酮(H1)[6-8]、健那绿B(JGB)[9-11]等。研究表明[8],在酸铜镀液中添加某些整平剂时,所得镀铜层的硬度在短时间内可以满足电子雕刻的要求,但只能维持2 ~ 3 d,随着存放时间的延长,镀铜层硬度会衰减,这给凹印制版的生产带来极大的不便。另外,镀铜层硬度的不断减小还会造成电子雕刻质量的下降以及产品之间质量的差异。因此,研究不同整平剂对电镀铜层质量的影响规律,探究整平剂的电化学行为与镀铜层质量之间的内在关系,对设计、筛选合适的整平剂具有重要的指导意义。
本文利用金相显微镜与维氏硬度计分别研究了4 种不同整平剂对电镀铜层表面微观形貌以及镀铜层硬度的影响规律,采用计时电位法表征了这4 种整平剂在沉铜过程中的电化学行为,最后筛选出最佳的电镀硬铜整平剂,并探究了整平剂之间的协同作用。
1 实验
1.1 试剂
五水硫酸铜(CuSO4·5H2O),广东致卓精密金属科技有限公司;浓硫酸( ρ = 1.84 g/mL)、十六烷基三甲基溴化铵(CTMAB),北京化工厂;氯化钠(基准试剂),天津市大茂化学试剂厂;聚乙二醇(PEG6000)、聚二硫二丙烷磺酸钠(SPS)、噻唑啉基二硫代丙烷磺酸钠(SH110)、聚乙烯亚胺烷基盐(PN)、四氢噻唑硫酮(H1),江苏梦得电镀化学品有限公司。
1.2 样品的制备
采用1.5 L 哈林槽为电镀槽,5 cm × 10 cm(有效面积45 cm2)的铜板为阴极,含磷量为0.04% ~ 0.065%的磷铜板为阳极(广东致卓精密金属科技有限公司),阴、阳极面积之比为1∶1。
电镀前,先将待镀铜板用10%(质量分数)稀硫酸溶液活化1 min,然后用蒸馏水冲洗干净,冷风吹干后固定于哈林槽中,在2 A/dm2的电流密度下电镀90 min,电镀过程中在阴极待镀板下方持续鼓入空气进行搅拌。电镀结束后断电,取出阴极铜板,用大量蒸馏水冲洗,冷风吹干后置于干燥器中保存14 d,然后进行微观形貌和硬度测试。
镀铜液组成为:CuSO4·5H2O 220 g/L,H2SO455 g/L,Cl-60 mg/L,SPS 3 mg/L,PEG6000 100 mg/L,不同浓度的单一或复合整平剂。
1.3 表征方法
利用舜宇XD30M金相显微镜观察镀铜层的表面微观形貌,并拍摄放大200倍的照片。借助上海联尔HV-1000显微维氏硬度计测定显微硬度,试验载荷为200 g,压力保持时间10 s,在每个样品上取5 个点进行测定,取平均值。
电化学行为测试采用三电极体系,借助上海辰华CHI660D 电化学工作站完成,工作电极为使用聚四氟乙烯包覆的铜棒电极,直径为2 mm,参比电极为汞–硫酸亚汞电极,辅助电极为铂网电极。采用计时电位法,输入电流密度为2 A/dm2。试验时,每隔200 s 往测试镀液中添加一次整平剂,观察电极电位变化的规律。
2 结果与讨论
2.1 整平剂对镀铜层表面微观形貌的影响
在酸铜镀液中添加不同浓度的单一整平剂,所得镀铜层的表面微观形貌如图1–4 所示。
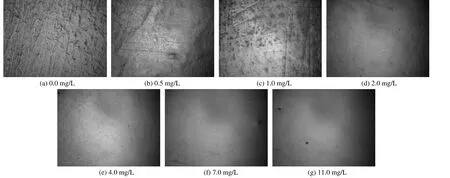
图1 使用不同质量浓度SH110 时镀铜层的表面形貌Figure 1 Surface morphologies of copper coatings obtained at different concentrations of SH110
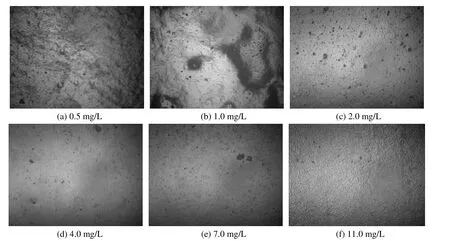
图2 使用不同质量浓度的CTMAB 所得镀铜层的表面微观形貌Figure 2 Surface morphologies of copper coatings obtained at different concentrations of CTMAB
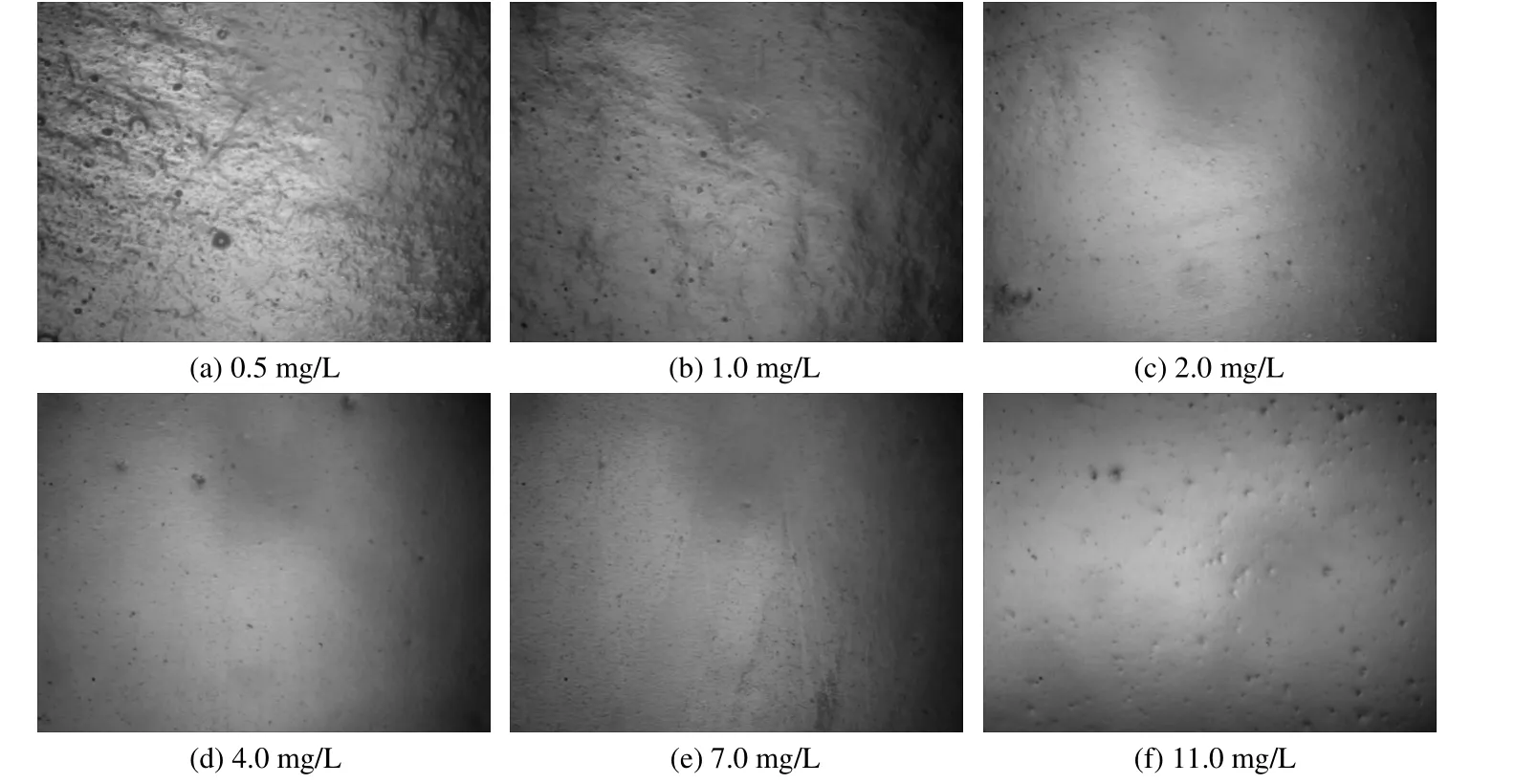
图3 使用不同质量浓度的PN 所得镀铜层的表面微观形貌Figure 3 Surface morphologies of copper coatings obtained at different concentrations of PN

图4 使用不同质量浓度的H1 所得镀铜层的表面微观形貌Figure 4 Surface morphologies of copper coatings obtained at different concentrations of H1
由图1 可知,随着镀液中SH110 质量浓度的增大,镀铜层表面越来越平整、光滑。当SH110 的质量浓度大于2.0 mg/L 时,镀层结晶细致,表面光滑,无明显凹坑或凸起。
由图2 可知,当选择CTMAB 为整平剂时,随着其质量浓度的逐渐增大,所得镀铜层表面逐渐趋于平整,当CTMAB 的质量浓度增大至11.0 mg/L 时,镀铜层表面出现大量细微褶皱。在CTMAB 质量浓度变化的整个区间内,镀铜层表面均有明显可见的小颗粒状凸起。
由图3 可知,随着镀液中PN 质量浓度的逐渐增大,镀铜层表面越来越平整、光滑,但当增至11.0 mg/L 时,镀铜层表面出现很多小凹坑。PN 质量浓度在2.0 ~ 7.0 mg/L 范围内变化时,镀铜层表面较为平整、光滑。
由图4 可知,整平剂H1 在本体系酸铜镀液中允许的质量浓度范围较窄。H1 的质量浓度在0.5 ~ 2.0 mg/L范围内变化时,镀铜层均十分平整、光滑;当H1 质量浓度为4.0 mg/L 时,镀铜层表面出现大量颗粒状凸起,说明镀液中添加剂组分之间的协同作用已经被破坏。
综上可知,整平剂的种类和添加量对镀铜层的表面形貌均有一定程度的影响,进一步来说,就是整平剂会影响铜的结晶过程[12]。一般而言,在整平剂与其他添加剂之间的协同作用被破坏之前,镀铜液中整平剂的浓度越高,铜结晶越细致,所得镀铜层表面就越平整。
2.2 整平剂对镀铜层显微硬度的影响
图5 为镀铜层显微硬度随不同添加剂含量的变化。由图5 可知,当镀液中不含任何整平剂时,所得镀铜层的显微硬度较低,仅51 HV。当往镀液中添加整平剂时,所得镀铜层显微硬度均有一定程度的增加,但使用不同整平剂时镀铜层显微硬度的变化规律不同。随着镀液中SH110 质量浓度的增大,镀铜层的显微硬度呈逐渐增大的趋势,但最高不超过130 HV。当使用CTMAB 或PN 为整平剂时,随着其质量浓度增大,镀铜层的显微硬度均出现一定程度的波动,但最高显微硬度也未能达到电子雕刻的要求。当选择H1 为整平剂时,镀铜层的显微硬度随着H1 质量浓度的增大呈现先增大后减小的趋势,在H1 的质量浓度为2 mg/L 时,镀铜层的显微硬度达到峰值,约为187 HV。需要指出的是,此镀铜层显微硬度可以长时间(14 d 以上)满足电子雕刻的要求。继续增大H1 的质量浓度,其显微硬度开始大幅下降,且镀层结晶粗糙(见图4d),表面出现颗粒状凸起。
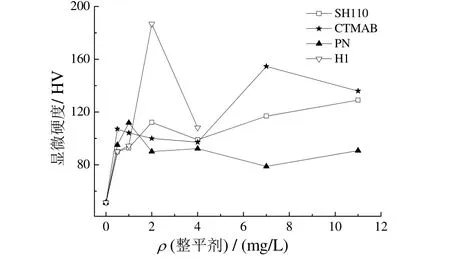
图5 镀铜层显微硬度随整平剂质量浓度的变化Figure 5 Variation of microhardness of copper coating with concentration of leveling agent
对比分析4 种整平剂对电镀铜层显微硬度的影响可知,它们对镀铜层显微硬度的调节能力强弱顺序为H1 >CTMAB > SH110 > PN。
2.3 整平剂的电化学行为研究
采用计时电位法研究4 种整平剂的电化学行为。测试时,每隔200 s 往测试镀液中添加一次整平剂,观察电极电位变化,结果如图6 所示。H1 含量大于4.0 mg/L 时,镀铜层表面粗糙,因此H1 的添加量最大为4.0 mg/L。
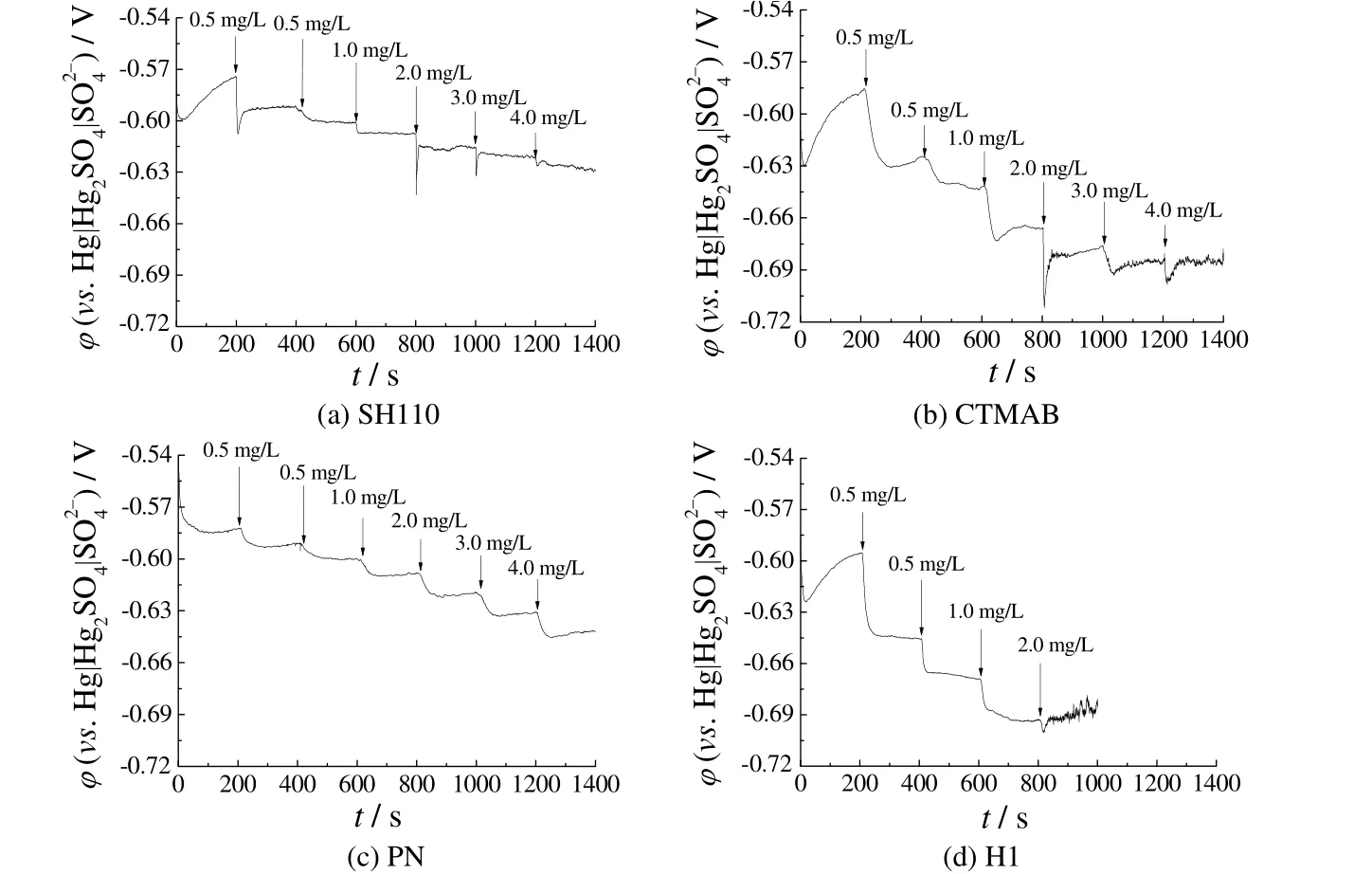
图6 采用不同整平剂时电极电位与电镀时间之间的函数关系曲线Figure 6 Curves showing the electrode potential as a function of plating time in the existence of different leveling agents
由图6 可知,当镀液中未加任何整平剂时,电极电位最大,向镀液中添加任何一种整平剂都会使电极电位减小(负移),整平剂的质量浓度越高,电极电位越负,即沉铜过程的阴极极化越强,沉铜过程越困难。对CTMAB和H1 而言,当其在镀液中的累积质量浓度分别达11.0 mg/L 和4.0 mg/L 时,电极电位均出现明显的波动。结合图2 和图4 可知,电极电位的波动是由工作电极表面铜层的不平整引起的。综合考虑镀铜层的微观形貌及电极电位的变化规律可知,当整平剂浓度在一定范围内变化时,镀液中所含整平剂的质量浓度越高,沉铜过程的阴极极化就越强,镀层表面就越平整。
对于H1 而言,其质量浓度大于2.0 mg/L 时,测试电位出现波动,因此以添加2.0 mg/L 整平剂引起的阴极极化值(即200 s 与800 s 时对应的电极电位之差)为比较对象,可知4 种整平剂对铜沉积阴极过程的影响强弱排序为:H1(97.4 mV)> CTMAB(78.4 mV)> SH110(60.5 mV)> PN(25.7 mV)。此排序规律与整平剂对镀铜层显微硬度调节能力的排序一致,说明计时电位法测试结果与镀铜层显微硬度变化规律之间存在某种联系。具体来说就是,对不同整平剂而言,其添加而引起的阴极极化值越大,所得镀铜层的显微硬度提高得就越多。
2.4 整平剂之间的协同作用
由上述讨论可知,整平剂H1 对镀铜层显微硬度的调节能力最强,且当镀液中H1 的含量为2 mg/L 时,镀层的显微硬度能满足电子雕刻要求。为了进一步探索提高电镀铜层显微硬度的方案,拓宽电镀硬铜配方的操作和应用范围,接下来分别对H1(质量浓度为1.0 mg/L)与其他3 种整平剂(质量浓度均为2.0 mg/L)之间的协同作用进行了研究,结果如图7 所示。
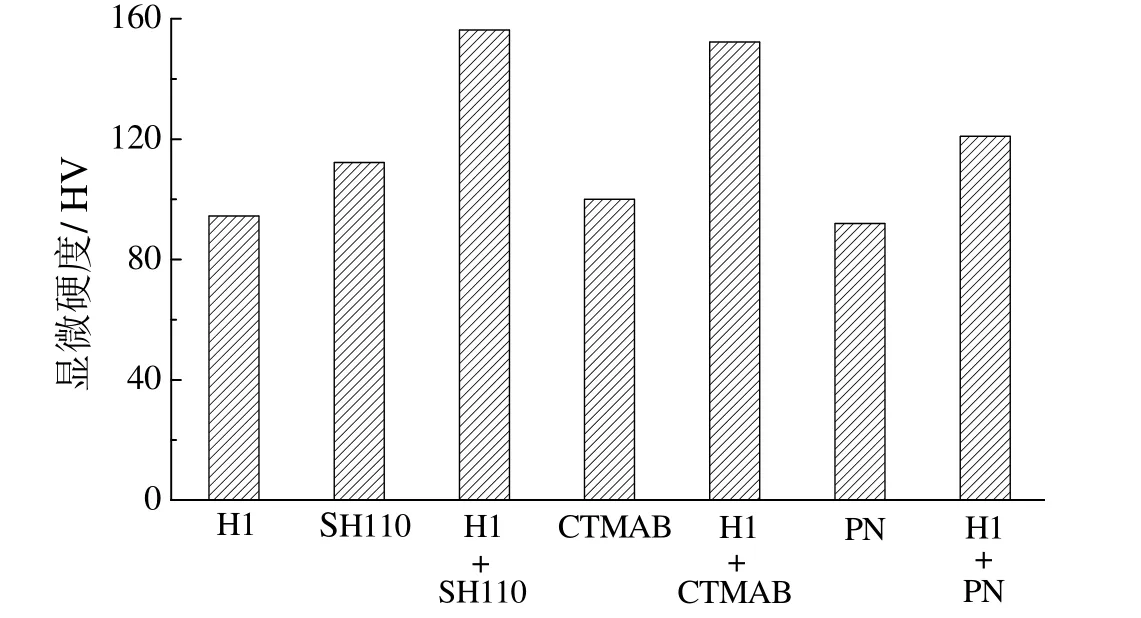
图7 选用不同整平剂时镀铜层的显微硬度Figure 7 Microhardness of copper coating when using different leveling agents
由图7 可知,当整平剂H1 与其他整平剂同时使用时,所得镀铜层的显微硬度均高于使用单一整平剂时所得镀铜层的显微硬度,说明整平剂H1 与SH110、CTMAB 及PN 之间均存在正协同作用。可按式(1)计算2 种整平剂之间的协同作用强度:

式中,x 为复合整平剂协同作用强度的评价因子;y复合为使用复合整平剂时所得镀铜层的显微硬度;y1和y2为使用单一整平剂时所得镀铜层的显微硬度。
3 结论
(1) 对单一整平剂而言,在一定的浓度范围内,其质量浓度越高,铜离子沉积过程的阴极极化越强,铜结晶越细致,铜层越平整、光滑,显微硬度越高。
(2) 4 种整平剂对镀铜层显微硬度的调节能力排序为:H1 > CTMAB > SH110 > PN。
(3) 选择H1 为整平剂,控制适当的添加浓度(2 mg/L)时,所得镀铜层显微硬度可以长时间(14 d 以上)满足电子雕刻的要求。
(4) 其他3 种整平剂与H1 之间的协同作用强度排序为:SH110 > CTMAB > PN。
[1] 王庆浩.铜镀层质量对电子雕刻的影响[J].电镀与环保, 2009, 29 (3): 10-14.
[2] 高泉涌, 赵国鹏, 胡耀红.酸性镀铜添加剂研究进展[J].电镀与涂饰, 2010, 29 (1): 26-29.
[3] 黄令, 张睿, 辜敏, 等.玻碳电极上铜电沉积初期行为研究[J].电化学, 2002, 8 (3): 263-268.
[4] ZHANG W, LU X C, LIU Y H, et al.Synergistic effect of ethylene thiourea and bis-(3-sulfopropyl)-disulfide on acid Cu electrodeposition [J].Journal of the Electrochemical Society, 2007, 154 (10): D526-D529.
[5] 刘俊峰, 彭良富, 刘源, 等.酸性镀铜有机添加剂的研究[J].材料保护, 2008, 41 (7): 40-41.
[6] 周绍民, 张瀛洲, 姚士冰, 等.某些光亮酸性镀铜添加剂的作用机理[J].厦门大学学报(自然科学版), 1980 (1): 54-70.
[7] 李权.表面活性剂四氢噻唑硫酮的整平作用机理研究[J].四川师范大学学报(自然科学版), 1998, 21(6): 684-687.
[8] 王庆浩, 谢洪波, 马学奎.有机中间体对电镀酸性硬铜硬度的影响[J].电镀与环保, 2006, 26 (4): 14-18.
[9] 李亚冰, 王为, 李永磊.封孔镀铜过程中JGB 作用机理研究[J].无机化学学报, 2008, 24(4): 534-540.
[10] DOW W P, LI C C, YIN M W, et al.Copper fill of microvia using a thiol-modified Cu seed layer and various levelers [J].Journal of the Electrochemical Society,2009, 156 (8): D314-D320.
[11] LI Y B, WANG W, LI Y L.Adsorption behavior and related mechanism of Janus Green B during copper via-filling process [J].Journal of the Electrochemical Society, 2009, 156 (4): D119-D124.
[12] 朱立群.酸性电沉积硬铜层研究[J].电镀与精饰, 1985 (6): 10-13.

