非离子型微乳液膜中金属离子Zn2+、Fe3+、Cr(Ⅵ)的迁移行为
郭振良, 蒙延峰, 唐清华
(鲁东大学化学与材料科学学院,山东烟台 264025)
0 引言
随着我国工业生产的迅速发展,工业废水的排放量迅速增加,环境中重金属离子积累急剧升高。含有重金属离子的工业废水是水体污染来源之一,其对人类和整个生态的危害引起了人们的强烈关注,因此电镀废水中重金属离子的分离、萃取已成为国内外学者的重要研究课题之一。微乳液[1]在化妆品、脱膜剂、洗井液、三次采油等[2]方面的应用都取得了良好的效果。与乳状液相比,微乳液更稳定,分散程度更高。在提取、迁移、分离金属离子方面,因微乳液比乳状液更稳定,液珠更小,因而能克服乳状液不稳定和破乳困难的缺陷,并且具有更大的传质面积,能够提高传质效率,具有良好的应用前景。目前以乳液液膜分离富集[3-5]、微乳液液膜萃取、迁移和富集分离金属离子的研究已有报道[6-17]。对于非离子型的表面活性剂OP形成的微乳液在这一方面的应用研究尚未见报道。同离子型表面活性剂微乳液相比,非离子型微乳液的与金属离子的结合不很紧密,更有利于破乳后金属离子与表面活性剂的分离。本文研究了OP/异戊醇/正己烷微乳液及其制乳条件,并考察了该微乳液对Zn2+,Fe3+,Cr(Ⅵ)等金属离子的迁移行为。
1 实验部分
1.1 仪器和试剂
仪器:7200型可见分光光度计(上海尤尼柯仪器公司);FA1604电子天平(上海天平仪器厂);XPT-7型偏光显微镜(江南光电股份有限公司)。
试剂:乳化剂OP,化学纯试剂;异戊醇,正己烷,NaCl,纯锌粒,FeCl3,K2Cr2O7均为分析纯试剂。水为去离子水。
1.2 实验方法
1.2.1 微乳液的制备
本实验选择OP为表面活性剂,异戊醇为助表面活剂,正己烷为油相。将OP与异戊醇按一定比例分别加入一定量的正己烷中,搅拌均匀,当形成均一稳定体系的油相后,与等体积的含金属离子的盐水(水相)混合,平衡后形成两相。当上相呈透明或半透明体系时,经相稀释法确定为W/O型微乳液,下相为过剩水相。试验中根据上相溶液的混浊与透明(或半透明)来区分乳状液和微乳液。因微乳液和溶致液晶都是透明或半透明液体,前者是各向同性,后者为各向异性,因此可借助于偏光显微镜来区分微乳液和溶致液晶。
1.2.2 金属离子的迁移及测定方法
考察了一些痕量金属离子在不同的表面活性剂浓度,盐度和酸度下从料相迁移到微乳相的迁移行为(尽可能避免微乳液的溶胀和泄漏,制乳水相和料相的盐度应一致),以金属离子的迁移率作为考察指标得到制乳和离子迁移的适宜条件:迁移率:
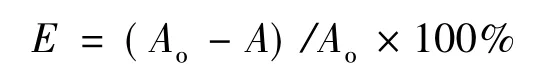
式中:Aο为金属离子原液在测定条件下的吸光度;A为过剩水相中金属离子在测定条件下的吸光度。用分光光度法测定金属离子,测定条件见表1。

表1 金属离子的测定条件
2 结果与讨论
2.1 微乳液制备的影响因素
2.1.1 表面活性剂与醇的比例的影响
本实验选择OP作为表面活性剂,异戊醇作为助表面活剂,使其在界面上能更多地吸附以及更紧密地排列以提高界面张力,并适当地增加体系中醇的量,降低膜和油之间的界面张力rW/O的数值,以达到降低膜和油之间的界面张力与膜和水之间的界面张力之比ri的目的,促使体系形成W/O型微乳液。常规乳液液滴的直径大于1 μm,而微乳液液滴直径小于0.1 μm,实验中通过目视法观测,混浊者为常规乳液。由于微乳液具有W/O型、层状液晶及O/W型三种类型,经偏振光分析,显示各向同性者为微乳液,显示各向异性者为层状结构的溶致液晶。
制乳时间随表面活性剂在油性溶剂中的含量的增加而缩短,表面活性剂的浓度越小,越难成乳,但微乳与料相平衡时间随表面活性剂浓度的增大而增加,且表面活性剂的浓度越大不仅微乳的黏度增大,不利于金属离子的迁移,而且微乳的稳定性差,与料相接触容易破乳。由此表明,表面活性剂与异戊醇的比例要适当。在本研究体系中,表面活性剂的浓度(体积比)应控制在30%~50%,当异戊醇与表面活性剂OP之间的物质的量比大于1时,随异戊醇量的增加,越容易形成透明的微乳液。本实验中异戊醇与表面活性剂OP之比选定为 1.4 ∶1.0。
2.1.2 盐度及酸度的影响
制乳时间、微乳与料相平衡时间随料相盐度的增大或酸度的减小而缩短。盐度越小或酸度越大,越难以成乳且形成的微乳越不稳定,与料相接触往往容易破乳。实验表明,制乳需一定的盐度和酸度,盐度大会减小表面活性剂在水中的溶解度有利于制乳;而酸度大会增加表面活性剂在水中的溶解度不利于制乳。本实验的酸度应以pH 5.0为宜。
2.2 金属离子迁移的影响因素
2.2.1 表面活性剂浓度对金属离子迁移的影响
固定制乳水相和料相的盐度(CNaCl=0.1 mol/L)和酸度(pH 5.0)及金属离子的浓度(10 μg/ml)。改变制乳油相中乳化剂OP的浓度,图1为金属离子的迁移率E随OP浓度的变化情况(制乳的油水体积比和微乳与料相的体积比均为1∶1)。由图1可知,随乳化剂OP浓度的增大,Zn2+和Fe3+的迁移率增大,而Cr(Ⅵ)在OP浓度为33%处出现最大迁移。但乳化剂的浓度过大,容易造成微乳液粘度太大影响金属离子的迁移,且易造成破乳。本实验选择OP∶异戊醇∶正己烷为2.5 ∶4.0 ∶2.0。

图1 OP浓度对金属离子迁移率的影响
2.2.2 盐度和酸度对金属离子迁移的影响
固定制乳油相中,OP∶异戊醇∶正己烷=2.5∶4.0∶2.0,水相和料相的酸度(pH 5.0)及金属离子的浓度(10 μg/ml),改变盐度。金属离子的迁移情况见图2。由图2可知,随着盐度的增加,金属离子的迁移率均趋于降低。故盐度大对金属离子的迁移不利,但盐度太小又对微乳的制备和稳定不利。由于聚氧乙烯链与阳离子之间相互作用,形成类似冠醚的配合物,而适量的卤化物的加入,会使聚氧乙烯链上的金属离子联结部分非水溶剂,增加了界面膜的强度,使制得的微乳液稳定[18-19]。因此本实验选择盐度为0.10 mol/L。

图2 盐度对金属离子迁移率的影响
固定制乳油相中,OP∶异戊醇∶正己烷=2.5∶4.0∶2.0,水相和料相的盐度(CNaCl=0.1 mol/L)及金属离子的浓度(10 μg/ml),改变料相的酸度。在pH 2.0~7.0范围内金属离子从料相到微乳相的的迁移情况见图3。由图可知,随着酸度的减小,Zn2+和Fe3+离子的迁移率增大,而Cr(Ⅵ)的迁移率与其他离子不同,应考虑离子的溶度积常数选择适宜的酸度,而酸度对Fe3+离子的迁移的影响远大于对Zn2+离子的影响。
2.2.3 金属离子迁移机理
固定制乳油相中异戊醇与表面活性剂OP之比为1.4∶1.0(物质的量比),将 OP、异戊淳溶入正己烷中,形成均一油相。向油相中滴加水相(CNaCl=0.1 mol/L),制备不同类型的乳液及微乳液。然后再与等体积的料相混合,水相和料相的酸度均为pH=5.0,金属离子的浓度均为10 μg/mL,待两相平衡后测定金属离子的迁移率。实验结果如表2所示。
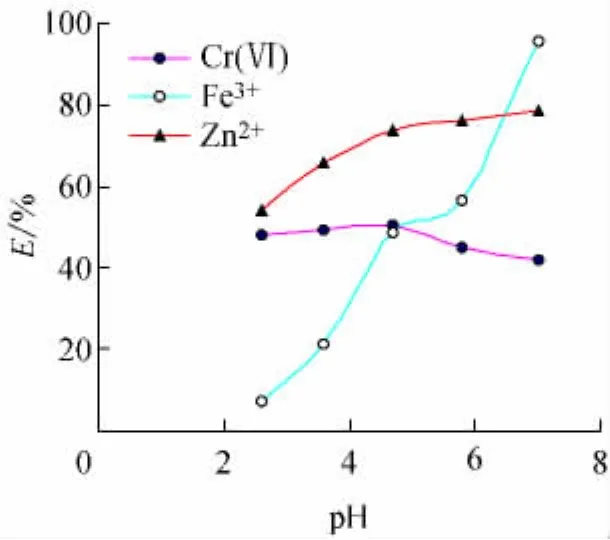
图3 酸度对金属离子迁移率的影响
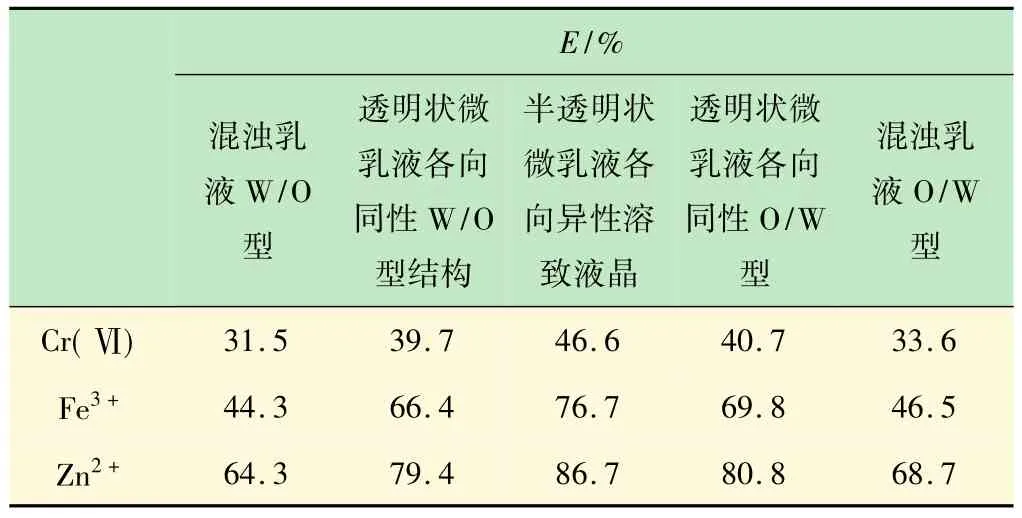
表2 微乳液类型对金属离子迁移率的影响
由表2可见,不同类型的乳液及微乳液迁移相同金属离子的迁移率大小不同,非离子型微乳液膜萃取、迁移重金属离子的机理跟乳状液膜是相同的,都是Ⅱ型促进机理。O/W型乳液及微乳液对同种金属离子的迁移率要大于W/O型乳液及微乳液,且微乳液的迁移率大于乳液的迁移率。这说明乳液液膜厚度比微乳液液膜厚度较大,会影响金属离子的迁移率;在适宜的迁移条件下,许多价态较高的金属离子表现出较高的迁移率。但实验中发现,溶致液晶及O/W型微乳液虽然对金属离子的迁移率较大,但在制乳时极易造成破乳,故实验中所应用的微乳液为W/O型微乳液。
OP的结构式为C9H18C6H4O(C2H4O)nH,该分子聚氧乙烯链上的氧原子具有孤对电子,而金属阳离子则有空轨道,故两者能形成弱的配键,发生化学弱吸附。形成类似冠醚的配合物,而适量的卤化物的加入,会使聚氧乙烯链上的金属离子联结部分非水溶剂,并且金属阳离子与聚氧乙烯链之间的作用,随阳离子的价态的升高,其结合力越强,更能增加界面膜的强度,使制得的微乳液稳定。因此料相中高价态的金属离子就容易从料相迁移到微乳相中与聚氧乙烯链上的氧结合或与低价态的金属阳离子发生交换,结果导致金属离子发生迁移。而OP分子中的聚氧乙烯链上的氧在酸作用下,能提供足够的H3O+,这不仅使聚氧乙烯链有足够的伸展,还能加强与醇分子中OH基团结合,形成稳定的氢键,使微乳液更加稳定。但酸度过高,必然会导致H+与金属离子竟争,使金属离子迁移受到影响;盐度增大的结果同样也会抑制金属离子迁移,这在盐度、酸度对金属离子的迁移实验中已得到证实。
利用微乳液作为液膜迁移金属离子的操作可简述为:①微乳液与料相混合,金属离子被迁移到微乳相中;②两相平衡,微乳相与料相分离。因此只要OP/异戊醇/正己烷微乳液中三者的比例适当,并在适宜的盐度和酸度下微乳液即可自发形成。在本文的实验条件下,金属阳离子的迁移行为很相似,而Cr(Ⅵ)可能因其主要以Cr2O2-7形式存在,导致迁移率较低。实验结果表明,结合金属离子的迁移机理,改变金属离子的迁移条件,利用微乳状液对不同离子间的迁移率大小不同的差别,有可能达到分离混合离子的目的。
3 结语
在酸性较大的条件下,该微乳液对Zn2+的迁移率远高于对Fe3+的迁移率,可实现Zn2+与Fe3+的分离。在碱性条件下,该微乳液对Zn2+和Fe3+均具有较高的迁移率。但对于Cr(Ⅵ),该微乳液体系对其迁移率均不高。可实现Zn2+,Fe3+与Cr(Ⅵ)的分离、萃取。
[1]Hoar T P,Schulman J H.Microemulsions[J].Nature,1943,152:102.
[2]Chan K S,Shah D O.J Dispersion Sci[J].Technol,1979(1):55.
[3]刘小玉,司学芝.项明星硫氰化铵-溴化十六烷基吡啶体系浮选分离和富集锗[J].分析试验室,2012(2):49-51.
[4]周 宁,程 迪,胡筱敏,等.应用液膜分离技术从百草枯生产废水中回收氰化物[J].环境工程,2011(1):102-105.
[5]张卫东,马竞男,任钟旗.大块液膜技术处理含六价铬废水[J].电镀与涂饰,2007(12):30-33.
[6]韩立新,李克安,童沈阳.适用于痕量金属离子迁移的微乳状液的制备及其迁移条件[J].分析化学,1997,25(3):182-186.
[7]韩立新,李克安,童沈阳.AOT-正庚烷微乳状液的制备及迁移痕量金属离子的研究[J].高等学校化学学报,1997,18(5):760-763.
[8]周文杰.适用于痕量钴离子迁移的微乳状液的制备及其迁移条件[J].广东化工,2005(8):32-35.
[9]周文杰.适用于痕量锌离子迁移的微乳液的制备及迁移条件[J].安徽化工,2006(3):26-29 .
[10]唐艳霞,李成海,龚福忠.微乳液在溶剂萃取中的应用研究[J].膜科学与技术,2002,22(1):44-48.
[11]钟 涛,乐长高.微乳液在萃取分离中的应用[J].化工时刊,2008,22(10):56-58.
[12]潘荣楷,陈 静,陈龙凤.微乳液膜法萃取Cu(Ⅱ)离子的研究[J].广东化工,2008(1):34-38.
[13]刘力恒,王立升,王天文.微乳液膜分离技术及其生物医药应用研究进展[J].时珍国医国药,2008,19(6):1388-1390.
[14]陈金清,朱志全,陈传林.W/O微乳液对强碱体系中钒的萃取[J].有色金属(冶炼部分),2010(4):29-32.
[15]胡伦明,杨开林,游 激,等.新型金属离子捕集剂-聚氧肟酸反相微乳液的合成及应用[J].广州化工,2010,38(3):55-57.
[16]刘占宇,夏传波,杨延钊.微乳液萃取钴的研究[J].山东化工,2007,36(1):1-3.
[17]周富荣,雷 新.HA/煤油/NaOH微乳体系萃取废水中Cd~(2+)和Zn~(2+)的研究[J].江汉大学学报(自然科学版),2012(2):28-32.
[18]田一农,解新安,李 雁.U型微乳水相增溶过程微观结构的模拟[J].化工学报,2012 ,63(6):10-13.
[19]郝 策,毕研枢,孙志刚,等.非离子型微乳液的热力学性质[J].化学学报,1993,51:1-5.

