豚鼠主动全身过敏试验两种阳性物质选择的探讨
高 梅,曹 冲,马 会,朱春花
(山东省药学科学院,山东省化学药物重点实验室,山东济南 250101)
豚鼠主动全身过敏试验两种阳性物质选择的探讨
高 梅,曹 冲,马 会,朱春花
(山东省药学科学院,山东省化学药物重点实验室,山东济南 250101)
目的比较两种阳性物质人血白蛋白、卵白蛋白对豚鼠主动全身过敏作用,为过敏性试验提供较好的阳性对照。方法 将豚鼠随机分为14组,以人血白蛋白、卵白蛋白(2、10、100 mg/只)、0.9%氯化钠注射液等受试物为对照,研究不同致敏剂量、激发剂量、激发时间等条件下,豚鼠全身主动过敏的反应情况。结果 在2~100 mg/只剂量范围内,人血白蛋白、卵白蛋白豚鼠主动全身过敏反应的发生率为100%。在2~10 mg/只剂量范围内,过敏症状发生程度随致敏剂量、激发剂量的增加而增加,相同剂量的卵白蛋白较人血白蛋白反应程度更强。结论
豚鼠主动全身过敏试验,阳性对照推荐使用卵白蛋白,剂量为2 mg/只。
主动全身过敏试验;人血白蛋白;卵白蛋白;过敏反应;豚鼠
《化学药物刺激性、过敏性和溶血性研究技术指导原则》[1]规定,通常局部给药发挥全身作用的药物(如注射剂和透皮吸收剂等)需考察I型过敏反应,如进行主动全身过敏试验(ASA),ASA通常选用体重为300~400 g的豚鼠,剂量设计中应设立阴性和阳性对照。阴性对照组应给予同体积的溶媒,阳性对照组给予牛血清白蛋白或卵白蛋白或已知致敏阳性物质。我们选用已知致敏阳性物质人血白蛋白、卵白蛋白为研究对象,比较不同致敏剂量、激发剂量、激发时间等可变因素下,两种蛋白对豚鼠主动全身过敏试验结果的影响,以便得出在I型致敏试验中致敏效果更好的阳性对照。
1 材料和方法
1.1 材料
1.1.1 试剂与仪器:注射用人血白蛋白,规格10 g,50 mL/瓶,蛋白质浓度20%,批号20121032,有效期36个月,广州双林生物制药有限公司生产;卵白蛋白,批号 326A052,分装批次 20120816,有效期2015.08,Sigma公司生产,北京索莱宝有限公司分装;0.9%氯化钠注射液,批号121002103,辰欣药业股份有限公司;电子秤,型号ACS-JJ型,梅特勒-托利多常州测量技术有限公司生产;电子分析天平,型号AUW-120D型,岛津有限公司生产。
1.1.2 实验动物:Hartley豚鼠,SPF级,体重300 g~400 g,雌雄各半,北京维通利华实验动物技术有限公司提供,实验动物生产许可证号:SCXK(京)2012-0001。实验在本中心屏障环境动物实验设施进行,实验动物使用许可证号:SYXK(鲁)2012 0004。并按实验动物使用的3R原则给予人道关怀。
1.2 方法[1,2]
1.2.1 试验药液配制:100 mg/mL人血白蛋白:吸取浓度为20%的注射用人血白蛋白5 mL,加0.9%氯化钠注射液稀释至10 mL;10 mg/mL人血白蛋白:吸取浓度为100 mg/mL的注射用人血白蛋白1 mL,加0.9%氯化钠注射液稀释至10 mL;2 mg/mL人血白蛋白:吸取浓度为10 mg/mL的注射用人血白蛋白2 mL,加0.9%氯化钠注射液稀释至10 mL;100 mg/mL卵白蛋白:称取卵白蛋白 1.0 g,加0.9%氯化钠注射液溶解稀释至10 mL;10 mg/mL卵白蛋白:吸取浓度为100 mg/mL的卵白蛋白1 mL,加0.9%氯化钠注射液稀释至10 mL;2 mg/mL卵白蛋白:吸取浓度为10 mg/mL的卵血白蛋白2 mL,加0.9%氯化钠注射液稀释至10 mL;阴性对照组:0.9%氯化钠注射液。
1.2.2 分组:56只豚鼠随机分为14组,每组4只,雌雄各半。1~14组分别为100 mg/只人血白蛋白组(第14天激发)、100 mg/只人血白蛋白组(第21天激发)、10 mg/只人血白蛋白组(第14天激发)、10 mg/只人血白蛋白组(第21天激发)、2 mg/只人血白蛋白组(第14天激发)、2 mg/只人血白蛋白组(第21天激发)、100 mg/只卵白蛋白组(第14天激发)、100 mg/只卵白蛋白组(第21天激发)、10 mg/只卵白蛋白组(第14天激发)、10 mg/只卵白蛋白组(第21天激发)、2 mg/只卵白蛋白组(第14天激发)、2 mg/只卵白蛋白组(第21天激发)、0.9%氯化钠注射液阴性对照组(第14天激发)、0.9%氯化钠注射液阴性对照组(第21天激发)。按不同实验因素进行试验分组情况见表1。
1.2.3 致敏:分别在动物实验的第1、3、5天进行腹腔注射致敏,0.5 mL/只,共注射3次。
1.2.4 激发:各组末次致敏后第14天、第21天一次静脉注射相应药液用于激发,1.0 mL/只。
1.2.5 结果判断:激发观察:激发后立刻至30 min按表2的症状详细观察每只动物的反应,症状出现及消失的时间。
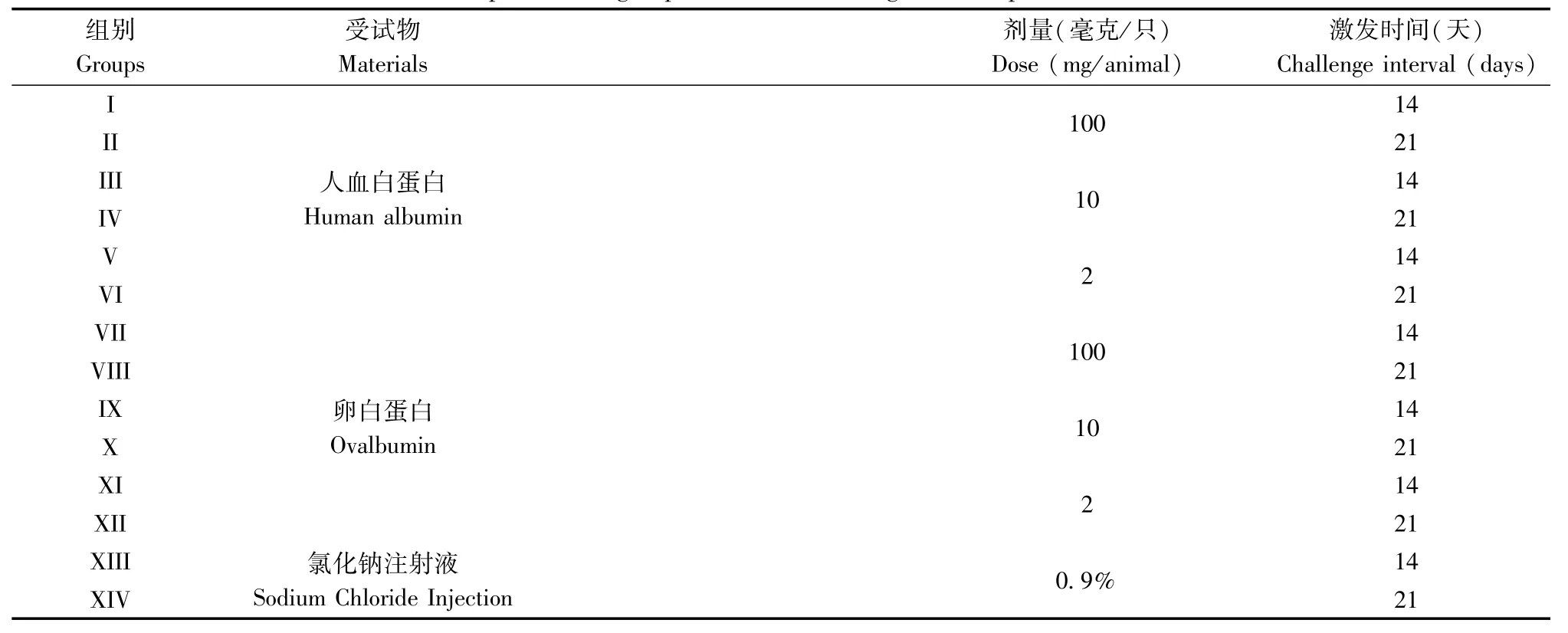
表1 按不同实验因素进行试验分组Tab.1 ExPerimental grouPs divided according to the exPerimental factors

表2 全身过敏反应评价标准[3]Tab.2 Evaluation criteria of the active systemic anaPhylaxis test
2 结果
2.1 不同剂量的人血白蛋白致豚鼠过敏反应结果(第14天激发)
I组:100 mg/只人血白蛋白组末次致敏后第14天激发,激发后立即出现跳跃、痉挛、潮式呼吸、排尿等表现并于1 min内全部死亡,过敏反应为极强阳性,过敏率为100%。
III组:10 mg/只人血白蛋白组末次致敏后第14天激发,激发后10 s~30 s内动物出现搔鼻、咳嗽、躁动、步态不稳、跳跃、呼吸急促、呼吸困难、喘息、旋转、潮式呼吸、痉挛、排尿等表现,1只动物于3 min内死亡,余下3只动物约15 min开始恢复自主活动,约30 min恢复活动无明显异常,过敏反应为极强阳性,过敏率为100%。
V组:2 mg/只人血白蛋白组末次致敏后第14天激发,激发后15 s~60 s内动物出现躁动、搔鼻、呼吸急促、呼吸困难、跳跃、俯卧不动等表现,约10 min开始恢复自主活动,约25 min恢复活动无明显异常,过敏反应为强阳性,过敏率为100%(表3)。
2.2 不同剂量的人血白蛋白致豚鼠过敏反应结果(第21天激发)
II组:100 mg/只人血白蛋白组末次致敏后第21天激发,激发后立即出现痉挛、潮式呼吸、排尿等表现并于1 min内全部死亡,过敏反应为极强阳性,过敏率为100%。
IV组:10 mg/只人血白蛋白组末次致敏后第21天激发,激发后15 s~30 s内动物出现搔鼻、咳嗽、躁动、步态不稳、跳跃、呼吸急促、呼吸困难、喘息、旋转、潮式呼吸、痉挛、排尿等表现并于3 min内全部死亡,过敏反应为极强阳性,过敏率为100%。
VI组:2 mg/只人血白蛋白组末次致敏后第21天激发,激发后15 s~60 s内动物出现躁动、搔鼻、呼吸急促、呼吸困难、步态不稳、跳跃、排尿、俯卧不动等表现,一只动物于5 min内死亡,余下三只动物约15 min开始恢复自主活动,约30 min恢复活动无明显异常,过敏反应为极强阳性,过敏率为100% (表4)。

表3 不同剂量人血白蛋白致豚鼠过敏反应结果(第14天激发)Tab.3 Results of allergic reaction induced with different doses of human albumin in the guinea Pigs(14 days to challenge)

表4 不同剂量人血白蛋白致豚鼠过敏反应结果(第21天激发)Tab.4 Results of allergic reaction induced with different doses of human albumin in the guinea Pigs(21 days to challenge)
2.3 不同剂量的卵白蛋白致豚鼠过敏反应结果(第14天激发)
VII组:100 mg/只卵白蛋白组末次致敏后第14天激发,药液未注射完毕动物即死亡,过敏反应为极强阳性,过敏率为100%。
IX组:10 mg/只卵白蛋白组末次致敏后第14天激发,激发后5 s~20 s内动物出现搔鼻、跳跃、呼吸急促、呼吸困难、潮式呼吸、痉挛、排尿等表现并于2 min内全部死亡,过敏反应为极强阳性,过敏率为100%。
XI组:2 mg/只卵白蛋白组末次致敏后第14天激发,激发后5 s~20 s内动物出现搔鼻、咳嗽、躁动、步态不稳、跳跃、呼吸急促、呼吸困难、喘息、旋转、潮式呼吸、痉挛、排尿等表现并于3 min内全部死亡,过敏反应为极强阳性,过敏率为100%(表5)。
2.4 不同剂量的卵白蛋白致豚鼠过敏反应结果(第21天激发)
VIII组:100 mg/只卵白蛋白组末次致敏后第21天激发,药液未注射完毕动物即死亡,过敏反应为极强阳性,过敏率为100%。
X组:10 mg/只卵白蛋白组末次致敏后第21天激发,激发后5 s~20 s内动物出现跳跃、呼吸急促、呼吸困难、潮式呼吸、痉挛、排尿等表现并于1 min内全部死亡,过敏反应为极强阳性,过敏率为100%。
XII组:2 mg/只卵白蛋白组末次致敏后第21天激发,激发后5~20 s内动物出现搔鼻、咳嗽、躁动、步态不稳、跳跃、呼吸急促、呼吸困难、喘息、旋转、潮式呼吸、痉挛、排尿等表现并于3 min内全部死亡,过敏反应为极强阳性,过敏率为100%(表6)。
2.5 0.9%氯化钠注射液致豚鼠过敏反应结果(第14、21天激发)
XIII、XIV组:0.9%注射液阴性对照组末次致敏后第14天、21天激发,激发后均未见明显异常反应,过敏反应为阴性,过敏率为0%。实验结果见表7。

表5 不同剂量卵白蛋白致豚鼠过敏反应结果(第14天激发)Tab.5 Results of allergic reaction induced with different doses of ovalbumin in the guinea Pig(14 days to challenge)

表6 不同剂量卵白蛋白致豚鼠过敏反应结果(第21天激发)Tab.6 Results of allergic reaction induced with different doses of ovalbumin in the guinea Pigs(21 days to challenge)

表7 0.9%氯化钠注射液致豚鼠过敏反应结果(第14、21天激发)Tab.7 Results of allergic reaction induced with 0.9%sodium chloride Injection in the guinea Pig(14 days and 21 days to challenge)
3 讨论
3.1 不同致敏、激发剂量对豚鼠主动全身过敏反应的影响
人血白蛋白、卵白蛋白在(2~100)mg/只剂量范围内,豚鼠主动全身过敏反应的发生率为100%,过敏症状发生的严重程度随致敏剂量、激发剂量的增加而增加。人血白蛋白、卵白蛋白剂量为100 mg/只时对豚鼠进行致敏与激发,动物产生过敏的反应率为100%,但是激发时由于动物过敏反应极为强烈、迅速,激发药液刚注射完毕或注射过程中动物即死亡,无法有效的观察到动物过敏反应过程,在(2~10)mg/只剂量范围内对豚鼠进行致敏与激发,动物产生过敏的反应率为100%,而产生过敏反应强度大大降低,可有效观察过敏反应。人血白蛋白发生豚鼠过敏反应的严重程度为100 mg/只>10 mg/只>2 mg/只,在(2~100)mg/只剂量范围内,人血白蛋白过敏反应的发生率并没有随着剂量的增大而发生变化,但是豚鼠过敏反应症状的严重程度却存在明显的差别。卵白蛋白发生豚鼠过敏反应的严重程度为100 mg/只≥10 mg/只>2 mg/只,卵白蛋白10、100 mg/只发生反应的严重程度并无明显区别,这说明致敏剂量大到一定剂量时,增加剂量并不会显著影响阳性反应程度。由此可见,过敏反应发生与否,或表现出来的阳性反应症状轻重是与剂量密切关系的,剂量过小,虽然在一定范围内也能发现过敏反应,但很可能由于过敏反应轻微,难以观察而被忽视。剂量过大,容易致动物快速死亡,无法有效全面的观察到阳性症状的发生过程[3]。
3.2 激发时间对豚鼠主动全身过敏反应的影响
人血白蛋白在(10~100)mg/只、卵白蛋白在(2~100)mg/只剂量范围内,第14天、第21天激发时出现的阳性反应率与反应强度并无明显区别,人血白蛋白在2 mg/只剂量时,致敏21天激发比致敏14天激发出现的阳性率要高些,强度要大些。陈怡然[4]研究发现,以0.1%人血白蛋白作为阳性对照,第14天激发时,反应级数为+++,第21天激发时,反应级数为++++。陈丹等[5]研究发现,以10%人血白蛋白作为阳性对照,第14天激发时,反应级数为++++。说明在剂量较大时,豚鼠发生过敏反应的强度与激发的时间之间关系不明显,在剂量较小时,豚鼠发生过敏反应的强度与激发的时间有较大关系,这可能是因为时间长动物体内产生的抗体更多的缘故。当然,究竟最后一次致敏后多少天激发才是最佳,这还值得进一步研究。
3.3 相同剂量下人血白蛋白、卵白蛋白对豚鼠主动全身过敏反应的影响
人血白蛋白、卵白蛋白在(2~100)mg/只剂量范围内,相同剂量下的卵白蛋白比人血白蛋白致豚鼠过敏反应程度更强。豚鼠主动全身过敏试验中常用的阳性对照物,文献报道较多的为卵白蛋白、人血白蛋白、牛血清白蛋白。研究发现,以人血白蛋白做阳性对照时,使用浓度在0.1% ~10%[4,5],以卵白蛋白做阳性对照时,使用浓度为5 mg/只[6],以牛血清白蛋白做为阳性对照时,推荐使用剂量为50 mg/kg[3]。通过比较发现,以三种蛋白作为阳性对照时,在一定范围内,均能得到较好的阳性效果,但是同时也要考虑症状发生过程、经济等原因。从经济因素考虑,三种蛋白相同规格的市场报价为人血白蛋白>牛血清白蛋白>卵白蛋白,从症状发生过程考虑,卵白蛋白使用剂量为2 mg/只时,便能观察到全面的阳性反应症状。
综上,豚鼠全身主动过敏反应与致敏剂量、激发剂量、激发时间等都有较大关系[7],通过比较0.9%氯化钠注射液对照组和不同剂量人血白蛋白组、卵白蛋白组(2、10、100 mg/只)豚鼠全身过敏反应发生的情况,我们发现,在本试验条件下,在一定剂量范围内,相同剂量的卵白蛋白较人血白蛋白反应程度更强,卵白蛋白使用剂量为2 mg/只时,便能观察到全面的阳性反应症状,而且卵白蛋白比人血白蛋白更经济实惠。因此,我们推荐豚鼠主动全身过敏反应中阳性物质选择卵白蛋白,剂量推荐2 mg/只。
[1]《化学药物刺激性、过敏性和溶血性研究技术指导原则》课题研究组.化学药物刺激性、过敏性和溶血性研究技术指导原则[S].国家食品药品监督管理局药品审评中心,2005:13 -27.
[2]袁伯俊,廖明阳,李波.药物毒理学实验方法与技术[M].北京:北京化学工业出版社,2007:247-261.
[3]翁谢川,樊星,王青秀,等.药物安全性评价中豚鼠全身过敏试验方法的研究[J].中国比较医学杂志,2012,22(5):51 -55.
[4]陈怡然.注射用齐多夫定对豚鼠的全身过敏性试验[J].中国药师,2006,9(6):535-536.
[5]陈丹,石佑恩,胡媛,等.日本血吸虫双价DNA疫苗肌肉刺激和全身过敏试验[J].中国血吸虫病防治杂志,2008,20(2):85-88.
[6]陈华英,李秀芳,金若敏,等.大鼠主动全身过敏试验方法的探讨[J].中成药,2012,34(7):1209-1215.
[7]张德波,杨幼琪,冯诚,等.过敏反应与致敏剂量和致敏时间的关系研究[J].中国药品标准,2007,8(3):18-20.
Exploration on the selection of positive materials in active systemic anaphylaxis in guinea pigs
GAO Mei,CAO Chong,MA Hui,ZHU Chun-hua
(Shandong Academy of Pharmaceutical Sciences,Shandong Provincial Key Laboratory of Chemical Drugs,Jinan 250101,China)
Objective The aim of this study was to Provide a better Positive control for allergic test by comParing the allergic effect of two kinds of Positive materials,human albumin and ovalbumin,on active systemic anaPhylaxis in guinea Pig.Methods Guinea Pigs were randomly divided into 14 grouPs,and were given human albumin,ovalbumin (2,10,100 mg/animal),or 0.9%sodium chloride injection as test substances,to assess the symPtoms and incidence of systemic allergic resPonses induced by different sensitizing substances in different challenge doses and different challenge intervals.Results In the range of 2 to 100 mg/animal,the guinea Pigs showed a 100%incidence rate of Positive allergic reaction to human albumin and ovalbumin,the severity of anaPhylactic symPtoms was increasing along with the increase of sensitizing doses and challenge doses,and the allergic reaction was more strong induced by the same dose of ovalbumin than human albumin.Conclusions Our findings indicate that in the active systemic anaPhylaxis test in guinea Pigs,we recommend ovalbumin as the Positive control in a dose of 2 mg/animal.
Active systemic anaPhylaxis;Human albumin;Ovalbumin;Allergic reaction;Guinea Pigs
R-33 < class="emphasis_bold">【文献标识码】A
A
1671-7856(2015)09-0051-05
10.3969.j.issn.1671.7856.2015.009.010
高梅(1983-),女,主管药师,研究方向:药物安全性评价。E-mail:gaomei729@163.com。
2015-08-01

