基于石墨烯的镉离子电化学传感器*
王穗萍, 韩 正, 杨 彤, 李位位, 张彩彤, 刘跃进
(1.湘潭大学 化工学院,重金属污染控制湖南省高校重点实验室,湖南 湘潭 411105;2.湖南大学 化学生物传感与计量学国家重点实验室,湖南 长沙 410082)
基于石墨烯的镉离子电化学传感器*
王穗萍1,2*, 韩 正1, 杨 彤1, 李位位1, 张彩彤1, 刘跃进1
(1.湘潭大学 化工学院,重金属污染控制湖南省高校重点实验室,湖南 湘潭 411105;2.湖南大学 化学生物传感与计量学国家重点实验室,湖南 长沙 410082)
采用电化学法还原氧化石墨烯,构建石墨烯修饰玻碳电极(GCE),选用方波伏安法(SWV)测定微量镉.实验研究了石墨烯修饰电极对镉的溶出伏安行为,优化了石墨烯用量、富集电位、富集时间、pH值、支持电解质.结果表明石墨烯修饰电极明显增强了镉溶出信号,响应电流值与Cd2+的浓度呈良好的线性关系,线性范围为0.001~1 μg/mL,线性方程y=27.859 2x+0.344 5 (R=0.998),检出限为0.001 μg/mL,所制备的修饰电极重现性和重复性较好,6次测定的相对标准偏差(RSD)分别为2.56%和2.51%.所提出的检测方法简单、灵敏、快速,无需复杂的样品前处理,修饰电极可重复使用,能应用于实际水样中镉的快速测定.
石墨烯;镉离子;电化学还原;方波伏安法
镉是对生物体有毒害的环境污染物,对人体的组织和器官可产生毒害,威胁人类的生命健康[1],因此镉的快速、准确检测及其方法的研究具有重要意义[2],镉的常见检测方法有双硫腙分光光度法、原子吸收光谱法、化学发光法、电化学方法等.石墨烯是一种由sp2杂化的碳原子构成的片状碳纳米材料[3],具有蜂窝状晶格结构[4,5],具有大的比表面积[6~8]、良好的导热[9]和导电性能[10]、高的机械强度[11]等优点,在许多领域引起了广泛关注,如催化剂[12,13]、能量存储[14]、传感器[15~17]等.
本文采用改进的Hummers法[14]制备了氧化石墨烯,应用电化学方法还原氧化石墨烯,构建石墨烯修饰玻碳电极(GCE),采用方波伏安法测定水中镉离子.该方法具有操作简单、灵敏度高、重现性好、能够应用于实际水样的测定等优点.
1 实验部分
1.1 主要仪器与试剂
CHI660D电化学工作站(上海辰华仪器有限公司);扫描电子显微镜(SEM,日本JEOL公司JSM-5600LV型);玻碳电极(GCE,天津艾达恒晟科技发展有限公司);铂电极(上海仪电科学仪器股份有限公司);饱和甘汞电极(SCE,上海仪电科学仪器股份有限公司).
石墨粉、硝酸钠(NaNO3)、高锰酸钾(KMnO4)、氯化钾(KCl)、过氧化氢(H2O2,30%,V/V)均购自国药集团化学试剂有限公司;浓硫酸、盐酸、硝酸均购自株洲市星空化玻有限责任公司;Cu2+、Pb2+、Cd2+、As3+标准溶液购自国家有色金属及电子材料分析测试中心;0.1 mol/L氯化钾溶液(pH=3.0)为支持电解质溶液.实验室所用化学试剂均为分析纯,实验所用水为超纯水(电阻率为18.25 MΩ·cm).
1.2 氧化石墨烯的制备
在实验之前,所有玻璃仪器用王水(VHCl︰VHNO3=3︰1)浸泡12 h,用超纯水清洗干净.采用改进的Hummers法[18]来制备氧化石墨烯:取0.5 g石墨粉和0.5 g硝酸钠加入到三颈烧瓶中,置于冰水浴中,接着加入23 mL浓H2SO4,剧烈搅拌5 min;缓慢加入3 g KMnO4,立即将烧瓶转移到35 ℃的水浴中,搅拌并加热1 h;缓慢加入40 mL超纯水,把温度升高到95 ℃,继续搅拌30 min;加入100 mL超纯水,随后缓慢加入3 mL H2O2(30%),待溶液的颜色由深棕色变成金黄色,把所得溶液先低速离心2 min(1 000 r/min),重复3次,去除离心后的固体沉淀,留取上层清液;然后对上层清液高速离心15 min(8 000 r/min),重复2次,留取离心后所得沉淀物;将沉淀物先用100 mL 10%盐酸进行清洗,然后再用超纯水清洗至中性;最后真空干燥,即得氧化石墨烯(GO).用电子天平秤取10 mg GO,加入到10 mL超纯水中,超声2 h,使得GO全部剥落成单片,所得溶液为1 mg/mL GO溶液.
1.3 传感器的制备
将玻碳电极用0.05 μm Al2O3粉浆抛光至镜面,分别用超纯水,无水乙醇、超纯水,超声清洗3 min,然后在处理好的玻碳电极上滴加5 μL的1 mg/mL GO溶液,自然干燥,即可得到GO修饰的玻碳电极GO/GCE.将GO/GCE置于0.5 mol/L NaCl(pH=7.0)中,在-1.3 V电位下还原300 s,得到石墨烯修饰的玻碳电极[19,20].
1.4 电化学测量
采用传统的三电极系统,参比电极为SCE,辅助电极为铂电极,工作电极为石墨烯修饰的玻碳电极.首先将Cd2+富集在电极表面,富集电位-1.0 V,富集时间300 s;然后采用方波伏安法进行溶出,记录出现在-0.83 V处的溶出峰电流值.支持电解质溶液为0.1 mol/L KCl(pH=3.0).操作参数为:振幅0.05 V,脉冲周期0.2 s,扫描电压范围-1.2~0 V,脉冲宽度0.05 s,静置时间2 s.
2 结果与讨论
2.1 石墨烯修饰电极形貌表征

图1所示为石墨烯修饰玻碳电极SEM图,从图中可以看到石墨烯呈薄片层状结构,表面有很多不平的皱褶,与文献[21]报道类似.
2.2 石墨烯修饰电极的电化学特性
图2为裸玻碳电极和石墨烯修饰电极在0.1 mol/L KCl(pH=3.0)中的方波伏安图.由图2可知,裸玻碳电极(a)、石墨烯修饰电极(c)均在-0.83 V处出现明显的镉溶出峰,石墨烯修饰电极响应电流值(27.57 μA)是裸玻碳电极(12.92 μA)的2.13倍;(b)为石墨烯修饰电极的空白对照实验信号(未加入Cd2+).实验结果表明石墨烯修饰电极对镉产生较大的响应电流值,这都归因于石墨烯具有良好的导电性及电催化性能.
2.3 实验条件优化
2.3.1 石墨烯用量对镉离子响应信号的影响 图3为不同用量石墨烯修饰电极对镉离子响应电流信号的影响.从图中可知,随着石墨烯用量的增加,镉离子的响应电流值先增大后减小,当石墨烯的用量为5 μL时,响应电流值达到最大,继续增加石墨烯用量,峰电流值减小,这可能是电极表面形成的石墨烯薄膜厚度过大,从而阻碍了电子传递并使界面稳定性降低.因此,选用5 μL为最优石墨烯用量.

2.3.2 富集电位对镉离子响应信号的影响 图4为富集电位对镉离子响应电流值的影响.由图4可知,随着电化学富集电位朝着负向增大,镉离子溶出峰电流值先增大后减小,在富集电位为-1.0 V时达到最大.富集电位越低,溶液中Cd2+越易于扩散至电极表面并能够得到充分还原,溶出时峰电流值相应增加;当电位低于-1.0 V时,由于出现析氢现象,从而干扰Cd2+测定,溶出峰电流值就会相应减小.因此富集电位选用-1.0 V.


2.3.3 富集时间对镉离子响应信号的影响 图5为富集时间对镉离子响应电流的影响.以0.1 mol/L KCl(pH=3.0)作为支持电解质,考察了富集时间在60~360 s范围内对镉响应信号的影响.由图5可知富集时间明显影响镉离子的响应信号,在60~300 s范围内,镉离子的响应电流信号随着富集时间的增加而增大,这是因为随着富集时间增加,富集在电极表面的Cd2+越多,还原越完全,溶出峰电流值也越大.当富集时间为300 s时达到最大,继续增加富集时间,响应电流变化基本趋于平衡.因此,选用300 s作为富集时间.
2.3.4 pH值对镉离子响应信号的影响 图6为采用Britton-Robison (BR)缓冲溶液作为支持电解质,考察pH值在2.0~6.0范围内对镉离子的溶出峰电流的影响.如图6所示,随着pH值的增大,镉离子的响应电流信号先增大后减小,当pH值为3.0时,镉离子的响应信号达到最大.因此,最优的pH值为3.0.

2.3.5 支持电解质对镉离子响应信号的影响 图7为支持电解质对镉离子响应电流的影响.比较Cd2+在0.1 mol/L HCl、PBS、KH2PO4、NaCl、KCl、Na2SO4、BR、H2SO4溶液(pH=3.0)中的溶出峰,以KCl作为支持电解质的响应电流值最大,且峰形最好.因此,我们选用0.1 mol/L KCl(pH=3.0)作为支持电解质.
2.4 传感器的分析性能
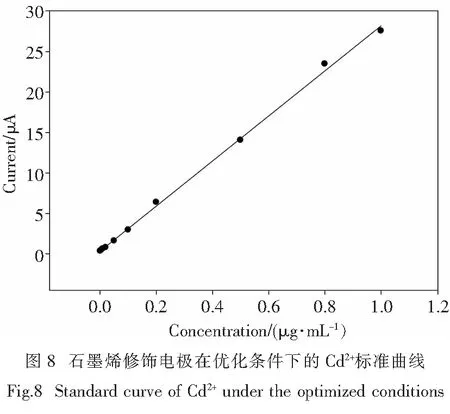
2.4.1 线性实验 图8为石墨烯修饰电极在优化条件下测得的响应电流值与Cd2+浓度之间的线性曲线.如图8所示,响应电流值与Cd2+的浓度在0.001~1 μg/mL范围内呈良好的线性关系.线性方程为y=27.859 2x+0.344 5,相关系数R=0.998,检出限为0.001 μg/mL.
2.4.2 干扰实验 选取Na+、K+、Cl-、NO3-、PO43-等地表水中常见的阴阳离子,重金属离子As3+、Cu2+、Pb2+进行干扰实验.实验结果表明:Na+、K+、Cl-、NO3-、PO43-、As3+对测试结果不产生干扰.加入等量的Cu2+在-0.18 V处产生新的溶出伏安峰,对镉离子测定产生负干扰;等量的Pb2+在-0.56 V处出现新的溶出伏安峰,对镉离子的测定同样产生负干扰.
2.4.3 重复性实验 采用6根石墨烯修饰电极测定1 μg/mL Cd2+,相对标准偏差(RSD)为2.56%,表明传感器具有良好的重现性.采用同一根石墨烯修饰电极测定1 μg/mL Cd2+,连续测定6次,相对标准偏差(RSD)为2.51%,表明传感器可以重复使用.
2.4.4 实际样品的测定 首先将刚取来的湘潭大学自来水和画眉潭水样静置0.5 h,然后过滤除杂,进行测定,结果未检测出镉离子,为了进一步证实所提出方法的可靠性,采用实际样品加标回收实验,以确定在实际应用中样品基质对镉离子的测定不产生干扰,结果如表1所示.

表1 实际样品加标回收实验
3 结 论
本实验提出了以电化学还原氧化石墨烯法制备石墨烯,构建石墨烯修饰玻碳电极,选用方波伏安法测定水中微量镉离子.电化学还原氧化石墨烯来制备石墨烯,不需要加入强还原剂(如肼),是一种绿色制备石墨烯的方法.石墨烯大的比表面积、良好的导电性以及电催化性能明显提高了镉离子的响应电流信号,改善了电极的分析性能.该方法简单灵敏,线性范围较宽(0.001~1 μg/mL),检出限较低(0.001 μg/mL),重现性及重复性好,能应用于实际水样中镉的快速测定.
[1] 刘杰. 镉的毒性和毒理学研究进展[J]. 中华劳动卫生职业病杂志, 1998, 16(1): 4-6.
[2] 李军, 汪模辉, 陈文. 镉、铅、铬、铜的电化学分析[J]. 广东微量元素科学, 2006, 13(7): 21-25.
[3] NOVOSELOV K S, GEIM A K, MOROZOV S V, et al. Electric field effect in atomically thin carbon films[J]. Science, 2004, 306(5696): 666-669.
[4] ALLEN M J, TUNG V C, KANER R B. Honeycomb carbon: a review of graphene[J]. Chemical Reviews, 2010, 110(1): 132-145.
[5] KWON S Y, CIOBANU C V, PETROVA V, et al. Growth of semiconducting graphene on palladium[J]. Nano Letters, 2009, 9(12): 3 985-3 990.
[6] PARK S J, RUOFF R S. Chemical methods for the production of graphenes[J]. Nature Nanotechnology, 2009, 4(4): 217-224.
[7] GEIM A K, NOVOSELOV K S. The rise of graphene[J]. Nature Materials, 2007, 6(3): 183-191.
[8] STOLLER M D, PARK S J, RUOFF R S, et al. Graphene-based ultracapacitors[J]. Nano Letters, 2008, 8(10):3 498-3 502.
[9] BALANDIN A A, GHOSH S, BAO W Z, et al. Superior thermal conductivity of single-layer graphene[J]. Nano Letters, 2008, 8(3): 902-907.
[10] BOLOTIN K I, SIKES K J, JIANG Z, et al. Ultrahigh electron mobility in suspended graphene[J]. Solid State Communications, 2008, 146(9): 351-355.
[11] LEE C G, WEI X D, HONE J, et al. Measurement of the elastic properties and intrinsic strength of monolayer graphene[J]. Science, 2008, 321(5887): 385.
[12] BAI X J, WANG L, ZONG R L, et al. Performance enhancement of ZnO photocatalyst via synergic effect of surface oxygen defect and graphene hybridization[J]. Langmuir, 2013, 29(9): 3 097-3 105.
[13] WENG B, WU J, XU Y J, et al. Observing the role of graphene in boosting the two-electron reduction of oxygen in grapheme-WO3nanorod photocatalysts[J]. Langmuir, 2014, 30(19): 5 574-5 584.
[14] LV W, TANG D M, YANG Q H, et al. Low-temperature exfoliated graphenes: vacuum-promoted exfoliation and electrochemical energy storage[J]. ACS Nano, 2009, 3(11): 3 730-3 736.
[15] CHEN D, TANG L H, LI J H. Graphene-based materials in electrochemistry[J]. Chemical Society Reviews, 2010, 39(8):3 157-3 180.
[16] GUO S J, DONG S J. Graphene nanosheet: synthesis, molecular engineering, thin film, hybrids and energy and analytical applications[J]. Chemical Society Reviews, 2011, 40(5): 2 644-2 672.
[17] GUO Y L, WU B, MA Y Q, et al. Electrical assembly and reduction of graphene oxide in a single solution step for use in flexible sensors[J]. Advanced Materials, 2011, 23(40): 4 626-4 630.
[18] COTE L J, KIM F, HUANG J X. Langmuir-Blodgett assembly of graphite oxide single Layers[J]. Journal of the American Chemical Society, 2009, 131(3): 1 043-1 049.
[19] GUO H L, WANG X F, XIA X H, et al. A green approach to the synthesis of graphene nanosheets[J]. ACS Nano, 2009, 3(9): 2 653-2 659.
[20] WANG Z J, ZHOU X Z, ZHANG H, et al. Direct electrochemical reduction of single-layer graphene oxide and subsequent functionalization with glucose oxidase[J]. The Journal of Physical Chemistry C, 2009, 113(32): 14 071-14 075.
[21] GEIM A K. Graphene: status and prospects[J]. Science, 2009, 324(5 934): 1 530-1 534.
责任编辑:朱美香
An Electrochemical Sensor for the Determination of Cd2+Based on Graphene
WANGSui-ping1,2*,HANZheng1,YANGTong1,LIWei-wei1,ZHANGCai-tong1,LIUYue-jin1
(1.Hunan College Key Laboratory of Heavy Metal Pollution Control, College of Chemical Engineering, Xiangtan University, Xiangtan 411105 2.State Key Laboratory of Chemo/Biosensing and Chemometrics, Hunan University, Changsha 410082 China)
An electrochemical sensor of Cd2+was constructed by electrochemical reduction of graphene oxide on the glassy carbon electrode (GCE). The determination of Cd2+was proceeded by square wave voltammetry (SWV). Stripping voltammetric behavior of Cd at graphene modified electrode was studied. The amount of graphene, deposition potential, deposition time, pH and the supporting electrolyte were optimized. In comparison with the bare glassy carbon electrode, the response signal of the graphene modified GCE was obviously increased. Under the optimal conditions, the linear calibration curve ranges from 0.001 to 1 μg/mL. The linear equation wasy= 27.859 2x+0.344 5 (R=0.998). The detection limit was 0.001 μg/mL. The reproducibility and repeatability were also investigated with RSD of 2.56% (n=6) and 2.51% (n=6), respectively. Owing to its simple fabrication, high sensitivity, fast response, good stability and repeatability, the developed sensor can serve as promising electrochemical platform for the detection of Cd2+in real samples.
graphene; Cd2+; electrochemical reduction; square wave voltammetry
2014-10-16
湘潭大学博士科研启动项目(11QDZ04);湖南省自然科学联合基金项目(13JJ9004);化学生物传感与计量学国家重点实验室开放课题(2012019)
王穗萍(1975— ),女,湖南 常德人,博士,副教授,硕士生导师.E-mail:suiping66@126.com
O65
A
1000-5900(2015)01-0047-05

