大青叶配方颗粒中靛玉红含量测定方法验证
王小敏,王盼盼,薛艳许,鲁倩倩,耿 硕,袁亚兰
(神威药业集团有限公司,河北 栾城 051430)
大青叶配方颗粒中靛玉红含量测定方法验证
王小敏,王盼盼,薛艳许,鲁倩倩,耿 硕,袁亚兰
(神威药业集团有限公司,河北 栾城 051430)
目的:确定所采用的HPLC法适用于大青叶配方颗粒中靛玉红的含量检测。方法:靛玉红含量测定采用HPLC法,色谱柱:Thermo ODS-C18柱(4.6mm×250mm,5μm);流动相:甲醇-水(75∶25);检测波长为289nm。对3个批次的大青叶配方颗粒进行含量测定方法学验证。结果与结论:大青叶颗粒中靛玉红的含量测定可采用HPLC法。
大青叶配方颗粒;靛玉红; HPLC法;含量测定
大青叶配方颗粒是由大青叶经过现代科学方法精制而成,具有清热解毒、凉血消斑的作用,用于治疗温病高热、神昏、发斑发疹、痄腮、喉痹、丹毒、痈肿。大青叶为十字花科植物菘蓝IsatisindigoticaFort.的干燥叶[1],其化学成分复杂,含有靛玉红、靛蓝、扶桑甾醇等多种成分,其活性成分为靛玉红和靛蓝[2]。药理研究表明,靛玉红和靛蓝具有抑菌、抗病毒、解热抗炎等功效。本文选择靛玉红作为指标,采用HPLC法进行含量测定,控制大青叶配方颗粒的质量。
1 材料
1.1 样品
大青叶配方颗粒(生产厂家:神威药业集团有限公司),批号14110621、15010121、15010821。规格:每袋装1.3g。
1.2 仪器与试药
高效液相色谱仪(戴安,U3000紫外检测器,化学工作站);电子分析天平(型号:CPA225D);甲醇为色谱纯(天津市科密欧化学试剂有限公司)、水为纯化水,其它试剂均为分析纯。靛玉红对照品为中国食品药品检定研究院提供(批号110717-200204)。
1.3 色谱条件
色谱柱:Thermo ODS-C18柱(4.6mm×250mm,5μm);流动相:甲醇-水(75∶25);紫外检测器检测,检测波长为289nm。理论塔板数按靛玉红峰计算应不低于4 000。
2 方法与结果
2.1 对照品溶液制备
精密称取靛玉红对照品0.009 97g、0.009 61g,分别置100mL量瓶中,加甲醇溶液并稀释至刻度,作为对照品储备液;精密量取1mL于50mL量瓶中,加甲醇适量,摇匀,加甲醇溶液并稀释至刻度,作为对照品溶液(10℃以下保存)。
2.2 供试品溶液制备
分别取上述三批大青叶配方颗粒适量,批号4110621:1.014 2g、1.013 2g;批号15010121:1.004 7g、1.004 1g;批号15010821:1.023 2g、1.019 6g。精密称定,各加甲醇25mL,称定重量,超声处理30min,放至室温,用甲醇补足减失的重量,滤过,取续滤液,即得。
2.3 含量测定
精密吸取对照品溶液与供试品溶液各20μL,注入液相色谱仪,测定,即得。上述三批样品所对应的峰面积测定结果见表1。含量测定结果见表2。
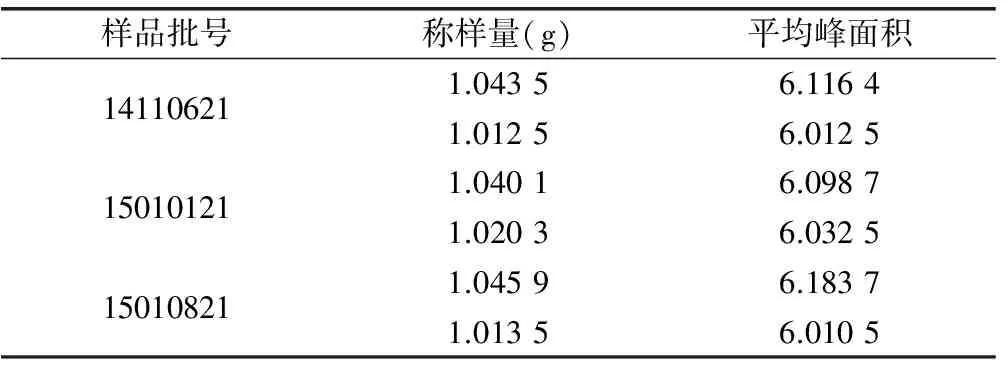
表1 不同批号样品峰面积测定结果
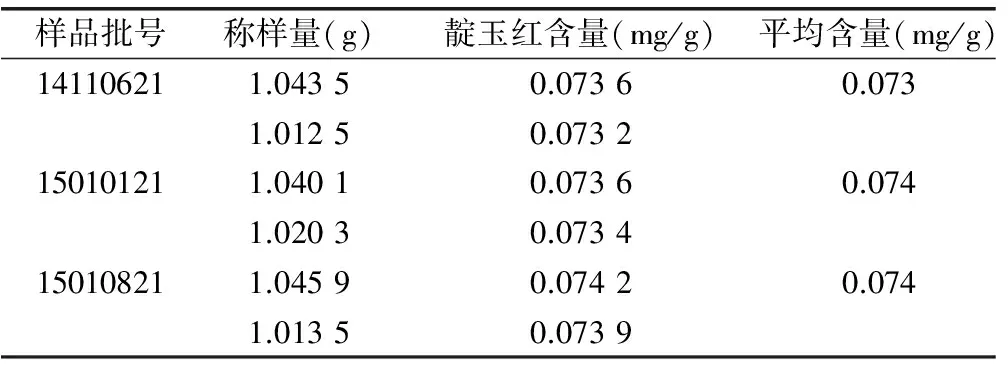
表2 含量测定结果
2.4 方法学验证
以下均取15010821批大青叶配方颗粒进行试验。
2.4.1 重复性考察 分别取供试品粉末各6份,精密称定,按“2.2”项下方法制备供试品溶液,按上述色谱条件进行分析,精密吸取对照品溶液20μL,供试品溶液20μL,注入液相色谱仪,测定,以外标两点法对数方程计算,即得。测得对照品20μL的平均峰面积为3.824 2;供试品结果见表3,RSD<2%,表明重复性良好。
2.4.2 靛玉红标准曲线绘制 精密吸取靛玉红对照品溶液5.0、10.0、15.0、20.0、25.0、30.0μL注入色谱仪,测定和记录靛玉红的面积,峰面积依次为:0.961 72、1.937 25、2.899 84、3.850 72、4.880 03、5.860 65。以面积为纵坐标,
以进样量为横坐标,得标准曲线方程为Y=101.82X-0.025 5,R2=0.999 9(r=0.999 7)。结果表明,靛玉红在0.01~0.06μg范围内具有良好的线性关系。标准曲线见图1。
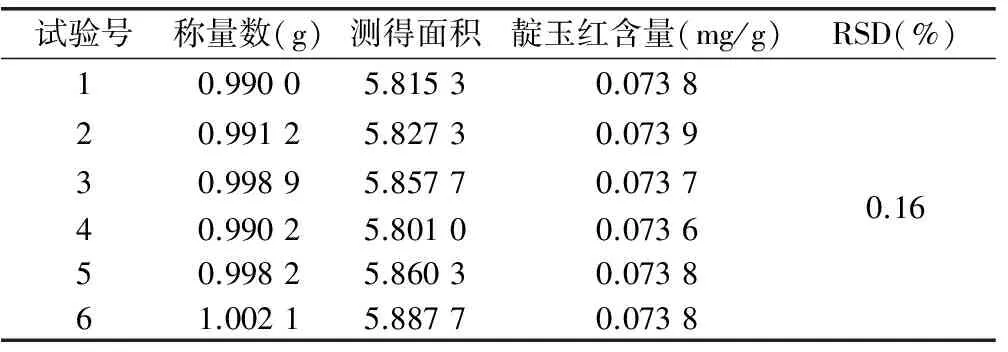
表3 重复性考察结果
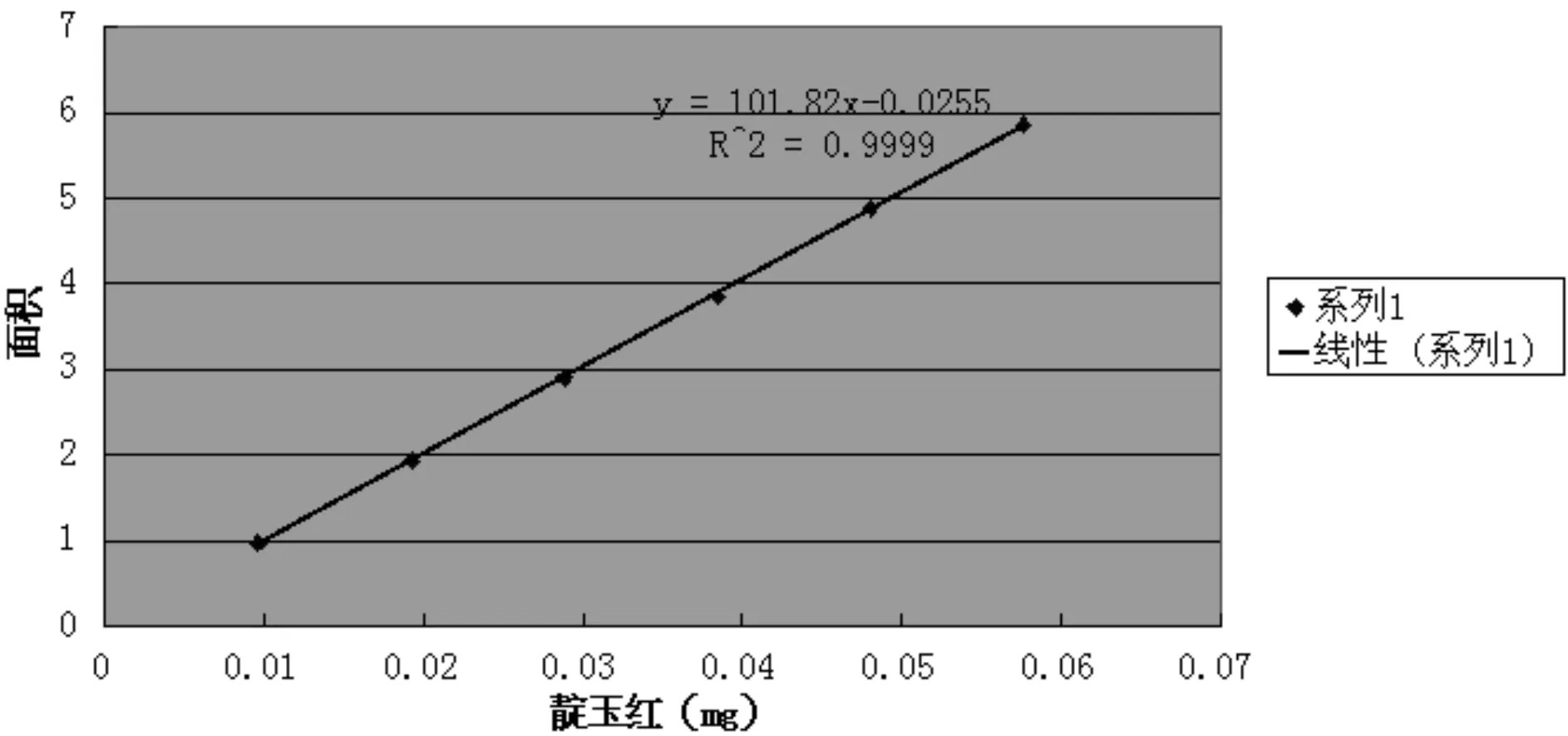
图1 靛玉红标准曲线
2.4.3 阴性对照试验 按照生产工艺制备阴性样品,取阴性样品适量,研细,精密称取1.021 5g,各加甲醇25mL,称定重量,超声处理30min,放至室温,用甲醇补足减失的重量,滤过,取续滤液,即得。精密吸取靛玉红对照品溶液、阴性对照品溶液、供试品溶液各20μL,注入液相色谱仪,记录色谱图。结果表明:阴性对照无干扰。各样品溶液HPLC图谱见图2-图4。
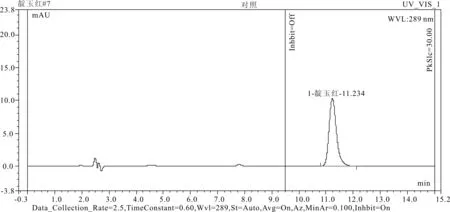
图2 靛玉红HPLC图谱
2.4.4 稳定性试验 精密称取15010821批供试品溶液1.001 9g,室温放置,在不同放置时间分别取样测定,按上述色谱条件进行分析,结果表明供试品溶液在8h内稳定,见表4。
2.4.5 回收率试验 分别精密称取供试品适量,精密加入定量的靛玉红对照品,按“2.2”项下方法制备供试品溶液,按上述色谱条件进行分析,进行回收率测定,结果见表5。
2.4.6 精密度试验 精密吸取15010821批溶液,连续进样6次,RSD=0.23%,表明该仪器精密度良好。测定结果见表6。
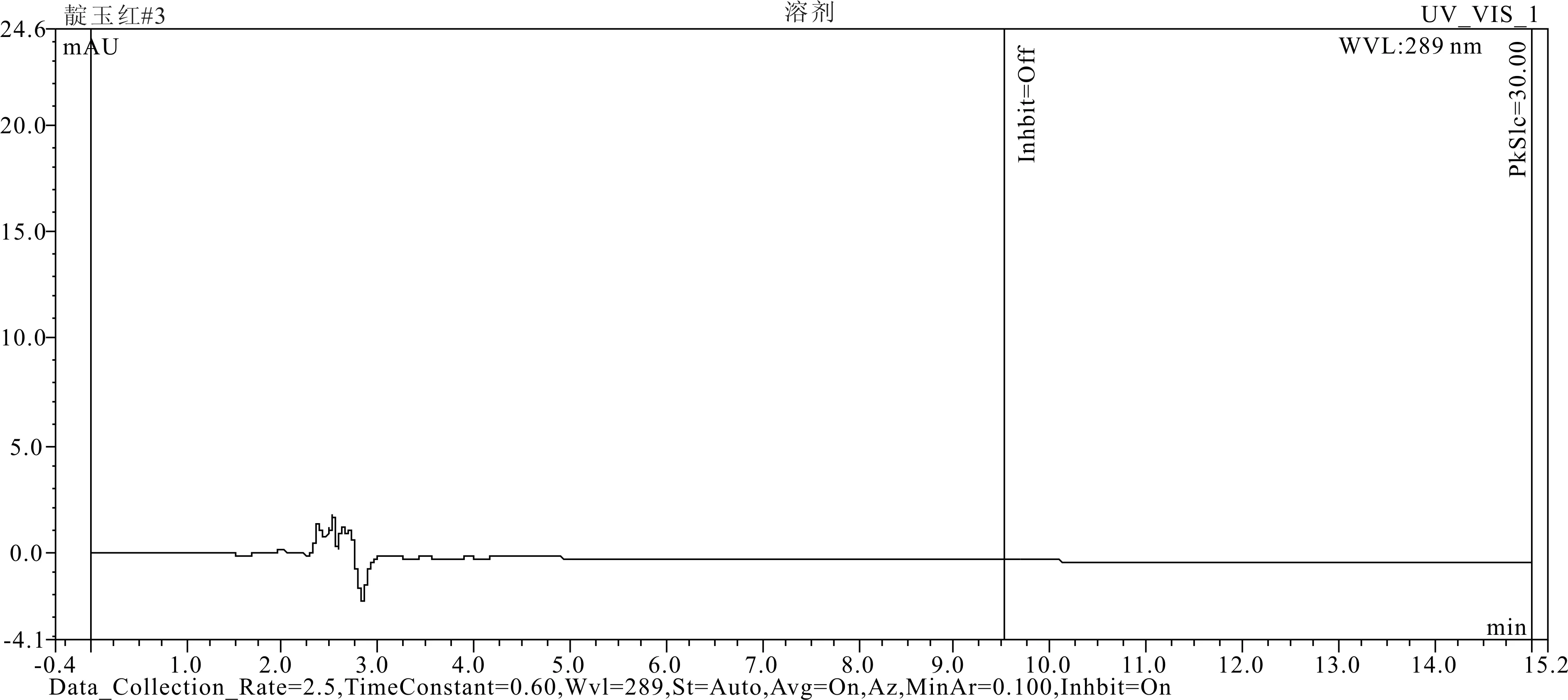
图4 阴性对照HPLC色谱

时间(h)样品面积RSD(%)05.908810.6725.8993145.9532065.9908685.97126
3 讨论
根据上述结果可以看出:大青叶配方颗粒中靛玉红含量采用Thermo ODS-C18柱(4.6mm×250mm,5μm)分离,检测波长为289nm,流动相为甲醇-水(75∶25),流速1.0mL/min,靛玉红在0.01~0.06μg范围内与峰面积呈良好线性关系,r=0.999 9,平均回收率为101.3%(RSD=1.3%,n=9)。所以大青叶配方颗粒在进行靛玉红含量检测时可以采用高效液相色谱法进行测定。

表5 样品回收率试验结果
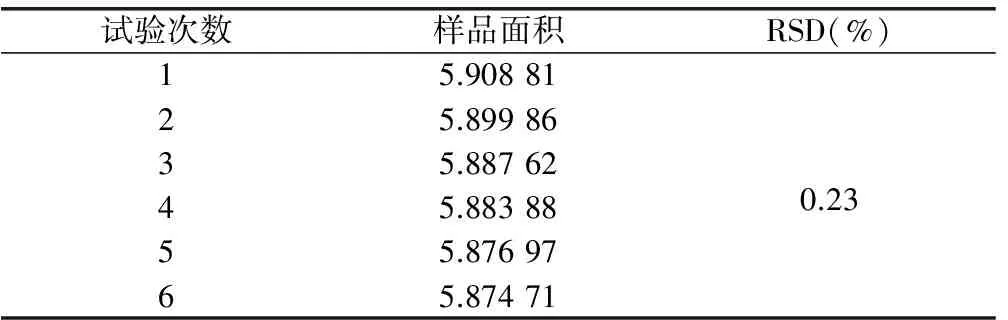
表6 精密度试验结果
[1] 国家药典委员会.中华人民共和国药典[M].一部.北京:中国医药科技出版社,2010:27.
[2] 赵国平,戴慎,陈仁涛.中国大辞典[M].第2版.上海:上海科学技术出版社,2006:165-166.
(责任编辑:魏 晓)
Verification Method of the Content of Indirubin in Folium Lsatidis Granules
Wang Xiaomin,Wang Panpan,Xue Yanxu,Lu Qianqian,Geng Shuo,Yuan Yalan
(Shineway Pharmaceutical Group Co.,ltd,Hebei 051430,China)
Objective:HPLC method for determining the suitable detection method of indirubin in Folium Isatidis granules.Methods:Determination of indirubin content by HPLC method,Thermo ODS-C18column(4.6mm×250mm,5μm); Methanol-water(75∶25) as mobile phase; The detection wavelength was 289nm.Validation of Folium Granule on 3 batches of content determination method.Results and Conclusion:the determination of indirubin in Folium Isatidis granules can be Indigo by HPLC method.
Folium Isatidis Granules;Indirubin;HPLC;Contented Determination
2015-07-01
王小敏(1981-),女,神威药业集团有限公司助理工程师,研究方向为化学药品检验。
R284.1
A
1673-2197(2015)23-0024-03
10.11954/ytctyy.201523010

