微波辅助合成高性能碳包覆Li4 Ti5 O12及其电化学性能
陈腾远,李在均
(江南大学化学与材料工程学院,江苏无锡214122)
锂离子电池作为高效的储能装置已经广泛应用于笔记本电脑[1-5]、移动电话及其他便携式电子产品中。电极材料决定了锂电池的性能,因此,提高锂电池性能的关键是发展新型高效的电极材料。锂电池中,负极一般采用碳材料,最常用的就是石墨。但是,石墨材料由于内部结构脆弱,大电流密度下使用寿命较短,难以在大功率动力电池中运用[6-7]。锂离子嵌入电压较低,容易导致其在首次充放电形成钝化膜(SEI),使材料的有效利用率大大降低。为解决这些问题,最近科研人员将研究重点放在Li4Ti5O12(LTO)上[8-9]。
Li4Ti5O12具有良好的循环稳定性(循环寿命在3 000次以上)、不与电解液反应、充放电电压平台稳定、安全性高和容易制备等优点。尖晶石型Li4Ti5O12在锂嵌入时,还原为深蓝色的Li7Ti5O12[10],理论充放电比容量为170 mA·h/g。生成的Li7Ti5O12的晶胞参数a变化很小,仅从0.836 nm增加到0.837 nm,几乎没有变化,故被称为“零应变”电极材料。另外,Li4Ti5O12在首次充放电过程中不形成SEI膜,这些性质从理论上解决了石墨材料结构充放电过程中存在的一些问题。同时,Li4Ti5O12还具有抗过充性能好、热稳定性能好和安全性能好等优点,使之作为负极材料在电动汽车和混合动力汽车等大功率动力电池领域有广泛的应用前景。
纯相Li4Ti5O12晶体固有电子电导率仅为1.1×10-7S/m左右,这使得该负极材料在高倍率工作环境下充放电比容量衰减较为严重,因此,对Li4Ti5O12进行改性提高其电导率以减少其大电流密度下充放电比容量的衰减成为研究重点。目前,解决方法大致可分为两种:一种方法是减小Li4Ti5O12晶体粒径以增加比表面积,从而提高电池材料与电解液的接触面积(如可以通过制备纳米级颗粒[11],多孔结构[12]等均一形貌的 Li4Ti5O12,提高材料的利用率)。但是,这种方法存在工业应用问题,Li4Ti5O12晶体粒径越小,该材料的振实密度越小,电池材料的体积比容量越小,而体积比容量是商品电池里面最为关键的参数,因此低振实密度的材料难以在电池工业中广泛的应用。另一种方法是通过对Li4Ti5O12改性以增加其电导率(通过掺杂金属元素[13]和碳元素[14]进行改性提高电导率,实现高倍率性能),这也存在缺陷:掺杂元素的加入,使得Li4Ti5O12晶型不够完整,这就影响了Li4Ti5O12“零应变”这一特性,进而减少了该材料的电池性能的循环寿命。因此,复合碳材料不失为最佳的一种做法。Li4Ti5O12的合成方法主要有固相法和液相法(溶胶-凝胶法),溶胶-凝胶法因合成步骤简单、纯度高、产率高等优点最受欢迎,并已成为材料科学领域的一个研究热点[15-21]。因此,文中采用微波辅助,以叔丁醇的“软模板”减小Li4Ti5O12的颗粒尺寸,并用P123减小Li4Ti5O12的二次团聚粒子的大小,在后续隔绝空气煅烧后制备得到Li4Ti5O12/C材料。这一方法得到的电池材料晶型不会改变,而且没有其他金属元素的掺杂,也不会影响材料的循环使用寿命。电化学性能测试发现,该复合材料表现出了优异的性能。
1 材料与方法
1.1 试剂与仪器
1.1.1 试剂 叔丁醇,二水醋酸锂,乙醇,N-甲基吡咯烷酮(NMP),均为分析纯,皆由国药集团化学试剂有限公司提供;钛酸四丁酯,乙炔黑,聚偏氟乙烯(PVDF),P123(聚环氧乙烷-聚环氧丙烷-聚环氧乙烷三嵌段共聚物),由SIGMA-ALORICH公司提供;LiPF6(LB-5275),由张家港国泰华荣化工新材料有限公司提供;实验用水为二次蒸馏水。
1.1.2 仪器 GZX-9030MBE数显鼓风干燥箱,上海博迅实业有限公司医疗设备厂制造;DZF-6020型真空干燥箱,BX5200H超声分散仪,均为上海新苗医疗器械制造有限公司制造;电化学工作站660D,上海辰华仪器有限公司制造;D8 Advance型X-射线衍射仪,德国Bruker AXS公司制造;S4800型扫描电镜,日本日立公司制造。
1.2 LTO/C 的制备
将10.2 g钛酸四丁酯和0.05 g P123超声分散于95 mL叔丁醇,配成A溶液(LA),微波加热回流,然后滴加B溶液(2.448 g醋酸锂溶于2 mL去离子水和20mL乙醇的混合液),滴加完毕后继续回流反应15 min,然后蒸干溶剂得到LTO前驱体。样品转入管式炉,于空气中350℃ 下保温3 h,然后惰性氛围中(V(Ar)∶V(H2)=95∶5)600℃煅烧8 h得到LTO/C。另外,对照LTO样品以相同的物料配比(10.2 g钛酸四丁酯和2.448 g醋酸锂)以传统的溶胶-凝胶法制备得到,并在空气中600℃煅烧8 h得到LTO晶体。反应流程如图1所示。
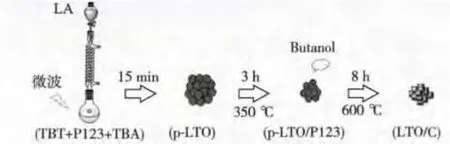
图1 LTO/C的制备Fig.1 Preparation process of LTO/C
1.3 电极片的制备及电池性能测试
将LTO/C或其他电活性材料,乙炔黑,聚偏氟乙烯按质量比为80∶10∶10混合均匀,加入适量N-甲基吡咯烷酮(NMP)分散,形成的浆料均匀地涂覆于铜箔上,110℃ 真空干燥10 h得电极片。以按上述方法制备的电极片为正极,金属锂片为负极,聚丙烯膜(Celgard 2400)和浓度为1 mol/L LiPF6分别作为隔膜和电解质,在充满氩气的手套箱中装配成CR2016型扣式电池。室温静置12 h,然后在LAND CT2001A电池测试系统进行电化学性能测试,电压范围为0.5~3 V。循环伏安测试中,扫描速率1 mV/s,温度保持为25℃,电压扫描范围为0.5~3 V。交流阻抗测试条件:开路电压设置为0.2 V,扰动电压为5 mV,频率范围100 ~0.01 kHz。
2 结果与讨论
2.1 材料表征
实验方法对形成的钛酸锂前驱体影响较大,文中通过扫描电镜(SEM)对上述合成材料的前驱体形貌进行表征。图2为采用不同方法制备的不同放大倍数下的LTO前驱体的SEM图。
由图2(a)和图2(b)可以看出,以叔丁醇作为溶剂的LTO前驱体分散均匀,具有较小的一次团聚粒子,二次团聚粒子表面光滑平整,大小均一,仅为2μm左右。这与传统溶胶-凝胶法制备得到的LTO前驱体(图2(c)和图2(d))形成了较为鲜明的对比:图2(c)、图2(d)中LTO前驱体分散混乱,形貌不均一,二次团聚粒子表面凹凸不平,粒径大小分布较广。这是因为传统的溶胶-凝胶法以乙醇为溶剂减缓钛酸四丁酯水解得到LTO前驱体,而文中采用具有“软模板”效应的叔丁醇作为溶剂,叔丁醇具有类似季铵盐的四面体结构,使其具有部分表面活性剂的性能,当叔丁醇与表面活性剂配伍时,使得一次粒子形成均一细小,团聚的二次粒子成球形,且形貌单一。前驱体粒子的细小和单一有益于煅烧过程中形成均质LTO晶体。
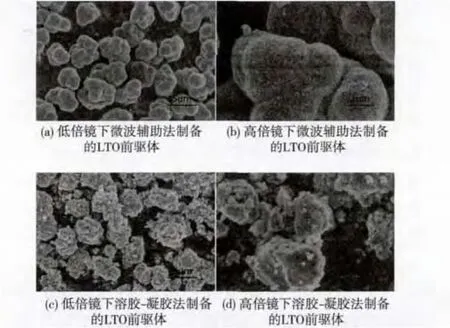
图2 不同方法制备的LTO前驱体SEM图Fig.2 SEM of LTO precursor by different preparation methods
采用扫描电镜和透射电镜对600℃温度下煅烧8 h后得到的LTO/C的形貌进行表征,具体结果如图3所示。

图3 LTO的SEM和TEM图谱Fig.3 SEM and TEM of the LTO
由图3(a)可以看出:LTO晶体表面平整,结晶完整,晶体尺寸在2μm左右。而在图3(b)中可以清晰看到,LTO晶体结构完整,整个晶体不均一,且具有相当明显的晶体棱角,说明晶体结晶生长结构完整,为较好的晶体。
XRD是材料结构表征的重要手段,可以对材料结构进行定性分析。图4为样品LTO/C和LTO的XRD图。由图4所知:LTO为尖晶石型结构,通过与PDF卡片(PDF No.49-0207)比较可以看出,尖晶石型 LTO 的主要特征峰值为:18.33°,35.57°,43.24°,47.35°,57.21°,62.83°,66.07°,74.34°,79.34° 都在图中清晰显示,并无杂峰存在。而图中XRD衍射峰的峰型尖锐,表明所有样品结晶良好。LTO/C和LTO的衍射峰没有明显的差异,说明使用微波辅助方法、更换传统溶胶法所用溶剂,并未对LTO的晶体结构产生明显的影响。
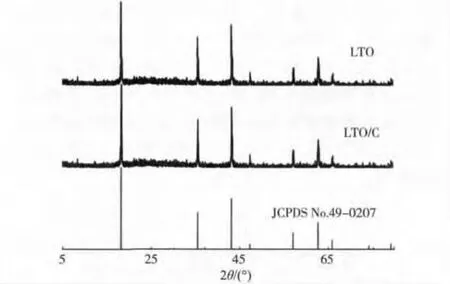
图4 LTO/C和LTO材料的XRD曲线Fig.4 XRD patterns of the LTO/C and LTO m aterials
2.2 电化学性能
文中考察了LTO/C和LTO电极材料的循环伏安行为,扣式电池正极中的LTO电极材料发生了氧化还原反应,其反应机理如下:

就理论而言,LTO电极材料的CV曲线会出现一个对称的氧化还原峰,这在图5中LTO/C和LTO电极材料的循环伏安曲线中得到了证实。图5中测试扫描速率为1 mv/s,扫描电压范围是从0.5~3 V。由图5可以看出,所有电极都在1.45 V和1.75 V表现出相似的氧化还原峰,且由于碳包覆LTO电极材料,LTO/C相对于LTO的氧化还原峰较为尖锐,最高峰电流两者分别达到0.7和0.4 mA/cm2,说明碳材料的加入,使得LTO/C材料具有较好的电子和离子导电性能,这在下面的交流阻抗中得到进一步证实。
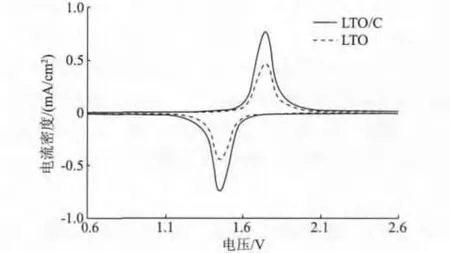
图5 LTO/C和LTO材料的CV曲线Fig.5 CV curves of the LTO/C and LTO materials
LTO/C和LTO的电化学交流阻抗谱如图6所示。两种电极的交流阻抗谱图都是由3个部分组成:高频区与实轴的焦点、中频区的半圆和低频区的直线部分。高频区与实轴的交点所截取的阻值为欧姆阻值,包括电解液阻抗和电极阻抗;中频区半圆代表电荷转移过程阻抗,即电子转移阻抗;低频区的直线代表Li+在电极材料中的扩散阻抗。图6中LTO/C的电子转移阻抗小于 LTO,说明 Li+在LTO/C中有更快的传输速率,这一结论与循环伏安相一致,同时可以证明LTO/C具有较为优异的电化学性能。
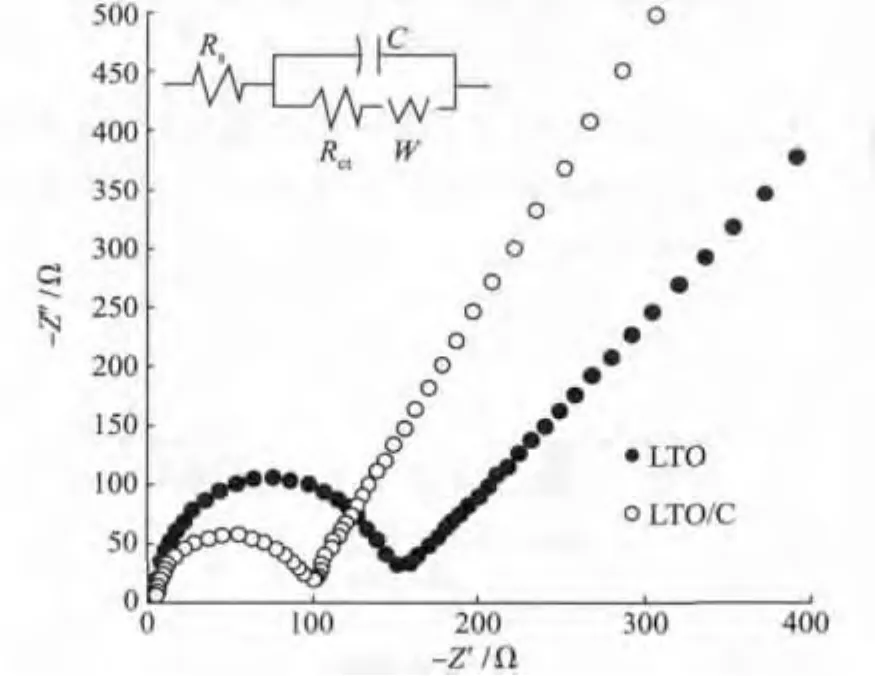
图6 LTO/C和LTO材料的交流阻抗图谱Fig.6 Electrochem ical im pedance spectroscopies of the LTO/C and LTO
表1为等效电路参数。由表1可以看出,相对于LTO,LTO/C在RS和RCT都有明显的改善,交换电流密度(J=RT/nFRCT)也得到了提高。这进一步证明了在晶体外部的碳材料的复合可以改善LTO晶体的电导率。
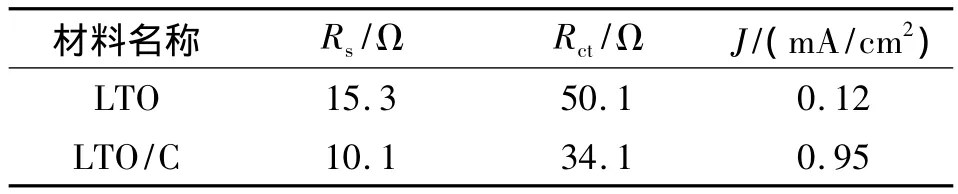
表1 等效电路阻抗参数Tab.1 Im pedance parameters calculated from equivalent circuits
LTO晶体为白色,不导电,在空气中能够稳定存在。由于LTO属于不导电物质,故在充放电过程中,容量和循环性能不能得到很好地发挥,尤其是倍率性能,因此改善LTO的电导率,就能提高LTO的电化学性能。图7为LTO/C和LTO在0.1C倍率下的充放电性能曲线。
微波辅助制备得到的LTO/C和传统溶胶法制备得到的LTO在0.1C倍率下的首次充放电比容量分别达到了159.7 mA·h/g和151.1mA·h/g,比较充放电容量可以得出:LTO/C相对于LTO表现出较高的放电容量,LTO/C提升了5%左右,提升效果不明显。
LTO/C 和LTO在不同倍率下(0.2C,0.5C,1C)的循环性能如图8所示。
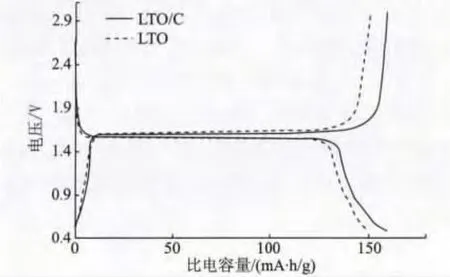
图7 0.1C倍率下LTO/C和LTO材料首次充放电曲线Fig.7 First charge discharge curves of LTO/C and LTO at 0.1C
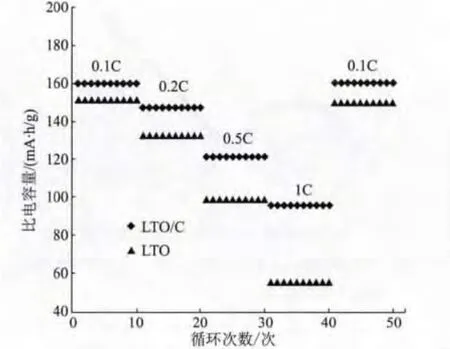
图8 LTO/C和LTO在不同倍率下的放电容量Fig.8 Discharge capacity of LTO/C and LTO at differentmagnification
由图8可以看出,LTO/C在0.2C倍率下,其放电容量为147.1 mA·h/g,仍具有较大的比电容量;尽管如此,随着充放电倍率的增加,其放电容量为0.5C 下121.2 mA·h/g,1C 倍率下95.3 mA·h/g,结果仍较为满意。但是,相对于LTO/C,LTO的衰减较为明显,随着充放电倍率的提高,其放电比容量呈迅速衰减趋势:在0.2C下为132.4 mA·h/g;0.5C 仅为98.4mA·h/g;1C下只剩55.2mA·h/g。由此可见,在相同情况下,LTO/C相比于LTO具有较好的倍率性能。
根据上述情况可以得到:改善后的LTO/C复合材料,不仅在低倍率情况下得到更好的比容量,而且在大倍率情况下,相对于传统溶胶-凝胶法制备得到的LTO具有相当优异的性能,其比容量提升了72.6%。上述结果表明,掺入适量的碳材料,不仅有利于材料倍率性能的提高,还有利于材料容量的发挥。导致上述现象的原因是:叔丁醇、P123、微波的辅助,减小了材料的颗粒尺寸,可以使LTO/C复合材料在电化学工作中缩短了Li+的迁移路径,增大了电解液接触面积,提高了电子导电性能。低倍率下充放电容量基本不变,LTO/C复合材料的循环性能优异。图9为LTO/C在0.1C时的循环稳定性实验结果。
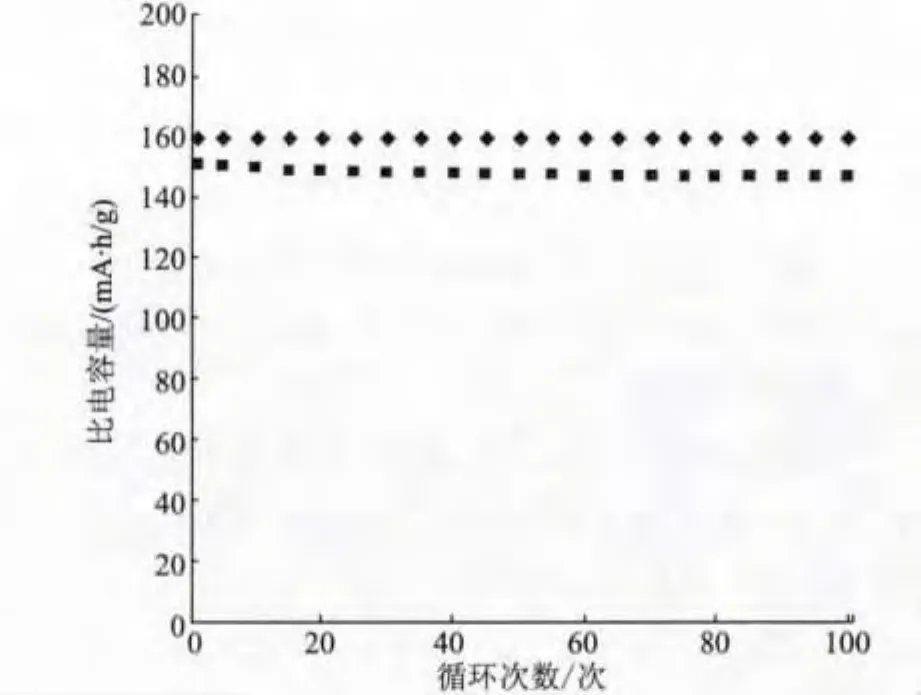
图9 LTO/C在0.1C下循环稳定性Fig.9 Cyclic performance of LTO/C at 0.1 C
由图9可以看出,扣式电池有非常好的寿命循环性。循环100次后容量仍保持158.9 mA·h/g,相当于首次放电容量的99.9%。而LTO材料循环100次后容量仅为147.1 mA·h/g,相当于首次充放电容量的97.4%,衰减效果明显。
3 结语
通过微波辅助和采用叔丁醇介质,以P123为表面活性剂成功合成了一种碳包覆LTO晶体,制备得到的细小的LTO前驱体高温下结晶完整形成大的LTO晶体,P123在隔绝空气中分解为无定型碳包覆与LTO晶体中形成LTO/C,相比于传统溶胶-凝胶法得到的LTO,具有较高的比电容量,又具有大倍率性能,可广泛应用于各种商品锂离子电池。
[1]卢俊彪,唐子龙,乐斌,等.锂离子电池正极材料LiFePO4的结构与电化学性能的研究[J].高等学校化学学报,2005,26(11):2093-2096.LU Junbiao,TANG Zilong,LE Bin.etal.Structure and electrochemical properties of LiFePO4as the cathode of lithium Ion battery[J].Chemical Research in Chinese Universities,2005,26(11):2093-2096.(in Chinese)
[2]傅强,陈彬,黄小文,等.锂离子电池正极材料LiMn2-xCrxO4电化学性能的研究[J].高等学校化学学报,2004,25(1):128-130.FU Qiang,CHEN Bin,HUANG Xiaowen.et al.Electrochemical properties of LiMn2-xCrxO4as cathodematerials of lithium ionic batteries[J].Chemical Research in Chinese Universities,2004,25(1):128-130.(in Chinese)
[3]唐致远,阮艳莉,宋全生,等.橄榄石复合LiFePO4正极材料的合成及其电化学性能研究[J].高等学校化学学报,2005,26(5):1905-1908.TANG Zhiyuan,RUAN Yanli,SONG Quansheng.et al.Synthesis and electrochemical performance of olivine LiFePO4-based composite cathodematerials[J].Chemical Research in Chinese Universities,2005,26(5):1905-1908.(in Chinese)
[4]周德凤,马越,赵艳玲,等.纳米炭/石墨碳混合材料的电化学性质研究[J].无机材料学报,2004,19(5):1111-1117.ZHOU Defeng,MA Yue,ZHAO Yanling,et al.Electrochemical performance of the composite materials of nano-carbon and graphite-carbon[J].Journal of Inorganic Materials,2004,19(5):1111-1117.(in Chinese)
[5]SHEN CM,ZHANG X G,ZHOU Y K,etal.Preparation and characterization of nanocrystalline Li4Ti5O12by sol-gelmethod[J].Materials Chemistry and Physics,2003,78(2):437-441.
[6]Akihiro M,Katsuhisa T,Hiroyuki F,etal.Charge-discharge characteristics of themesocarbonmiocrobeads heat-treated at different temperatures[J].Adv Mater,2012,25(7):1938-1944.
[7]Matsumura Y,WANG S,Mondori J.Mechanism leading to irrecersible capacity loss in Li ion rechargeable batteries[J].J Electrochem Soc,1995,142(9):2194-2198.
[8]刘志远,陈效华,李燕,等.钛酸锂作负极锂离子电池体系研究[J].华南师范大学学报:自然科学版,2009,11(A02):81-83.LIU Zhiyuan,CHEN Xiaohua,LI Yan.et al.Study on the lithium ion cell system of using Li4Ti5O12as cathode material[J].Journal of South China Normal University:Natural Science Edition,2009,11(A02):81-83.(in Chinese)
[9]陈京才,崔燕,夏信德,等.石墨-钛酸锂复合阳极材料的制备及性能[J].电源技术,2010,34(6):539-542.CHEN Jingcai,CUIYan,XIA Xinde,et al.Preparation and performance of graphite-Li4Ti5O12composite anode for Li-ion cells[J].Chinese Journal of Power Sources,2010,34(6):539-542.(in Chinese)
[10]SUN L,WANG G X,LIU H K,et al.Synthesis of nonstoichiometric amorphous Mg-based alloy electrodes by mechanicalmilling[J].Electrochemical and Solid State Letter,2000,3(3):121-124.
[11]李星,翟美臻.提高Li4Ti5O12高倍率性能和振实密度的研究进展[J].电源技术,2008,32(6):409-412.LIXing,ZHAIMeizhen.Research progress of improving the rate capability and tap density of Li4Ti5O12[J].Chinese Journal of Power Sources,2008,32(6):409-412.(in Chinese)
[12]Erin M S,Scott J B,Jun H K,et al.Three-dimensionally ordered macroporous Li4Ti5O12:effect of wall structure on electrochemical properties[J].Chem Mater,2006,18(2):482-489.
[13]刘瑶,陈猛,武洪彬,等.铬元素掺杂对Li4Ti5O12电化学性能的影响[J].电池工业,2009,14(5):322-324.LIU Yao,CHEN Meng,WU Hongbin,et al.Effects of Cr-doping on the electrochemical performance of Li4Ti5O12[J].Chinese Battery Industry,2009,14(5):322-324.(in Chinese)
[14]HUANG J J,JIANG Z Y.The preparation and characterization of Li4Ti5O12/carbon nano-tubes for lithium ion battery[J].Electrochimica Acta,2008,53(26):7756-7759.
[15]HU M J,JIANG Y Z,YANM.High rate Li4Ti5O12-Fe2O3and Li4Ti5O12-CuO composite anodes for advanced lithium ion batteries[J].Journal of Alloys and Compounds,2014,603:202-206.
[16]YANG C C,HU H C,LIN S J,et.al.Electrochemical performance of V-doped spinel Li4Ti5O12/C composite anode in Li-half and Li4Ti5O12/LiFePO4-full cell[J].Journal of Power Sources,2014,258:424-433.
[17]Kitta M,Akita T,Tanaka S,et al.Two-phase separation in a lithiated spinel Li4Ti5O12crystal as confirmed by electron energy-loss spectroscopy[J].Journal of Power Sources,2014,257:120-125.
[18]Izumi A,Sanada M,Furuichi K,et al.Rapid charge and discharge property of high capacity lithium ion battery applying threedimensionally patterned electrode[J].Journal of Power Sources,2014,256:244-249.
[19]WEN R,YUE J,MA Z F,et al.Synthesis of Li4Ti5O12nanostructural anodematerials with high charge-discharge capability[J].Chinese Science Bulletin,2014,59(18):2162-2174.
[20]LIN C F,FAN X Y,XIN Y L,et al.Monodispersed mesoporous Li4Ti5O12submicrospheres as anode materials for lithium-ion batteries:morphology and electrochemical performances[J].Nanoscale,2014,6(12):6651-6660.
[21]Ziebarth B,Klinsmann M,Eckl T,et al.Lithium diffusion in the spinel phase Li4Ti5O12and in the rocksalt phase Li7Ti5O12of lithium titanate from first principles[J].Physical Review B,2014,89(17):432-441.

