(S)-富马酸替诺福韦二吡呋酯的合成*
黄小光,朱少璇,余柱明,廖 维,陈 溪,刘 毅
(广州白云山制药股份有限公司广州白云山制药总厂,广东广州 510515)
富马酸替诺福韦二吡呋酯(6)是美国Gilead sciences公司研制的核苷酸逆转录酶抑制剂,主要用于艾滋病和慢性乙肝治疗[1-2]。6具有耐受性好、耐药率低、停药反弹率低和肾毒性小等优点,临床应用效果较好[3]。
6的化学结构中含有一个R-构型的手性中心[4-5]。分子药理学研究表明,含有手性因素的化学药物异构体,在人体内的药理活性、代谢过程和毒性存在显著差异[6]。因此,为研究6的原料药中S-构型杂质(S)-6的药理性质,本文以腺嘌呤(1)为原料,与(S)-碳酸丙烯酯反应得(S)-1-(6-胺基-9H-嘌呤-9-基)丙基-2-醇(2);2 与对甲苯磺酰氧甲基膦酸二乙酯(DESMP)反应得(S)-二乙基 【{[1-(6-氨基-9H-嘌呤-9-基)丙基-2-醇]氧}甲基】磷酸酯(3);3与三甲基溴硅烷反应得(S)-替诺福韦(4);4与氯甲基异丙基碳酸酯反应得(S)-替诺福韦二吡呋酯(5);5与富马酸反应合成了(S)-富马酸替诺福韦二吡呋酯[(S)-6,Scheme 1],总收率10.0%,其结构经1H NMR 和ESI-MS确证。该反应路线原料廉价易得,过程简单,便于工业化生产。
1 实验部分
1.1 仪器与试剂
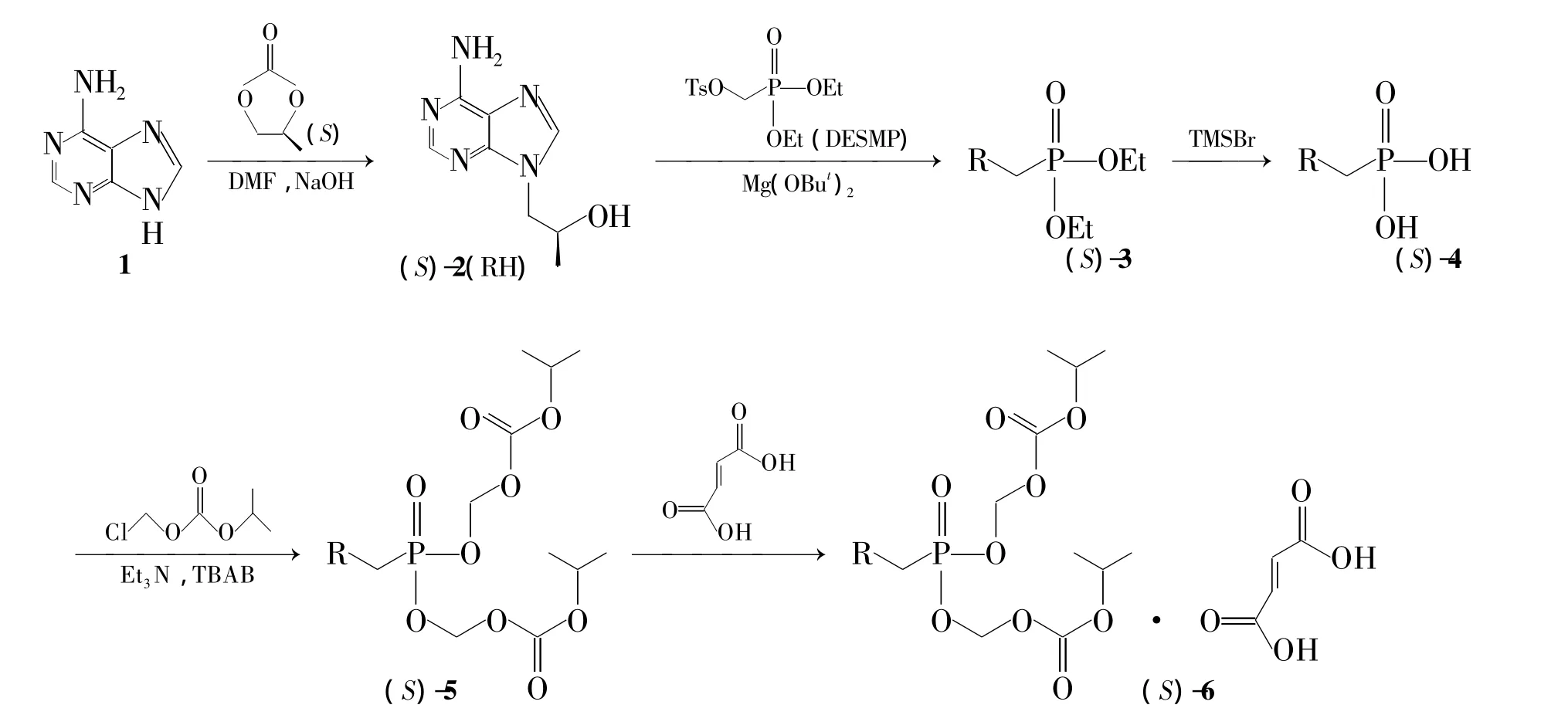
Scheme 1
Bruker-AVANCE AV 400 MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);Finnigan-LCQDeca XP LC-MS型质谱仪;Foss Heraeus-240 CHN Rapid型元素分析仪。
所用试剂均为分析纯。
1.2 合成
(1)(S)-1-(6-胺基-9H-嘌呤-9-基)丙基-2-醇[(S)-2]的合成
在三口瓶中依次加入1 80.00 g(592 mmol),DMF 380 mL,氢氧化钠9.48 g(237 mmol)和(S)-碳酸丙烯酯78.60 g(770 mmol),搅拌下于130℃反应18 h。降温至40℃,加入混合溶液A[A=V(甲醇)∶V(异丙醇)=1 ∶1]480 mL,于12 ℃析晶1 h;过滤,滤饼于4℃用混合溶液A 80 mL洗涤,抽干后于45℃真空干燥4.5 h得白色固体(S)-2 87.70 g,收率 76.7%,+44.9°(c 1,甲醇);1H NMR δ:8.31(s,1H),7.81(s,1H),5.58(s,2H),4.29 ~4.19(m,2H),4.11(dd,J=13.8 Hz,7.2 Hz,1H),2.95(s,1H),1.28(d,J=6.4 Hz,3H);ESI-MS m/z:Calcd for C8H11N5O{[M+H]+}193.1,found 194.2。
(2)(S)-二乙基 【{[1-(6-氨基-9H-嘌呤-9-基)丙基-2-醇]氧}甲基】磷酸酯[(S)-3]的合成
在三口烧瓶中依次加入(S)-2 8.00 g(41 mmol),N-甲基吡咯烷酮32 mL和叔丁醇镁12.40 g(73 mmol),搅拌下滴加对甲苯磺酰氧甲基膦酸二乙酯(DESMP)16 mL(62 mmol),滴毕,于78℃反应5 h。降温至20℃,滴加冰醋酸6.1 mL,滴毕,于0℃加入乙酸乙酯220 mL,搅拌0.5 h,静置0.5 h;倾出上层清液,减压浓缩得(S)-3的N-甲基吡咯烷酮溶液,直接投入下一步反应。
(3)(S)-替诺福韦[(S)-4]的合成
于室温在(S)-3的N-甲基吡咯烷酮溶液中滴加三甲基溴硅烷19.2 mL(145 mmol),滴毕,于78℃反应15.5 h。减压浓缩,依次加水32 mL和乙酸乙酯64 mL,分液,水相用乙酸乙酯(32 mL)洗涤,搅拌下于5℃滴加40%氢氧化钠溶液4.7 mL(pH 2.8 ~3.2),析晶 6 h。过滤,滤饼依次用 5℃冷水(10 mL)和5℃丙酮(10 mL)洗涤,于90℃真空干燥 15.5 h 得白色固体(S)-4 4.67 g,收率39.3%,- 29.8°(c 1,0.1 mol·L-1NaOH);1H NMR δ:8.15(s,2H),7.25(s,2H),5.39(bs,2H),4.28(dd,J=14.4 Hz,4.0 Hz,1H),4.17(dd,J=14.4 Hz,5.6 Hz,1H),3.97 ~ 3.86(m,1H),3.59(qd,J=13.2 Hz,9.6 Hz,2H),1.03(d,J=6.3 Hz,3H);ESI-MS m/z:Calcd for C9H14N5O4P{[M - H]-}287.1,found 286.2。
(4)(S)-替诺福韦二吡呋酯[(S)-5]的合成
在干燥的三口烧瓶中加入(S)-4 4.67 g(16 mmol)和N-甲基吡咯烷酮19 mL,搅拌10 min;于45℃滴加三乙胺9 mL(65 mmol),滴毕,搅拌10 min;加入四正丁基溴化铵5.26 g(16 mmol),搅拌5 min;缓慢滴加氯甲基异丙基碳酸酯11 mL(0.081 mmol),滴毕,于53℃反应4 h。加入正庚烷28 mL,充分摇匀后静置25 min。分液,有机相加入正庚烷28 mL,充分摇匀,静置25 min;分液,依次加入乙酸乙酯47 mL和水24 mL,摇匀,分液;水相用乙酸乙酯28 mL萃取,合并有机相,依次用5℃冷水(3×28 mL)和饱和食盐水(28 mL)洗涤,无水硫酸钠干燥,减压浓缩得浅黄色油状粗品5 4.85 g,收率57.3%。5 不经纯化,直接投入下一步反应。
(5)(S)-6的合成
在单口烧瓶中加入(S)-5 4.85 g(9.30 mmol)和异丙醇16 mL,搅拌至澄清;加入富马酸1.36 g(11.70 mmol),于 58 ℃ 反应 2 h。冷却至25℃,搅拌15 min;搅拌下于0℃析晶2 h。过滤,滤饼用5℃异丙醇洗涤,于45℃真空干燥2 h得白色固体[(S)-6]3.40 g,收率57.6%,[α]20D+9.7°(c 1,甲醇);1H NMR δ:13.12(s,2H),8.13(s,1H),8.03(s,1H),7.19(s,2H),6.63(s,2H),5.62 ~5.46(m,4H),4.91 ~4.74(m,2H),4.26(dd,J=14.4 Hz,4.0 Hz,1H),4.17(dd,J=14.4 Hz,6.1 Hz,1H),4.05 ~3.90(m,3H),1.24(d,J=6.2 Hz,12H),1.06(d,J=6.2 Hz,3H);ESI-MS m/z:Calcd for C19H30N5O10P·C4H4O4{[M+H]+}519.2,found 520.2。
[1]崔岚,安富荣,王晓珉.核苷酸逆转录酶抑制剂替诺福韦 DF[J].中国新药杂志,2004,13(11):1054 -1058.
[2]张久聪,聂青和.治疗慢性乙型肝炎新药——替诺福韦酯[J].世界华人消化杂志,2008,16(24):2679-2688.
[3]周洪林,王永怡,董时军.替诺福韦DF治疗治疗慢性乙型肝炎和HIV感染的研究动态[J].传染病信息,2008,21(4):221 -224.
[4]吴燕,陈国华,胡杨,等.富马酸泰诺福韦酯的合成[J].中国医药工业杂志,2011,42(2):81 -83.
[5]Clercq E D.Highlights in the discovery of antiviral drugs:A personal retrospective[J].Journal of Medicinal Chemistry,2010,53(4):1438 -1450.
[6]Clercq E D.The clinical potential of the acyclic(and cyclic)nucleoside phosphonates:The magic of the phosphonate bond[J].Biochemical Pharmacology,2011,82:99-109.

