配位体修饰氟化锶纳米分层微球的可控合成*
任建学,张晓蓉,欧阳艳,何晓燕
(伊犁师范学院凝聚态相变与微结构重点实验室,新疆伊宁 835000)
无机纳米发光材料具有独特的物理化学性质,在光纤通讯、激光系统、生物成像、医学诊断和太阳能电池等领域中有重要研究及应用价值[1-2]。氟化物具有绝缘性好、禁带宽度大、声子能量较低、电子云扩展效应小和折射率较小等优点,是目前最好的上转换和下转换基质材料之一[3-5]。研究表明,基质材料性质与其尺寸和形貌等有密切关系[6-7]。因此,可通过调控基质材料尺寸和结构,可控合成组分理想、结构特定和尺寸可调的优质基质材料。
目前,氟化物合成已取得显著进展,但是合成方法环保化和合成产物功能化仍面临诸多困难[8-11]。以配位体作为结构修饰剂,合成方法简易、环保、可控,在氟化物合成研究中具有极大潜力,但相关报道较少。
基于此,本文以硝酸锶为锶源,氟化钠为氟源,乙二胺四乙酸二钠(EDTANa2)为配位体,经微波促进合成了配位体修饰氟化锶纳米分层微球(1),其结构和形貌经XRD和SEM表征。物料比r[n(EDTANa2)∶n(Sr2+)]和反应温度(t)对形貌影响较大。在最佳反应条件[n(Sr2+)5 mmol,r=7,于120℃/600 W反应]下合成的分层清晰,分散性好,球体均匀,直径600 nm~800 nm。
1 实验部分
1.1 仪器与试剂
DX-2700型X-射线衍射仪;KYKY-2800B型扫描电镜;XH-300A型微波合成/萃取仪。
所用试剂均为分析纯。
1.2 合成
在反应瓶中加入Sr(NO3)21.06 g(5 mmol),EDTANa29.31 g(25 mmol)和去离子水 150 mL,搅拌使其溶解;置于微波合成/萃取仪(功率600 W,温度 120℃),加热至沸腾,缓慢滴加 NaF 0.52 g(12.5 mmol)的去离子水(50 mL)溶液,滴毕,反应20 min。析出白色沉淀,用去离子水(3×200 mL)洗涤,于室温干燥得1。
仅改变物料比r[n(EDTANa2)∶n(Sr2+)]和反应温度(t),用类似的方法制备1rt。
2 结果与讨论
2.1 表征
(1)XRD
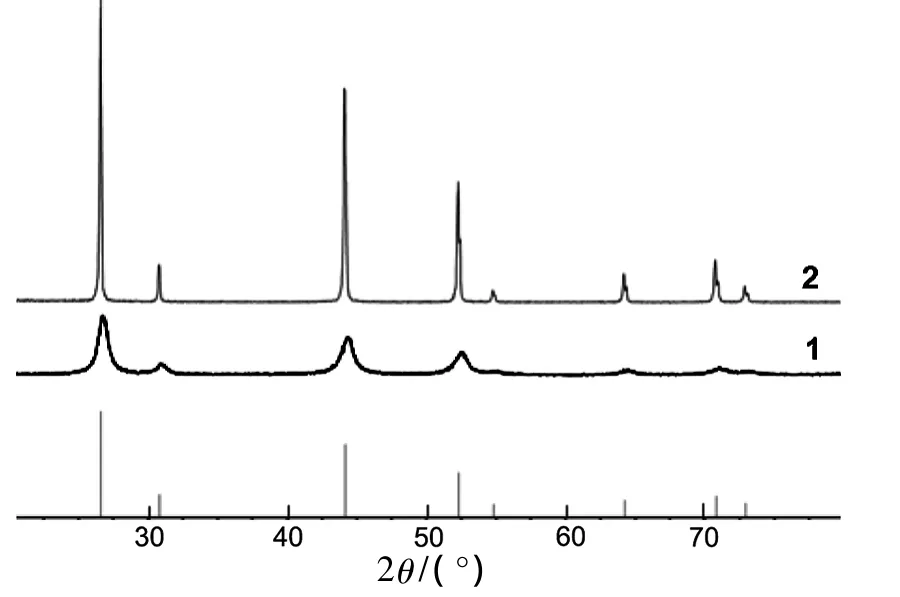
图1 1的XRD谱图*Figure 1 XRD spectra of 1
图1为1和2的XRD谱图。由图1可见,1的衍射峰与标准卡片JCPDS No.86-2 418完全符合,均对应立方相晶体SrF2,但1衍射峰峰强减弱,峰形宽化。
(2)SEM
图2为配位剂种类对1形貌影响的SEM图。由图2可见,酒石酸钠对1结构控制效果不明显,EDTANa2修饰所得1不团聚、分散性好,且具有分层结构。
2.2 合成
为研究1的生长机理和EDTANa2在1生长中所起的作用,考察了物料比r[n(EDTANa2)∶n(Sr2+)]和反应温度(t)对形貌的影响。
(1)r
(2)t
r=7.0,其余反应条件同 1.2,考察 t对 17t微观形貌的影响,结果见图4。由图4可见,t=40℃时,合成的为大量不规则原始粒子;t=60℃时,合成的为粒径1 μm的微米球;t=80℃时,合成的为堆积的微米球,该微米球并不稳定,尺寸逐渐变大;温度升高至120℃,合成的为分层结纳米球,粒径约600 nm~800 nm。由此可见,t对1的最终微观形貌同样有重要的作用[13]。
此外,用类似的方法考察了反应时间对1微观形貌的影响。SEM图分析表明,其影响并不显著。
综上所述,形貌较佳的1的合成条件为n(Sr2+)5 mmol,r=7,于120℃/600 W反应。
2.3 反应机理
根据实验结果和文献报道[14-15],推测1的形成机理为:(1)EDTA2-与 Sr2+形成 Sr-EDTA,水溶液中Sr2+含量降低;(2)氟化钠解离出的F-与Sr-EDTA中缓慢释放出的Sr2+在水溶液中迅速形成1的晶核;(3)晶核在微波促进下形成1的原始粒子,并随着反应时间推移而聚集和生长为1。

图2 1的SEM图*Figure 2 SEM images of 1

图3 的SEM图Figure 3 SEM images of

图4 的SEM 图Figure 4 SEM images of
[1]Jelínek M,Kubeěek V,Su L,et al.Pulsed and continuous-wave laser operation of TGT-grown Nd,Y-codoped:SrF2single crystal[J].Laser Phys Lett,2014,11(5):055001.
[2]Wei L,Tian W,Liu J,et al.Mode-locked Nd3+,Y3+:SrF2laser with 181 fs pulse duration[C].San Jose:Optical Society of America,2014.
[3]Rakov N,Maciel G S,Xiao M.Upconversion fluorescence and its thermometric sensitivity of Er3+:Yb3+co-doped SrF2powders prepared by combustion synthesis[J].Electron,Lett,2014,10(5):985 -989.
[4]Sun Y,Jia P.Hydrothermal synthesis and luminescent properties of SrF2and SrF2:Ln3+(Ln=Eu,Ce,Tb)nano-assembly with controllable morphology[J].JNN,2014,14(5):3957 -3960.
[5]Liu J,Fan M W,Su L B,et al.Laser performance of diode-pumped Nd,Y-codoped CaF2-SrF2mixed crystal[J].Laser Phys,2014,24(3):035802.
[6]Wang X,Yan Y,Xia Y,et al.Size and shape modifications,phase transition and enhanced luminescence of fluoride nanocrystals induced by doping[J].J Mater Chem,2013,18(1):3158 -3166.
[7]Sun J,Xian J,Zhang X,et al.Hydrothermal synthesis of SrF2:Yb3+/Er3+micro-/nanocrystals with multiform morphologies and upconversion properties[J].J Rare Earth,2011,29(1):32 -38.
[8]Schmidt L,Emmerling F,Kirmse H,et al.Sol-gel synthesis and characterisation of nanoscopic strontium fluoride[J].RSC Advances,2014,4(1):32 - 38.
[9]Chen D,Wang Y.Impurity doping:A novel strategy for controllable synthesis of functional lanthanide nanomaterials[J].Nanostruct Mater,2013,5(11):4621 - 4637.
[10]Chen M,Jiang D,Li D,et al.Controllable synthesis of fluorapatite nanocrystals with various morphologies:Effects of pH value and chelating reagent[J].J Am Ceram Soc,2009,485(1):396 -401.
[11]Wang J,Zhu H,Ma C,et al.High-pressure behaviors of SrF2nanocrystals with two morphologies[J].J Phys Chem C,2013,117(1):615 -619.
[12]Burda C,Chen X B,Narayanan R,et al.Chemistry and properties of nanocrystals of different shapes[J].Chem Rev,2005,105(4):1025 -1102.
[13]Zhu L P,Zhang W D,Xiao H M,et al.Facile synthesis of metallic Co hierarchical nanostructured microspheres by a simple solvothermal process[J].J Phys Chem C,2008,112(27):10073 -10078.
[14]Penn R L.Kinetics of oriented aggregation[J].J Phys Chem B,2004,108(34):12707 -12712.
[15]Xu Z H,Kang X J,Li C X,et al.Ln3+(Ln=Eu,Dy,Sm,and Er)ion-doped YVO4nano/microcrystals with multiform morphologies:Hydrothermal synthesis,growing mechanism and luminescent properties[J].Inorg Chem,2010,49(14):6706 -6715.

