富锂固溶体正极材料中锰含量的测定
马小利 白晓艳 卢华权 刘美子 唐海波 张超 卢世刚
(北京有色金属研究总院动力电池研究中心,北京100088)
富锂固溶体正极材料中锰含量的测定
马小利 白晓艳 卢华权 刘美子 唐海波 张超 卢世刚
(北京有色金属研究总院动力电池研究中心,北京100088)
为了制定富锂固溶体正极材料的生产工艺,需要对其前驱体中锰含量进行准确测定,以硝酸铵为氧化剂,采用磷酸固定锰的价态,用硫酸亚铁铵标准溶液滴定锰的容量法来测定锰含量,并对溶样方法及温度控制、磷酸的加入量、加入硝酸铵时的温度控制和硝酸铵的加入量等条件进行了优化实验,实验结果表明:称样量为0.300 0g,溶样消耗盐酸10mL,加入10mL H3PO4,溶液温度240℃时加入1.2 g硝酸铵进行氧化,测定准确度最高,加标回收率为99.70%~100.5%,相对标准偏差小于0.24%,方法耗时短,不需要加入任何掩蔽剂,适合实际分析采用。
富锂固溶体;硝酸铵氧化;硫酸亚铁铵滴定;锰含量
0 前言
锂离子电池具有高电压平台、质量轻、无记忆效应、安全性能好、寿命长等优点,目前已被广泛应用到众多领域[1-5],是人类应对能源危机最重要的手段之一。富锂固溶体正极材料因其具有高比容量、良好的循环稳定性和新的充放电机制等优势受到了广泛关注[6-12],该材料中Mn元素比例的提高降低了Co的含量,使得材料成本随之降低,且对环境友好,被视为下一代锂离子电池正极材料的理想之选[13],因此Mn含量的准确测定也成为评价该材料的关键指标。目前,国内外测定Mn含量大多采用光谱法[1415]、电位滴定法[16]、分光光度法[17]和化学滴定法,但由于设备价格昂贵造成仪器分析成本较高,所以分析工作者多采用传统的化学滴定法进行高Mn含量的测定,这样能够很好地避免样品溶解后多次稀释造成的误差。有一些文献报道采用络合滴定法[18]测定锰含量,但由于分析步骤复杂,试剂种类太多,应用到电池正极材料测试中难以满足实际分析的需要。李青霞[19]等人采用硝酸铵氧化滴定法测定锰矿中的锰含量,而本文采用盐酸快速溶样、硝酸铵氧化法,测定电池正极材料富锂固溶体中高锰的含量,样品溶解迅速、操作简单、试剂用量少,并对测定过程中的溶样方法、溶样温度、硝酸铵加入量、磷酸加入量等条件进行了优化实验,确定了该方法测定锰的最佳实验条件,可以有效地进行产品成分的质量控制。
1 实验部分
1.1 主要试剂
盐酸(1+1);磷酸;硝酸铵;分析中所用试剂为分析纯试剂和三级水,符合GB/T 6682的规定。
N-苯代邻氨基苯甲酸指示液(2g/L):称取0.1g N-苯代邻氨基苯甲酸溶于50mL的Na2CO3(2g/L)溶液中,加热溶解完全。
硫酸亚铁铵标准溶液[c((NH4)2Fe(SO4)2·6H2O)≈0.1mol/L]:按GB/T 601—2002中的方法进行配制及标定。
1.2 实验方法
称取0.3g(精确至0.000 1g)试样,置于300mL的锥形瓶中,用少量水润湿,加入10mL盐酸(1+1)加热至150℃溶解,试样溶解后再加入10mL磷酸,摇匀后加热煮沸,至液面平静并微微冒白烟,移离热源,立即加入一定量的硝酸铵(根据试样中Mn含量的不同,加入硝酸铵的量不同),并充分摇匀,在通风厨风力吹除作用下让黄烟赶尽,稍冷后加入50 mL水,充分摇动使盐类溶解,冷却至室温。用硫酸亚铁铵标准滴定溶液滴定至浅红色,临近终点时加入两滴N-苯代邻氨基苯甲酸指示液,继续滴定至溶液由红色变为亮黄绿色即为终点。
2 结果及讨论
2.1 溶样温度
称取1#试样5份,分别移取10mL的盐酸溶液在电加热板设置的不同温度下溶解试样,测定结果见表1。
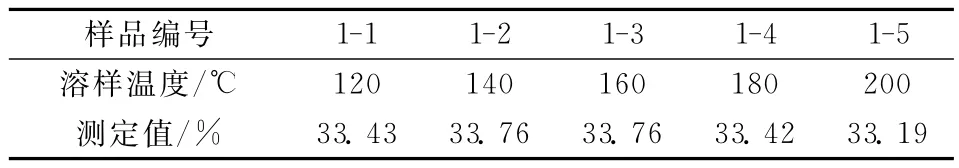
表1 溶样温度对测定结果的影响Table 1 Effect of solution temperature on measurement results
实验结果表明,当电热板显示温度低于140℃或温度高于160℃时,试样中Mn含量偏低。当温度高于160℃时,盐酸挥发严重,试液会随着杯壁上升,高温溶解不合理;当温度低于140℃,部分试样溶解不完全,但肉眼观察不到,这样结果就会比实际偏低。实验采用盐酸溶解试样,电加热板显示温度应在140~160℃,实验通常设置温度为150℃,而由于电加热板显示温度与试液实际温度有差别,此时试液实际温度约为100℃。
2.2 H3PO4加入量的选择
硝酸铵将二价锰氧化为三价锰的反应中,由于二价锰和三价锰的电位差较小,氧化反应速度很慢,加入H3PO4后,H3PO4与三价锰生成[Mn(HPO4)2]-,拉大了电位差,使得加快氧化反应速度。称取0.300 0g试样,改变H3PO4的加入量,测定结果如图1,结果表明,称样量为0.3g时,加入8~14mL H3PO4能将二价锰定量地氧化至三价,因此为保证全部二价锰被氧化,实验时选择加入H3PO4的量为10mL。
2.3 加入NH4NO3时温度的选择
采用硝酸铵作为氧化剂氧化二价锰,硝酸铵应在适宜的温度条件下加入。若温度太低,氧化不完全;温度太高或加热时间太长,则可能有焦磷酸(H4P2O7)析出,刻蚀玻璃器皿,并影响测定结果,一般以在试样分解完全后磷酸液面平静并开始冒白烟时加入硝酸铵为适宜。按规定称取1#试样7份置于7个锥形瓶中,溶液中插入温度计,改变温度条件,共测定7次,结果如表2。
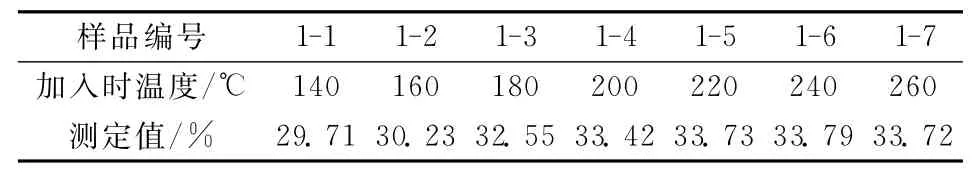
表2 NH4NO3加入时温度控制对测定结果的影响Table 2 Effect of solution temperature of adding NH4NO3on measurement results
实验结果看出:140~200℃温度下,测定结果较低;220~260℃温度下,测定结果在33.75%左右波动,结果趋于稳定;但当温度为260℃时,溶液中的磷酸脱水变为焦磷酸,并附着于杯壁。故实验时选择240℃时加入NH4NO3。
有经验者为方便操作,分析过程中可不使用温度计控制,肉眼观察到冒微烟即可加入NH4NO3进行氧化。
2.4 NH4NO3加入量的选择
硝酸铵作为氧化剂,其用量也应适量,加入太少氧化不完全导致测定结果偏低;加入太多导致试剂浪费;按规定称取1#试样7份,改变NH4NO3加入量,按上述分析步骤测定Mn含量,测定结果如图2。
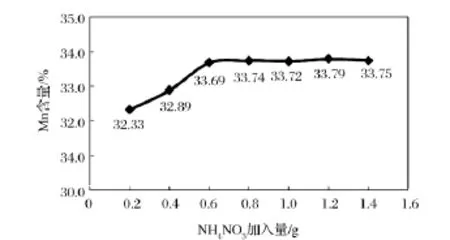
图2 NH4NO3加入量对测定结果的影响Figure 2 Effect of dosage of NH4NO3on measurement results.
结果表明,当硝酸铵加入量大于0.6g时,Mn的测定结果趋于稳定,为保证二价锰氧化完全,实验时选择硝酸铵的加入量为1.2g。
2.5 精密度实验
选择3个富锂固溶体实际样品,按照实验方法重复测定Mn含量8次,结果见表3。由表3可以看出:实验中测定Mn含量的相对标准偏差小于0.24%,可见测量精密度高,适用于规模化生产中产品质量的控制。
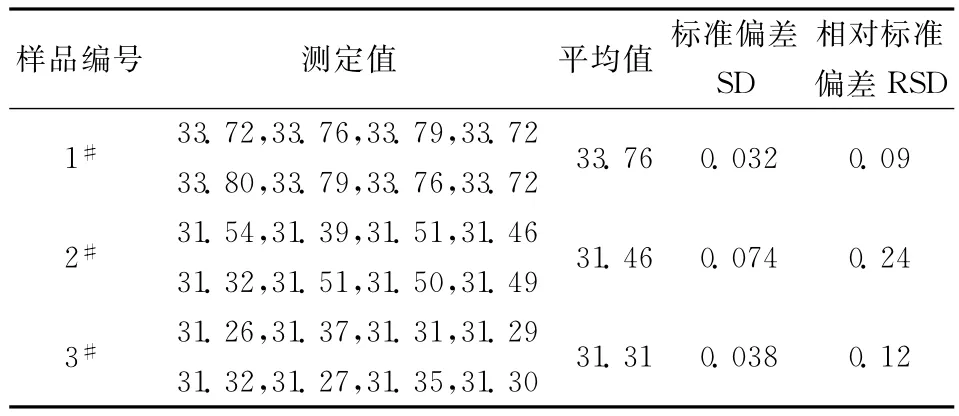
表3 试样中Mn分析结果的精密度Table 3 Precision of the methods /%
2.6 准确度实验
按照本实验方法,分别向样品中加入不同含量的Mn标准溶液进行加标回收率实验,测定结果如表4。实验表明,Mn的加标回收率为99.70%~100.5%,说明该方法的准确度较高。
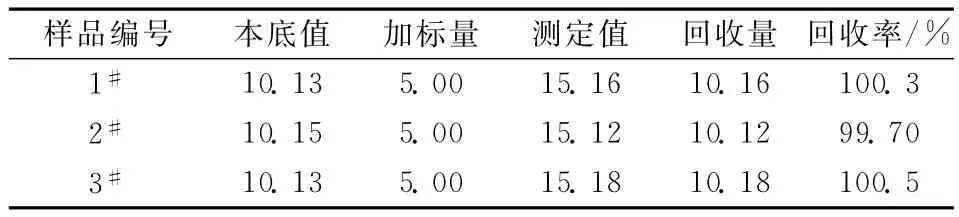
表4 加标回收率实验Table 4 Recovery of the methods /mg
3 结论
用硫酸亚铁铵标准滴定溶液测定富锂固溶体正极材料中锰含量的相对标准偏差小于0.24%,实验加标回收率在99.70%~100.5%。测定结果准确可靠,适合实际分析检测应用。
[1]Li JinHui,Shi PingXin,Wang ZeFeng,et al.A combined recovery process of metals in spent lithium-ion batteries[J].Chemosphere,2009,77:1132-1136.
[2]Wang Rong-Chi,Lin Yu-Chuan,Wu She-Huang.A novel recovery process of metal values from the cathode active materials of the lithium-ion secondary batteries[J].Hydrometallurgy,2009,99:194-201.
[3]Yoshio N.Lithium ion secondary batteries;past 10 years and the future[J].J.Power Sources,2001,100:101-106.
[4]周燕芳,钟辉.锂离子电池正极材料的研究进展[J].材料开发与应用,2003,18(2):34-38.
[5]马小利,白晓艳,刘美子,等 .减压过滤除碳方式对碳包覆磷酸铁锂中铁含量测定结果的影响[J].冶金分析,2014,34(10):21-24.
[6]Lu Zhong-Hua,Mac Neil.D D,Dahn J R..Layered Cathode Materials Li[NixLi(1/3-2x/3)·Mn(2/3-x/3)]O2for Lithium-Ion Batteries[J].Electrochem.Solid St,2001,4(11):A191-A194.
[7]Shin S.S,Sun Y.K,Amine K.Short communication Synthesis and electrochemical properties of Li[Li(1-2x)/3NixMn(2-x)/3]O2as cathode materials for lithium secondary batteries[J].J.Power Sources,2001,112(2):634-638.
[8]Kim J S,Johnson C S,Thackeray M M.Layered xLi-MO2·(1-x)Li2M’O3electrodes for lithium batteries:a study of 0∶95LiMn0.5Ni0.5O2·0∶05Li2TiO3[J].Electrochem.Commun.,2002,4(3):205-209.
[9]Kang S.H,Thackeray M.M.Stabilization of xLi2MnO3·(1-x)LiMO2Electrode Surfaces(M=Mn,Ni,Co)with Mildly Acidic,Fluorinated Solutions[J].J.Electrochem.Soc.,2008,155(4):A269-A275.
[10]Croy J.R,Kang S.H,Balasubramanian M,et al.Li2MnO3-based composite cathodes for lithium batteries:Anovel synthesis approach and new structures[J].Electrochem.Commun.,2011,13(10):1063-1066.
[11]李节宾,徐友龙,董鑫,等.xLi2MnO3·(1-x)LiNi1/3Co1/3Mn1/3O2(x=0.1、0.2、0.3和0.4)固溶体材料性能研究[J].无机化学学报,2012,28(6):1125-1130.
[12]谌谷春,唐新村,王志敏,等 .废旧锂电池中镍钴锰的回收及正极材料LiCo(1/3)Ni(1/3)Mn(1/3)O2的制备[J].无机化学学报,2011(10):1987-1992.
[13]杜柯,杨菲.柠檬酸(铵)处理对Li[Li0.2Mn0.54Ni0.13Co0.13]O2电化学性能影响的研究[J].无机化学学报,2013,29(4):786-792.
[14]何小虎,甘日星,韦莉 .微波消解-电感耦合等离子体原子发射光谱法(ICP-AES)测定高速工具钢中锰、磷、镍、铜、铬、钒[J].中国无机分析化学,2014,4(2):50-53.
[15]王彬果,徐静,赵靖,等.X射线荧光光谱法测定电解锰中锰、硅、磷和铁含量[J].中国无机分析化学,2011,1(3):43-45.
[16]雷忠平,李金岩,田宗平 .湿法冶锰废渣中锰的形态分析与应用[J].矿产与地质,2008,22(1):83-86.
[17]杨雁泽,王荔,何涌.电极材料中锰的分析方法[J].电源技术,2002,26(增刊):255-257.
[18]于永丽,王乃芝,张秀娟,等 .正极材料锰酸锂中锰的价态分析[J].冶金分析,2007,27(6):20-23.
[19]李青霞.硝酸铵氧化滴定法测定锰矿中锰含量[J].化学分析计量,2007,16(3):50-52.
Determination of Manganese Content in Lithium-Enriched Solid Solution
MA Xiaoli,BAI Xiaoyan,LU Huaquan,LIU Meizi,TANG Haibo,ZHANG Chao,LU Shigang
(General Research Institute for Nonferrous Metals Power Cell Research Center,Beijing100088,China)
In order to formulate the production process of lithium-enriched solid anode material,it is necessary to accurately determine the content of manganese.Ammonium nitrate is employed as an oxidant and phosphoric acid is used to fix the valence of manganese.The content of Mn can be determined by titration of ferrous ammonium sulfate titration.In addition,an optimized experiment was conducted regarding the conditions of measurement process such as sample dissolution method,temperature control,phosphoric acid volume,the temperature control when adding NH4NO3and NH4NO3dosage.Experiment conditions were optimized as follows:0.300 0g of the sample,10mL of hydrochloric acid for sample digestion solution,10mL of H3PO4added,oxidation of ammonium nitrate(1.2g)at 240℃The recovery was 99.70%~100.5%,and the relative standard deviation was less than 0.24%.The proposed method is simple,rapid,and it can be applied for practical analysis needing no masking agent.
lithium-enriched solid solution;ammonium nitrate;ferrous ammonium sulfate;manganese content
O655.2
:A
:2095-1035(2015)02-0043-04
2014-12-25
:2015-02-28
国家863计划项目(2012AA110102);国家自然科学基金青年科学基金项目(51302017)资助
马小利,女,工程师,主要从事锂电材料分析研究工作。Email:maxiaoliabc@126.com
10.3969/j.issn.2095-1035.2015.02.009

