伊立替康联合雷替曲塞治疗晚期结直肠癌的临床观察
潘 旋 郭仁宏 孙 宁 李 晟 周国仁
南京医科大学附属江苏省肿瘤医院肿瘤内科,江苏南京 210009
伊立替康联合雷替曲塞治疗晚期结直肠癌的临床观察
潘 旋 郭仁宏 孙 宁 李 晟 周国仁▲
南京医科大学附属江苏省肿瘤医院肿瘤内科,江苏南京 210009
目的观察伊立替康联合雷替曲塞方案治疗晚期结直肠癌的有效性和安全性。方法收集28例一线化疗方案治疗失败或缓解后再进展的晚期结直肠腺癌患者,行伊立替康联合雷替曲塞化疗,方案:伊立替康150~180mg/m2,静脉滴注,第一天;雷替曲塞3mg/m2静脉滴注,第一天;21d为1个周期,21d后再重复给药,每2~3个周期后评价疗效,治疗期间评估不良反应。结果所有患者均可评价疗效,其中PR 2例,SD 19例,PD 7例,无CR者,ORR为7.14%,DCR为75%。中位PFS 6个月,中位OS不小于11.5个月。最常见的毒副反应是中性粒细胞减少和腹泻。结论雷替曲塞联合伊立替康方案有效率高,毒副反应小,可以作为晚期结直肠癌的二线治疗方案。
晚期结直肠癌;雷替曲塞;伊立替康;二线化疗
在全球范围内,结直肠癌发病率居男性恶性肿瘤第三位,女性恶性肿瘤第二位[1]。2012年估计有1 460 600例新发病例,693 900例患者死于结直肠癌。氟尿嘧啶(5-FU)一直是晚期/转移性结直肠癌(mCRC)有效的化疗药物,近年来,新的细胞毒药物以及分子靶向药物的发展显著改善了mCRC患者的生存。我科对收治的28例一线行FOLFOX或XELOX方案化疗,出现复发、转移后的结直肠癌患者应用伊立替康联合雷替曲塞方案治疗,现报道如下。
1 资料与方法
1.1 一般资料
选择2011年1月~2014年12月我院接受过一线化疗方案(FOLFOX、XELOX)治疗失败或缓解后再进展的mCRC患者共28例;组织学证实为结直肠腺癌;至少有一个可测量病灶;其中男10例,女18例;年龄36~71岁,中位年龄52.5岁;ECOG评分0~2分,预期寿命≥3个月;患者入组时距离末次化疗时间>4周,化疗前全面检查,血常规、肝肾功能符合化疗标准;心肺功能基本正常。
1.2 方法
28例患者均采用伊立替康(江苏恒瑞医药股份有限公司,H20020687)+雷替曲塞(南京正大天晴制药有限公司,H20090325)方案静脉化疗,具体给药方案:伊立替康180mg/m2静脉滴注1h,d1;雷替曲塞3mg/m2静脉滴注15min,d1,21d重复,每2~3个周期复查CT评估疗效,至病情进展毒副反应不能耐受为止,最多接受8周期化疗。化疗前给予5-HT3受体拮抗剂预防性止吐,化疗后监测血常规、肝肾功能等,如出现骨髓抑制、肝肾功能损伤,给予升血细胞及保肝治疗。对完成化疗2个周期以上的病例进行疗效评价,对全部病例进行安全性评价。
1.3 疗效及不良反应的评价标准
按RECIST1.1疗效标准评价近期疗效:完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD),客观缓解率(ORR)=CR+PR,疾病控制率(DCR)=CR+PR+SD。无进展生存时间(PFS)定义为:患者从接受治疗开始,到观察到疾病进展或者发生因为任何原因的死亡之间的这段时间。总生存时间(OS)定义为:化疗开始至任何原因引起死亡的时间或末次随诊的时间。随访时间从化疗结束开始至患者死亡、失访或研究确定的随访截止日期。毒性反应按NCI-CTC 3.0标准评定,分为0~5级。
1.4 统计学方法
应用SPSS16.0软件进行统计学分析,采用Kaplan-Meier法绘制生存曲线。
2 结果
2.1 近期疗效
28例患者均按计划完成化疗,其中PR 2例,SD 19例,PD 7例,无CR者。ORR为7.14%,DCR为75%。见表1。
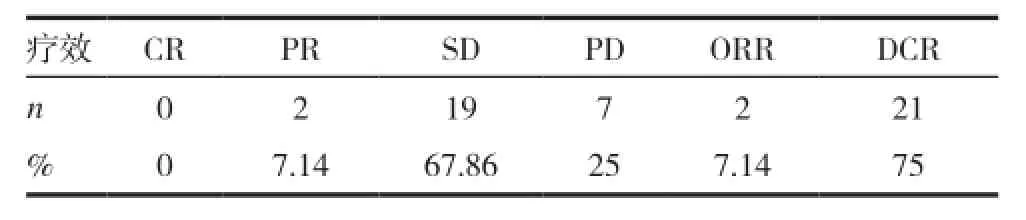
表1 伊立替康联合雷替曲塞治疗mCRC的近期疗效
2.2 远期疗效
随访截止至2015年5月1日,28例患者中8例死亡,20例仍存活,中位PFS为6个月(95%CI:4.963~7.037个月),见图1。中位OS不小于11.5个月,见图2。
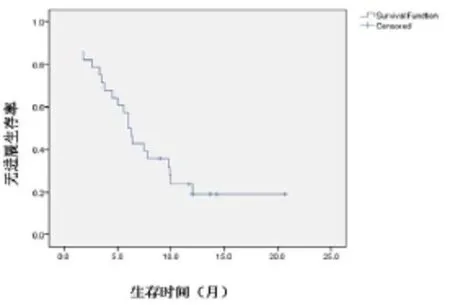
图1 28例mCRC患者无进展生存期(PFS)曲线
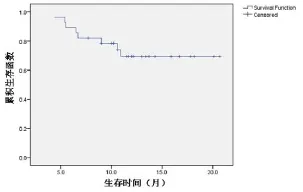
图2 28例mCRC患者总生存期(OS)曲线
2.3 毒副反应
28例患者均可评价毒副反应,常见的毒副反应包括骨髓抑制、恶心呕吐、迟发性腹泻、肝功能异常等。不良反应较轻,多为1~2级,3~4级不良反应常见于中性粒细胞减少,腹泻,肝功能异常,发生率低,并且治疗后有好转。28例患者均未观察到心脏毒性及周围神经毒性。见表2。
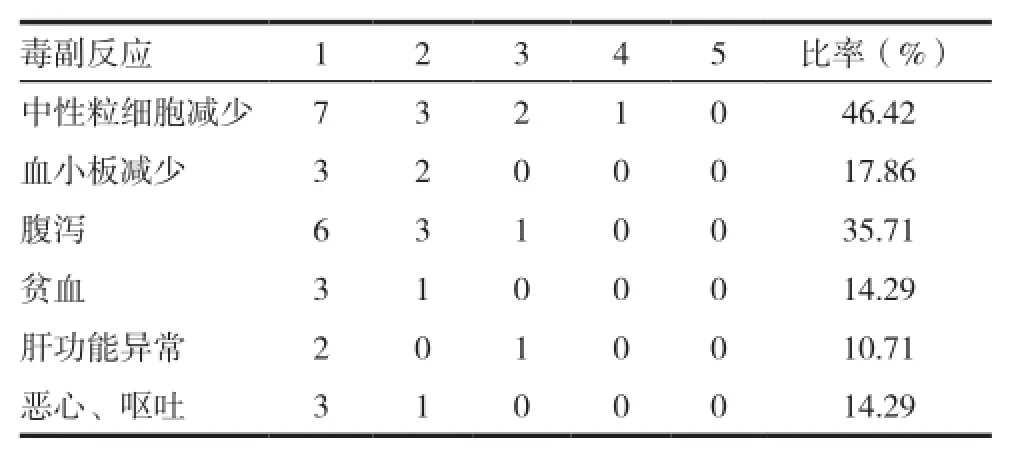
表2 伊立替康联合雷替曲塞方案主要的毒副反应
3 讨论
在过去的十年里,结直肠癌发病率平均每年下降3.4%,超过62岁的人群下降幅度最大[1]。改善就医途径,早期筛查以及标准化的治疗等都使结直肠癌发病率有显著的改善,但近年来,结直肠癌的发病率有年轻化的趋势,可能与高脂饮食、肥胖及吸烟相关[2]。据估计,截至2020年,筛查等措施的介入、化疗的使用将使美国的结直肠癌死亡率下降50%[2]。分子靶向药物,如抗血管生成的药物贝伐珠单抗、阿柏西普,抑制表皮生长因子受体的药物西妥昔单抗、帕尼单抗,以及蛋白激酶抑制剂瑞戈非尼等,大大改善了晚期结直肠癌的生存。一些研究表明,随着联合化疗方案的进步,有远处转移的患者中位生存期已超过20个月。我国目前晚期肠癌一线化疗多选择FOLFOX、XELOX方案,化疗失败或缓解后再进展,常选择以伊立替康为主的二线化疗方案,包括了FOLFIRI或者伊立替康单药方案,有效率4 ~ 10%,PFS 2.6~3.9个月[3-4]。但其有效率低,因此优化晚期肠癌的二线治疗方案显得尤为重要。
伊立替康是喜树碱的半合成衍生物,是拓扑异构酶Ⅰ的特异性抑制剂,伊立替康通过由拓扑异构酶Ⅰ和DNA链的复合体的稳定结合,引起DNA链断裂,最终导致细胞的死亡[5-6]。1998年,美国FDA批准伊立替康作为晚期结直肠癌治疗的药物,对于奥沙利铂一线治疗失败的晚期mCRC,FOLFIRI方案的二线治疗能获得更长的生存期并改善患者的生活质量。雷替曲塞是一种喹啉叶酸盐类似物,为特异性水溶性胸苷酸合成酶(TS)抑制剂,能干扰癌细胞的DNA合成,对晚期结直肠癌、肺癌及乳腺癌有很好的疗效[7]。氟尿嘧啶等是晚期/转移性结直肠癌化疗方案的基石,但其持续泵入的给药方式,耗时长,常常引起严重的消化道反应,以及心脏毒性、心肌缺血。自雷替曲塞应用以来,多个大型的临床试验均证实雷替曲塞对晚期结直肠癌患者的抗癌活性与氟尿嘧啶相似,反应率、生存率与氟尿嘧啶相等[8-11]。并且,因雷替曲塞在体内半衰期长,可以每三周给药一次,15min即可完成给药,给药非常方便。并且大量的临床试验均观察到,雷替曲塞的毒副反应少于5-Fu,尤其是3 ~ 4度的骨髓抑制及心脏毒性[12-15]。Ransom D等研究发现既往接收5-Fu或卡培他滨治疗后出现心脏毒性不能耐受继续治疗的患者在改为雷替曲塞化疗之后,心脏毒性未见加重,安全性好[16]。因此,雷替曲塞是5-Fu耐药或者不适用5-Fu患者的有效替代药物。基于雷替曲塞的优势,在本研究中,我们选择了一线行FOLFOX或XELOX方案化疗,出现复发、转移的晚期结直肠癌患者,采用伊立替康联合雷替曲塞作为二线化疗方案进行研究,观察其近期及远期疗效,以及毒副反应。
本研究显示,伊立替康联合雷替曲塞作为二线化疗方案,近期疗效:ORR虽然只有7.14%,但DCR达到了75%,具有较高的临床获益,与文献报道相似[17-18]。至随访结束时,有20例患者仍存活,中位PFS为6.0(1.7~20.7个月),中位OS不小于11.5个月(4.4~20.7个月)。该方案主要的毒副反应为骨髓抑制、恶心、呕吐、迟发性腹泻,但多数患者都能耐受,顺利完成化疗。
综上所述,在晚期结直肠癌二线治疗中,伊立替康联合雷替曲塞方案毒副反应少,疗效确切,可作为晚期结直肠癌有效的二线治疗方案。但因本研究样本量小,需扩大样本量进一步研究该方案的疗效。此外,随着分子靶向药物的研究进展,化疗和分子靶向药物的联合应用,可能取得更好的疗效,为晚期结直肠癌患者带来更多的生存获益,对于二线方案,仍需探索优化。
[1] Lindsey A,Torre,Freddie Bray,et al.Global Cancer Statistics,2012[J].CA Cancer J Clin,2015,5-6.
[2] Center MM,Jemal A,Smith RA,et al.Worldwide variations in colorectal cancer[J].CA Cancer J Clin,2009,59:366-378.
[3] Peeters M,Price TJ,Cervantes A,et al.Randomized phase III study of panitumumab with fluorouracil,leucovorin,and irinotecan (FOLFIRI) compared with FOLFIRI alone as second-line treatment in patients with metastatic colorectal cancer[J].J Clin Oncol,2010,28(31):4706-4713.
[4] Sobrero AF,Maurel J,Fehrenbacher L,et al.EPIC:phase III trial of cetuximab plus irinotecan after fluoropyrimidine and oxaliplatin failure in patients with metastatic colorectal cancer[J].J Clin Oncol,2008,26(14):2311-2319.
[5] 陈银芸,廖江涛,吴娟.雷替曲塞与奥沙利铂在老年晚期结直肠癌患者中的联合应用研究[J].中国当代医药,2014,21(2):78-79.
[6] 朱大高,王辉.雷替曲塞联合奥沙利铂治疗晚期结直肠癌的临床疗效观察[J].中国医学创新,2015,12(7):51-53.
[7] Schwartz GK,Harstrick A,Gonzalez Baron M.Raltitrexed(Tomudex) in combination with 5-fluorouracil for the treat-ment of patients with advanced colorectal cancer:preliminaryresults from phase I clinical trials[J]. Eur J Cancer,1999,35(1):S9-13.
[8] Cunningham D,Zalcberg JR,Rath U,et al.‘Tomudex'(ZD1694):results of a randomised trial in advanced colorectal cancer demonstrate efficacy and reduced mucositis and leucopenia.The‘Tomudex' Colorectal Cancer Study Group[J].Eur J Cancer,1995,31(A):1945-1954.
[9] Cocconi G,Cunningham D,Van Cutsem E,et al.Open,randomized,multicenter trial of raltitrexed versus fluorouracil plus high-dose leucovorin in patients with advanced colorectal cancer.Tomudex Colorectal Cancer Study Group[J].J Clin Oncol,1998,16(9):2943-2952.
[10] Hind D,Tappenden P,Tumur I,et al.The use of irinotecan,oxaliplatin and raltitrexed for the treatment of advanced colorectal cancer:systematic review and economic evaluation[J].Health Technol Assess,2008,12:15.
[11] Popov I,Carrato A,Sobrero A,et al.Raltitrexed(Tomudex) versus standard leucovorin-modulated bolus 5-fluorouracil:Results from the randomised phase III Pan-European Trial in Adjuvant Colon Cancer 01(PETACC-1) [J].Eur J Cancer,2008,44(15):2204-2211.
[12] Jackman AL,Farrugia DC,Gibson W,Kimbell R,Harrap KR,Stephens TC,et al.ZD1694 (Tomudex):a new thymidylate syn-thase inhibitor with activity in colorectal cancer[J].Eur J Cancer,1995,31A(7-8):1277-1282.
[13] Gravalos C,Salut A,García-Girón C,et al. A randomized phase II study to compare oxaliplatin plus 5-fluorouracil and leucovorin (FOLFOX4)versusoxaliplatin plus raltitrexed (TOMOX) as firstline chemotherapy for advanced colorectal cancer[J].Clin Transl Oncol,2012,14(8):606-612.
[14] Barni S,Ghidini A,Coinu A,et al.A systematic review of raltitrexed-based first-line chemotherapy in advanced colorectal cancer[J].Anticancer Drugs,2014,25(10):1122-1128.
[15] Liu Y,Wu W,Hong W,et al.Raltitrexed-based chemotherapy for advanced colorectal cancer[J].Clin Res Hepatol Gastroenterol,2014,38(2):219-225.
[16] Ransom D,Wilson K,Fournier M,et al.Final results of Australasian Gastrointestinal Trials Group ARCTIC study:an audit of raltitrexed for patients with cardiac toxicity induced by fluoropyrimidines[J].Ann Oncol,2014,25(1):117-121.
[17] 王勇.雷替曲塞联合伊立替康治疗晚期直肠癌的临床观察[J].中国医药,2012,7(4):421-422.
[18] 谢晓素,顾康生.伊立替康联合雷替曲塞方案二线治疗晚期胃癌的临床研究[J].安徽医药,2014,18(8):1557-1599.
Clinical observation of irinotecan plus raltitrexed as second-line chemotherapy for advanced colorectal cancer
PAN Xuan GUO Renhong SUN Ning LI Sheng ZHOU Guoren
Department of Medical Oncology,Nanjing Medical University Affiliated Cancer Hospital of Jiangsu Province, Nanjing 210009,China
ObjectiveTo observe the efficacy and toxicity of irinotecan plus raltitrexed as second-line chemotherapy for advanced colorectal cancer.MethodsTwenty-eight patients with advanced colorectal cancer who failed to first-line chemotherapy.The doses of drugs were as follows,CPT-11 150-180mg/m2ivgtt on day 1 and raltitrexed 3mg/m2on day 1.One cycle lasted 21 days.After every two or three cycles,therapeutic efficacy was evaluated.The efficacy,side effects,and safety of the treatment were observed.ResultsAll patients successfully completed the the treatment plan. There was 0 case of complete recovery, 2 partial recovery, 19 stable disease,and 7 progressive disease.The overall response rate was 7.14%,the disease control rate was 75%.The mean progression free survival was 6 months,and the mean overall survival was no less than 11.5 months.The most common side effects were neutropenia and diarrhea.ConclusionIrinotecan plus raltitrexed as second-line chemotherapy for advanced colorectal cancer has a high efficacy with acceptable tolerability,and is a therapy worth considering for advanced colorectal cancer.
Advanced colorectal cancer;Irinotecan;Raltitrexed;Second-line chemotherapy
R735.3
A
2095-0616(2015)18-12-04
2015-07-03)
吴阶平基金(320.6750.13115);江苏省“六大人才高峰”高层次人才培养计划(2013-WSW-035)。
▲通讯作者

