天晴甘平联合苦参碱对急性白血病化疗后肝功能损害的保护作用
刘东芳,张宝琴,赵小亮,甘 静,郑雅珍,张成侠,冯志刚,刘艳芬,訾建杰,刘 欣,李素欣
(唐山市人民医院血液科1、检验科2,河北 唐山063000)
天晴甘平联合苦参碱对急性白血病化疗后肝功能损害的保护作用
刘东芳1,张宝琴2,赵小亮1,甘 静2,郑雅珍1,张成侠1,冯志刚1,刘艳芬1,訾建杰1,刘 欣1,李素欣1
(唐山市人民医院血液科1、检验科2,河北 唐山063000)
目的探讨天晴甘平(甘草酸二铵肠溶胶囊)联合苦参碱对急性白血病化疗后肝功能损害的保护效果。方法将51例急性白血病化疗后出现轻度肝损伤患者,随机分为观察组26例和对照组25例,观察组采取天晴甘平与苦参碱氯化钠注射液联合治疗,对照组仅采取苦参碱氯化钠注射液治疗,两组均持续治疗两周。比较两组患者治疗前后的肝功能指标和疗效。结果观察组肝功能损害治疗总有效率为80.8%,对照组为48.0%,两组比较差异具有统计学意义(P<0.05);观察组治疗1周、2周时谷丙转氨酶(ALT)、谷草转氨酶(AST)指标值均明显低于同期对照组,差异均具有统计学意义(P<0.05),治疗后在总胆红素(T-Bil)指标值方面比较,两组差异无统计学意义(P>0.05)。结论天晴甘平联合苦参碱对急性白血病化疗后肝功能损害治疗效果优于单纯苦参碱氯化钠注射液治疗,且安全、可靠,值得临床推广运用。
天晴甘平;苦参碱;急性白血病;肝功能损害
急性白血病属于较为难治的血液系统恶性肿瘤之一,起病急骤,进展迅速,致死率较高。其常用的治疗方法目前仍以多种化疗药物联合为主,虽然可以取得一定的疗效,但多种化疗药物对患者肝脏的损害却无法回避,且由于肝脏功能损害又可以限制联合化疗的足量应用,从而影响急性白血病的治疗效果。Takai等[1]的研究指出,在进行联合化疗的600例急性白血病患者中,有7.3%的患者出现化疗相关性肝脏功能损害,而国内研究也显示,联合化疗的急性白血病患者中,有11%~40%的患者会出现化疗相关性肝脏功能损害[2]。因此,如何保护化疗患者的肝脏功能显得尤为重要。本科对26例急性白血病化疗后出现轻度肝功能损伤患者应用甘草酸二铵肠溶胶囊(天晴甘平)联合苦参碱氯化钠注射液进行肝保护治疗,效果显著,现报道如下:
1 资料与方法
1.1 一般资料 选择我科在2012年5月至2014年4月收治的急性白血病化疗后出现肝损伤患者51例,随机分为观察组26例和对照组25例。观察组中,男性18例,女性8例;年龄18~61岁,平均(49.3±10.5)岁;急性髓细胞白血病(Acute myeloid leukemia,AML)21例,急性淋巴细胞白血病(Acute lymphobiastic leukemia,ALL)5例。对照组中,男性18例,女性7例;年龄18~60岁,平均(48.8±9.6)岁;AML20例,ALL5例。两组患者化疗前的门冬氨酸氨基转移酶(AST)、谷丙转氨酶(ALT)、总胆红素(T-Bil)、血清总蛋白(TP)、胆汁酸(TBA)等血液生化指标比较,差异均无统计学意义(P>0.05),具有可比性,见表1。
表1 两组患者化疗前的各项血液生化指标比较(±s)
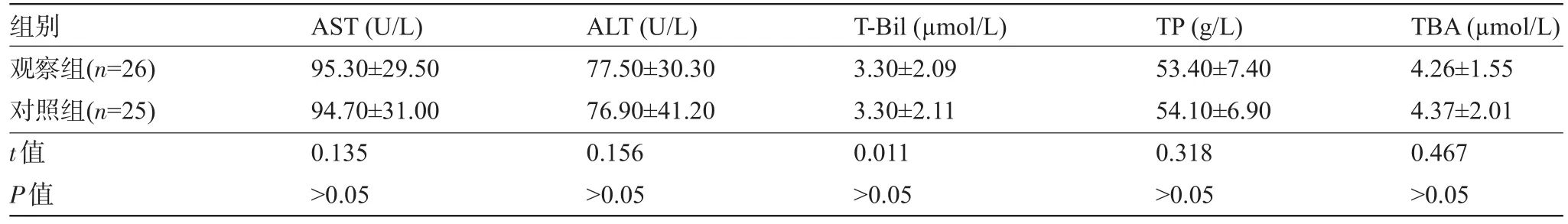
表1 两组患者化疗前的各项血液生化指标比较(±s)
组别观察组(n=26)对照组(n=25)t值P值AST(U/L)95.30±29.5094.70±31.000.135>0.05 ALT(U/L)77.50±30.3076.90±41.200.156>0.05 T-Bil(µmol/L)3.30±2.093.30±2.110.011>0.05 TP(g/L)53.40±7.4054.10±6.900.318>0.05 TBA(µmol/L)4.26±1.554.37±2.010.467>0.05
1.2 病例筛选 (1)入组标准:所有患者均符合急性白血病MICM分型的诊断标准[3];进行联合化疗前均检查各项常规理化指标,均无特殊,尤其是肝脏功能无特殊,乙肝病毒标志物(-),肝脏彩超均无特殊等;联合化疗结束后患者出现ALT、AST或ALP检测值超过正常上限值2倍,且低于10倍或/和T-Bil升高,且小于85.5µmol/L,即表明符合轻度肝损伤诊断标准[4];采取常规联合化疗方案,所运用的联合化疗药物包括甲氨蝶呤(MTX)、柔红霉素(DNR)、阿霉素(ADM)、环磷酰胺(CTX)等;同型的急性白血病患者化疗用药方案为相同或近似;对本组研究知情并自愿参加,并经医院伦理委员会讨论通过。(2)排除标准:非联合化疗导致的的肝功能损害,如乙肝、酒精性肝炎、肝硬化等;各种严重的感染以及胆道系统疾病者;心肺功能严重障碍者;非血液系统的其他恶性肿瘤等;化疗药物过敏者;严重精神疾病患者。
1.3 治疗方法 (1)观察组:自血液检查提示肝脏功能损害日起算,采用甘草酸二铵肠溶胶囊(商品名:天晴甘平,江苏正大天晴药业股份有限公司生产,国药准字H20040628)口服,150mg/次,3次/d;苦参碱氯化钠注射液(湖南汉森制药股份有限公司,国药准字H20046177)静脉缓慢滴注,100ml/次,1次/d。两种药物持续治疗两周。(2)对照组:自血液检查肝脏功能损害日起算,采用苦参碱氯化钠注射液治疗,药物类型、用法、用量等均与观察组相同。另外,所有患者常规口服肌苷、维生素C等药物,持续治疗两周。两周后对两组进行各项理化指标检查。
1.4 疗效判定 采用世界卫生组织(WHO)所制定的化疗药物肝脏损害分级标准进行评估损害程度,肝功能疗效标准:(1)显效,肝损临床症状基本消失,或者有显著的改善,ALT、T-Bil值达到正常,肝功能总体恢复至正常水平,机体状态良好;(2)有效,肝损临床症状有所缓解,ALT、T-Bil指标值比治疗之前降低了≥50%;(3)无效,肝损临床症状未得到缓解或者症状越发严重,ALT、T-Bil指标值与治疗前比较,降低幅度<50%。治疗总有效率=显效率+有效率。
1.5 统计学方法 应用SPSS17.0统计学软件包进行数据分析,计量资料以均数±标准差(±s)表示,两组间比较采用t检验,计数资料以百分比(%)表示,采用χ2检验,以P<0.05为差异具有统计学意义。
2 结 果
2.1 两组患者的肝功能损害治疗效果比较 观察组患者的肝功能损害治疗总有效率明显高于对照组,差异具有统计学意义(χ2=4.366,P<0.05),见表2。

表2 两组肝功能损害治疗效果比较 [例(%)]
2.2 两组患者治疗前后的肝功能ALT、T-Bil指标比较 两组患者入组时的ALT、T-Bil、AST指标值比较差异均无统计学意义(P>0.05);观察组治疗1周、2周时ALT、AST指标值均明显低于同期对照组,差异均有统计学意义(P<0.05),治疗后两组T-Bil指标值比较,差异无统计学意义(P>0.05)。观察组和对照组患者治疗1周、2周时的ALT、T-Bil、AST指标值均比入组时明显降低,差异均有统计学意义(P<0.05),见表3。
2.3 药物不良反应 观察组仅2例患者出现轻微畏寒和发热症状,先停药后,给予一般性对症处理后好转,其余患者均未出现明显不良反应。对照组1例患者出现畏寒,其余也均未出现明显的不良反应。
表3 两组患者治疗前后的肝功能ALT、T-Bil、AST指标比较(±s)
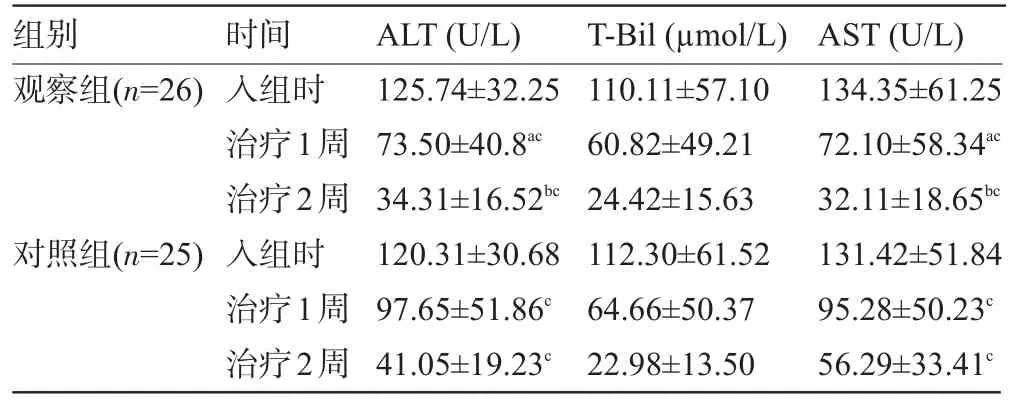
表3 两组患者治疗前后的肝功能ALT、T-Bil、AST指标比较(±s)
注:与同期对照组比较,aP<0.05,bP<0.05;与同组入组时比较,cP<0.05。
组别观察组(n=26)对照组(n=25)时间入组时治疗1周治疗2周入组时治疗1周治疗2周ALT(U/L)125.74±32.2573.50±40.8ac34.31±16.52bc120.31±30.6897.65±51.86c41.05±19.23cT-Bil(µmol/L)110.11±57.1060.82±49.2124.42±15.63112.30±61.5264.66±50.3722.98±13.50 AST(U/L)134.35±61.2572.10±58.34ac32.11±18.65bc131.42±51.8495.28±50.23c56.29±33.41c
3 讨 论
众所周知,几乎所有的恶性肿瘤化疗药物都会对人体肝脏产生毒性,因而导致药物性肝损害。其药物毒理作用主要包括中毒性肝损害以及变态反应性肝损害,前者以微粒体酶机制、胆红素代谢机制、活性氧的毒性机制等多见;后者则以肝脏特异性免疫抗体机制、细胞过度免疫机制、胆汁淤积因子作用等为主[5-6]。一般而言,联合化疗后对肝脏的损害存在两种类型:一是体制性肝细胞损害,其机理在于人体自身对某些化疗药物或这些药物的中间代谢产物过度敏感;二是药物源性损害,机制在于化疗药物及其各种中间代谢产物在人体肝脏代谢过程中对肝脏细胞产生的直接性破坏。这两种损害都会最终导致人体出现肝脏细胞坏死,肝细胞脂肪变性,肝脏胆汁淤积以及肝脏内血管破坏[7]。这些负面情况一旦出现,就会极大影响联合化疗的进程,甚至中断联合化疗[8]。因此,如何有效的在联合化疗过程中保护肝脏细胞,减少化疗药物对肝脏的不良刺激,保障化疗进程顺利进行就显得尤为重要。
苦参碱是常规使用的保肝药物,现代药理学研究指出[9],苦参碱具有清热解毒、利湿消肿的作用,可以明显改善各种病理性肝损害症状与体征、起到退黄以及降酶的作用。另外,苦参碱还有镇痛、抗炎、抗病毒、抗肿瘤、杀虫等作用。一些研究也表明,苦参碱氯化钠注射液能改善人体免疫机能,提高自然杀伤细胞的活性[10]。而甘草酸二铵近年来逐渐在临床广泛使用,多项临床研究指出[11-12]:甘草酸二铵可以显著提高机体的抗炎能力、调节人体免疫、尤其可以保护肝脏细胞膜,使细胞膜稳定存在,并且可以改善人体胆红素代谢过程、防止肝脏出现纤维化进程。急性白血病在联合化疗过程中,为保护肝功能,应当及早使用甘草酸二铵注射液,但因为传统药物制剂工艺的限制,剂型较为单一,药物使用过程中容易出现疗程限制、输液反应、停药后肝脏损害容易反复等不利情况[13]。甘草酸二铵胶囊自问世以来,丰富了产品剂型,弥补了单一静脉给药的缺陷。分子药理学显示,甘草酸具有高亲水性、高极性的大分子物质特性,传统的口服剂型人体肠道吸收率低,导致血药浓度无法达到应有的治疗水平。而甘草酸二铵肠溶胶囊(天晴甘平)采取了特殊的制剂工艺,是甘草酸与磷脂结合形成的脂质复合体,这样极大的增加了药物的水溶性,有效利用甘草酸主要是人体肠道吸收的特质,制成特有的肠溶剂型,使得药物定点在肠道内有效释放,进而利于药物有效成分的吸收,加强了药物的临床疗效[14]。甘草酸二铵肠溶胶囊与苦参碱氯化钠注射液联合使用,具有相互协同作用。从本组联合使用结果来看,天睛甘平联合苦参碱治疗的观察组,其治疗总有效率明显高于单纯使用天晴甘平治疗的对照组(P<0.05),并且观察组治疗后患者肝功能ALT、AST指标均优于对照组(P<0.05)。在两组药物不良反应方面,两组均未出现明显的药物副作用。
综上所述,天睛甘平联合苦参碱对急性白血病化疗后肝功能损害治疗效果优于单纯苦参碱治疗,且安全、可靠,值得临床推广应用。
[1]Takai S,Tsururni H,Ando K,et al.Prevalence of hepatitis B and C virus infection in haematological malignancies and liver injury following chemotherapy[J].Eur J Haematol,2005,74(2):158-165.
[2]蒋波涛,李福兵,廖建生,等.药物性肝损害146例临床分析[J].中西医结合肝病杂志,2014,24(2):91-93.
[3]Miyazaki M,Rosenblum JS,Kasahara Y,et al.Determination of enzymatic source of alanine aminotransferase activity in serum from dogs with liver injury[J].J Pharmacol ToxiclMethods,2009,60(3):307-315.
[3]Maria VA,Victorino RM.Development and validation of a clinical scale for the diagnosis of drug-induced hepatitis[J].Hepatology,1997,26(3):664-665.
[4]Shi Q,Hong H,Senior J,et al.Biomarkers for drug-in-dueced liver injury[J].Expert Rev Gastroenterol Hepatol,2010,4(2):225-234.
[5]Floyd J,Mirza I,Sachs B,et al.Hepatotoxicity of chemotherapy[J]. Semin Oncol,2006,33(1):50-67.
[6]Daly AK.Drug-induced liver injury:past,present and future[J]. Pharmacogenornics,2010,11(5):607-608.
[7]Tsuruoka N,Abe K,Wake K,et al.Hepatic protection by glycyrrhizin and inhibition of iNOS expression in concanavalin A-induced liver injury in mice[J].Inflamm Res,2009,58(9):593-594.
[8]宋通微.不同化疗方案治疗弥漫大B细胞淋巴瘤的疗效观察[J].海南医学,2012,23(23):30-32.
[9]吴 涛,王乐民.人参皂苷Rg1与氧化苦参碱协同保肝作用及其机制研究[J].国际中医中药杂志,2014,36(10):894-898.
[10]Kim R,Em Mi,Tanabe K,et al.Therapeutic potential of antisense Bcl-2 as achemosensitizer for cancer therapy[J].Cancer,2004,101 (11):2491-2502.
[11]贾贻红,张玉泉.凯西莱与甘利欣治疗抗结核药物性肝病的疗效比较[J].中国老年学杂志,2012,32(24):5432-5433.
[12]杨 威.右旋雷贝拉唑钠肠溶片处方及工艺的研究[J].海峡药学,2013,25(7):38-39.
[13]唐明珍,张 松.甘利欣在治疗肿瘤化疗所致肝损害中的临床应用探讨[J].齐齐哈尔学院学报,2012,33(9):1169-1170.
[14]凌青霞,金宏慧,郑建铭,等.甘草酸二铵脂质复合物肠溶胶囊与甘草酸二铵胶囊对照治疗慢性病毒性肝炎687例荟萃分析[J].中华肝脏病杂志,2014,22(6):411-415.
Protective effect of glycyrrhizic acid diamine capsules and matrine sodium chloride injection on liver function damage for acute leukemia after chemotherapy.
LIU Dong-fang1,ZHANG Bao-qin2,ZHAO Xiao-liang1,GAN Jing2,ZHENG Ya-zhen1,ZHANG Cheng-xia1,FENG Zhi-gang1,LIU Yan-fen1,ZI Jian-jie1,LIU Xin1,LI Su-xin1. Department of Hematology1,Department of Clinical Laboratory2,Tangshan People's Hospital,Tangshan063000,Hebei, CHINA
ObjectiveTo study the protective effect of Tian-Qing-Gan-Ping(glycyrrhizic acid diamine capsules)and matrine sodium chloride injection on liver function damage after chemotherapy in patients with acute leukemia.MethodsFifty-one patients of acute leukemia with mild liver damage after chemotherapy were randomly divided into observation group(26 cases)and control group(25 cases).The observation group was treated by glycyrrhizic acid diamine capsules combined with matrine sodium chloride injection,while the control group was only treated with matrine sodium chloride injection,for a treatment course of2 weeks.The liver function index and curative effect before and after treatment were compared between the two groups.ResultsThe total effective rate for liver function damage reached80.8%in the observation group and48.0%in the control group,with statistically significant difference between the two groups(P<0.05).One week,2 weeks after treatment,the levels of alanine aminotransferase (ALT)and aspartate aminotransferase(AST)in the observation group were significantly lower than those in the control group(P<0.05).The levels of T-Bil indexes showed no statistically significant difference between the two groups after treatment(P>0.05).ConclusionGlycyrrhizic acid diamine capsules combined with matrine sodium chloride injection has better clinical efficacy for liver function damage after chemotherapy in patients acute leukemia,compared with only matrine sodium chloride injection,which is safe,reliable,and worthy of clinical promotion.
Glycyrrhizic acid diamine capsules;Matrine;Acute leukemia;Liver function damage
R733.71
A
1003—6350(2015)22—3292—03
2015-06-24)
10.3969/j.issn.1003-6350.2015.22.1195
河北省卫生厅项目(编号:20150979)
刘东芳。E-mail:tsliudongfang15@163.com