胆甾-3β,5α,6β-三醇衍生物的合成
刘跃金, 包立娇, 王钰楠
(沈阳化工大学 制药与生物工程学院, 辽宁 沈阳 110142)
胆甾-3β,5α,6β-三醇衍生物的合成
刘跃金, 包立娇, 王钰楠
(沈阳化工大学 制药与生物工程学院, 辽宁 沈阳 110142)
研究了胆甾-3β,5α,6β-三醇的水溶性衍生物的合成.以胆固醇为原料在质量分数为88 %的甲酸中以质量分数为30 %的过氧化氢(H2O2)溶液氧化、甲醇中碱水解得胆甾-3β,5α,6β-三醇,收率83.5 %,m.p.228~230 ℃,再以胆甾-3β,5α,6β-三醇与草酰氯于丙酮中0 ℃反应15 min,吡啶为催化剂,然后加入少量水继续反应约30 min,得胆甾-3β,5α,6β-三醇-3,6-二草酸单酯,收率61.5 %,m.p.207~209 ℃.经IR和1H-NMR确证结构正确.
胆甾-3β,5α,6β-三醇-3,6-二草酸单酯; 胆甾-3β,5α,6β-三醇; 合成
20世纪70年代中期,Cheng KP(郑国平)等在法国斯特拉斯堡路易巴斯德大学天然物质有机化学研究室,从有抗癌活性的中药僵蚕(BombyxcumBotryte)中提取出7β-羟基胆固醇(7β-Hydroxycholesterol).体外实验发现此化合物在33 mg·L-1的质量浓度下,对肝癌细胞株HTC和ZHC有细胞毒作用,但在≤80 mg·L-1的质量浓度下,对正常小鼠纤维细胞(3T3 cells)无细胞毒作用,表明此化合物有较好的选择性.7β-羟基胆固醇的另一个重要作用是作用于细胞膜,这种细胞膜作用不同于传统的抗肿瘤药物(基本上作用于细胞的遗传物质).然而,7β-羟基胆固醇的低水溶性使它的生物学研究遇到困难.此后关于甾体化合物抗癌活性的报道逐渐增多,如2001年,Ana Rueda 等[1]从柳珊瑚(plexaurellagrisea)中分离得到豆甾-24(28)-烯-3β,5α,6β-三醇,药理实验证实它对HT29肿瘤细胞株有很强的选择性细胞毒性,ED50为0.1 mg·L-1.基于此,2007年,刘跃金等[2]合成了3β,5α,6β-三羟基胆-24-酸甲酯,并对其进行了小鼠L1210白血病细胞体外增值抑制实验,IC50为14.36 mg·L-1,表明其对L1210白血病细胞有较好的抗癌活性;2008年,又合成了胆甾-3β,5α,6β-三醇,并对它和3β,5α,6β-三羟基胆-24-酸甲酯进行了体内小鼠肉瘤S180抗癌活性实验,灌服1 320 μg·g-1的抑瘤率分别为47.6 %和 19.2 %,皆有明显的抑制作用[3].2009年,刘跃金等[4]合成了胆甾-3β,5α,6β-三醇-3-O-β-D-吡喃葡萄糖苷,为胆甾-3β,5α,6β-三醇的强水溶性衍生物,推测会改善抗癌活性.因此,本文进一步合成胆甾-3β,5α,6β-三醇的水溶性衍生物,以提高抗癌活性,改善水溶性.
1 合成路线
以胆固醇为原料,在质量分数为88 %的甲酸中以质量分数为30 %的H2O2溶液氧化、甲醇中碱水解得胆甾-3β,5α,6β-三醇.再以胆甾-3β,5α,6β-三醇与草酰氯反应,吡啶为催化剂,丙酮作溶剂,0 ℃反应15 min,然后加入少量水继续反应约30 min,生成胆甾-3β,5α,6β-三醇-3,6-二草酸单酯.合成路线如下所示.

2 实验与结果
2.1 仪器与原料
熔点用毛细管测定,温度计未经校正;红外光谱用Bruker IFS-55红外分光光度计测定,KBr压片;核磁共振氢谱用Bruker ARX-300B核磁共振仪测定.
胆固醇,分析纯,国药集团化学试剂有限公司;草酰氯,化学纯,国药集团化学试剂有限公司;其他试剂,分析纯,沈阳市化学试剂厂.
2.2 胆甾-3β,5α,6β-三醇的合成
将胆固醇20 g(0.052 mol)加入200 mL质量分数为88 %的甲酸中,搅拌,加热升温到75 ℃保持5 min,冷却至室温,加入质量分数30 %的H2O2溶液35 mL(4.5 mol),恒温28 ℃搅拌5 h,升温至40 ℃保持10 min后倾入沸水300 mL中,冷却后,抽滤,用饱和碳酸氢钠水溶液洗涤,烘干,得产物28.4 g.将其溶于600 mL甲醇中,加入质量分数25 %的氢氧化钠溶液20 mL,搅拌回流1 h,冷却后,用稀盐酸调pH至6~7,加水200 mL稀释,放置,抽滤,干燥,得白色固体18.4 g,收率83.5 %,m.p.228~230℃(文献值[5]226~228 ℃).1H-NMR(DMSO-d6)δ:3.80(1H,m,3α-H),3.64(1H,t,6α-H),1.02(3H,s,19-CH3),0.88(3H,d,21-CH3),0.84(6H,d,26-CH3& 27-CH3),0.62(3H,s,18-CH3).
2.3 胆甾-3β,5α,6β-三醇-3,6-二草酸单酯的合成
将0.5 g胆甾-3β,5α,6β-三醇加入到30 mL丙酮中,室温至完全溶解后加入草酰氯0.8 g、吡啶0.2 mL,10 ℃反应0.5 h.加入水10 mL水解10 min.加入饱和碳酸氢钠调pH值到5.0,减压蒸馏,以V(乙酸乙酯)∶V(乙醇)=10∶1为洗脱剂,经硅胶柱层析得产品0.41 g.收率61.5 %,m.p. 207~209 ℃.IR(σ/cm-1,KBr压片):3 373(O—H),2 935(C—H),2 869(C—H),1 728(C==O),1 187(C—O—C),1 126(C—O—C),1 074(C—O—C),1 039(C—O—C);1H-NMR(CDCl3)δ:4.31(1H,t,6α-H),4.12(1H,m,3α-H),3.51(1H,dd,4α-H),1.21(3H,s,19-CH3),0.91(3H,d,21-CH3),0.84(6H,d,26-CH3& 27-CH3),0.80(3H,s,18-CH3).
3 讨论与结论
胆固醇具有甾体化合物的结构,位于B环的5,6双键的羟基化为反式羟基化,最后产物为5α,6β-二羟基构型.实验中,首先3β-羟基甲酰化,H2O2使甲酸氧化成过氧甲酸,过氧甲酸再进攻双键.由于A环1,3碳原子上的α氢原子是直立键(Hα),对5,6双键的同侧π轨道产生空间位阻,使过氧甲酸只能在另一侧进攻π轨道,形成一个环氧丙烷环,且呈β-构型,A环和B环为顺式构型,见图1(a)、图1(b)、图1(c).在开环阶段,由于A环2,4位的Hα和19甲基的空间位阻,使甲酸只能进攻环氧丙烷环6位碳原子的β位,形成6β-甲酰氧基-5α-羟基构型,此时A环和B环为反式构型见图1(c)、图1(d).碱水解后成为3β,5α,6β-三羟基构型,A环和B环为反式构型,见图1(e).
Pran K.Datta等[5]从海笔中提取分离得到胆甾-3β,5α,6β-三醇,并确定了结构,其1H-NMR 与本文相同,也证实了5α,6β-二羟基构型的正确.
胆甾-3β,5α,6β-三醇和胆甾-3β,5α,6β-三醇-3,6-二草酸单酯经IR和1H-NMR确证了结构正确,胆甾-3β,5α,6β-三醇-3,6-二草酸单酯为未见文献报道的化合物.

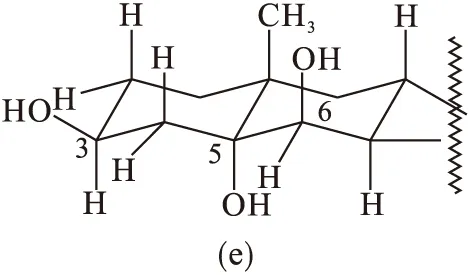
图1 5,6双键反式羟基化形成5α,6β-二羟基构型
Synthesis of Cholesta-3β,5α,6β-triol-3,6-dimonooxalate
LIU Yue-jin, BAO Li-jiao, WANG Yu-nan
(Shenyang University of Chemical Technology, Shenyang 110142, China)
To produce a derivative of Cholesta-3β,5α,6β-triol Cholesta-3β,5α,6β-triol was synthesized from Cholesterol as raw materials through 30 % H2O2oxidation in 88 % formic acid,and the yield was found to be 83.5 %,m.p.228~230 ℃.Cholesta-3β,5α,6β-triol-3,6-dimonooxalate was synthesized from Cholestan-3β,5α,6β-triol and oxalyl chloride as raw materials esterificating at 0 ℃ in the acetone with pyridine as a catalyst in 15 min and then hydrolysing at 0 ℃ in 30 min by addition of a little water.The yield was found to be 61.5 %,m.p.207~209 ℃.The two compounds were corroborated structurally by IR and1H-NMR.Key words: cholesta-3β,5α,6β-triol; cholesta-3β,5α,6β-triol-3,6-dimonooxalate; synthesis
2013-11-15
刘跃金(1964-),男,吉林九台人,副教授,博士,主要从事生物化学与药物化学方面的研究.
2095-2198(2015)01-0010-03
10.3969/j.issn.2095-2198.2015.01.003
R914.5
A

