HPLC法同时测定痛经贴剂中柚皮苷、橙皮苷和新橙皮苷的含量
张丽君,田 军,刘 永
(1.安徽中医药大学,安徽合肥 230012;
2.安徽省食品药品检验研究院,安徽省中药研究与开发重点实验室,安徽合肥 230051)
痛经贴剂由枳壳、陈皮、赤芍、当归、延胡索、冰片等八味中药组成,具有行气止痛,活血化瘀的功效,用于治疗气滞血瘀型原发性痛经。本方中枳壳和陈皮同属芸香科植物,具有理气作用,故作为君药。柚皮苷、新橙皮苷为枳壳主要有效成分,橙皮苷为陈皮主要有效成分,且柚皮苷、橙皮苷和新橙皮苷均属黄酮类成分[1-3]。为有效控制痛经贴剂的质量,本实验采用高效液相色谱法同时对柚皮苷、橙皮苷和新橙皮苷进行测定并进行了方法学考察,方法简单、可靠、稳定性好。
1 仪器与试药
岛津LC-10AT型高效液相色谱仪(单元泵,SPD紫外检测器,岛津 LC solution Lite色谱工作站);TU-1810紫外可见分光光度计(北京普析通用仪器有限责任公司);As3120B型超声波清洗器(北京恒奥德仪器仪表有限公司);METTLER TOLEDO XS105型电子天平(郑州龙腾达仪器设备有限公司)。柚皮苷对照品(批号:110722-200108);橙皮苷对照品(批号:110721-200512);新橙皮苷对照品(批号:111857-201102)均购自中国药品生物制品检定所;甲醇、乙腈为色谱纯;水为娃哈哈纯净水;其它试剂均为分析纯。痛经贴剂,自制,批号分别为:20141218、20141226、20150112。
2 方法与结果
2.1 色谱条件 色谱柱:Cosmosil-C18色谱柱(5 μm,4.6 mm × 250 mm);流动相:乙腈—0.1% 磷酸(21∶79);流速:1.0 mL · min-1;检测波长:分别取柚皮苷、橙皮苷和新橙皮苷对照品液适量,在200~400 nm波长范围内扫描,并参考药典,最终确定最大吸收波长为283 nm;柱温:25℃;进样量:10 μL。
2.2 对照品溶液的制备 精密称取柚皮苷、橙皮苷、新橙皮苷对照品适量,加甲醇制成每1 mL中含柚皮苷80μg、橙皮苷60μg、新橙皮苷60μg的混合溶液,即得混合对照品溶液。
2.3 供试品溶液的制备 本品贴剂除去盖衬,取约1 g,精密称定,置锥形瓶中,加甲醇50 mL,称定重量,加热回流1.5 h,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.4 空白溶液的制备 根据处方组成,取除枳壳和陈皮外的其余药材,按制备工艺要求制备不含枳壳和陈皮的空白样品,照“2.3”项下方法制备空白溶液,精密吸取10μL,按上述色谱条件进行测定,结果在柚皮苷、橙皮苷和新橙皮苷位置未见峰出现,表明空白溶液对样品测定无干扰。测定结果见图1。
2.5 对照品精密度试验 取“2.2”项下的混合对照品溶液,按上述色谱条件进行测定,连续进样6次,结果柚皮苷、橙皮苷和新橙皮苷峰面积RSD分别为 1.035%、1.716%和 0.899%,表明本法对照品精密度良好。
2.6 线性范围考察 精密称取柚皮苷、橙皮苷和新橙皮苷对照品适量,加甲醇制成每1 mL中含柚皮苷 0.34 mg、橙皮苷 0.25 mg、新橙皮苷 0.26 mg的混合对照品溶液,采用等比稀释法,即从10 mL上述对照品溶液中取5 mL,用甲醇定容至10 mL,再从10 mL中取5 mL用甲醇定容至10 mL,依次操作,分别得含柚皮苷 340、170、85、42.50、21.25、10.63 mg·L-1,橙皮苷 250、125、62.50、31.25、15.63、7.81 mg· L-1和新橙皮苷 260、130、65、32.50、16.25、8.13 mg·L-1的 6 份混合对照品溶液,按“2.1”项下色谱条件注入液相色谱仪进行测定,记录峰面积。以对照品进样量(μg)为横坐标X,以峰面积为纵坐标Y进行线性回归,得线性回归方程:柚皮苷 Y=18 015X -23 049,r=0.999 9(n=6);橙皮苷 Y=19 172X -20 620,r=0.999 9(n=6);新橙皮苷 Y=20 985X -23 203,r=0.999 9(n=6)。结果表明:柚皮苷在 10.63 ~340 mg·L-1浓度范围内线性关系良好,橙皮苷在7.81~250 mg·L-1浓度范围内线性关系良好,新橙皮苷在8.13~260 mg·L-1浓度范围内线性关系良好。
2.7 供试品精密度试验 取同一批号(批号:20141218)供试品,按“2.3”项下制备供试品溶液,再按“2.1”项下色谱条件注入液相色谱仪,连续进样6次,结果柚皮苷、橙皮苷和新橙皮苷峰面积RSD 分别为1.02%、1.29%和1.94%,表明本法供试品精密度良好。
2.8 重复性试验 取同一批(批号20141218)痛经贴剂样品,按“2.3”项下供试品溶液制备方法制备6份供试液,按“2.1”色谱条件注入液相色谱仪进行测定,并按外标法以峰面积计算含量,结果柚皮苷的含量为 6.09、6.05、5.97、5.81、5.89、5.97 mg·g-1,平均值为5.96 mg·g-1;橙皮苷的含量为5.23、5.14、5.1、5.14、5.01、5.06 mg·g-1,平均值为5.11 mg · g-1;新橙皮苷的含量为 3.76、3.72、3.66、3.85、3.8、3.82 mg·g-1,平均值为 3.77 mg·g-1。柚皮苷、橙皮苷和新橙皮苷的溶液含量的RSD分别为1.71%、1.48% 和 1.86%,表明本法重现性良好。
2.9 稳定性试验 取同一批(批号20141218)的供试品溶液,分别于 0、1、2、4、6、8 h,按“2.1”项下色谱条件测定,记录其峰面积,结果柚皮苷的峰面积分别为 2 253 621、2 272 347、2 317 384、2 255 391、2 282 744、2 203 981,平均值为 2 264 245;橙皮苷的峰面积为2 143 612、2 160 111、2 155 815、2 086 990、2 202 010、2 127 881,平均值为 2 146 070;新橙皮苷的峰面积为 1 640 164、1 651 908、1 650 799、1 582 536、1 608 589、1 598 429,平均值为 1 622 071。柚皮苷、橙皮苷和新橙皮苷峰面积RSD分别为1.65%、1.78% 和 1.83%。结果表明,供试品溶液在8 h内稳定。
2.10 加样回收率试验 精密称取除去盖衬的同一批号已知含量的痛经贴剂(批号20141218,柚皮苷、橙皮苷和新橙皮苷的含量分别为5.86 mg·g-1、5.04 mg · g-1和3.68 mg · g-1)6 份,每份约0.5 g,置锥形瓶中,再分别加入柚皮苷、橙皮苷和新橙皮苷浓度分别为 0.312 4、0.263 2 和 0.185 8 mg·mL-1的对照品混合溶液10 mL,精密加入甲醇40 mL,称定重量,加热回流1.5 h,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,按“2.1”项下色谱条件进行测定,计算回收率。结果见表1~3。
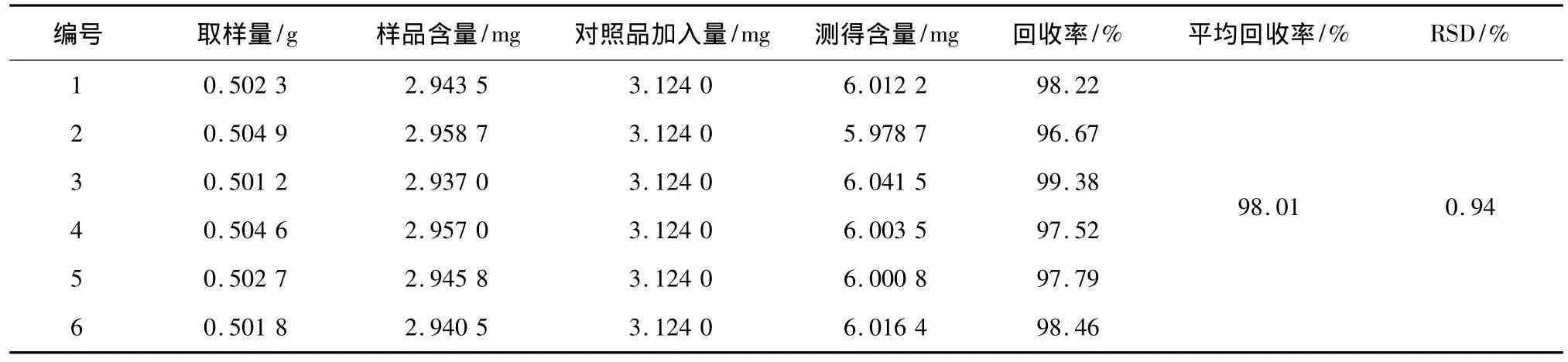
表1 柚皮苷加样回收率(n=6)
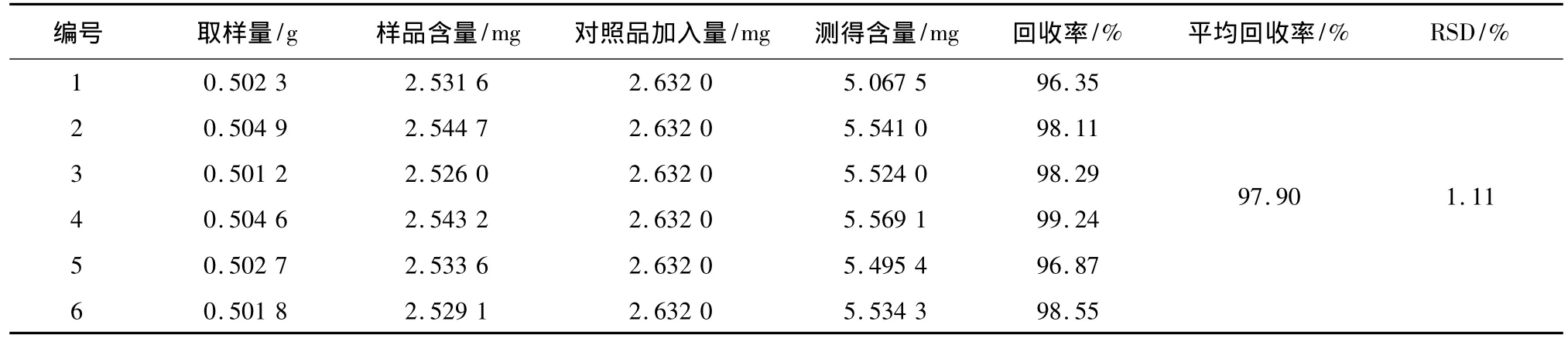
表2 橙皮苷加样回收率(n=6)
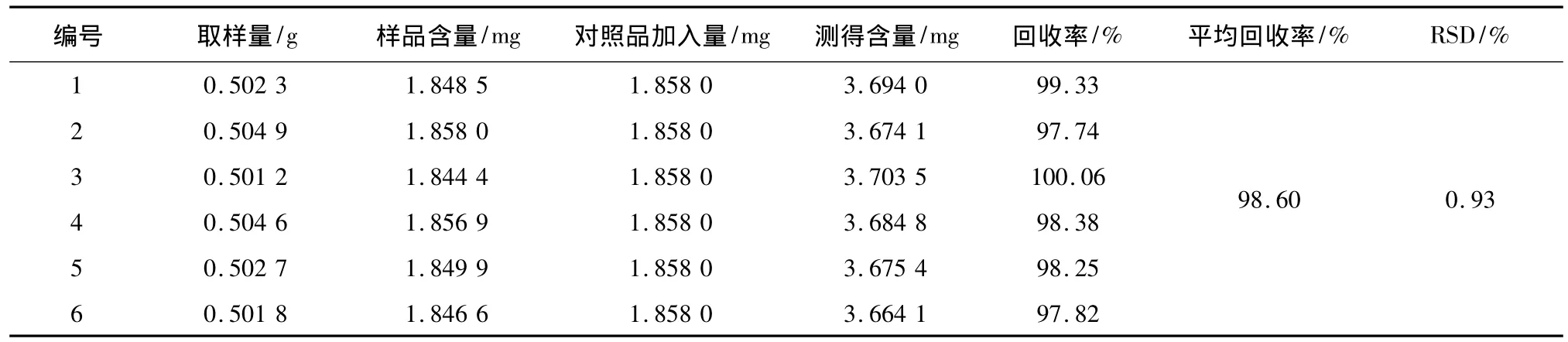
表3 新橙皮苷加样回收率(n=6)
2.11 样品测定 取本品样品 3批(批号:20141218,20141226,20150112),按“2.3”项下制备供试品溶液,按“2.1”项下色谱条件测定,3批样品中柚皮苷、橙皮苷和新橙皮苷的含量结果见表4。
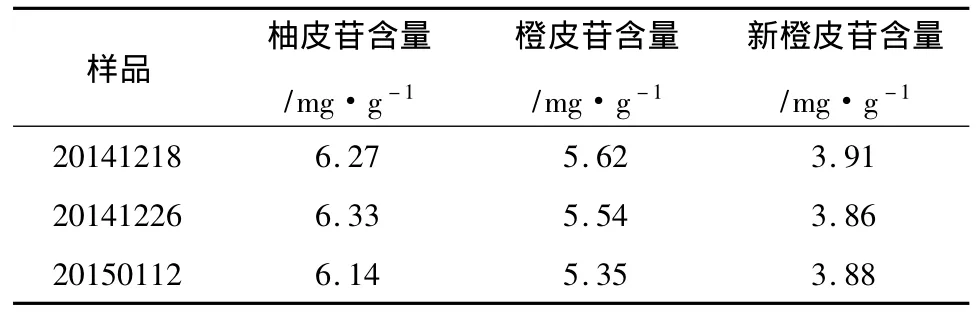
表4 柚皮苷、橙皮苷和新橙皮苷含量测定结果
3 讨论
3.1 波长的选择 药典2010版一部枳壳、陈皮采用高效液相色谱法测定柚皮苷、橙皮苷和新橙皮苷含量,测定波长均为283 nm,且采用紫外分光光度计在200~400 nm波长范围内扫描,结果显示柚皮苷、橙皮苷和新橙皮苷均在283 nm下有最大吸收,参考相关文献[4-5],最终确定选择283 nm为最大测定波长。
3.2 流动相的选择 分别对甲醇—醋酸—水[6-8]和乙腈—0.1%磷酸[9-11]两种流动相的不同比例进行了考察,结果甲醇—醋酸—水系统为流动相时橙皮苷峰形较宽,且新橙皮苷峰与杂质峰分离效果较差,当甲醇—醋酸—水比例为(35∶1∶64)时,新橙皮苷峰分离效果较好,但出峰时间较长,而乙腈—0.1%磷酸系统为流动相时出峰时间短,峰形和分离度都较好,通过对其流动相不同比例进行比较,结果表明柚皮苷、橙皮苷和新橙皮苷在乙腈—0.1%磷酸(21∶79)流动相下的峰形、分离度和出峰时间都较为理想,且空白对照无干扰。
3.3 提取方法的选择 分别比较了用甲醇超声提取[12-13]30、60 和90 min 及用甲醇加热回流提取[14]30、60和90 min,根据柚皮苷、橙皮苷和新橙皮苷的含量测定结果,最终确定用甲醇加热回流提取90 min,可将这三种成分提取的比较完全。
3.4 柱温的选择 分别比较考察了20、25、30℃柱温对柚皮苷、橙皮苷和新橙皮苷出峰时间及峰形的影响,结果表明25℃柱温下效果最好,故选择25℃作为柱温。
3.5 色谱柱的选择 本实验分别考察了3种色谱柱 Cosmosil-C18(5 μm,4.6 mm ×250 mm)、Phenomenex-C18(5 μm,4.6 mm ×250 mm)、Welchrom-C18(5μm,4.6 mm ×250 mm)对样品中柚皮苷、橙皮苷和新橙皮苷的分离效果,结果Welchrom-C18色谱柱分离度较差,Cosmosil-C18和Phenomenex-C18色谱柱的分离效果、峰形均良好,但Cosmosil-C18柱的出峰时间较早,故选择Cosmosil-C18柱作为本实验的色谱柱。
4 结论
本实验建立的HPLC法同时测定痛经贴剂中柚皮苷、橙皮苷和新橙皮苷的含量方法,具有操作方便、准确可靠及重复性和稳定性好的优点,可作为痛经贴剂的质量控制方法。
[1] 李伟伟,张国伟.陈皮黄酮类成分研究进展[J].中国医学创新,2014,11(24):154 -156.
[2] 龚丽丽.枳壳类药材化学成分及药理研究[J].亚太传统医药,2014,10(16):39 -40.
[3] 季 忆,陈建真,陈建明.枳壳黄酮类成分的研究进展[J].中国中医药信息杂志,2010,17(11):105 -107.
[4] 国家药典委员会.中国药典(一部)[S].北京:中国医药科技出版社,2010:229-230.
[5] 徐海燕,金 艺,张红霞,等.HPLC同时测定胃力片中柚皮苷、橙皮苷和新橙皮苷的含量[J].中成药,2010,32(8):1355-1357.
[6] 杨佳静,薛 佳,周华方,等.HPLC法同时测定胃苏颗粒中柚皮苷、橙皮苷和新橙皮苷的含量[J].中国药房,2014,25(4):372-374.
[7] 王祝枝,王晓华,朱 玉,等.正交实验法优选佛手的醇提工艺[J].安徽医药,2014,18(1):26 -29.
[8] 马向东.HPLC测定枳术安胃胶囊中柚皮苷和新橙皮苷的含量[J].海峡药学,2014,26(7):65 -66.
[9] 康四和,周 锐,聂 晶.HPLC测定小儿消积止咳口服液中柚皮苷、橙皮苷和新橙皮苷的含量[J].中成药,2010,32(12):2088-2091.
[10]陈晓明,王 巍,闵庆璐.HPLC同时测定木香分气丸中柚皮苷、橙皮苷和新橙皮苷的含量[J].中国实验方剂学杂志,2012,18(19):115 -117.
[11]蒋俊春,孟建升.HPLC法同时测定及砂和胃胶囊中橙皮苷、柚皮苷和新橙皮苷的含量[J].中华中医药学刊,2014,32(6):1496-1498.
[12]刘玉春,张 静.HPLC同时测定橘红枇杷胶囊中橙皮苷、柚皮苷的含量[J].安徽医药,2013,17(12):2044 -2045.
[13]丁 毅,弓晓东,谈瑄忠,等.HPLC同时测定通腑理气颗粒中柚皮苷、橙皮苷和新橙皮苷含量[J].中国中医药信息杂志,2012,19(5):53 -55.
[14]张金莲,何 敏,谢一辉,等.高效液相色谱法测定枳壳饮片中柚皮苷、橙皮苷和新橙皮苷的含量[J].中国实验方剂学杂志,2010,16(6):68 -70.

