小儿感冒颗粒的质量标准研究
杨 堃
(重庆市食品药品检验所,重庆市药物过程与质量控制工程技术研究中心,重庆,401121)
小儿感冒颗粒的质量标准研究
杨 堃
(重庆市食品药品检验所,重庆市药物过程与质量控制工程技术研究中心,重庆,401121)
目的:建立小儿感冒颗粒的质量标准。方法:用TLC法鉴别了小儿感冒颗粒中广藿香、菊花、连翘和用HPLC法测定了小儿感冒颗粒中连翘苷的含量;色谱柱为DiamonsilTMC18柱(5 μm,4.6 mm×250 mm),柱温为30 ℃,以乙腈-水(24∶76)为流动相,检测波长为202 nm,流速1.0 mL/min。结果:在TLC色谱中均能检出百秋李醇、菊花、连翘苷;且特征斑点明显,阴性无干扰;连翘苷在0.023 62 μg~0.590 5 μg范围内呈良好的线性关系,r=0.99999(n=6),平均回收率为99.06%,RSD=1.5%.结论:方法简便、准确、重现性好;可用于小儿感冒颗粒的质量控制。
小儿感冒颗粒;质量标准;TLC;HPLC;连翘苷
小儿感冒颗粒是由广藿香、菊花、连翘、地黄、白薇、地骨皮、石膏、大青叶、板蓝根等共10味药组成的复方制剂,收载于《中华人民共和国药典》2010年版一部[1],功用为疏风解表,清热解毒。原标准仅收载大青叶、板蓝根的薄层色谱鉴别。本文在既往研究的基础上,本文采用薄层色谱法对方中广藿香、连翘、菊花进行了定性鉴别,并采用高效液相色谱法制定了方中连翘(以连翘苷计)含量测定方法,为更好地控制小儿感冒颗粒的质量提供依据。
1 材料与方法
1.1 材料 小儿感冒颗粒(批号为:20120206、20120207、20120208,云南白药集团股份有限公司生产,广藿香、连翘、菊花等处方中的各味药材由太极集团重庆桐君阁药厂有限公司提供。百秋李醇(批号:772-200008)、菊花(批号:121384-200801)、连翘苷(批号:110821-200805),购自中国药品生物制品检定研究院。
1.2 仪器 高效液相色谱仪:Agilent HP1100(包括四元泵,柱温箱,自动进样器,二级管阵列检测器);KQ3200B型超声波清洗器(功率500W,频率40KHZ)。
1.3 试药 硅胶G(化学纯,青岛海洋化工厂),其余试剂、试药均为分析纯。
2 方法
2.1 薄层鉴别
2.1.1 广藿香的薄层鉴别[2]取本品24 g,研细,加乙醚适量,浸泡24 h以上,时时振摇,滤过,滤液低温蒸干,残渣加乙酸乙酯1 mL使溶解,作为供试品溶液。另取百秋李醇对照品,加乙酸乙酯制成每1 mL含1 mg的溶液,作为对照品溶液。照薄层色谱法(附录Ⅵ B)试验,吸取供试品溶液20~30 μL,对照品溶液1~2 μL,分别点于同一硅胶G薄层板上,以石油醚(30~60 ℃)-乙酸乙酯-冰醋酸(95∶5∶0.2)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸试液,加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点,且阴性对照无干扰。(见图1)

图1 小儿感冒颗粒广藿香的TLC鉴别图谱
注:1.阴性对照(缺广藿香)25 μL;2.样品(云南白药集团,批号:20120206)20 μL;3.样品(云南白药集团,批号:20120207)20 μL;4.样品(云南白药集团,批号:20120208)20 μL;5.百秋李醇对照品2 μL
2.1.2 菊花的薄层鉴别[3-4]取本品6 g,研细,加甲醇30 mL,超声处理20 min,滤过,滤液蒸干,残渣加水20 mL使溶解,用稀盐酸调pH值至2~3,用乙酸乙酯振摇提取3次,每次20 mL,合并乙酸乙酯提取液,蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。另取菊花对照药材1 g,加稀盐酸1 mL和乙酸乙酯20 mL,超声处理30 min,滤过,滤液蒸干,残渣加乙酸乙酯1 mL使溶解,作为对照药材溶液。照薄层色谱法(附录Ⅵ B)试验,吸取供试品溶液1~2 μL,对照药材溶液2 μL,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯-甲酸(7∶3∶0.5)为展开剂,展开,取出,晾干,喷以5%三氯化铝乙醇试液,加热至斑点显色清晰,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,且阴性对照无干扰。(见图2)
2.1.3 连翘的薄层鉴别[5-7]取本品6 g,研细,加甲醇30 mL,超声处理20 min,滤过,滤液蒸干。残渣加0.2%氢氧化钠溶液20 mL,加热使溶解,用水饱和的正丁醇振摇提取3次,每次20 mL;取正丁醇提取液,再用正丁醇饱和的水洗涤2次,每次30 mL,合并正丁醇液,蒸干,残渣加0.2%氢氧化钠溶液20 mL,加热使溶解,再用三氯甲烷振摇提取3次,每次20 mL;合并三氯甲烷提取液,滤过,滤液蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。另取连翘苷对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。吸取供试品溶液10 μL~15 μL和对照品溶液10 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇-甲酸(9∶1∶0.1)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸试液,加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点,且阴性对照无干扰[8]。(见图3)
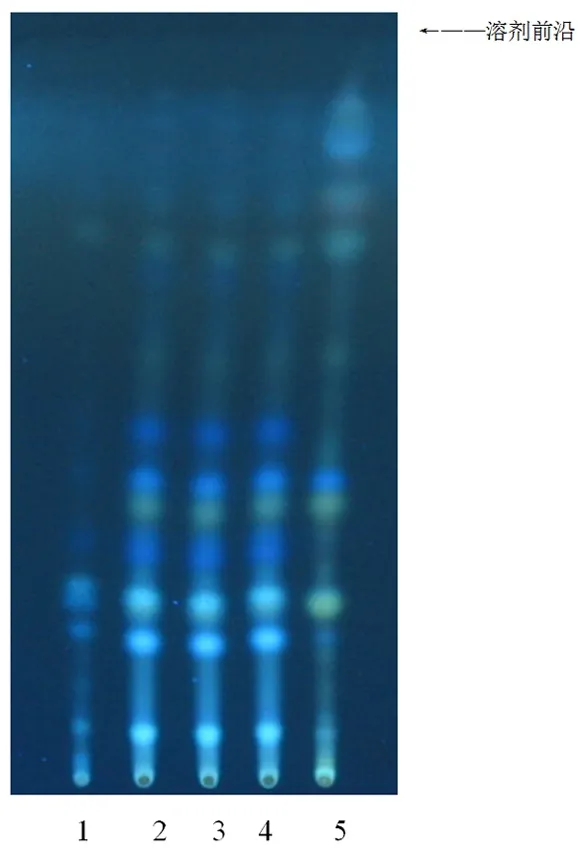
图2 小儿感冒颗粒菊花的TLC鉴别图谱
注:1.阴性对照(缺菊花)2 μL;2.样品(云南白药集团,批号:20120206)1 μL;3.样品(云南白药集团,批号:20120207)1 μL;4.样品(云南白药集团,批号:20120208)1 μL;5.菊花对照药材3 μL

图3 小儿感冒颗粒连翘的TLC鉴别图谱
注:1.阴性对照(缺连翘);2.样品(云南白药集团,批号:20120206);3.样品(云南白药集团,批号:20120207);4.样品(云南白药集团,批号:20120208);5.连翘苷对照品
2.2 含量测定
2.2.1 药味的选择 按处方中君臣药味的要求,我们先对方中广藿香[9-10](百秋李醇计)的GC含量测定[11]方法进行了研究,其含量太低,无测定意义,故对连翘[12](以连翘苷计)含量测定方法进行了研究,通过试验考察,建立了HPLC含量测定方法。
2.2.2 色谱条件[13]色谱柱:用十八烷基硅烷键和硅胶为填充剂;流动相:乙腈-水(24∶76);检测波长:202 nm;柱温30 ℃;流速:1.0 mL/min;理论塔板数:按连翘苷峰计应不低于3 000。
2.2.3 对照品溶液的制备 精密称取在110 ℃干燥至恒重的连翘苷对照品适量,加50%甲醇制成每1 mL含20 μg的溶液,即得。
2.2.4 供试品溶液的制备[14-15]取装量差异项下的本品,研细,取约6 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,密塞,称定重量,超声处理(功率500 W,频率40 kHz)30 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液10 mL,蒸干,残渣加适量70%乙醇使溶解,加在中性氧化铝柱(100~200目,5 g,内径1.5 cm)上,用70%乙醇溶液100 mL洗脱,收集洗脱液,蒸干,残渣加50%甲醇适量使溶解,转移至5 mL量瓶中,加50%甲醇稀释至刻度,摇匀,滤过,取续滤液,作为供试品溶液。精密量取10 μL,进样,记录色谱图[6-9]。
2.2.5 阴性对照试验 取缺连翘的阴性对照约6 g,同供试品溶液的制备方法制成阴性对照溶液,注入液相色谱仪,结果在连翘苷对照品出峰时间处无对应色谱峰出现,表明阴性对照无干扰。(见图4)

图4 小儿感冒颗粒HPLC图
注:1.连翘苷对照品;2.小儿感冒颗粒样品;3.阴性对照(缺连翘)
2.2.6 测定波长的选择 我们用二级管阵列检测器分别对连翘苷对照品、小儿感冒颗粒样品进行光谱分析,结果发现202 nm为连翘苷最大吸收,且其他成分峰在此处吸收值很小,故选用202 nm作为测定波长。
2.2.7 线性范围 分别精密吸取连翘苷对照品溶液(浓度0.023 62 mg/mL)1 μL、5 μL、10 μL、15 μL、20 μL、25 μL,注入液相色谱仪测定峰面积,结果见表1。

表1 线性关系试验结果
以连翘苷峰面积(A)为纵坐标,连翘苷对照品进样量(g)为横坐标,绘制标准曲线,并进行线性回归,得回归方程:y=9692.2x+17.929r=1。
上述结果表明,连翘苷对照品进样量在0.023 62 μg~0.590 5 μg的范围内,与峰面积呈良好的线性关系。
2.2.8 精密度实验 精密吸取连翘苷对照品溶液(浓度0.023 62 mg/mL)10 μL,重复进样5次,按上述色谱条件测定峰面积,结果见下表。试验结果表明,仪器精密度良好。

表2 仪器精密度试验结果
2.2.9 稳定性试验 分别吸取常温下放置的同一供试品溶液10 μL,于0、2、4、8、12 h进样,测定,结果见下表。试验结果表明,供试品溶液至少在12 h内稳定。

表3 供试品溶液稳定性试验结果
2.2.10 重复性试验 取同一批号样品(批号20120207),按含量测定项下供试品制备方法平行制备5份供试品溶液,并测定含量,结果见下表。试验结果表明,方法重复性良好。

表4 重复性试验结果
2.2.11 回收率试验 取本品(批号20120207,已测定连翘苷含量为0.046 0 mg/g)3 g,共6份,精密称定,分别精密加入连翘苷对照品溶液(5.905 μg/mL)25 mL,称定重量,同供试品溶液的制备方法制备,并按拟订的色谱条件测定连翘苷含量,按下式计算回收率,结果见表5。试验结果表明,加样回收率均在95%~105%间,符合有关的技术要求。


表5 加样回收试验结果
2.2.12 方法耐用性试验 按正文拟订的含量测定方法,分别对样品2采用不同牌号的色谱柱,分别测定连翘苷的含量,计算,结果见表6。试验结果表明,方法耐用性试验良好。

表6 方法耐用性试验结果
2.2.13 样品测定 取样品3批,按上述色谱条件和方法测定连翘苷的含量,测定结果见表7。

表7 小儿感冒颗粒中连翘苷的含量测定结果
3 讨论
在连翘的TLC鉴别方法中,若采用含量测定的方法处理样品,所得样品中连翘苷的斑点显色不理想,整个样品斑点底色较重,故采用的是正文中样品处理办法,结果很好。我们曾选用连翘同法制备对照药材溶液,结果显示:其在与样品相应位置上的斑点显色不清晰,较小,且阴性对照有个别斑点干扰,故放弃。
样品含量测定的处理方法参照文献经过试验摸索,曾对连翘苷的提取方法考察了:TLC法中样品处理方法;直接甲醇超声提取进样;和甲醇超声提取蒸干后,水溶解再用三氯甲烷提取等方法。所得样品存在杂质峰较多,主峰与杂质峰不能分离,重现性不好和回收率低等问题。同时我们考察了正文方法中甲醇超声时间,过柱用中性氧化铝用量,洗脱溶剂的浓度和用量,最终确定的正文方法能将样品中所含的连翘苷提取完全,回收率平均在100%上,且样品溶液色谱图中连翘苷色谱峰分离度好、峰形尖锐、对称性好,理论板数大于3 000,各项参数能满足HPLC的相关要求。
小儿感冒颗粒为儿科常用药,有有糖型和无糖型两种剂型;且生产厂家众多,包装规格也不同,我们当时选取市面上上述两种剂型和不同厂家规格的共18批次进行试验,按此质量标准,均能检出;此标准可行。
[1]国家药典委员会.中华人民共和国药典(一部)[S].北京:化学工业出版社,2010:500-501.
[2]韩桂茹,董占军.小儿感冒颗粒的薄层鉴别和定量测定研究[J].中成药,2004,26(11):445-446.
[3]田雅琴.HPLC法测定小儿感冒颗粒中绿原酸及连翘苷含量[J].中成药,2009,31(12):484-485.
[4]范磊.小儿感冒颗粒的质量控制方法研究[J].中国医药指南,2013,11(35):661-663.
[5]国家中医药管理局.国家中成药标准汇编—外科妇科分册[S],483-484.
[6]国家中医药管理局.国家中成药标准汇编—口腔肿瘤儿科分册[S],49-50.
[7]孙武强,李海峰.小儿感冒颗粒质量标准研究[J].河南中医,2004,24(8):223-224.
[8]国家中医药管理局.桑菊感冒合剂[M].国家中成药标准汇编—内科—肺系(一),2002.
[9]张颖梅.HPLC法同时测定广藿香中雷杜辛黄酮醇及广藿香酮的含量[J].中国实验方剂学杂志,2013,19(16):254-456.
[10]张小龙,孙晓,马新飞.气相色谱法同时测定小儿感冒颗粒中百秋李醇、薄荷脑、α-蒎烯、β-蒎烯的含量[J].首都医药,2014(22):311-312.
[11]王春燕.气相色谱法测定小儿感冒颗粒中百秋李醇的含量[J].首都医药,2011(4):187-188.
[12]吴平平,李桂龙.小儿感冒颗粒中绿原酸测定方法的改进[J].中草药,2011,42(6):212-214.
[13]张伟,张汉明,等.HPLC法测定连翘药材及感冒退热颗粒中连翘苷的含量[J].中成药,1999,21(9):329-330.
[14]《卫生部药品标准》.新药转正标准第二册[S].1993,7.
[15]刘杰,陈卓,马开.薄层扫描法测定双黄连制剂中连翘苷的含量[J].中成药,1999,21(8):314-316.
(2014-04-26收稿 责任编辑:张文婷)
Study of Quality Standard of Xiao’er Ganmao Granules
Yang Kun
(ChongqingInstituteforFoodandDrugControl,ChongqingEngineeringresearchCenterforPharmaceuticalProcessandQualityControl401121,China)
Objective:To establish the quality standards for Xiao’er Ganmao Granules. Methods: Pogostemonis herba, chrysanthemi flos, and forsythiae fructus were identified with TLC. Phillyrin was meatured by HPLC. DiamonsilTMC18(5 μm,4.6 mm×250 mm) column was used. The column temperature was at 30 ℃. Acetonitrile-water (24∶76) was used as a mobile phase. The detection wavelength was at 202 nm. The flow rate was 1.0 mL/min. Results: Patchouli alcohol, chrysanthemi flos, and forsythiae could be detected by TLC, with the feature spot obvious, negative interference-free. Phillyrin showed a good linear relationship at the range of 0.02362~0.5905μg,r=0.99999 (n=6),The average recovery rate was 99.06% and RSD was 1.5%. Conclusion: TLC method proves to be simple, accurate and with good reproducibility, thus can be used for quality control of Xiao,er Ganmao Granule.
Xiao’er Ganmao Granules; Quality standards; TLC; HPLC; Phillyrin
杨堃,重庆市食品药品检验所中药室,E-mail:yk418@tom.com
R284.1
A
10.3969/j.issn.1673-7202.2015.03.032

