脂质体技术的转化应用分析及关键问题研究
柯 刚 伍振峰, 杨 明, 任桂林 黄居敏 胡鹏翼 王赛君
(1 江西中医药大学现代中药制剂教育部重点实验室,南昌,330004; 2 成都中医药大学,成都,610075)
脂质体技术的转化应用分析及关键问题研究
柯 刚1伍振峰1,2杨 明1,2任桂林2黄居敏1胡鹏翼1王赛君1
(1 江西中医药大学现代中药制剂教育部重点实验室,南昌,330004; 2 成都中医药大学,成都,610075)
目的:研究脂质体制剂科研成果转化应用情况。方法:对国家自然科学基金委对脂质体技术的资助情况及其研究成果概况、国家知识产权局数据库脂质体国内外专利、国内外公开发表的脂质体相关文章情况进行统计分析。结果:当前脂质体研究存在研究偏于基础,基础研究与实际应用脱节,转化困难等问题。结论:脂质体的基础研究应结合工业生产,在转化医学概念指引下,从脂质体转化的关键问题出发,以加速基础研究转化为实际应用。
脂质体;基础研究;应用研究;转化医学
脂质体是由一种或多种两亲性分子双层膜包裹而成的具有一个或多个水性腔室的微泡,将药物包裹或镶嵌在脂质体中形成脂质体药物[1]。脂质体具有类生物膜结构,可包封水溶性和脂溶性药物,其选择性高、无毒性、无免疫原性、适于生物体内降解[2]。脂质体作为药物载体,具有高度的靶向性、能有效保护被包裹药物并可控释缓释药物、可显著提高药物治疗指数、降低药物的不良反应,已成为国内外医药界研究的热点[3-5]。现在国内外对脂质体的研究报道已经非常之多,但是上市用于临床的制剂却相差甚远,怎样在转化医学[6]概念的指导下将更多的脂质体研究成果转化成临床上安全稳定、疗效确切的药物,还有待科研工作者的努力。
我们通过统计分析国家自然基金对脂质体研究的资助及研究成果、脂质体专利概况和脂质体文献报道,分析脂质体技术转化情况,对目前脂质体基础研究与转化应用现状进行分析,以期加快脂质体转化运用。
1 脂质体发展历史与应用
1965年,由英国科学家Alec Bangham在研究磷脂悬浮于水时,首次展示了脂质体是球形的、自我封闭的、分散在水中并且包封一部分水性递质的脂质粒子[7],之后各种各样的脂质体制备技术和表征方法不断诞生,促使一个新的研究领域快速发展。脂质体作为药物的使用可以追溯到脂质体被正式发现以前,早在1934年IG Farbenidustrie的英国专利已经描述了使用磷脂和胆固醇的水分散体作为药物载体,作为药物传递方面的运用。在脂质体正式提出后Bangha和Gregoriadis等科学家就在脂质体作为药物传递系统的应用做了很多研究,1971年Gregoriadis等首次将脂质体用于生物活性物质的转运[8],经过40多年的发展,脂质体在很多领域得到了应用,可以作药物控释的载体、疫苗佐剂、用于心血管疾病的诊断与治疗、基因治疗的加载系统等[10-12]。另外脂质体作为药品还有很多前沿研究[13],如脂质体作为生物技术医药产品新剂型、血红蛋白脂质体等研究。现如今脂质体作为一种药物载体已经实现了商业化,如1995年美国食品药品管理局(FDA)批准世界上第一个临床运用的抗肿瘤药物脂质体Doxil[14],另外,还有很多项目处于临床试验阶段。从目前脂质体药物开发主要方向来看,主要有:化疗药物,疫苗和核酸类药物这三类药物。
2 脂质体基础研究转化现状
2.1 数据来源与选取 国家自然基金资助与成果检索以国家自然科学基金委员会科学基金网络信息系统和科学基金共享服务网及丁香园数据库为数据来源。脂质体专利检索以国家知识产权专利数据库作为数据来源。脂质体文献检索以中国知网(CNKI)收录期刊全文、会议论文、报纸全文、博士、硕士学位论文数据库和Pubmed数据库作为文献来源。全面统计2000—2013年脂质体国家自然基金资助及成果、专利申请量和授权量、文献报道量。
2.2 脂质体国家自然基金资助与成果
2.2.1 自然基金资助研究趋势 以“脂质体”为关键词对项目名称进行检索,结果见图1,2000年以后自然基金对脂质体研究资助项目数量和资助金额逐渐增加,2000—2013年共资助项目256项,资助金额达8 295.5万元,2012年资助项目和金额最多,项目数和资助金额是2001年的43倍和137倍。以“脂质体”为关键词对项目名称、项目摘要和主题词进行检索,2000年以后涉及脂质体的项目共资助项目518个,资助金额达17 280.5万元。在自然基金脂质体资助项目里,其资助主要方向涉及了脂质体主要的热门研究方向,包括新型脂质体制备及修饰、脂质体在抗肿瘤中的基础研究、脂质体做载体在基因等方面研究、脂质体探针等检测方面研究等。

图1 国家自然基金脂质体中标量及中标金额分布
2.2.2 自然基金资助研究成果 根据国家自然科学基金委员会科学基金共享服务网提供数据,查询所有项目名称中含有“脂质体”自然基金项目成果,统计结果见表1。在2000—2011年之间,国家自然科学基金委员会科学基金共享服务网查询到的已经结题项目共60项,资助金额共计1 376.5万元,其中主要成果以论文形式,包括发表的SCI、EI等国际与国内核心期刊论文有307篇和国际与国内会议论文59篇。另外还有著作7部,以及不同级别的奖励9项。
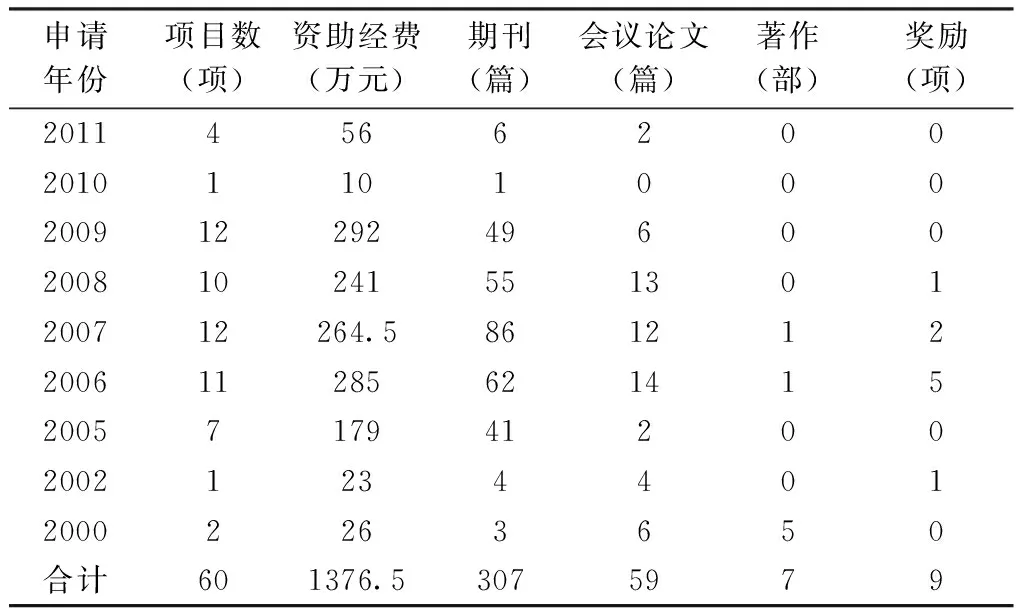
表1 已结题脂质体自然基金项目成果统计
2.3 脂质体文献与专利转化研究
2.3.1 国内外脂质体相关文献报道 截止2013年9月16日通过“Pubmed”“CNKI”等文献检索网站检索自2000年以来脂质体文章发布情况。“Pubmed”检索到题目中含有“liposome”的文章有24 332篇,“CNKI”检索题目和关键词中含有“脂质体”的文章有6 297篇,分布情况见图2。在CNKI中统计仅来自于国家自然基金的脂质体相关文献,结果见表2,来自于国家自然基金资助脂质体相关项目文章报道量仅占中文总文献的10%~20%,可见国家自然基金对脂质体研究的投入仅占整个国内脂质体研究投入的一部分,国家及地方各种项目对脂质体研究的资助经费总额远远大于自然基金的金额。
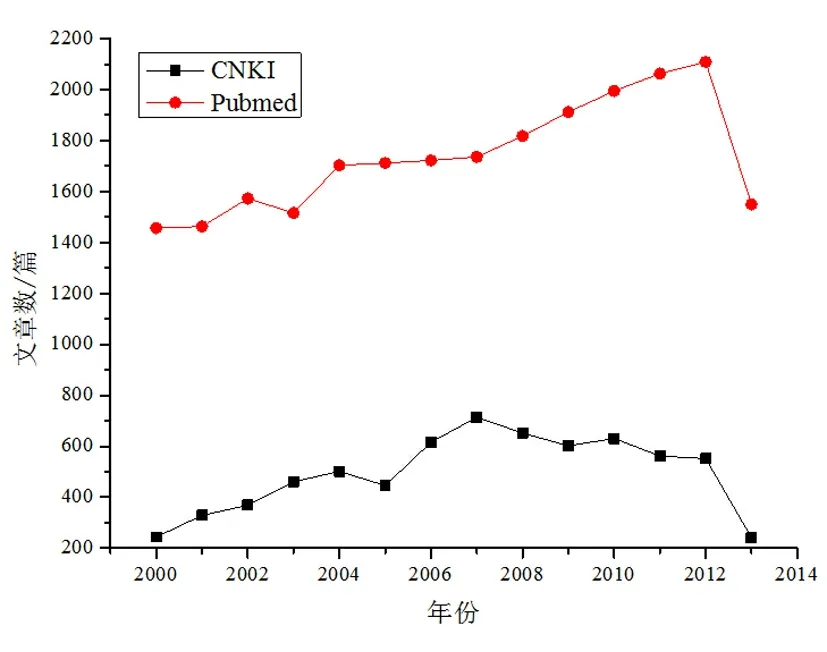
图2 2000—2013年国内外脂质体文献报道分布
文献增长率[15]是当年文献报道量与上一年的文献报道量的比值,以此判断文献增长情况,由表2结果可知脂质体相关文献报道总量基本是逐年增加,因脂质体属于热门研究,研究者更多的是将研究成果发表在SCI,所以外文报道较多且呈逐年增加趋势,而2007年后中文文献报道量呈下降趋势。
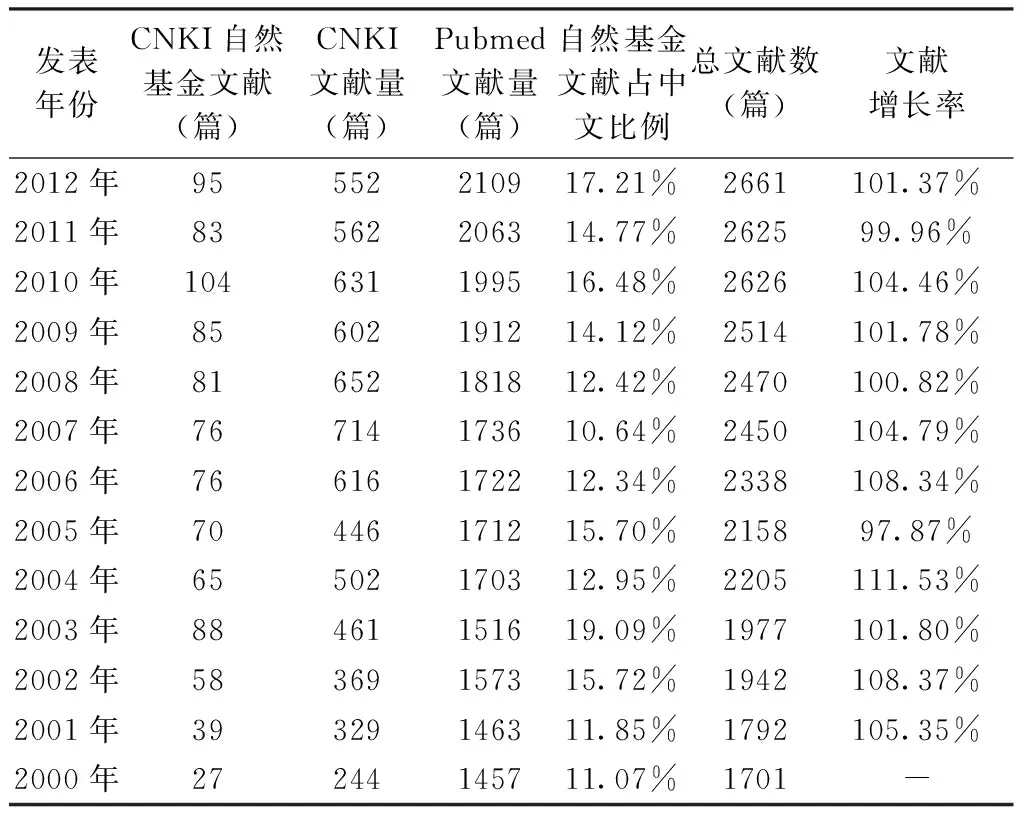
表2 2000—2012年脂质体相关文献报道情况
2.3.2 脂质体专利报道分析 通过国家知识产权局网站专利数据库,分别在中国专利检索、中外专利联合检索和外国及港澳台专利检索数据库,以“脂质体”和“liposome”为关键字,对发明专利和实用新型专利进行检索统计。截止检索日,2000年以来中国专利申请量共有1 778个(截止2012年共1 722个),2000—2012年具有授权的中国专利555个。国外专利有4 757个(截止2012年共4 740个)。

表3 2000—2013年脂质体专利状况
专利授权率是当年专利授权量与当年专利申请量的比值,以此判断专利申请授权情况。专利成长率是当年的专利授权量与上一年的专利授权量的比值,以此判断专利的增长状况。科研成果专利转化率是每一年的脂质体专利授权量与当年公开发表的脂质体相关论文的比值,以此判断脂质体研究领域的科研成果向专利的转化程度[15]。
由表3可知在2000年以后,脂质体专利申请授权率基本在30%左右,专利授权率保持稳定,未随申请量的变化出现大幅度变化。脂质体专利成长率成增长趋势,仅有少数几年专利授权量有所下降,这与当年专利申请量减少有一定关系。而科研成果转化率偏低,仅2009—2011三年超过了10%,其余年份均未超过10%,在2000—2012年之间,科研成果转化率最高的2011年仅有14.59%。考虑到脂质体研究的新颖性,国内研究多以SCI发表,脂质体科研成果专利转化率还要更低。以国内外脂质体总申请量比国内外脂质体文献报道量,总的专利申请量仅占文献报道总数的15.53%,以国内专利授权率平均值34%来计算,国内外专利授权量仅占文献报道量的5.28%。由此可见国内外脂质体科研成果转化率都很低。
2.4 国内外上市脂质体分析 根据国家食品药品监督管理总局(CFDA)、FDA、欧洲药品管理局(EMA)数据库查询国内外脂质体上市制剂,结果见表4、表5。
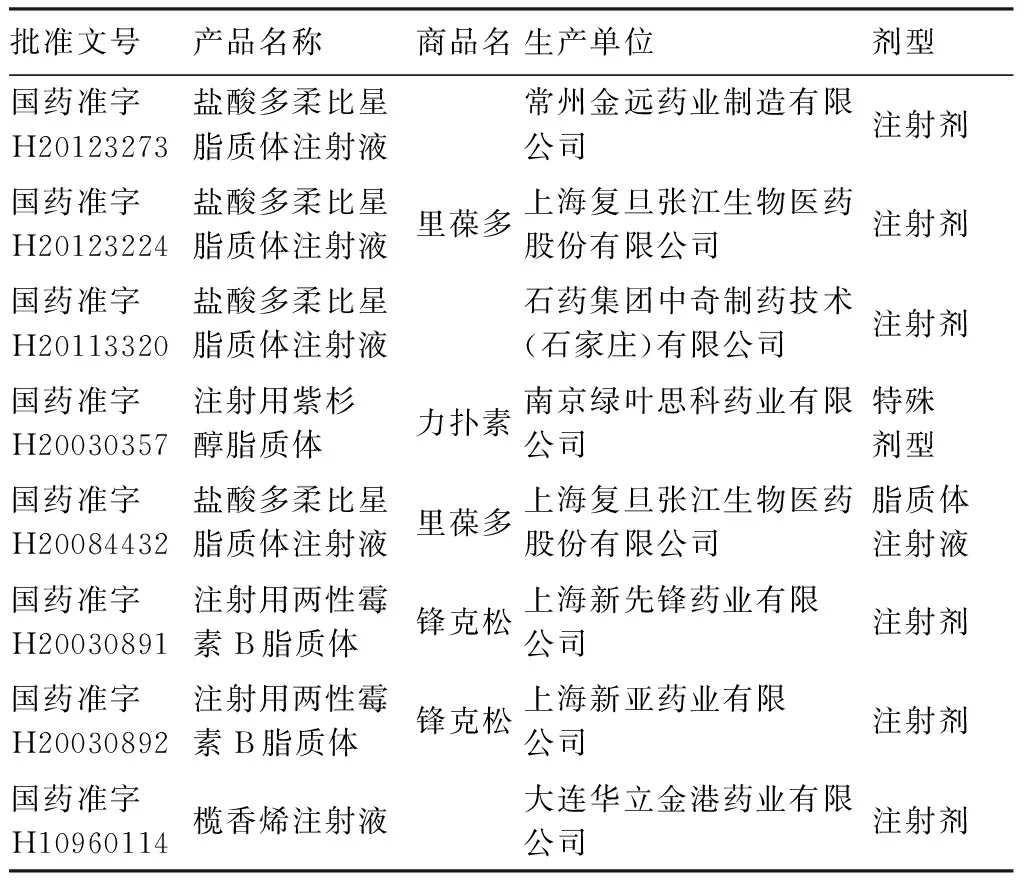
表4 国内上市脂质体产品
目前国内上市脂质体制剂共8个,剔除不同厂家同一药物和同一厂家同一药物不同剂量,仅有盐酸多柔比星脂质体注射液、注射用紫杉醇脂质体、注射用两性霉素B脂质体和榄香烯注射液4个国产药物,而国外共有19个,剔除部分相同成分药物,共15个药物。与国外上市脂质体产品相比,我国国内自主研发的脂质体制剂相关产品的种类和数量还是过少,这也部分反映出我国制药行业从科研成果到实际产品的转化能力不强,科研与生产和市场的脱节仍然存在。

表5 国外上市脂质体产品
3 中药脂质体的研究分析
中药作为传统医学的瑰宝,其在脂质体方面的研究早在20世纪80年代开始,现如今研究报道也有很多。我国脂质体制剂的研究开发有很大比重是作为中药活性成分的载体,其应用主要在抗癌、抗菌、免疫调节等方面,但其成果尚未成熟,绝大多数还是停留在动物实验阶段[16]。中药脂质体主要用于包裹毒性大、不稳定或吸收效果差的中药有效部位或单体。而中药多成分脂质体,由于制备难度大,质量难以控制,其研究较为少见。由于中药成分复杂,应用于临床多为复方且作用机理尚不完全清楚,而中药脂质体对中药活性成分的吸收、分布、代谢、排泄是否影响,需要更加深入研究。中药脂质体多以单一活性成分脂质体的研究为主,从本质上看与化药脂质体的研究无任何区别,难以体现中药多成分多靶点的特色。而中药多成分脂质体的研究虽然能够体现出中药的特色,也符合中药的用药特点,但其质量控制及制备工艺的合理性评价是主要难题。文献统计分析发现中药脂质体的研究重点主要在提高药物包封率和成品稳定性,通过研究将脂质体表面修饰成为主动靶向,制备成合适的前体药物,改善药物的分配行为;进一步阐明脂质体作用机理和临床疗效等方面。大量报道的中药提物有效成分脂质体中,仅紫杉醇脂质体一个制剂上市,灯盏花素、和厚朴酚、紫杉醇、羟基喜树碱、长春新碱五种脂质体制剂在进行临床研究。
4 脂质体转化研究的关键问题
4.1 脂质体实验室研究到临床的转化 新药研发是一个时限性很强、复杂而又高度规范化的过程,包括一系列的临床研究,近年因为研发费用的上涨和Ⅲ期临床高达45%的失败率,使新药研发成本不断上升,产出却越来越少,一个药物从研发到应用到人群中产生流行病学效果需要12~25年的时间。[17]2013年1月美国Celsion公司宣布其研发的热敏脂质体包裹阿霉素的产品ThermoDox,三期临床试验失败,给公司带来巨大损失。在此之前前列腺素E1脂质体三期临床也宣告失败,可见一个药物从实验室到临床运用需要经历一个漫长的过程,期间需要大量的资金投入,而结果却往往不尽如人意。这是很多研究停留在实验室,没有进入临床的重要原因之一。
根据CFDA数据库查询国内脂质体临床研究情况,对数据进行整理统计,目前共有34种脂质体药物进行临床研究,包括盐酸多柔比星脂质体注射液和注射用两性霉素B脂质体等已上市的脂质体药物;灯盏花素前体脂质体胶囊等中药提取物脂质体和制备脂质体用脂质等脂质体药物和辅料。但是与脂质体众多热门研究方向和大量的文献报道量相比,进入临床研究的数量明显不足。药物的临床研究是保证上市产品的“安全、有效”,保障人民的用药安全的关键之一。如果脂质体药物研究停留在实验室的制备和动物实验中,仅仅具有一定的学术价值,将更多脂质体药物实验室研究转化进入临床研究,才能发挥脂质体药物的优势,获得更多优良的脂质体药物。
4.2 脂质体从实验室研究到工业生产的转化
4.2.1 脂质体制备工艺因素控制及工业化 脂质体制剂制备复杂,关键是磷脂的水化、粒径的控制及药物的装载。在生产过程中常用有机溶剂溶解磷脂材料,故在质量控制中必然需要考虑有机溶剂残留的控制;脂质体的粒径会显著影响其在体内行为,进而影响脂质体药物的疗效和毒性,粒径的控制是制备的关键因素之一;脂质体多为针剂,灭菌方法的可靠性和制剂稳定性是其重要的因素;由于游离药物的不良反应,脂质体的包封率、载药量和渗漏率也是关键控制指标,因此对生产过程中的影响因素进行严格控制,才能保证脂质体的安全有效。近年来越来越多文献报道对包封率、载药量和稳定性提高等进行报道[18-19],同时有机溶剂残留,渗漏率和粒径等的控制也在逐步完善,但是这些都仅限于实验室小试,进行工业化放大生产却非常困难。实验室制备脂质体的常用的薄膜法、乳化法、复乳法、pH梯度法、硫酸铵梯度法等方法[20-21],有些工艺无法满足产业化的需求,如传统的薄膜分散法。因此适合工业生产的工艺是脂质体运用受到的限制之一。
4.2.2 脂质体制备用辅料的研究 脂质是脂质体形成双分子层结构原材料,是脂质体制备的重要辅料。脂质主要来源于植物卵磷脂和动物卵磷脂,其生产首先要进行脱胶,以尽量降低磷脂含量而避免进一步精制出现问题。然后进一步精制,使其微生物指标合格。经过脱胶和精制的卵磷脂其组成随原料来源的不同而变化较大。即使同样是大豆卵磷脂,大豆种类、地理区域、气候、储存和加工过程对卵磷脂的质量也有非常显著的影响。由于卵磷脂组成不同,决定了其最终的应用功能的不同,因此有必要对不同质量的卵磷脂粗品混合以得到标准化(指最终组成一致,功能统一)的产品[22]。不同批次之间脂质的差异以脂质自身的稳定性,为脂质体及其辅料的研究和生产带来困难。然而不同的加工过程可以得到组成和功能各不相同的磷脂,为脂质体研究带来多样性,可以满足不同用途的需要,但是最终使用者需要了解和掌握这些产品的不同性质以更好地使用。随着长循环脂质体、热敏脂质体等[23-24]新型脂质体的出现,对辅料的结构修饰和改性,也成为脂质体辅料研究的重点方向。目前国内生产使用的辅料全为进口,国家食品药品监督管理局数据库显示,目前国内仅有两个制备脂质体用脂质在进行研究。脂质体制备所需的辅料短缺,增加了其产业化的成本。
4.2.3 脂质体制备用装备问题研究 制药工艺是药物生产过程的核心,而制药装备则是实现其核心的有力工具,只有先进的装备与生产工艺对接好,才能使工艺条件得以顺利实现,并制造出优质的产品[25]。目前脂质体实验室小试到中试到大生产方法-工艺-设备的不配套、不适应,实验室研究的制备使用的装备与工业生产的严重脱节,从而造成实验室制备出的脂质体无法实现工业化。脂质体制备过程中常用高压均质对粒径进行控制,然而国内医药行业使用的超高压匀质机几乎全部来源于进口,主要是因为国产高压均质机的核心部件高压均质腔无法达到行业所需的技术要求。然而使用高压均质机可能会导致产品中带有惰性金属粒子,从而引起不良发应。如2010年FDA因第一代碰撞型均质机使产品中可能含有惰性金属颗粒物质而发布公告,在全美召回11批丁酸氯维地平注射用乳剂。因此研制适合脂质体研制和生产可行的装备,与脂质体生产工艺相匹配,才能更好的将脂质体研究成果转化到实际生产。
5 小结
脂质体作为一种新型制剂,其高度靶向性能提高药物治疗指数、降低药物的不良反应,在肿瘤治疗、基因工程、心血管疾病、疾病诊断及中药新剂型等方面的巨大潜力,使其越来越受到人们的关注。目前我国对脂质体研究高额的投入,得出数量可观的论文和专利,但是上市能够用于临床使用的产品却很少。脂质体转化的难题在于其研究成果难以实现工业化生产。实验室小试与大生产工艺和设备不配套,其扩大生产后有机溶剂的残留、批次与批次之间的粒径差异的控制等重大问题,导致很多研究停留在实验室阶段,难以实现产业化。脂质体制剂技术的规模化生产、稳定性问题及脂质体有些给药途径的作用机制和转运途径还有待深入的研究,随着新型脂质体的研究与开发,这些问题正逐步解决[26]。
中药是新药开发的热点领域,将具有助溶和靶向等作用的脂质体新剂型与以天然绿色植物为来源的中药结合起来,解决部分中药提取物难溶等问题,突破了中药产品大多以传统剂型为主的现状,为中药的新药开发提供了一种新的发展参考模式,带来了新的发展前景与发展思路。目前已有中药提取单体脂质体制剂上市,为中药脂质体的研究成果转化开辟了先路,为更多中药脂质体的研究转化带来经验。临床试验设计、市场需求以及生产过程的适应性问题是影响新药研发的关键因素[27],从脂质体的转化研究可知我国制药业从科研成果到实际产品的转化能力不强,科研与生产和市场需求存在巨大的鸿沟。解决他们之间的鸿沟,在他们之间架起桥梁,这正是转化医学的目的[28-29]。通过对基础研究成果的利用,将其转化为新的药品、设备或对患者治疗的新方案,这并没有结束,转化成功是下一个研究的开始[30],将成功转化的药品产业化经验返回实验室指导和加快药品的继续转化,转化医学就是要建立这样一个双通的道路。将转化医学的理念引入到新药研发的每个阶段[31],从基础研究开始,注重研究成果产业化,科学地利用获得的有效信息,降低研发成本和缩短研究时间,提高研发效率和速度,使更多的研究成果转化成为临床可用的产品。
[1]崔福德.药剂学[M].7版.北京:人民卫生出版社,2011:402-413.
[2]Tyagi P,Wu PC,Chancellor M,et al.Recent advances in intravesical drug/gene delivery[J].Mol Pharm,2006,3(4):369-79.
[3]Carvalho B,Roland LM,Chu LF,et al.Single-dose,extended-release epidural morphine(DepoDur)compared to conventional epidural morphine for post-cesarean pain[J].Anesth Analg,2007,105(1):176-183.
[4]Ando K,Mori K,Corradini N,et al.Mifamurtide for the treatment of nonmetastatic osteosarcoma[J].Expert Opin Pharmacother,2011,12(2):285-292.
[5]邓杰英.脂质体技术[M].2版.北京:人民卫生出版社,2007:141-178.
[6]Lean ME,Mann JI,Hoek JA,et al.Translational research[J].BMJ,2008,337:a863.
[7]Bangham AD,Standish MM,Watkins JC.Diffusion of univalent ionsacross the lamella of swollen phospholipids[J].Journal of Molecular Biology,1965,13:238-252.
[8]Gregoriadis G,Leathwood PD,Ryman B.E.Enzyme entrapment in liposomes[J].FEBS Letter,1971,14(2):95-99.
[9]Lasic D.D.Novel applications of liposomes[J].Trends in Biotechnology,1998(16):307-321.
[10]Lasic D.D.Recent developments in medical applications of liposomes:sterically stabilized liposomes in cancer therapy and gene delivery in vivo[J].Journal of Controlled Release,1997(48):203-222.
[11]Liu F,Huang L.Development of non-viral vectors for systemic gene delivery[J].Journal of Controlled Release,2002(78):259-266.
[12]Kabanov AV,Lemieux P,Vinogradov S,et al.Pluronic block copolymers: novel functional molecules for gene therapy[J].Advanced Drug Delivery Reviews,2002(54):223-233.
[13]陆彬.药物新剂型与新技术[M].2版.北京:人民卫生出版社,2005:147-152.
[14]Barenholz Y,Haran G.Method of amphiphatic drug loading in liposomes by ammonium ion gradient[P].US 5,316,771,1994:16p.
[15]郭良玉,杨旭杰.基于聚类分析的中药复方专利年度发展状况研究[J].中草药,2012,43(10):2083-2088.
[16]张晶晶,方芸,谈恒山,等.中药脂质体的制备及应用[J].南京中医药大学学报,2006,22(3):202-204.
[17]Merlo Pich E.Understanding pharmacology in humans:PhaseⅠand PhaseⅡ(date generation)[J].Curr Opin Pharmacol,2011,11(5):557-562.
[18]杨涛,金大德,崔福德.紫杉醇脂质体药物含量及包封率的测定[J].药物分析杂志,2008,28(2):231-234.
[19]王梅,高晓黎.新型前体脂质体载药及影响因素考察[J].药学学报,2006,41(12):1204-1207.
[20]王振中,陈俊,徐连明,等.pH梯度法制备澳洲茄边碱脂质体[J].世界科学技术-中医药现代化,2011,13(6):1103-1106.
[21]刘陶世,蔡宝昌,赵新慧,等.硫酸铵梯度法结合微滤膜挤出制备马钱子碱脂质体的研究[J].中成药,2005,27(11):1247-1250.
[22]邓杰英.脂质体技术[M].2版.北京:人民卫生出版社,2007:10-12.
[23]李翔,张婧,王东凯,等.叶酸受体靶向两亲性嵌段共聚物修饰多烯紫杉醇脂质体的制备及体外性质考察[J].药学学报,2012,47(9):1219-1226.
[24]吴燕,张福成,吴诚,等.盐酸表阿霉素长循环热敏脂质体大鼠药代动力学考察[J].药学学报,2010,45(3):365-370.
[25]杨明,伍振峰,王雅琪,等.中药制药装备技术升级的政策、现状与途径分析[J].中草药,2013,44(3):247-252.
[26]周荣丽.药用脂质体研究近况[J].中国医院药学杂志,2008,28(20):1786-1788.
[27]杨明,伍振峰,岳鹏飞,等.三维导向转换模式在新药研究开发中的应用[J].中草药,2012,43(3):417-421.
[28]Ledford H.Translational research:the full cycle[J].Nature,2008,453:843-845.
[29]Finkelstein SE,Heimann DM,KIebanoff CA,et al.Bedside to bench and back again:how animal models are guiding the development of new immunotherapies for cancer[J].J Leukoc Biol,2004,76:333-337.
[30]Woof SH.The meaning of translational research and why it matters[J].JAMA,2008,299(2):211-213.
[31]刘昌孝.转换医学在新药研究开发中的应用[J].现代药物与临床,2010,25(5):321-326.
(2015-02-02收稿 责任编辑:洪志强)
Analysis on the Transformation and Application of Liposome Technology and Key Issues
Ke Gang1, Wu Zhenfeng1,2, Yang Ming1,2, Ren Guilin2, Huang Jumin1, Hu Pengyi1, Wang Saijun1
(1KeyLaboratoryofModernPreparationofTCM,MinistryofEducation,JiangxiUniversityofTraditionalChineseMedicine,Nanchang330004,China; 2ChengduUniversityofTraditionalChineseMedicine,Chengdu610075,China)
Objective:To reveal the status of transforming liposome preparations into application. Methods: We analyzed research programs funded by the National Natural Science Foundation (NNSF) on liposome technology, pertinent patents in the State Intellectual Property Office (SIPO) database, and pertinent research papers published. Results: We have seen some issues during our research, eg. inadequate transformation from basic research to application. Conclusion: Our proposal is liposome research should be take more of industrial production into consideration under the guidance of the translational medicine, put more resource on key issues of liposome transformation, in order to speed up the transformation from basic research into industrial production.
Liposome; Basic research; Exploratory development; Translational medicine
江西省教育厅青年科学基金项目(编号:81173565);江西省卫生厅中医药科研基金课题(编号:2011A138)
杨明(1962—),教授,博士生导师,研究方向:中药新剂型、新技术、新工艺研究,Tel/Fax:(0791)87118658,E-mail:yangming16@126.com;伍振峰(1982—),讲师,研究方向:中药新剂型与新技术/中药制药装备研究,Tel/Fax:(0791)87118658,E-mail:zfwu527@163.com
R944.9
A
10.3969/j.issn.1673-7202.2015.03.007
作者介绍:柯刚(1990—),男,硕士研究生,研究方向中药新剂型与新技术研究,Tel:(0791)87118108,E-mail:kg_rgl@126.com

