柠檬酸插层MgAl水滑石对水溶液中 Zn2+的吸附性能
申延明,张 僖,赵晓蕾,刘东斌,樊丽辉,李士凤
(沈阳化工大学 化学工程学院,沈阳 110142)
含Zn2+废水主要源于电镀、采矿、冶炼及化工等行业,Zn2+排入环境将造成土壤和地下水污染,进而对人体健康产生威胁[1-2]。在众多的处理方法中,吸附法具有高效、节能、可循环、利用、环保等特点,是一种成熟的、简单易行的水处理方法,特别适于水量大、污染物浓度低的废水[3]。天然矿物、纳米材料、农副产品、工业废弃物、生物材料等多种材料被开发为吸附剂[4-8]。但是开发廉价、高效率、无污染、可再次利用的吸附剂仍是重金属离子吸附研究的主要方 向[9]。
水滑石作为一种层状双金属氢氧化物(Layered double hydroxides,LDHs),层板是由带正电荷的二价 或三价金属离子构成的八面体相互连接而组成,表面富含OH-,而层间由具有可交换的阴离子组成[10]。由于这种特殊的结构形式,使得LDHs材料具有很强的吸附性能以及阴离子交换能力,使得其在重金属吸附上展现出良好的应用前景[11-12]。水滑石对重金属的吸附主要通过沉淀、表面吸附、同构取代以及层间阴离子的螯合作用实现的[12]。ZHAO等[13]采用CO32-插层的Mg-Al LDHs吸附溶液中的Pb2+,结果表明:Pb2+能够快速地被吸附,30 ℃的吸附容量可达66.16 mg/g。臧运波等[14]研究Cr6+在带结构正电荷的Mg-Al LDHs上的吸附性能,结果显示该类水滑石对Cr6+有很强的吸附能力,饱和吸附量达105 mg/g。如果将有机螯合离子引入水滑石层间,吸附能力会大大提高。EDTA是常用的螯合剂,将EDTA离子插入水滑石层间,利用EDTA对重金属离子的螯合作用可以显著提高对重金属的吸附率[15-18]。但是,EDTA不易被降解,易造成污染。而相比来说,柠檬酸、酒石酸、马来酸、谷氨酸等有机酸易被降解,来源广泛,且同样具有螯合能力[19],有机酸插层水滑石具有更好的应用前景[20-21]。
鉴于有机酸插层水滑石高的重金属离子吸附能力,本文作者制备柠檬酸插层MgAl水滑石吸附剂,考察其对溶液中的Zn2+的吸附性能以及吸附的热力学和动力学特性。
1 实验
1.1 吸附剂的制备
按照Mg和Al摩尔比为2:1配制Mg、Al混合硝酸盐溶液A,按照NaOH和Na2CO3的摩尔比为2:1配制混合碱溶液B。将A、B溶液搅拌下同时缓慢滴加至300 mL去离子水中,控制滴加速度以保持pH值在9~10,滴加完毕后,在60 ℃晶化12 h,离心、洗涤、过滤、经80 ℃干燥后,制得CO32-插层水滑石,记为MgAl-CO3LDHs,作为前体待用。
按照柠檬酸与前趋体质量比为0.40:1称取柠檬酸溶于乙二醇溶液,用0.1 mol/L的NaOH调节pH为4.5左右,投入定量的水滑石前体,用柠檬酸调节pH在4~5,经150 ℃的油浴中晶化5 h后,离心、抽滤、洗涤、经80 ℃真空干燥后,制得柠檬酸插层水滑石,记为MgAl-CA LDHs。
1.2 吸附剂的表征
采用Bruker D8 Advance型X射线粉末衍射仪表征样品的晶体结构,加速电压为40 kV,电流为30 mA,Cu靶Kα射线,扫描范围为3°~70°。采用美国Nicolet公司生产的NEXUS470型傅立叶变换红外吸收光谱仪测定样品的结构特征,KBr压片,扫描范围为400~ 4000 cm-1。采用日本JEOL公司生产的JSM-6360LV扫描电镜进行SEM分析,加速电压为10 kV。采用北京金埃谱科技有限公司生产的V-sorb 2800P比表面积及孔径分析仪分析样品的比表面积及孔径。
1.3 吸附实验
按照实验设计的浓度配置Zn(NO3)2溶液,取200 mL放入烧瓶中,投入定量的水滑石,在一定温度下恒温磁力水浴锅中恒温搅拌,同时计时,定时取样,离心分离吸附剂后取上层清液,采用双硫腙分光光度法测定Zn2+浓度[22]。Zn2+的吸附率(η)、单位质量吸附剂上的瞬时吸附量(Qt,mg/g)及平衡吸附量(Qe,mg/g)分别按式(1)~(3)计算:

式中:ρ0、ρt和ρe分别为起始溶液、吸附时间t 以及吸附平衡时溶液中Zn2+浓度,mg/L;V为溶液体积,mL;m为吸附剂质量,g。
2 结果与讨论
2.1 吸附剂的表征
图1所示为MgAl-CO3LDHs及MgAl-CA LDHs的XRD谱。从图1中可以看出,衍射峰呈现良好的倍数关系,具有水滑石的特征衍射峰。峰型尖锐,强度高,说明LDHs晶相单一,结晶度较高[23]。由(003)晶面的衍射峰位置可以反映层板的间距,可以发现柠檬酸离子插入层间替代CO32-后,(003)衍射峰的位置向左发生较大位移,层间距加大[24]。
图2所示为不同样品的IR谱。图2的IR谱图中3440 cm-1附近的吸收峰对应于层间水和层板羟基的伸缩振动峰,400~800 cm-1范围内归属于层板骨架的吸收峰。主要的特征峰变化体现在1000~2000 cm-1范围。MgAl-CO3LDHs谱中CO32-特征峰出现在1384 cm-1处,而1640 cm-1处的吸收峰归属于OH-振动峰。柠檬酸插入水滑石层间后,MgAl-CA LDHs谱图中1616和1361 cm-1处的吸收峰应归属于柠檬酸根中羧酸根离子的不对称和对称伸缩振动吸收峰,同柠檬酸 中的羧酸根离子的振动峰相比,发生了蓝移,表明层间插入的柠檬酸根离子与层板存在着一定的键合力。
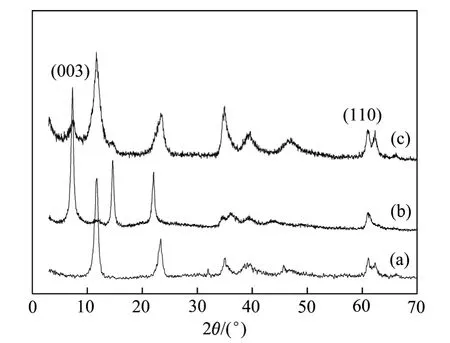
图1 不同样品的XRD谱 Fig.1 XRD patterns of different samples:(a) MgAl-CO3 LDHs; (b) MgAl-CA LDHs; (c) Zn-adsorbed LDHs
图3 所示为MgAl-CA LDHs的TG-DTA曲线。由图3可知,MgAl-CA LDHs的热分解主要有3个阶段,200 ℃以前,主要是脱除表面吸附的水以及层间弱吸附的水,质量损失率约为11%;200~245 ℃之间的吸收峰应为层间与柠檬酸结合水的脱除,质量损失率约为5%;245 ℃之后强的放热峰是由于插入层间的大量有机物柠檬酸根在空气中受热氧化分解燃烧所造成的,质量损失率约为37%。柠檬酸的分解温度在200 ℃以下,而TG-DTA结果表明:MgAl-CA LDHs的分解温度超过245 ℃,说明柠檬酸根进入LDHs层间后,由于层间客体柠檬酸根与主体LDHs层板之间存在相互作用,使柠檬酸根的热稳定性得到提高[23],这也说明了柠檬酸根成功地进入了LDHs层间。

图3 MgAl-CA LDHs的TG-DTA曲线 Fig.3 TG-DTA curves of MgAl-CA LDHs
图4 所示为MgAl-CA LDHs吸附前后的SEM像。由图4可以看出,MgAl-CA LDHs呈现片层结构,但是各片层相互堆积。比表面积测试结果显示该材料的比表面积为74.13 m2/g,孔体积为0.43 cm3/g,平均孔径为22.59 nm,较大的比表面积可以提供丰富的吸附中心,利于Zn2+的吸附,而适宜的孔径又保障了Zn2+在吸附剂孔内扩散,到达吸附中心。
2.2 吸附性能测试
2.2.1 水滑石投加量对Zn2+吸附率的影响
水滑石投加量对吸附率的影响如图5(a)所示。实验条件如下:25 ℃,Zn2+初始浓度为100 mg/L,溶液pH值保持在6左右。
由图5(a)可以看出,在最初的60 min内,70%以上平衡吸附量的Zn2+能够被MgAl-CA LDHs吸附,随着吸附时间的增加,吸附率缓慢增加至平衡值。同时,可以看出,随着吸附剂投加量的增加,吸附率逐渐增加,这是由于吸附剂的增加提供了更多的吸附位,吸附率越高[15]。但是单位质量吸附剂上Zn2+的平衡吸附量(Qe)逐渐减低(见图5(b)),这是由于吸附剂量的增加增加了单位吸附剂上的吸附位,但是投入过多的吸附剂会相互聚集,致使表面吸附位降低,Zn2+吸附率反而下降。兼顾考虑吸附率与单位质量吸附剂的吸附量,MgAl-CA LDHs投加量以2~3 g/L为宜。
2.2.2 Zn2+初始浓度对吸附率的影响
在25 ℃的条件下,加入MgAl-CA LDHs为2 g/L,针对pH为6,初始浓度在10~200 mg/L的溶液探讨Zn2+初始浓度对吸附率影响,其结果如图6(a)所示。

图6 Zn2+初始浓度对吸附率及平衡吸附量的影响 Fig.6 Effect of initial Zn2+ concentration on adsorption rate(a) and equilibrium adsorption amount(b)
由图6(a)可以看出,随着溶液中起始Zn2+浓度的增加,吸附率逐渐减低,而单位吸附剂的平衡吸附量逐渐增加(见图6(b))。溶液中Zn2+浓度越大,吸附推动力越大,单位质量吸附剂上的吸附量越大,但是在高浓度Zn2+的情况下,吸附剂表面的吸附中心相对较少,致使吸附率降低。当Zn2+浓度由10 mg/L增加至80 mg/L时,吸附率由96%降至65%,Qe由4.84 mg/g增加至26.03 mg/g。当Zn2+浓度大于80 mg/L,Qe增加缓慢,基本趋于定值。由实验结果得出,MgAl-CA LDHs吸附剂以处理Zn2+浓度不超过80 mg/L的溶液为宜。
2.2.3 初始pH对Zn2+吸附率的影响
在吸附温度为25 ℃,Zn2+溶液初始浓度为100 mg/L,水滑石投量为2 g/L,初始pH对吸附率的影响如图7所示。由图7可以看出,随着pH值的增加,吸附率逐渐增加,至pH为7时达到最大值,继续增加pH值,吸附率反而下降。这一结果主要是由于pH较低时,溶液呈酸性,溶液中有较多的H+与Zn2+竞争吸附到吸附剂的表面,pH值增加,H+浓度降低,因而吸附率增加。但是,当pH值过高,溶液中的Zn2+可能生成Zn(OH)2沉淀附着在水滑石表面,造成Zn2+吸附率下降。由Zn(OH)2的Ksp=6.8×10-17[25]可以推算出实验体系中Zn2+形成Zn(OH)2沉淀的pH值约为7,由此得出MgAl-CA LDHs吸附剂在弱酸性下使用为宜。
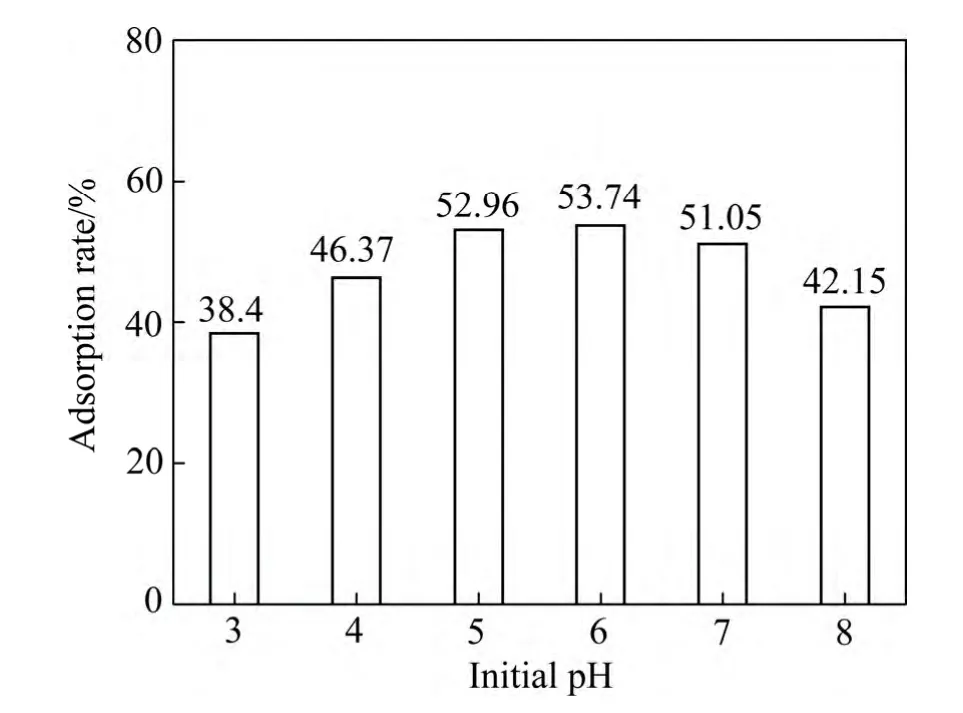
图7 初始pH对吸附率的影响 Fig.7 Effect of pH on adsorption rate
2.2.4 吸附温度对吸附率的影响
在初始浓度为100 mg/L的Zn2+溶液中加入2 g/L的MgAl-CA LDHs,保持pH为6,在25、30、40、50 ℃测试吸附率随温度的变化,其结果如图8所示。由图8可看出,吸附温度越高,吸附率越大,表明高温有利于Zn2+的吸附。
2.3 动力学研究
对于金属离子吸附过程一般符合一级和二级动力学特征[26],动力学方程可以表示为

图8 温度对吸附率的影响 Fig.8 Effect of temperature on Zn2+ adsorption rate
一级动力学方程:

二级动力学方程:

式中:kl为一级动力学吸附速率常数,min-1;k2为二级吸附速率常数,g/(mg·min)。一级、二级动力学对不同温度下的吸附数据的拟合结果如表1所列。为了评价拟合结果的优劣,引入参数归一化标准差(Normalized standard deviation,NSD)[27]:

式中:Qexp、Qcal是实验测量值和按模型计算的相应值;N为实验组数。
考虑到动力学方程主要受吸附前期的影响较大,本文作者针对180 min以前的数据进行动力学方程的拟合,其结果如图9所示。拟合的动力学参数列于表1中。从表1的结果准二级动力学模型具有较高的R2和较低的标准方差(SN),更好地描述MgAl-CA LDHs吸附Zn2+的过程。同时,二级动力学中的k2值随着温度的不断增加,表明随着温度的增加,吸附速率不断加快。
2.4 吸附热力学研究
2.4.1 吸附等温线
在吸附研究领域中,Langmuir吸附理论作为最基本的理论之一沿用至今[28]。Langmuir吸附模型假设吸附剂表面均一,各处吸附能相同,且吸附是单分子层,其表达式为

表1 动力学拟合参数 Table1 Kinetics fitting parameters

式中:Qe、Qmax分别为平衡吸附量和最大吸附量,mg/g;ρe为吸附平衡时溶液中Zn2+的浓度,mg/L;KL为Langmuir常数。
Freunlich 吸附等温式是一个常用的吸附等温线经验公式,它可以用来描述表面不均一或者活性位吸附粒子后相互作用的表面吸附过程。Freundlich吸附等温公式为

式中:KF为Freundlich常数;n为吸附强度,一般认为,0.1<1/n<0.5时,易于吸附;而当1/n>2时,难以吸附。
Redlich-Peterson (R-P)模型结合Langmiur和Freundlich模型而提出的较合理的经验模型,模型方程表示为

式中:A是与吸附量有关的常数;B是与吸附能力有关的经验常数;指数g为介于0和1之间的经验常数。
引入残差均方根误差Sr(Residual root mean square error,RMSE)及卡方检验(Chi-square test,χ2)两个统计参数评价吸附模型的拟合结果,分别定义为
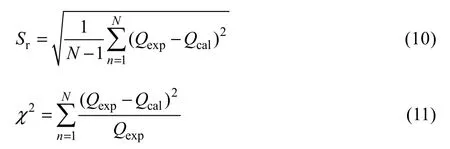
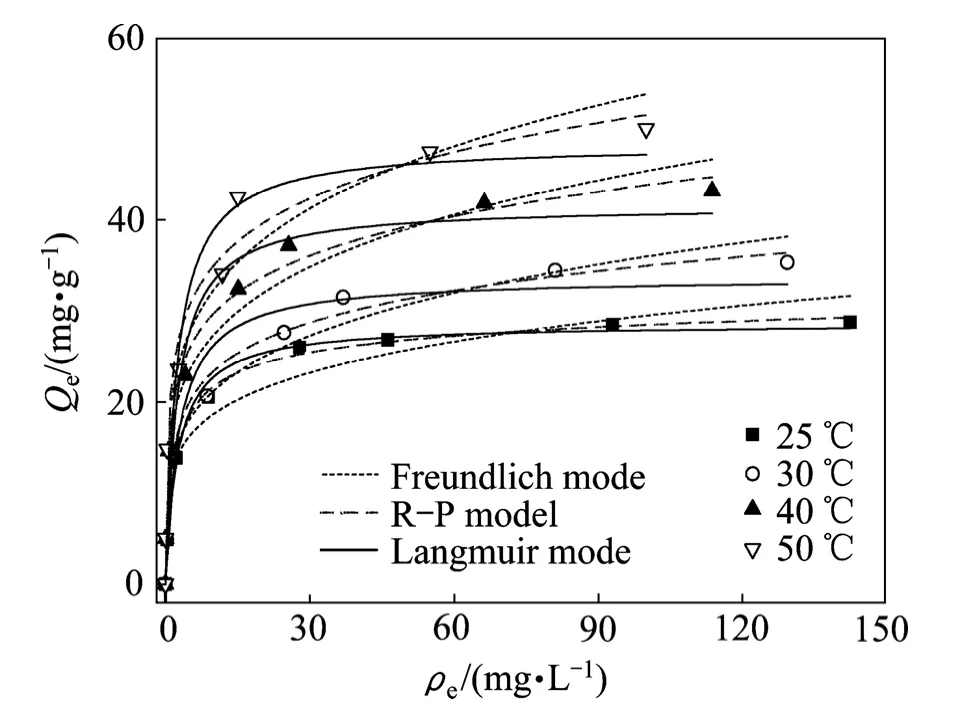
图10 不同温度下的吸附等温线 Fig.10 Adsorption isotherms at different temperatures
吸附等温线的拟合结果如图10所示。由表2发 现,Langmuir模型相对于Freundlich模型拟合结果较好,得出的最大吸附容量与实际平衡吸附容量相近,其理论吸附容量略大于实验时的平衡吸附量[29]。但是Langmuir模型均匀表面的假设似乎对于MgAl-CA LDHs吸附剂吸附Zn2+并不十分适用,由于柠檬酸离子插入MgAl LDHs层间后,MgAl-CA LDHs具有了不同的吸附中心,一是LDHs表面的OH-,另外还有层间柠檬酸离子,因此,结合Langmuir和Freundlich模型的R-P模型,更好地描述吸附情况。
2.4.2 吸附热力学参数
热力学参数ΔGΘ、ΔHΘ和ΔSΘ符合下列关系:

对于液-固吸附体系,ΔGΘ、ΔHΘ、ΔSΘ与固-液分配系数Kd之间存在下列关系[30]:

式中:vs、ve为活度系数,稀溶液中均取1。以ln(Qe/ρe)对Qe作图,令Qe→0,即可得到ln Kd。根据实验数据可求出25、30、40和50 ℃下的ln Kd值分别为3.88、3.89、4.82、4.97。再以1/T为横坐标,ln(Kd)为纵坐标作图,通过线性回归分析得到一条直线,由其斜率和和的值[31]。计算结果如表3所列。 截距可以求出

表2 吸附等温线的相关参数 Table2 Parameters of isotherms
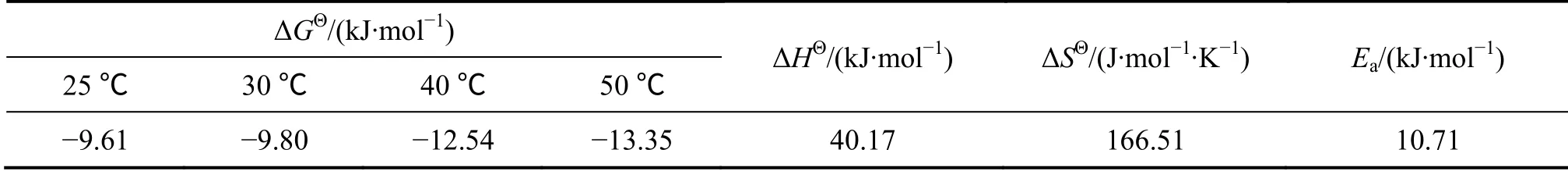
表3 热力学参数 Table3 Thermodynamics parameters
吸附活化能(Ea)反映了吸附速率随温度的变化关系,也能对吸附类型进行初步的判断[32]。吸附活化能Ea与温度存在下列关系:

以表1二级动力学的反应数率常数k2数据,以ln k2对1/T作图,通过直线的斜率求得Ea。
由表3中可知,ΔGΘ<0,说明MgAl-CA LDHs吸附Zn2+的过程是一个自发的过程。ΔHΘ>0,说明吸附为吸热反应,升高温度有利于反应的进行。一般来说,当吸附力为范德华力时,吸附热ΔHΘ为4~10 kJ/mol;当吸附力为氢键力时,ΔHΘ为40 kJ/mol左右;而吸附力为化学键力时,ΔHΘ大于60 kJ/mol[33]。实验得出ΔHΘ=40.17 kJ/mol,说明吸附力应为氢键力。ΔSΘ>0,表明吸附过程中熵增加的过程主要是由于吸附过程中伴随着Zn2+的脱附,从而使系统的熵变增加。
2.5 吸附机理
水滑石吸附溶液中的重金属离子主要通过表面沉淀、表面络合、同构替代以及螯合等反应实现[12]。首先,由图1的XRD谱可以看出,吸附Zn2+后的MgAl-CA LDHs仍保持水滑石的结构,但是出现了CO32-插层后的水滑石的衍射峰,这些CO32-离子是由于吸附过程中溶液吸附CO2所致。没有明显的其它物相衍射峰出现,表明吸附过程中并未形成其它的物相,这也说明吸附过程中并未发生表面沉淀的反应。其次,表4的EDX分析结果表明,吸附前Mg和Al摩尔比为2.04,而吸附后变为1.95,说明部分Mg2+在吸附的过程中发生了溶解,从层板上脱落[34],而吸附后,MgAl-CA LDHs的XRD谱中(110)晶面向高角度方向移动(见图1),表明层板上电荷密度降低,金属离子的间距加大[35],应为较大离子半径的Zn2+替代Mg2+造成的。XRD和EDX结果说明:层板上的Mg2+与Zn2+发生了同构替代。另外,水滑石表面富含OH-,这些OH-能够吸附溶液中的Zn2+形成配合物,吸附过程可以描述为[12]

此过程受pH值的影响,图7的结果表明了pH值影响吸附效率,随着pH值的增加,吸附效率随之增加,但pH值过高也会造成形成Zn(OH)2沉淀附着在水滑石表面,阻止了水滑石进一步吸附溶液中的Zn2+。最后,对比MgAl-CA LDHs吸附前后的IR谱发现,1616 cm-1的柠檬酸根中羧酸根离子的振动峰移动到1610 cm-1处,表明羧酸根离子与Zn2+形成了配合物,说明层间的柠檬酸离子通过配合作用吸附了溶液中的Zn2+。
综上所述,MgAl-CA LDHs吸附水溶液中Zn2+主要通过同构替代、表面络合以及层间柠檬酸的螯合作用实现的。
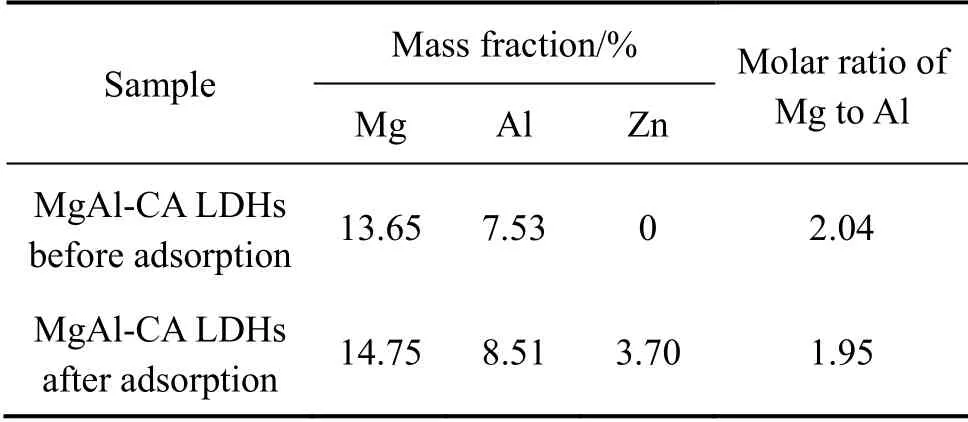
表4 MgAl-CA LDHs吸附前后EDX分析结果 Table4 EDX analysis results of MgAl-CA LDHs before and after adsorption
3 结论
1) 以碳酸根插层的MgAl水滑石为前体,采用离子交换法制备柠檬酸插层MgAl水滑石。由于层间插入了柠檬酸离子,柠檬酸柱撑MgAl水滑石对于溶液中Zn2+有良好的吸附能力。
2) 通过探讨水滑石投加量、Zn2+初始浓度、吸附pH以及吸附温度对Zn2+吸附率的影响得出,水滑石投加量增加,Zn2+吸附率增加,但单位质量吸附剂的吸附量降低,水滑石投加量以2~3 g/L为宜;Zn2+初始浓度过大,Zn2+吸附率明显下降,Zn2+初始浓度不超过80 mg/L可以维持吸附率在60%以上;溶液中pH的变化会影响溶液中离子的存在状态,进而影响Zn2+的吸附,实验发现pH为5~6时,Zn2+吸附率较高;吸附温度的增加有利于提高Zn2+的吸附,说明吸附为吸热过程。
3) 动力学研究结果表明:吸附过程符合二级动力学特征,吸附活化能为10.71 kJ/mol。
4) 热力学研究结果表明:吸附等温线可用R-P方程描述,吸附为自发过程,且吸附过程为吸热过程。
[1] 王未君,耿存珍. 吸附材料处理重金属废水的研究进展[J]. 环境科技,2014,27(1):58-63.
WANG Wei-jun,GENG Cun-zhen. Removing heavy mental ions from wastewater using absorbent material:A review[J]. Environmental Science and Technology,2014,27(1):58-63.
[2] 周兰娟,荆国华,周作明. 超声场中活性炭上Zn2+的吸附/脱附[J]. 中国环境科学,2011,31(5):755-760.
ZHOU Lan-juan,JI Guo-hua,ZHOU Zuo-ming. Effect of ultrasound on adsorption and desorption of Zn2+on activated carbon[J]. China Environmental Science,2011,31(5):755-760.
[3] KURNIAWAN T A,CHANG Y S,LO W H,BABEL S. Physico-chemical treatment techniques for wastewater laden with heavy metals[J]. Chemical Engineering Journal,2006,118(1/2):83-98.
[4] SUD D,MAHAJAN G,KAUR M P. Agricultural waste material as potential adsorbent for sequestering heavy metal ions from aqueous solutions:A review[J]. Bioresource Technology,2008,99(14):6017-6027.
[5] 叶 玲,张敬阳. 蒙脱石的电动电位调控及其对重金属离子吸附性能的影响[J]. 矿物学报,2013,33(1):19-24.
YE Ling,ZHANG Jing-yang. Montmorillonite ζ-potential regulation and its adsorption capacity for heavy metal cations[J]. Acta Mineralogica Sinica,2013,33(1):19-24.
[6] AHMARUZZAMAN M. Industrial wastes as low-cost potential adsorbents for the treatment of wastewater laden with heavy metals[J]. Advances in Colloid and Interface Science,2011,166(1/2):36-59.
[7] 李青竹,覃文庆,柴立元,王庆伟. 巯基化改性麦糟对Zn(Ⅱ)的吸附特性[J]. 中国有色金属学报,2014,24(4):1076-1083.
LI Qing-zhu,ZHAO Wen-qing,CHAI Li-yuan,WANG Qing-wei. Adsorption characteristics of Zn(Ⅱ) on thiol-functionalized spent grain[J]. The Chinese Journal of Nonferrous Metals,2014,24(4):1076-1083.
[8] 李小燕,刘义保,花 明,李金轩,高 柏. 改性玉米芯吸附溶液中U(Ⅵ)的热力学特征[J]. 中国有色金属学报,2013,23(4):1168-1172.
LI Xiao-yan,LIU Yi-bao,HUA Ming,LI Jin-xuan,GAO Bai. Adsorption thermodynamic characteristics of U(Ⅵ) on modified corncob in aqueous solution[J]. The Chinese Journal of Nonferrous Metals,2013,23(4):1168-1172.
[9] 张 帆,李 菁,谭建华,王 波,黄 福. 吸附法处理重金属废水的研究进展[J]. 化工进展,2013,32(11):2749-2756.
ZHANG Fan,LI Jing,TAN Jian-hua,WANG Bo,HUANG Fu. Advance of the treatment of heavy metal wastewater by adsorption[J]. Chemical Industry and Engineering Progress,2013,32(11):2749-2756.
[10] CAVANI F,TRIFIRÒ F,VACCARI A. Hydrotalcite-type anionic clays:Preparation,properties and applications[J]. Catalysis Today,1991,11(2):173-301.
[11] 朱洪涛,马玉晶. 水滑石类材料在重金属废水治理中的应用进展[J]. 水处理技术,2011,37(8):11-14.
ZHU Hong-tao,MA Yu-jing. Progress in application of hydrotalcite-like materials in heavy metal wastewater treatment[J]. Technology of Water Treatment,2011,37(8):11-14.
[12] LIANG X,ZANG Y,Xu Y,TAN X,HOU W G,WANG L,SUN Y B. Sorption of metal cations on layered double hydroxides[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2013,433:122-131.
[13] ZHAO D,SHENG G,HU J,CHEN C L,WANG X K. Adsorption of Pb(Ⅱ) on Mg2Al layered double hydroxide[J]. Chemical Engineering Journal,2011,171(1):167-174.
[14] 臧运波,侯万国,王文兴. Cr(Ⅵ)在Mg-Al型类水滑石上的吸附-脱附性研究Ⅰ. 吸附性[J]. 化学学报,2007,65(9):773-778.
ZANG Yun-bo,HOU Wan-guo,WANG Wen-xing. Adsorption-desorption of chromium(Ⅵ) on Mg-Al hydrotalcite-like compounds part Ⅰ. Adsorption[J]. Acta Chimica Sinica,2007,65(9):773-778.
[15] 林 楠,沙 宇. 改性镁铝水滑石的合成及其对水中Cu2+的去除性能研究[J]. 水处理技术,2008,34(9):30-34.
LIN Nan,SHA Yu. The synthesis of mg-al layered double hydroxide intercalated with edta anion and application to the adsorption of Cu2+from an aqueous solution[J]. Technology of Water Treatment,2008. 34(9):30-34.
[16] 申延明,刘东斌,李长龙,李天舒,方晓杰. MgAl-EDTA柱撑水滑石的制备及其应用[J]. 化学通报,2010,73(10):905-909.
SHEN Yan-ming,LIU Dong-bin,LI Chang-long,LI Tian-shu,FANG Xiao-jie. Synthesis and application of EDTA pillared layered double hydroxides[J]. Chemistry,2010,73(10):905-909.
[17] 朱洪涛,马玉晶. EDTA插层水滑石的合成及其对Cd2+的去除性能研究[J]. 现代化工,2011,31(2):58-60.
ZHU Hong-tao,MA Yu-jing. Synthesis of EDTA intercalated hydrotalcite and application in removal of Cd2+[J]. Modern Chemical Industry,2011,31(2):58-60.
[18] 王军涛,徐 芳. MgZnAl-EDTA柱撑水滑石的制备及其对Pb(Ⅱ)的吸附[J]. 化学研究与应用,2014,26(4):581-585.
WANG Jun-tao,XU Fang. Preparation of EDTA pillared MgZnAl LDHs and its adsorption of Pb(Ⅱ)[J]. Chemical Research and Application,2014,26(4):581-585.
[19] KAMEDA T,TAKEUCHI H,YOSHIOKA T. Hybrid inorganic/organic composites of Mg–Al layered double hydroxides intercalated with citrate,malate,and tartrate prepared by co-precipitation[J]. Materials Research Bulletin,2009,44(4):840-845.
[20] KAMEDA T,TAKEUCHI H,YOSHIOKA T. Uptake of heavy metal ions from aqueous solution using Mg-Al layered double hydroxides intercalated with citrate,malate,and tartrate[J]. Separation and Purification Technology,2008,62(2):330-336.
[21] 王 蕾,肖 鹏. 谷氨酸插层水滑石吸附水中铅离子[J]. 离子交换与吸附,2013,29(3):253-261.
WANG Lei,XIAO Peng. Removal of lead ion from aqueous solution using glutamate intercalated layereddouble hydroxide[J]. Ion Exchange and Adsorption,2013,29(3):253-261.
[22] GB-T 7472—1987. 水质-锌的测定-双硫腙分光光度法[S]. GB-T 7472—1987. Water quality-determination of zinc- spectrophotometric method with dithizone[S].
[23] 张 杰,李殿卿,任玲玲,EVANS D G,段 雪. 新原料路线共沉淀法组装超分子结构柠檬酸根插层水滑石[J]. 无机化学学报,2004,20(10):1208-1212.
ZHANG Jie,LI Dian-qing,REN Ling-ling,EVANS D G,DUAN Xue. Assembly of citrate-pillared LDHs with supermolecular structure[J]. Chinese Journal of Inorganic Chemistry,2004,20(10):1208-1212.
[24] 王剑峰,张亚非,郭宪吉. 柠檬酸柱撑水滑石的制备及结构表征[J]. 四川理工学院学报(自然科学版),2009,22(1):68-71.
WANG Jian-feng,ZHANG Ya-fei,GUO Xian-ji. Preparation and structrural characterization of citric acid-pillared hydrotalcites[J]. Journal of Sichuan University of Science and Engineering (Natural Science Edition),2009,22(1):68-71.
[25] 大连理工大学无机化学教研室. 无机化学[M]. 5版. 北京:高等教育出版社,2006.
Inorganic Chemistry Teaching and Research Section of Dalian University of Technology. Inorganic chemistry[M] 5th ed. Beijing:Higher Education Press,2006.
[26] SEN GUPTA S,BHATTACHARYYA K G. Kinetics of adsorption of metal ions on inorganic materials:A review[J]. Advances in Colloid and Interface Science,2011,162(1/2):39-58.
[27] HOSSAIN M A,NGO H H,GUO W S,NGUYEN T V. Palm oil fruit shells as biosorbent for copper removal from water and wastewater:Experiments and sorption models[J]. Bioresource Technology,2012,113:97-101.
[28] RANGABHASHIYAN S,ANU N,GIRI NANDAGOPAL M S,SELVARAJU N. Relevance of isotherm models in biosorption of pollutants by agricultural byproducts[J]. Journal of Environmental Chemical Engineering,2014,2(1):398-414.
[29] 陈 灿,王建龙. 酿酒酵母吸附Zn2+、Pb2+、Ag+、Cu2+的动力学特性研究[J]. 环境科学学报,2007,27(4):544-553.
CHEN Can,WANG Jian-long. Biosorption of heavy metal ions by a brewery's waste:kinetic and equilibrium[J]. Acta Scientiae Circumstantiae,2007,27(4):544-553.
[30] KHAN A A,SINGH R P. Adsorption thermodynamics of carbofuran on Sn(Ⅳ) arsenosilicate in H+,Na+and Ca2+forms[J]. Colloids and Surfaces,1987,24(1):33-42.
[31] 丁志江,宋来洲,贺 君,王帅杰. 聚丙烯酸一聚偏氟乙烯共混膜对Cu(Ⅱ)、Zn(Ⅱ)吸附性能的研究[J]. 离子交换与吸附,2009,25(4):327-337.
DING Zhi-jiang,SONG Lai-zhong,HE Jun,WANG Shuai-jie. Adsorption characteristics of Cu(Ⅱ) and Zn(Ⅱ) ions onto the polyacrylic acid-polyvinylidene fluoride blended membrane[J]. Ion Exchange and Adsorption,2009,25(4):327-337.
[32] 熊春华,姚彩萍. D113弱酸性树脂对锌(Ⅱ)的吸附性能[J]. 中国有色金属学报,2008,18(4):745-749.
XIONG Chun-hua,YAO Cai-ping. Sorption behavior of weak acid resin(D113) for Zinc(Ⅱ)[J]. The Chinese Journal of Nonferrous Metals,2008,18(4):745-749.
[33] QIU T,ZENG Y,YE C,TIAN H. Adsorption thermodynamics and kinetics of p-xylene on activated carbon[J]. Journal of Chemical and Engineering Data,2012,57(5):1551-1556.
[34] 张 伟,曾虹燕,杨永杰,刘鸣达. Mg-Al水滑石的改性机理和吸附性能[J]. 材料研究学报,2012,26(4):437-442.
ZHANG Wei,ZENG Hong-yan,YANG Yong-jie,LIU Ming-da. Modification mechanism of Mg-Al hydrotalcites and adsorption performance[J]. Chinese Journal of Materials Research,2012,26(4):437-442.
[35] 倪哲明,潘国祥,王力耕,方彩萍,李 丹. 二元类水滑石层板组成、结构与性能的理论研究[J]. 无机化学学报,2006,22(1):91-95.
NI Zhe-ming,PAN Guo-xiang,WANG Li-geng,FANG Cai-ping,LI Dan. Theoretical studies on layer composition,structure and properties of hydrotalcite[J]. Chinese Journal of Inorganic Chemistry,2006,22(1):91-95.

