次氯酸钠应用于南方地区供水管网二次加氯消毒的试验
钟 宁,游浩荣,余华章,吴晨光,周绮婷,叶 斌,江圣辉
(1.瀚蓝环境股份有限公司,广东佛山 528200;2.广东省城市水循环与水质安全保障技术企业重点实验室(产学研)培育基地,广东佛山 528200;3.哈尔滨工业大学城市水资源与水环境国家重点实验室,黑龙江哈尔滨 150090)
由于氯消毒具有对细菌灭活能力强和持续消毒能力等特点,自20世纪初,氯就开始被用于饮用水消毒,至今仍被大范围和大规模地应用。城市供水管网中维持一定的余氯浓度在一定程度上能保证水质,但氯消毒过程中会产生对人类健康有潜在威胁的卤代消毒副产物。《生活饮用水卫生标准》(GB 5749—2006)中规定,三氯甲烷不超过 0.06 mg/L,三溴甲烷不超过0.1 mg/L。新标准推动了科学研究者对氯消毒副产物的控制技术进行更多的研究[1]。
二次加氯能更高效地控制供水管网的余氯浓度,避免自来水出厂前投加过高浓度的消毒剂。与传统方式消毒相比,二次加氯具有下列优势:降低总投氯量;减少副产物形成的可能;管网余氯更均匀的分布;增加系统抵御和应对事故或蓄意污染物侵害的稳固性[2]。
次氯酸钠是一种高效、广谱的消毒剂,与液氯相比优势明显,便于贮存,消毒出水中三氯甲烷和卤乙酸含量均比液氯消毒低,除此之外其CODMn、TP和NH3-N的去除效果也更佳[3,4]。本文针对南方水质特点,使用次氯酸钠作为二次消毒剂,探索二次加氯对消毒剂的衰减以及消毒副产物的生成规律的影响并进行分析。
1 材料与方法
1.1 试验材料与仪器
主要化学试剂:次氯酸钠(溶液),四水合酒石酸钾钠,碘化汞,碘化钾,高锰酸钾,草酸钠,硫酸。
主要仪器:清时捷Q-CL501便携式余氯·二氧化氯五参数快速测定仪;Hach公司2100AN浊度仪;上海仪电科学仪器pHS-3B型pH计;岛津公司UV-2550紫外可见分光光度计;气相色谱仪(配ECD检测器);TOC分析仪。
1.2 试验用水
试验用水取自南方某城市某水厂的滤后水,使用蠕动泵投加消毒剂,通过调节蠕动泵的转速和投加时间来调节总投加量。该水厂夏季水源水情况:温度为 30~32℃,pH 值为 7.58~7.76,浊度为12.4 ~ 36.2 NTU ,CODMn为1.53 ~2.28 mg/L,氨氮浓度为0.12~0.21 mg/L。试验中所取滤后水的主要水质指标:温度为27~30℃,pH 值为7.49~7.65,CODMn为 0.69 ~ 0.99 mg/L,氨氮浓度为0.007~0.025 mg/L,TOC 浓度为0.683 ~0.840 mg/L。
1.3 试验装置与方法
试验反应器示意图如图1所示,由两段平行敷设的管径为100 mm的环形管路组成,每段管路总长约360 m,其中大部分埋于地下,管材分别为钢管(水泥砂浆衬里)和PE管。本装置建设于水厂中,可直接取滤后水或出厂水进行试验研究,能较好地模拟实际管网中水质的变化过程。

图1 动态模拟装置示意图Fig.1 Schematic Diagram of Dynamic Simulation Experiment Equipment
图2为测控PLC示意图。测控PLC可实时监测并采集部分管道中的水质数据,包括温度、压力、流速和余氯浓度,还能对变频器和阀门进行调控以改变管网的运行工况,或通过对投氯设备的控制、切换,调节不同消毒剂的投加量以模拟不同消毒方案。

图2 测控PLC示意图Fig.2 Schematic Diagram of Measure and Control PLC of Reactor
抽取滤后水进行试验,测定滤后水的pH值、浊度、CODMn、氨氮和TOC浓度。然后使用投氯设备定量投加次氯酸钠溶液调节不同的初始氯浓度,待水样余氯浓度衰减一定程度后再次投加次氯酸钠溶液进行二次消毒。运行过程中在不同的反应时间测定余氯和三氯甲烷浓度。各指标检测仪器及方法如下:氯采用DPD光度法测定(便携式余氯测定仪);三氯甲烷浓度采用气相色谱法测定(气相色谱仪,配ECD检测器);浊度采用光散射法测定(浊度仪);pH值采用玻璃电极法测定(精密pH计);CODMn采用酸性高锰酸钾法测定;氨氮浓度采用纳氏试剂分光光度法测定;TOC浓度采用燃烧氧化—非色散红外吸收法测定(TOC分析仪)。
2 结果与讨论
2.1 不同投加配比的影响
试验反应温度为28.5℃,四组试验总投氯量相当,初次投氯量和二次投氯量按一定的配比进行投加,其中二次加氯在余氯浓度为0.10 mg/L时进行,每隔一段时间提取一定量水样测定相关指标,从而考察不同的投加配比对余氯衰减及副产物生成情况的影响。对四组试验的余氯衰减曲线进行对数拟合计算,得出衰减常数kb和相关系数R2,结果如表1所示。
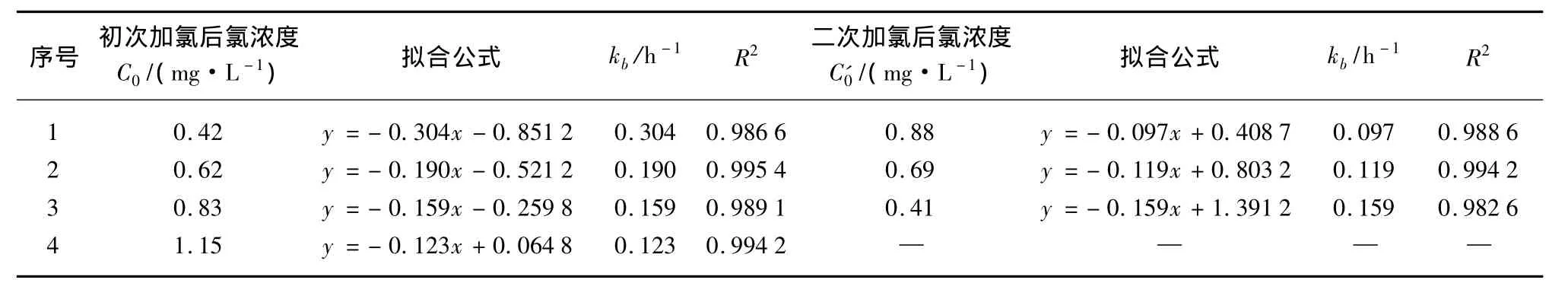
表1 钢管中不同投氯量下氯的衰减规律拟合结果Tab.1 Fitting Results of Residual Chlorine Decay with Different Dosages of Disinfectant in Steel Pipelines
图3为钢管中不同投氯量下氯的衰减规律。由图3可知,在总投氯量相当的情况下,进行二次加氯的试验中氯的衰减速率明显比只进行一次加氯的慢,其中初次加氯与二次加氯配比为1∶2(初次加氯0.42 mg/L;二次加氯0.88 mg/L)的试验中氯的衰减速率最慢。利用拟合得到的结果进行计算,四次试验氯消毒剂从初始投加到衰减至0.05 mg/L所耗时间t0.05分别为34.95、31.92、27.56 h 和 24.90 h,其中试验1最长,相对只进行一次加氯的长40.36%,说明二次加氯能明显降低氯的衰减速率,有利于氯消毒剂在管网中更持久地发挥消毒作用。另一方面,假设初始投氯量为0.42 mg/L,余氯衰减至0.10 mg/L时进行二次加氯使其浓度增加至0.69 mg/L,按表1所示拟合公式计算:22.55 h,得t0.05=t1+t2=27.32 h>24.90 h,而此方案总投氯量为1.01 mg/L,与一次性投加相比总投加量降低12.2%。
研究表明[5,6],初始氯浓度与氯的衰减速率呈负相关关系,因此二次加氯后氯浓度的升高会减缓其衰减速率,且二次加氯的比例越高,减缓效果则越明显。另一方面进行二次加氯时,水中部分有机物已与初始投加的氯完成反应,此时较低的有机物浓度也使得反应速率变缓。
图4为钢管中不同投氯量下三氯甲烷的生成规律。由图4可知,三氯甲烷的生成呈现先快后慢的趋势;初始三氯甲烷的生成量与初始投氯量呈明显的正相关关系;四组试验中三氯甲烷的生成总量相近。研究表明DBPs的生成量与投氯量、消毒副产物前驱物的浓度、氯化反应时间、温度和 pH值等因素有关[7,8]。本试验中总投氯量相近,被认为能较好反映前驱物浓度的TOC、UV254水平也相近,其余反应条件基本相同,因此三氯甲烷生成量差别不大。但是二次加氯能减缓三氯甲烷的形成,可以看出前1 000 min,进行二次加氯的试验的三氯甲烷浓度明显低于只进行一次加氯的,即二次加氯能明显降低上游节点的三氯甲烷浓度。

图4 钢管中不同投氯量下三氯甲烷的生成规律Fig.4 Trichloromethane Formation with Different Dosages of Disinfectant in Steel Pipelines
2.2 不同管材的影响
两套试验管道分别为钢管和PE管,两次试验总投氯量分别为1.18 mg/L和1.12 mg/L,每隔一
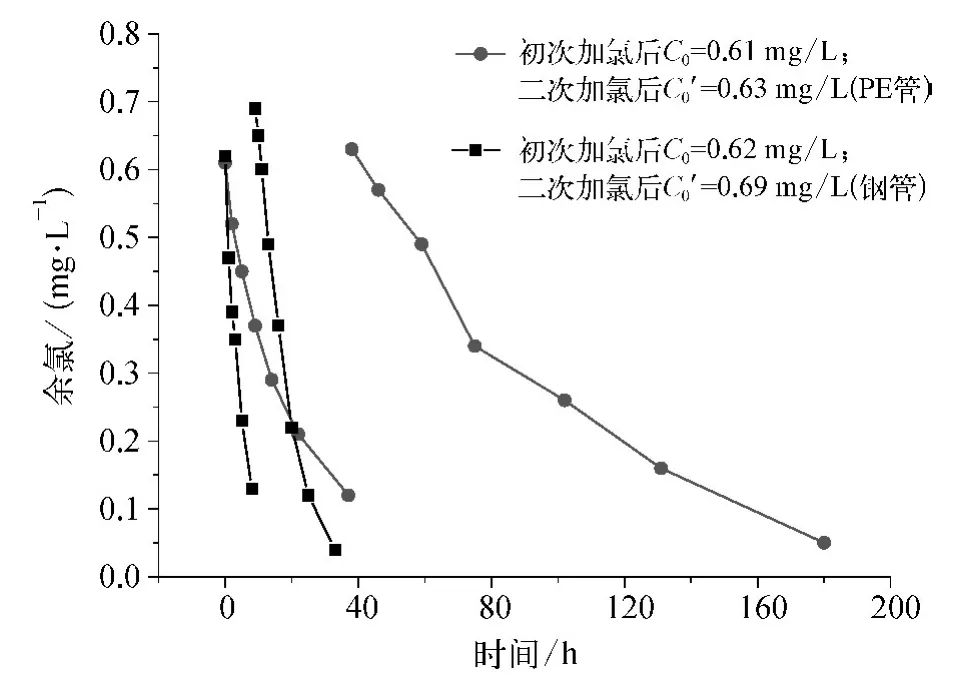
图5 不同管材中氯的衰减规律Fig.5 Residual Chlorine Decay in Different Pipe Material
由图5和图6可知,钢管中氯的衰减速率和三氯甲烷的生成速率均比PE管快得多。对两次试验的余氯衰减曲线进行对数拟合计算,得出衰减常数,结果如表2所示。
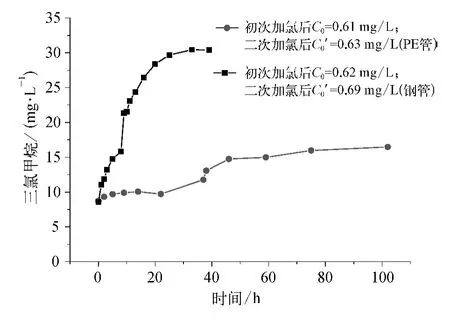
图6 不同管材中三氯甲烷的衰减规律Fig.6 Trichloromethane Formation in Different Pipe Material
由表2可知,钢管中氯的衰减速率约为PE管中的5倍。PE管的主要成分是聚乙烯,其化学性质稳定,不与水发生化学反应,耐多种化学介质的侵蚀,段时间提取一定量水样测定相关指标,考察不同的管材对余氯衰减及副产物的生成情况的影响,结果如图5、图6所示。而且无结垢层因此不易发生二次污染[9-10],试验中也看到三氯甲烷生成量相对钢管的要低。但是PE管也存在一些缺点:塑料在水中可能发生溶解反应而浸出化学物质,同时管道内发生的各种化学反应也有可能改变其聚合物及基质树脂分子,而使管道性质发生不可逆变化[11];其机械性和承压能力不如钢管,因此大管径的PE管应用受到限制;不宜明敷。

表2 不同管材中氯的衰减规律拟合结果Tab.2 Fitting Result of Residual Chlorine Decay in Different Pipe Material
3 结论
(1)二次加氯能明显降低氯的衰减速率,有利于氯消毒剂在管网中更持久地发挥消毒作用。试验中初次加氯与二次加氯配比为1∶2时,氯的衰减速率最慢,合适的二次加氯方案能使总投氯量降低12%以上。
(2)以不同配比进行二次加氯对三氯甲烷的生成总量影响不大,但相对只进行一次加氯能明显降低前16 h的三氯甲烷生成量;同时进行二次加氯能一定程度上降低总投氯量,即能减少消毒过程中三氯甲烷的生成。
(3)城市配水管网中氯在钢管(水泥砂浆衬里)中的衰减速率远大于在PE管中的衰减速率,前者约为后者的5倍;钢管中三氯甲烷的生成速率比PE管中的要大,相同投氯量和投加方式下前者生成量约为后者的2倍。
[1]鄂学礼,王丽,邢方潇.饮水消毒副产物及其标准研究进展[J].环境与健康杂志,2010,27(1):2-4.
[2]马力辉,刘遂庆,信昆仑.城市供水管网二次加氯研究进展[J].环境污染与防治,2006,28(9):693-697.
[3]李述茂,吴德礼.液氯和次氯酸钠对饮用水消毒效果的生产性试验研究[J].工业用水与废水,2011,42(2):14-17.
[4]张胜利,刘丹,曹臣.次氯酸钠氧化脱除废水中氨氮的研究[J].工业用水与废水,2009,40(3):23-26.
[5]Nicholas B H,Hua Fang,West J.R.Bulk decay of chlorine in water distribution systems[J].Journal of Water Resources Planning and Management,2003,129(1):78-81.
[6]钟丹.给水管网余氯衰减规律及影响因素研究[D].哈尔滨:哈尔滨工业大学,2010.
[7]Kampioti A A,Stephanou E G.Simultaneous determination of halogenated neutral and acidic disinfection by-products in drinking waterby closed-loop stripping extraction and capillary gas chromatography[J].Journal of Chromatography A,1999,857(1):217-229.
[8]Yang X,Shang C.Chlorination byproduct formation in the presence of humic acid,model nitrogenous organic compounds,ammonia,and bromide[J].Environmental Science & Technology,2004,38(19):4995-5001.
[9]刘骋.城市再生水管网余氯衰减规律及影响因素的实验研究[D].天津:天津大学,2012.
[10]姜旋.聚乙烯(PE)管在供水系统中的应用[J].净水技术,2014,33(s2):49-52.
[11]童祯恭,刘遂庆,陶涛.供水管网中管材对水质影响的探讨[J].城市公共事业,2006,20(1):22-24.

