聚乙二醇化干扰素α-2b联合恩替卡韦治疗慢性乙型肝炎的疗效观察
朱琼香,李小丹,秦永照,向红梅
(湖北省恩施州中心医院感染科 445000)
慢性乙型肝炎(chronic hepatitis B,CHB)是一种广泛流行的全球性传染病,中国是乙型肝炎病毒(hepatitis B virus,HBV)感染的高发区,估计HBV感染者约9 300万人,其中,CHB患者近2 000万人[1]。慢性HBV感染与病毒持续复制是导致病情进展或恶化的主要原因,高达40%的患者可能发展为肝硬化、肝癌等严重肝脏疾病[2-3]。当前,对于CHB的治疗方法主要包括抗病毒、抗炎保肝、调节免疫及防止纤维化等措施,其中,抗病毒治疗是关键。虽然临床上单纯应用一种抗病毒药物能够获得一定的疗效,但其总体治疗效果仍不能令人满意。本研究采用聚乙二醇化干扰素α-2b联合恩替卡韦用于CHB治疗,旨在观察其临床疗效并探索更加合理、有效的治疗方案。
1 资料与方法
1.1 一般资料 选取2012年2月至2014年6月本院收治的CHB患者120例,年龄18~45岁,其中,男82例,女38例。有明确急性肝炎病史或长期携带病毒史,病程2~12年。经医院伦理委员会批准后,将其分为聚乙二醇化干扰素α-2b治疗组(PEGα-2b组)、恩替卡韦治疗组(ETV组)和聚乙二醇化干扰素α-2b联合恩替卡韦治疗组(PEGα-2b+ETV组),每组40例。3组患者年龄、性别、体质量、病程及既往用过PEGα-2b和ETV药物的构成比方面比较,差异无统计学意义(P>0.05),具有可比性(表1)。纳入标准:(1)年龄在18~45岁范围内;(2)既往有乙型肝炎发病史或者乙型肝炎表面抗原(HBsAg)阳性6个月以上,现 HBsAg或者HBV-DNA仍呈阳性,符合2010年版《慢性乙型肝炎防治指南》的诊断标准[4];(3)血清丙氨酸氨基转移酶(ALT)未超过正常上限的6倍者;(4)6个月内未使用过核苷类似物或干扰素抗病毒治疗者;(5)受试者知情且同意加入本研究。排除标准:(1)合并有甲型肝炎病毒(HAV)、丙型肝炎病毒(HCV)、丁型肝炎病毒(HDV)、戊型肝炎病毒(HEV)和人类免疫缺陷病毒(HIV)重叠感染者;(2)并发严重的心脑血管、肺、肾及内分泌系统疾病患者;(3)并发肝硬化、恶性肿瘤及精神疾病患者;(4)妊娠期及哺乳期女性患者。
1.2 方法
1.2.1 治疗方法 所有患者接受相同的常规对症治疗,PEGα-2b组患者皮下注射1μg/kg聚乙二醇化干扰素α-2b(上海罗氏制药有限公司,国药准字S20040028号),每周1次,连续治疗48周。ETV组患者口服0.5mg/d的恩替卡韦(江苏正大天晴药业股份有限公司,国药准字H20100019号),连续治疗48周。PEGα-2b+ETV组患者在每周1次皮下注射1 μg/kg聚乙二醇化干扰素α-2b的基础上复合口服0.5mg/d的恩替卡韦治疗,连续治疗48周。
1.2.2 观察指标 (1)肝功能指标:包括ALT、门冬氨酸氨基转移酶(AST)及γ-谷氨酰基转移酶(GGT)的水平;(2)HBVDNA、HBeAg转阴率及HBeAg血清转换率;(3)临床治疗效果:治疗效果分为显效(完全应答)、有效(部分应答)及无效(无应答)。治疗后HBeAg及HBV-DNA转阴,且ALT值恢复至正常水平为完全应答;HBV-DNA水平明显降低,而HBeAg仍维持阳性或者ALT水平仍未降至正常为部分应答;HBVDNA未转阴或者持续阳性,且ALT值未见显著改善为无应答[5]。总有效率=[(显效数+有效数)/总数]×100%。其中,ALT、AST、GGT采用日立公司生产的全自动生化分析仪检测;HBV-DNA采用荧光定量PCR法检测;HBeAg采用罗氏E601化学发光免疫分析仪检测。
1.3 统计学处理 采用SPSS 17.0统计软件对数据进行分析处理,计量资料以x±s表示,组间均数比较采用单因素方差分析,组间两两比较采用SNK-q检验;计数资料以率表示,采用χ2检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 3组患者治疗前、后肝功能比较 对肝功能进行分析发现,治疗前,各组患者的ALT、AST、GGT水平均高于正常范围,但3组间比较差异无统计学意义(P>0.05)。抗病毒治疗48周后,3组患者的ALT、AST、GGT水平均明显下降,与治疗前比较,差异有统计学意义(P<0.05);组间比较发现,PEGα-2b+ETV组患者的ALT、AST、GGT水平明显低于其他两组,差异均有统计学意义(P<0.05),而 PEGα-2b组与ETV组患者的ALT、AST、GGT水平比较差异无统计学意义(P>0.05),见表2。
2.2 3组患者 HBV-DNA和 HBeAg转阴率、HBeAg血清转换率及有效率比较 治疗后,PEGα-2b+ETV组患者的HBVDNA和HBeAg转阴率、HBeAg血清转换率及治疗有效率均明显高于其他两组,差异有统计学意义(P<0.05);与PEGα-2b组比较,ETV组患者的HBV-DNA和HBeAg转阴率更低(P<0.05),但两组患者在HBeAg血清转换率及治疗有效率方面比较差异无统计学意义(P>0.05),见表3。
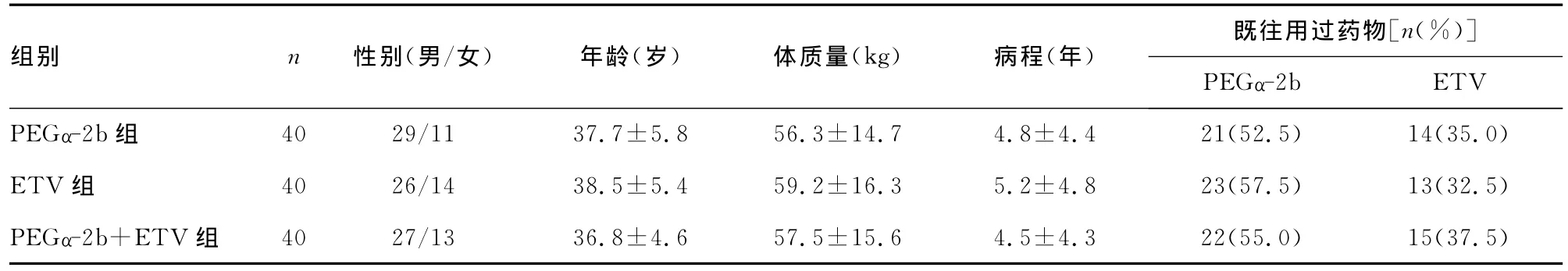
表1 3组患者一般资料比较(x±s)
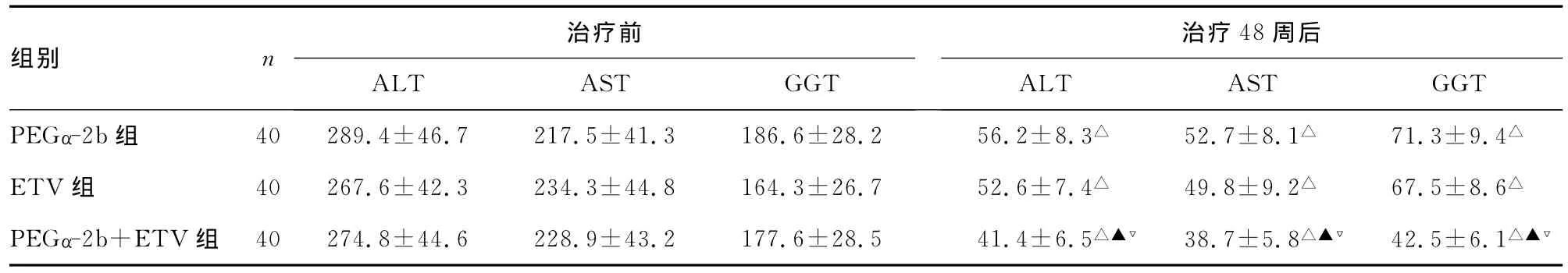
表2 3组患者治疗前、后肝功能比较(x±s,U/L)

表3 3组患者HBV-DNA和HBeAg转阴率、HBeAg血清转换率及有效率比较[n(%)]
3 讨 论
积极抗病毒治疗能够有效阻止患者体内HBV复制,使患者获得充分的病毒学应答,以维持良好的肝脏功能和延缓其并发症。当前,临床上用于治疗CHB的抗病毒药物主要有干扰素和核苷(酸)类似物(nucleoside/nucleotide,NAs)2类,二者各有一定的优点和缺点。因此,联合抗病毒治疗可能更具有优势,并已逐步成为一个新的研究方向。
干扰素除具有直接抑制HBV作用外,还可上调被感染肝细胞的主要组织相容性复合抗原(MHC-1)表达,并激活各种细胞因子及调节免疫途径来抑制 HBV复制[6]。其优点是HBeAg血清转换率和HBsAg消失率相对较高、疗程相对固定、无耐药性及兼有免疫调节作用,但其适应证较局限、不良反应多、需注射给药及不能用于失代偿期肝硬化和重型肝炎患者,患者难以耐受导致依从性差[7-8]。中国批准使用的干扰素类药物包括普通干扰素α和聚乙二醇化干扰素α(PEGα-2α和2b),以聚乙二醇化干扰素α的疗效更佳。
与干扰素的免疫调节作用不同,NAs的作用机制为在体内磷酸化生成具有抑制病毒DNA聚合酶作用的三磷酸核苷类似物,终止HBV-DNA链的延长和合成,从而达到抑制病毒复制的作用[9]。相对而言,NAs的适用范围更广,可在各种临床类型的CHB患者中使用,其抑制病毒复制能力更强、服药方便、患者依从性好,但HBeAg血清转换率和HBsAg消失率低、疗程不固定、需长期服药及存在耐药突变风险[10]。恩替卡韦是一种新型的抗HBV药物,属于环戊酸鸟苷类似物,在细胞内可转化为三磷酸盐,与HBV多聚酶的天然底物三磷酸脱氧鸟嘌呤核苷竞争抑制HBV-DNA聚合酶而发挥作用[11]。自2005年在中国上市以来,其出色的抗病毒能力以及极低的耐药率,使其成为治疗CHB的一线药物。由于恩替卡韦具有较高的耐药基因屏障,其存在耐药突变的风险是当今NAs中最低的,初治患者经过恩替卡韦治疗后,4年耐药率的发生小于1%[12]。
在本研究中,作者选择聚乙二醇化干扰素α-2b联合恩替卡韦用于治疗CHB,理论上有助于降低治疗不良反应,并可能发挥协同的抗病毒疗效。本研究结果显示,采用单纯聚乙二醇化干扰素α-2b或者恩替卡韦治疗都具有良好的抗病毒疗效,并有效地改善了CHB的肝功能。虽然聚乙二醇化干扰素α-2b组在HBV-DNA和HBeAg转阴率方面比恩替卡韦组更高(P<0.05),但两组患者的肝功能和有效率比较差异无统计学意义(P>0.05)。然而,与单纯聚乙二醇化干扰素α-2b组或者恩替卡韦组比较,两药联合治疗组的HBV-DNA和HBeAg转阴率、HBeAg血清转换率都明显更高(P<0.05),肝功能和治疗有效率也明显优于其他两组(P<0.05)。本研究结果表明,聚乙二醇化干扰素α-2b联合恩替卡韦治疗CHB疗效更为显著,二者具有较强的互补性,值得在临床上推广应用。
[1]Lu FM,Zhuang H.Management of hepatitis B in China[J].Chin Med J,2009,122(1):3-4.
[2]Chen CJ,Yang HI,Su J,et al.Risk of hepatocellular carcinoma across a biological gradient of serum hepatitis B virus DNA level[J].JAMA,2006,295(1):65-73.
[3]Iloeje UH,Yang HI,Su J,et al.Predicting cirrhosis risk based on the level of circulating hepatitis B viral load[J].Gastroenterology,2006,130(3):678-686.
[4]中华医学会肝病学分会,中华医学会感染病学分会.慢性乙型肝炎防治指南(2010年版)[J].中华肝脏病杂志,2011,19(1):13-24.
[5]杨强.两种药物联合应用治疗慢性乙型肝炎60例[J].检验医学与临床,2013,10(9):1136-1138.
[6]Brunetto MR,Bonino F.Interferon therapy of chronic hepatitis B[J].Intervirology,2014,57(3/4):163-170.
[7]李成伟,赵连荣,丁洋,等.聚乙二醇化干扰素-α-2a治疗慢性乙型肝炎病毒动力学变化与疗效关系研究[J].中国实用内科杂志,2013,33(6):482-484.
[8]亢西,王芳.干扰素α-2b注射液治疗慢性乙型肝炎合并2型糖尿病临床研究[J].传染病信息,2013,26(2):115-117.
[9]Rawal RK,Singh US,Chavre SN,et al.2′-Fluoro-6′-methylene-carbocyclic adenosine phosphoramidate(FMCAP)prodrug:in vitro anti-HBV activity against the lamivudineentecavir resistant triple mutant and its mechanism of action[J].Bioorg Med Chem Lett,2013,23(2):503-506.
[10]Fung J,Lai CL,Seto WK,et al.nucleoside/nucleotide analogues in the treatment of chronic hepatitis B[J].J Antimicrob Chemother,2011,66(12):2715-2725.
[11]张健珍,杨葆业,陈铿,等.替比夫定与恩替卡韦治疗HBeAg阳性慢性乙型肝炎的对比研究[J].实用医学杂志,2010,26(14):2609-2611.
[12]Khungar V,Han SH.A systematic review of side effects of nucleoside and nucleotide drugs used for treatment of chronic hepatitis B[J].Curr Hepat Rep,2010,9(2):75-90.

