部分糊化玉米淀粉浆液的性能
王 娟,徐 进,孙月玲,蒋龙宇,史博生,王 强,高卫东,范雪荣
(1.生态纺织教育部重点实验室(江南大学),江苏无锡 214122;2.江苏联发纺织股份有限公司江苏省生态染整技术重点实验室,江苏 海安 226601;3.天华企业发展(苏州)有限公司,江苏 苏州 215124)
淀粉浆料的传统调浆方式是在95℃以上使淀粉完全糊化,但这种调浆方式调浆时间长,浆液黏度随温度的降低显著增加,甚至凝胶,不能低温上浆,特别是这种调浆方式使原淀粉黏度过高难以直接应用,需变性降黏处理。为改善传统调浆方式中淀粉完全糊化应用的局限性,提出了“部分糊化淀粉浆液”的新调浆方式以及全新的上浆概念。文献[1]对部分糊化玉米淀粉浆液的制备和黏度性质进行了研究,分别采用恒温和蒸汽升温法制备了部分糊化淀粉浆液,通过对其黏度和黏度稳定性的比较认为,蒸汽升温法制备的部分糊化淀粉浆液具有黏度低、性质稳定、低温不凝冻、浓度对黏度影响小等特点,更具实际应用价值。
本文研究采用偏光显微镜、激光粒度分析仪、X射线衍射仪、差示热扫描分析仪等手段对蒸汽升温法制备的部分糊化淀粉浆液的偏光性、糊化度、结晶度、粒径分布进行了测试,并与原淀粉进行了比较,研究了蒸汽升温法制备部分糊化淀粉浆液过程中淀粉颗粒结构的变化。
1 实验部分
1.1 材料与仪器
玉米淀粉(山东邹平天美纺织助剂有限公司)。
DF-101s型集热式磁力搅拌器(上海谷宁仪器有限公司),TG16-WS型台式高速离心机(湖南湘仪实验室仪器开发有限公司),D8型 X射线衍射仪(德国布鲁克AXS有限公司),Q200 DSC示差扫描量热仪(沃特世科技上海有限公司),冷冻干燥机(北京博医康实验仪器有限公司),偏光显微镜(德国卡尔蔡司公司),S3500型激光粒度分析仪(美国Microtrac公司)。
1.2 部分糊化淀粉浆液的制备
蒸汽升温制备法:室温下配制体积为250 mL、质量分数为10.0%的淀粉乳浆液,置于加热装置中密封搅拌升温,待浆液温度升至55℃时停止水浴加热,立即通过乳胶管导入蒸汽(注:乳胶管须插入浆液底部并快速搅拌浆液,使浆液受热均匀),利用蒸汽继续加热使淀粉乳升温至62℃,停止蒸汽加热,制得62℃部分糊化淀粉浆液,记为S-62。采用相同方法,分别制备63~68℃时的部分糊化淀粉浆液,分别记为S-63~S-68。
1.3 淀粉浆液偏光性观察
室温下,取少量质量分数稀释为1%的部分糊化淀粉乳液于载玻片上,并沿液滴一侧轻轻盖上玻片。采用Leica DMLP型偏光显微镜观察淀粉颗粒形态并收集偏光数据[2]。
1.4 结晶度测定
用X射线衍射仪进行测试,测试条件:Cu靶Kα射线,管压为40 kV,Ni片滤波,波长为1.5406×10-10m,管流30 mA,发射及防反射狭缝 1°,接受狭缝0.2 mm,衍射角(2θ)的旋转范围为 3°~40°,扫描速度为 2(°)/min[3]。参考文献[4]的方法,应用JD801软件,计算部分糊化淀粉的相对结晶度值。
1.5 糊化度测定
采用DSC(Q200)差示扫描量热分析仪对部分糊化淀粉浆液的糊化情况进行检测。淀粉与蒸馏水比例为1∶3,密封且避光平衡24 h后测试。测试条件为:升温范围40~90℃,升温速率5℃/min。通过DSC谱图分析得出△H(糊化焓值)、To(糊化起始温度)、Tp(糊化峰值温度)、Te(终止糊化温度),QGD(糊化度)计算公式[5]为
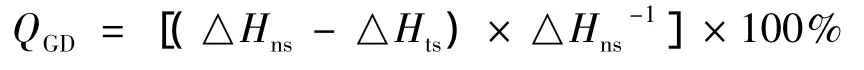
式中:△Hns为原淀粉未经加热处理的热吸收焓;△Hts为加热处理的部分糊化原淀粉热吸收焓。
1.6 粒径测定
取10 mL质量分数为10.0%的部分糊化淀粉浆液,去离子水稀释至100 mL,35℃下搅拌使浆液分散均匀。将待测液滴入激光粒径仪样品池中进行测试,用体积平均粒径表示淀粉颗粒的平均直径[6]。
1.7 膨胀势测定
取10 mL部分糊化淀粉浆液,6000 r/min离心15 min。倒出上层清液,称取下层沉淀质量W1,将下层沉淀在105℃烘箱中干燥至恒重,记为膨胀势PSP为

式中:W1为离心后下层沉淀的质量;W2为下层沉淀干燥的质量。
2 结果与讨论
2.1 部分糊化淀粉浆液的偏光特性
部分糊化淀粉浆液及原淀粉的偏光图像如图1所示。淀粉颗粒属于球晶结构,颗粒内部存在结晶和非晶2种结构,在偏振光照射时有光学各向异性现象产生,从而在偏光显微镜内观察淀粉颗粒时会出现偏光十字[8]。
由图1可见,原淀粉颗粒的偏光十字比较明显。62、63℃时制备的部分糊化淀粉浆液,少部分颗粒的偏光十字发生变化。这是因为随蒸汽导入量的增加浆液温度逐渐升高,淀粉颗粒受热吸水膨胀,其中少量体积较大的淀粉颗粒首先糊化,颗粒内部有序排列的结晶区被破坏,导致少量偏光十字消失。

图1 原淀粉和部分糊化淀粉浆液的偏光显微镜照片(×400)Fig.1 Polarized light microscopic images for native corn starch and partially gelatinized starch(×400).(a)Native corn starch;(b)S-62;(c)S-63;(d)S-64;(e)S-65;(f)S-66;(g)S-67;(h)S-68
蒸汽升温法64℃时制备的部分糊化淀粉浆液,随着蒸汽导入量的增加,浆液温度升高使淀粉颗粒糊化的比例明显增加(偏光面积减少,亮度减弱)。浆液主要由可逆吸水膨胀的未糊化颗粒、未糊化态向糊化态转变的过渡态颗粒、糊化颗粒等组成。该混合状态下大部分淀粉颗粒都处于糊化过程的中间阶段(不可逆吸水阶段),这种状态下,趋于糊化的过渡态颗粒与糊化甚至瓦解的淀粉颗粒形成大的颗粒团,部分未糊化的膨胀颗粒填充于上述大颗粒团间的缝隙,从而使形成的混合体系黏度小,稳定性好,不易出现凝胶状态。该浆液在使用过程中,长时间放置才出现分层现象,但简单搅拌就可混合均匀。
随着制备温度的进一步提高,65~67℃时制备的部分糊化淀粉浆液中淀粉颗粒发生剧烈膨胀,较多淀粉颗粒糊化,大面积偏光十字消失,甚至部分糊化颗粒破碎瓦解。68℃制备的部分糊化淀粉浆液,淀粉颗粒偏光十字消失,说明淀粉颗粒结晶结构被完全破坏,淀粉颗粒已趋于完全糊化状态[9]。
2.2 部分糊化淀粉浆液的结晶度分析
图2为原淀粉和部分糊化淀粉浆液的X射线衍射图。与原淀粉相比,蒸汽法62℃制备的部分糊化淀粉浆液的X射线衍射图没有明显变化,蒸汽法68℃制备的部分糊化淀粉浆液已接近完全糊化状态而无明显的X射线衍射峰,因此62、68℃部分糊化淀粉浆液的X射线衍射图未在图2中显示。
由图2 可见,玉米原淀粉在2θ为15°、17°、18°、23°附近出现强的衍射峰,同时在17°、18°附近出现2个相连的强衍射峰,符合A型晶体淀粉的X射线衍射波谱特征[10-11],通过软件计算得玉米原淀粉的相对结晶度为39.42%。
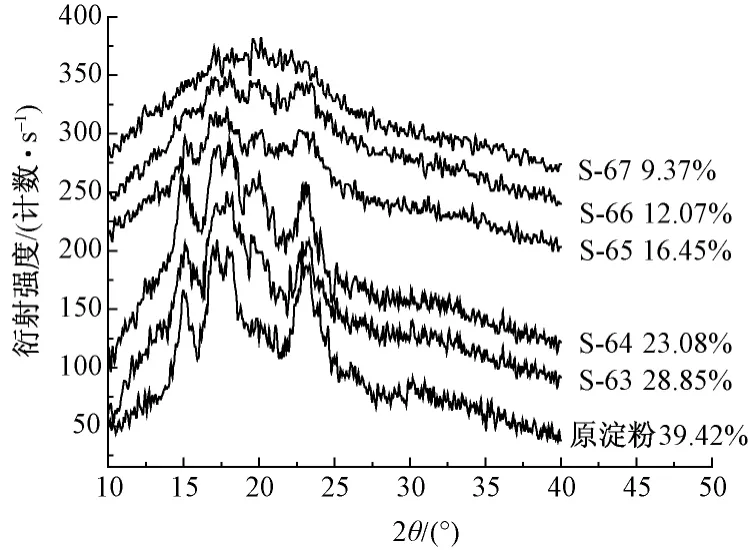
图2 原淀粉和部分糊化淀粉浆液的X射线衍射图Fig.2 X-ray powder diffraction spectra for native corn starch and partially gelatinized starch
蒸汽法63℃制备的部分糊化淀粉浆液的X射线衍射峰强度减弱,峰形和原淀粉颗粒的峰形相似,但相对结晶度(28.85%)略有下降。虽然63℃部分糊化淀粉浆液的制备温度低于玉米原淀粉的起始糊化温度(64.76℃,见图3),但部分糊化淀粉浆液制备时导入蒸汽的温度较高(≥100℃),调浆时可使与其接触的淀粉颗粒在有充足水分存在时发生瞬间糊化,因此,可解释即使低于淀粉的起始糊化温度的温度制备同样可使少量淀粉颗粒发生糊化现象。
部分糊化淀粉浆液的制备温度为64℃时,淀粉颗粒衍射峰强度减弱,甚至尖锐的微晶衍射峰消失。这是因为浆液温度随蒸汽导入量的增加而升高,淀粉颗粒内排列的紊乱程度增加,淀粉颗粒的结晶区逐渐向非晶区转变,糊化的淀粉颗粒比重明显增加,使浆液黏度得到一定程度的提高。同时浆液中有较多吸水膨胀的未糊化颗粒而赋予浆液流动的性质[9]。
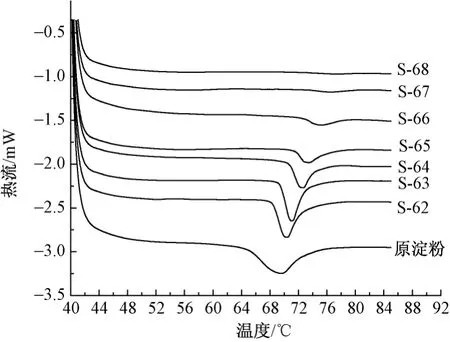
图3 原淀粉和部分糊化淀粉浆液的DSC图谱Fig.3 DSC thermograms of partially gelatinized starch and native corn starch
当部分糊化淀粉浆液的制备温度(65、66、67℃)明显高于淀粉的起始糊化温度时,淀粉颗粒糊化数目增加,颗粒内部有序排列进一步被打乱,结晶度(16.45%、12.07%、9.37%)明显降低,使得浆液黏度升高。
2.3 部分糊化淀粉浆液糊化度分析
淀粉糊化过程伴随着能量变化,因此在DSC差热分析时会出现热吸收峰。原淀粉和部分糊化淀粉浆液的糊化特性如图3所示,糊化特征值见表1。
由图3可见,原淀粉颗粒的吸收峰比较宽,随着蒸汽导入量的增加,制备温度从62℃提高至68℃时,淀粉颗粒的吸收峰逐渐变窄,峰值向高温方向推移,同时吸收峰面积随制备温度的升高而减小。这是因为淀粉颗粒的结晶区在湿热条件下逐渐降低,且结晶区中有序结构首先遭到破坏所致,这进一步反映了淀粉颗粒的糊化度随制备温度的升高而增大[12]。图中68℃制备的部分糊化淀粉浆液淀粉颗粒热吸收峰较小甚至趋于一条直线,进一步验证了图1所得出的结论,即在该处理温度下淀粉颗粒已接近完全糊化状态。
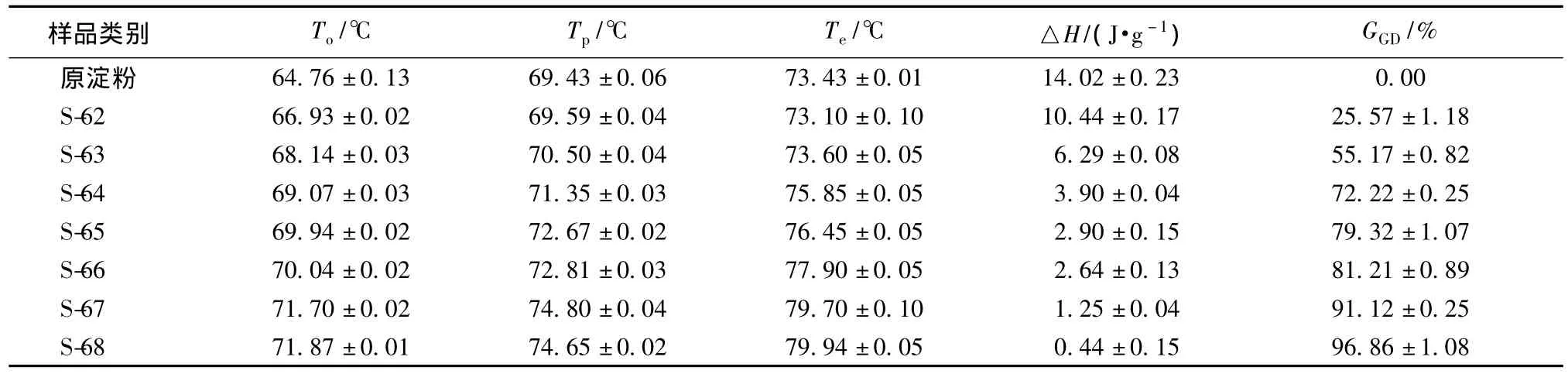
表1 原淀粉和部分糊化淀粉浆液的糊化特征值Tab.1 Gelatinization properties of native corn starch and partially gelatinized starch measured by DSC
通过表1数据可知,部分糊化淀粉浆液的To、Tp、Te值随着制备温度的提高而明显增大。当制备温度升高至68℃时,部分糊化淀粉的△H值降低至(0.44±0.15)J/g,同时糊化度增加至(96.86±1.08)%,表明68℃时制备的淀粉试样已接近完全糊化。
文献[7]对部分糊化淀粉糊化特性的研究表明,部分糊化淀粉的糊化温度值较玉米原淀粉高,这与本实验研究得出的结论一致。
62、63℃时制备部分糊化淀粉浆液时,淀粉颗粒的糊化比例较少。由于制备温度较低,大部分结构完整的淀粉颗粒均匀分散在浆液中,少量与蒸汽直接接触的淀粉颗粒受热后,部分水分子进入颗粒微晶区致使颗粒吸水膨胀,破坏其有序结构,进而淀粉颗粒发生有限程度的糊化。
64℃时制备的部分糊化淀粉浆液,糊化度为(72.22±0.25)%。因其蒸汽导入量增加,浆液温度继续升高,淀粉颗粒吸水膨胀更加明显,较多颗粒糊化,甚至部分糊化淀粉颗粒外侧的支链淀粉发生不同程度的涨裂,浆液糊化度明显增加,使浆液黏稠度增加。
当制备温度大于64℃时,所制得的部分糊化淀粉浆液的△H值显著低于原淀粉,说明淀粉颗粒糊化的比重增大,但即使制备温度升高至65~68℃,浆液中仍有少部分未糊化的淀粉颗粒存在[13]。
2.4 部分糊化淀粉浆液颗粒粒度分析
玉米原淀粉颗粒的平均直径比经过蒸汽湿热处理的部分糊化淀粉颗粒小。随着部分糊化淀粉浆液制备温度的增加,淀粉颗粒不断膨胀吸水,甚至糊化破裂[14],使颗粒的平均直径逐渐增大。原淀粉和部分糊化淀粉浆液颗粒的粒度分布情况见表2。
根据表2数据可知:原淀粉颗粒的平均粒径为19.64 μm,峰值集中在15.80 μm;62 ℃时制备的部分糊化淀粉颗粒的平均粒径为39.22 μm,峰值集中在18.26 μm。由于浆液制备温度不高,蒸汽导入量较少,淀粉颗粒吸热膨胀较少,其平均直径只发生有限的增加,同时颗粒峰值增大并不明显。
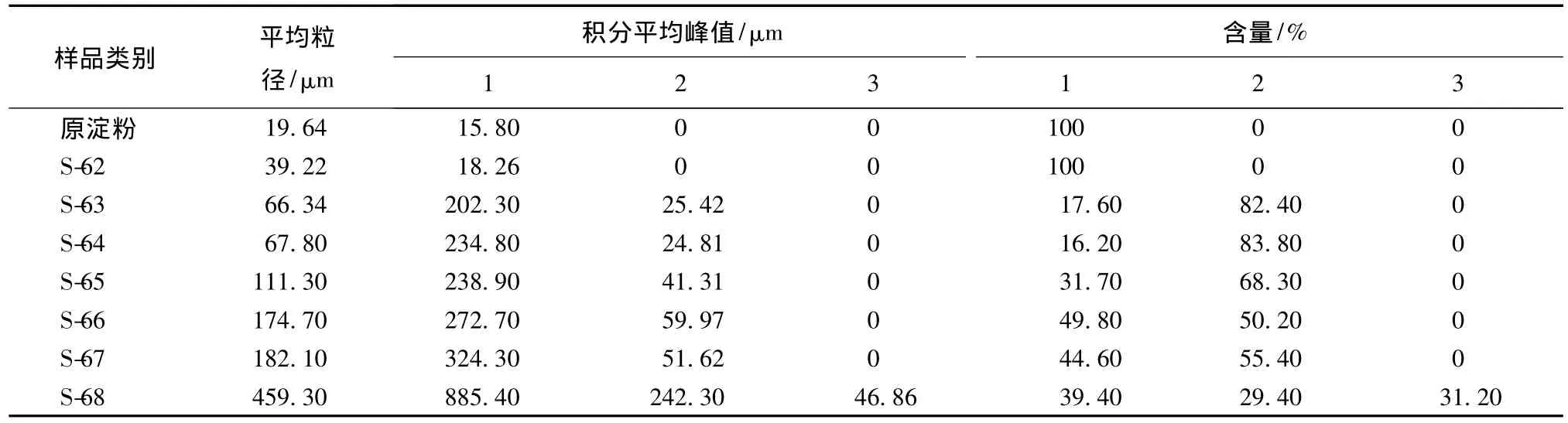
表2 原淀粉和部分糊化淀粉浆液淀粉颗粒的粒径分布Tab.2 Granular size distribution of partially gelatinized starch and native corn starch
63℃时制备的部分糊化淀粉的粒径继续增加,并出现2个峰值,子峰出现在较大粒径处,但所占比例较小。主要是由于蒸汽导入量增加,高温蒸汽与颗粒瞬间接触使其急剧吸热膨胀甚至糊化,进而分峰出现较大值。64℃时制备的部分糊化淀粉浆液的平均粒径继续增加。
制备温度继续升高至65~67℃,淀粉颗粒的平均直径增加至原淀粉的5~10倍。当制备温度为68℃时,粒径出现3个峰值,说明该制备温度下淀粉颗粒膨胀糊化,部分淀粉囊腔破碎瓦解,从而粒径分布范围变宽。
2.5 部分糊化淀粉浆液颗粒膨胀势分析
淀粉颗粒易在湿热条件下发生不同程度的润胀,淀粉颗粒吸水膨胀能力随着处理温度的升高而逐渐增强。不同温度下制备的部分糊化淀粉浆液颗粒的膨胀势如表3所示。

表3 部分糊化淀粉浆液颗粒的膨胀势变化Tab.3 Swelling power(PSP)of partially gelatinized starch
当制备温度(62、63℃)低于玉米淀粉的初始糊化温度(64.76℃)时,仅有少量与蒸汽接触的淀粉颗粒内游离水进入结晶区,使颗粒体积膨胀,浆液中大部分淀粉颗粒内游离水只能进入颗粒的非结晶区,颗粒只发生有限的润胀[15]。
当制备温度(64℃)接近淀粉的初始糊化温度(64.76℃)时,与蒸汽直接接触吸热的淀粉颗粒数目增多,同时大部分颗粒通过溶液温度升高而间接吸热,使其吸水膨胀能力增强,进而淀粉颗粒膨胀势明显增加。
随着制备温度的继续升高(65~68℃),淀粉颗粒膨胀势逐渐增大。由于大量游离水进入淀粉颗粒的晶区,淀粉颗粒润胀明显甚至崩解,使得部分糊化淀粉浆液凝胶化概率明显增大。
因此,64℃时制备的部分糊化淀粉浆液的颗粒膨胀势(4.46)比较适中,刚好接近62℃和68℃时制备的部分糊化淀粉浆液淀粉颗粒的膨胀势均值,这说明适当的颗粒膨胀势可赋予浆液较好的悬浮稳定性[16]。
3 结论
1)蒸汽升温法在不同温度下制备的部分糊化淀粉浆液具有不同的偏光特性;随着制备温度的提高,部分糊化淀粉浆液中淀粉颗粒结晶度下降,而其糊化度、粒径、膨胀势均呈增大趋势。
2)64℃蒸汽升温法制备的部分糊化淀粉浆液中存在X射线衍射结晶峰,糊化度为72.22%。该状态下的淀粉颗粒未完全糊化,同时淀粉颗粒具有适当的膨胀势和粒径,可赋予浆液较好的悬浮稳定性。
[1] 王娟,徐进,范雪荣,等.部分糊化玉米淀粉浆液的制备及黏度性质研究[J].棉纺织技术,2014,442(6):23-27 WANG Juan,XU Jin,FAN Xuerong,et al.Preparation and viscosity properties of partial-gelatinized slurry of corn strach[J].Cotton Textile Technology,2014,42(6):23-27.
[2] 王秀艳,董丽松.变性淀粉结晶性和形态研究[J].中国粮油学报,2005,20(3):26-29.WANG Xiuyan,DONG Lisong.Study on crystalline and morphological of modified starch[J].Journal of the Chinese Cereals and Oils Association,2005,20(3):26-29.
[3] 张翠兰,张本山,陈福泉.淀粉结晶度计算的新方法[J].食品科学,2011,32(9):68-71.ZHANG Cuilan,ZHANG Benshan,CHEN Fuquan.A novel method for calculating starch crystallinity[J].Food Search,2011,32(9):68-71.
[4] SANDHU Kawaljit Singh,LIM Seung-Taik.Structural characteristics and in vitro digestibility of mango kernel starches(Mangifera indica L)[J].Food Chemistry,2008,107(1):92-97.
[5] 田翠华,严守雷,李洁,等.莲藕淀粉的颗粒特性研究[J].安徽农业科学,2008,36(10):4062-4064.TIAN Cuihua,YAN Shoulei,LI Jie,et al.Study on the granule properties of lotus root starch[J].Journal of Anhui Agricultural Sciences,2008,36(10):4062 -4064.
[6] 朱凯艳,张文斌,杨瑞金,等.粉碎处理对花生水酶法提取油脂和蛋白质的影响[J].食品与机械,2012,28(2):119-122.ZHU Kaiyan,ZHANG Wenbin,YANG Ruijin,et al.Influence of pulverization treatment on aqueous enzymatic extracion of peanut oil and protein hydrolysates[J].Food & Machinery,2012,28(2):119-122.
[7] FU Zongqiang,WANG Lijun,LI Dong,et al.Effects of partial gelatinization on structure and thermal properties of corn starch after spray drying[J].Carbohydrate Polymers,2012,88(4):1319-1325.
[8] 赵永青,张本山,李芬芬,等.热-醇处理对玉米淀粉颗粒偏光特性的影响[J].粮食与饲料工业,2010(6):21-23.ZHAO Yiongqing,ZHANG Benshan,LI Fenfen,et al.Effects of treatment with heating and ethanol on polarized properties of corn starch granules[J].Cereal& Feed Industry,2010(6):21-23.
[9] RATNAYAKE Wajira S,JACKSON David S.A new insightinto the gelatinization process of native starches[J].Carbohydrate Polymers,2007,67(4):511-529.
[10] CHEETHAM Norman W H,TAO Leping.Variation in crystalline type with amylosecontent in maize starch granules:an X-ray powderdiffractionstudy [J].Carbohydrate Polymers,1998,36(4):277 -284.
[11] 王中荣.不同直链淀粉含量的玉米淀粉理化性质及其应用研究[D].重庆:西南大学,2007:31-34.WANG Zhongrong.Studies on physical-chemical properties and application of corn starch with different content of amylose[D].Chongqing:South West University,2007:31-34.
[12] 莫紫梅.糯米淀粉分子结构及其物化性质的研究[D].武汉:华中农业大学,2010:28-31.MO Zimei.Study on molecular structure and physicochemical charaeteristics of glutinous rice starch[D]. Wuhan:Central China Agricultural University,2010:28-31.
[13] 叶怀义,杨素玲,叶蹾昊.高压对淀粉糊化特性的影响[J].中国粮油学报,2000,15(1):10-13.YE Huaiyi,YANG Suling,YE Dunhao.Effect of high pressure on gelatinization of strach[J].Journal of the Chinese Cereals and Oils Association,2000,15(1):10-13.
[14] KOGANTI Nagamani,MITCHELL John R,IBBETT Roger N,et al.Solvent effects on starch dissolution and gelatinization[J].Biomacromolecules,2011,12(8):2888-2893.
[15] 田翠华,严守雷,李洁,等.莲藕淀粉的糊化特性研究[J].食品科学,2009,30(11):29-32.TIAN Cuihua, YAN Shoulei, LI Jie, et al.Gelatinization characteristics of lotus root starch[J].Food Science,2009,30(11):29-32.
[16] 高群玉,谢钦.淀粉糊化过程的数字图像分析技术动态监测[J].华南理工大学学报,2011,39(12):105-109.GAO Qunyu,XIE Qin.Application in monitoring the gelatinization process of starch based on digital image analysis technique[J]. Journal of South China University of Technology,2011,39(12):105-109.
——微网状透光防炫目汽车前挡风玻璃膜的设计研究

