铜(II)离子对橙皮素清除自由基作用的影响
邹淑君,许树军,张 蕾,徐 暘
(黑龙江中医药大学 药学院,哈尔滨 150040)
铜(II)离子对橙皮素清除自由基作用的影响
邹淑君,许树军,张 蕾,徐 暘
(黑龙江中医药大学 药学院,哈尔滨 150040)
为探讨Cu2+存在对橙皮素(Hsp)清除自由基作用的影响.将Hsp与Cu2+混合即生成不稳定配合物(Hsp-Cu),利用UV-Vis光谱测定Hsp及Hsp-Cu对1,1-二苯基-2-三硝基苯肼自由基(DPPH·)、羟基自由基(·OH)、超氧阴离子自由基(O2-·)的清除作用.在实验条件下Hsp-Cu对DPPH·及·OH有一定的清除作用,但清除能力不如Hsp.Hsp-Cu不能有效清除O2-·,且在邻苯三酚自氧化过程中表现出促氧化作用.表明Hsp作为抗氧化剂使用时,应避免与Cu2+接触,以免影响其抗氧化能力.
橙皮素;铜(II)离子;自由基;清除
橙皮素(简写为Hsp),分子式C16H14O6,化学名5,7,3′-三羟基-4′-甲氧基二氢黄酮,为柑橘果实中主要活性成分橙皮苷的水解产物.国内在医药方面,主要疗效有健胃、祛痰、镇咳、驱风、利尿、止逆和止胃痛等[1].在国外,橙皮素用做心血管保健药物,也做为抗氧化剂用于化妆品和食品添加剂中[2].可见橙皮素有着广泛的应用.橙皮素分子具有4-羰基、5-羟基结构,理论上易与过渡金属离子配位形成配合物.铜是常见的过渡金属元素,也是人体重要的必需微量元素之一,与机体内的抗氧化关系密切[3].许多文献报道黄酮类化合物能与与金属配位,且配位后对自由基的清除作用均明显高于黄酮本身[4-5].但也有文献指出:黄酮类化合物具有抗氧化和促氧化的双重作用,Cu2+、Fe3+等过渡金属离子是黄酮类化合物促氧化作用的重要因素[6].因此,本实验模拟生理pH条件下将橙皮素与铜(II)离子混合(简写为Hsp-Cu),分析其是否存在配位作用,并对比测试有无铜(II)离子存在下其对自由基的清除作用,以考察Cu2+的引入对橙皮素抗氧化作用的影响,为橙皮素的合理应用开发提供实验依据.
1 试剂与仪器
1.1 药品与试剂
橙皮素(Hsp 98%,上海晶纯实业有限公司);DPPH(98%,日本东京化成株式会社);三羟甲基氨基甲烷 (简称Tris ,99.8%,上海博宏生物科技有限公司);其他试剂均为国产分析纯.
1.2 仪器
UV-1601型紫外可见分光光度计(日本岛津);PB-20型pH计(德国赛多利斯);SK250LH型超声波清洗器(上海科导);XS105DU型电子分析天平(瑞士梅特勒).
1.3 实验方法
1.3.1Hsp与铜(II)离子的混合
按物质的量比l∶l将氯化铜的乙醇溶液在搅拌下缓慢滴加到橙皮素乙醇溶液中,用Tris-HCl缓冲液调至生理pH=7.4左右,有沉淀产生,室温下搅拌2 h,静置,离心,沉淀物用乙醇洗涤,干燥得暗黄绿色固体(定为Hsp-Cu).
1.3.2对DPPH·自由基的清除作用
根据Hsp及Hsp-Cu的溶解度情况,确定配制二者初始溶液质量浓度为0.08 mg/mL,分别取两种溶液0.5、1.0、1.5、2.0、3.0、4.0、5.0 mL于不同比色管中,去离子水定容至10 mL作为不同质量浓度的待测样品;6.5×10-5mol/L的DPPH·溶液为供试液.均以去离子水为参比,于517 nm下测试,且待测液均在40 ℃时避光恒温30 min后进行测试.测得等体积去离子水与DPPH·溶液混匀后的吸光度A0;等体积待测样品溶液与DPPH·溶液混匀后的吸光度Ai;等体积待测样品溶液与去离子水混匀后的吸光度Aj.根据抑制率=[1-(Ai-Aj)/A0] ×100%进行计算,以测试时样品质量浓度为横坐标对抑制率作图[5, 7].
1.3.3对·OH自由基的清除作用
待测样品初始质量浓度同1.2.2项下.另配制2 mmol/L硫酸亚铁铵溶液、3 mmol/L的H2O2溶液、6 mmol/L水杨酸溶液作供试液.均于510 nm下测吸光度.在比色管中依次加入硫酸亚铁铵溶液3 mL、H2O2溶液1 mL,摇匀,37 ℃水浴加热15 min后,加入水杨酸溶液3 mL,再于37 ℃水浴继续加热15 min后加去离子水定容至25.0 mL,测定吸光度A0;另在不同的比色管中分别加入硫酸亚铁铵溶液3 mL、H2O2溶液1 mL,摇匀,分别加入待测样品溶液为1.0、2.0、3.0、4.0、6.0、8.0、10.0 mL,于37 ℃水浴加热15 min后再加入水杨酸溶液3 mL,继续水浴加热15 min后去离子水定容至25.0 mL,测吸光度Af.按清除率=[(A0-Af)/A0]×100%进行计算,以测试时样品质量浓度对清除率作图[5, 7].
1.3.4对O2-·的清除作用
待测样品初始质量浓度同1.2.2项下.另配制pH值为8.2的Tris-HCl缓冲溶液、3 mmol/L的邻苯三酚溶液作供试液.均于320 nm下测吸光度.等体积Tris-HCl缓冲溶液与去离子水混合做空白溶液,向10 mL比色管中加入Tris-HCl缓冲溶液5.0 mL、去离子水4.7 mL及邻苯三酚溶液0.3 mL混匀,测定吸光度,计算不加待测液时邻苯三酚自氧化速率v0.向两组不同的比色管中加入Tris-HCl缓冲溶液5.0 mL、待测样品溶液分别为0.1、0.2、0.3、0.4、0.6、0.8、1.0、1.2 mL,其中一组加去离子水定容至10 mL做空白溶液;另一组加邻苯三酚溶液0.3 mL、并迅速加去离子水定容至10 mL摇匀测吸光度,计算加待测液时邻苯三酚自氧化速率vc.测定吸光度时均每30 s记录1次,直到反应启动后3 min结束.以时间为横坐标,吸光度值为纵坐标进行线性回归得到直线斜率即为v0和vc[7].
1.3.5数据处理分析
测试结果用Origin8.5软件进行统计分析并作图.
2 结果分析
2.1 Hsp-Cu及Hsp的紫外-可见光谱
Hsp可溶于甲醇、乙醇、DMSO(二甲基亚砜)、DMF(氮氮二甲基甲酰胺)中,难溶于水;Hsp-Cu难溶于甲醇、乙醇,微溶于水,可溶于DMSO、DMF中.因此将二者溶解于DMSO中进行测试.图1为紫外可见光谱曲线.可见Hsp最大吸收波长为290 nm,在331 nm处有一较低的肩峰.Hsp-Cu有2个峰,且均向长波方向移动,吸收波长分别移至307 nm和371 nm,说明Hsp与Cu2+进行了配位.即橙皮素与Cu2+在pH=7.4的条件下可发生配位作用.

图1 Hsp-Cu及Hsp的紫外-可见光谱
但是将Hsp-Cu放置,随着时间的延长,发现Hsp-Cu所呈现的吸收峰逐渐降低,直至约36 h左右消失,最后呈现出Hsp峰.说明Hsp与Cu2+生成的配合物不稳定,容易分解.
2.2 Hsp-Cu及Hsp对DPPH·自由基的清除作用
Hsp-Cu和Hsp对DPPH·的抑制作用比较结果如图2所示.

图2 Hsp-Cu及Hsp对DPPH·自由基的清除作用
由图2可见,Hsp对DPPH·有较好的清除能力,清除率随着Hsp质量浓度的增大而增大,呈现一定的量效关系.Hsp-Cu对DPPH·的清除率也随着质量浓度的增大而增大,呈现一定的量效关系,但清除能力明显弱于Hsp.
2.3 Hsp-Cu及Hsp对·OH自由基的清除作用
图3是Hsp-Cu和Hsp对·OH自由基清除作用比较结果.
从图3可见,在实验浓度范围内,Hsp对·OH自由基有较好的清除作用,清除率随浓度的增大而变大,呈现一定的量效关系.Hsp-Cu对·OH具有一定的清除能力,但整体表现Hsp-Cu对·OH的清除能力明显不如Hsp.
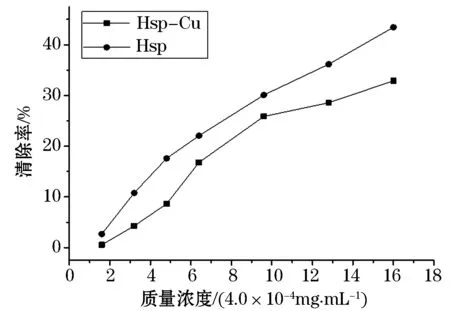
图3 Hsp-Cu及Hsp对羟基自由基的清除作用
2.4 Hsp-Cu及Hsp对O2-·的清除作用
在本实验测试条件下测得不加待测样品时邻苯三酚自氧化速率v0=151×10-5s-1.表1是邻苯三酚在不同质量浓度Hsp-Cu(以Hsp的含量计)及Hsp存在下的自氧化速率.
表1 不同质量浓度Hsp-Cu及Hsp存在下邻苯三酚自氧化速率 (vc×10-5·s-1)

质量浓度/(×4.0×10-3mg·mL-1)2.04.06.08.010.012.016.020.0Hsp146144140135128120110101Hsp-Cu189202209212208194198218
从表1可见,实验浓度下,Hsp使邻苯三酚自氧化速率vc均比v0小,且vc随Hsp质量浓度增大而减小,说明Hsp对O2-·具有明显的清除能力,随着浓度的增大清除效果增强.但Hsp-Cu却在邻苯三酚自氧化过程中,vc均比v0大,起到加速氧化的作用,低浓度下,vc随Hsp-Cu质量浓度增大而增大;高浓度下,关系不稳定,总之,Hsp-Cu在邻苯三酚自氧化体系中起到了促氧化作用.
3 讨 论
橙皮素是一种二氢黄酮类化合物,从其结构来看,其清除自由基活性能力由5,7,3′位三个羟基提供.但由于4′位是-OCH3,所以3′-OH清除自由基的活性应该较弱.按文献分析,橙皮素清除自由基活性能力主要是由A环的5,7位羟基提供的,且A环5-OH对抗氧化活性贡献较大[8].当5-OH和4-C=O共同与Cu2+发生配位形成橙皮素铜(Ⅱ)配合物后,体系供氢能力减弱,配合物若共面性不强,供电子能力也减弱,所以其清除自由基活性降低;另外,由于配合物不稳定,在实验体系中配合物中解离出的Cu2+也会降低体系对DPPH·和·OH的清除能力,这一点与文献相符[9].至于橙皮素铜(Ⅱ)配合物加速邻苯三酚自氧化过程,可能是解离出的Cu2+催化邻苯三酚自氧化起了主导作用[10-11],也可能是Cu2+对橙皮素起到促氧化作用[4],具体机理有待进一步研究.可见,Cu2+的引入,降低了橙皮素的抗氧化活性,甚至可能促进氧化.因此,橙皮素作为抗氧化剂应用于食品或药品时,应尽量避免与Cu2+接触,以免生成配合物而影响其抗氧化能力.
[1] CAI Y, Q LUO, SUN M,etal. Antioxidant activity and phenolic compounds of112 traditional Chinese medicinal plants associated with anticancer [J]. Life Sciences, 2004, 74(17): 2157-2184.
[2] 徐 春, 徐萌萌, 王建芳, 等. 橙皮素的药效研究及应用[J]. 天然产物分离, 2006, 4(6): 1-4.
[3] 李万立, 罗海吉. 微量元素铜与人类疾病关系的研究进展[J]. 微量元素与健康研究, 2008, 25(1): 62-65.
[4] 谭 君, 王伯初, 祝连彩. 槲皮素铜(II)配合物清除自由基活性的研究[J]. 时珍国医国药, 2007, 18(4): 800-801.
[5] 任志秋, 陈 平. 橙皮苷锌配合物合成及清除自由基能力的研究[J].哈尔滨商业大学学报:自然科学版, 2009, 25(6): 688-693.
[6] 龚金炎, 洪 辉, 吴晓琴, 等. 黄酮类化合物的促氧化作用及其细胞毒性研究进展[J]. 中草药, 2008, 39(12): 1905-1909.
[7] 邹淑君, 于子惠, 许树军, 等. 橙皮苷及橙皮素清除自由基活性的研究[J]. 中医药学报, 2013, 41(1): 65-67.
[8] 冯 涛, 庄海宁. 黄酮类化合物结构特征与抗氧化性关系研究进展[J]. 粮食与油脂, 2008(10): 8-11.
[9] 闫家凯, 张国文, 周 佳, 等. 不同因素对夏枯草总黄酮稳定性及DPPH自由基清除活性的影响[J]. 南昌大学学报(理科版), 2012, 36(4): 341-346.
[10] 刘杏恋, 孙领霞, 王春霞, 等. 金属离子对连苯三酚自氧化法测SOD活性的干扰及消除[J]. 河北医科大学学报, 1997, 18(6): 346-348.
[11] 徐 阳,邹 翔,曲中原,等.天然药物有效成分抗氧化作用及机制研究[J]. 哈尔滨商业大学学报:自然科学版,2015,31(3):259-262.
Study on effect of copper (II) ion on radical scavenging of hesperetin
ZOU Shu-jun, XU Shu-jun, ZHANG Lei, XU Yang
(School of Pharmacy, Heilongjiang University of Traditional Chinese Medicine, Harbin 150040, China)
To study the affection of Copper (II) ions on radical scavenging of hesperetin. Unstable hesperetin-copper (II) complex was generated when hesperetin was mixed with copper (II) chloride dihydrate. By the contrast tests on the scavenging reaction to DPPH radical, hydroxyl radical (·OH), and superoxide free radical (O2-·) of hesperetin-copper (II) complex and hesperetin, proves that the scavenging activity of DPPH·and·OH of hesperetin-copper (II) complex was weaker than that of hesperetin. The hesperetin-copper (II) complex can’t scavenge O2-·showing accelerated oxidation in the process of pyrogallol autoxidation. Hesperetin was used as an antioxidant, cannot coexist with Cu2+, so as not to affect the antioxidant capacity of hesperetin.
hesperetin; copper (II) ion; free radical; scavenging
2014-11-28.
黑龙江省教育厅资助项目(12531648);黑龙江中医药大学校基金科研课题(201103)
邹淑君(1974-),女,博士,副教授,研究方向:药物分析研究.
R285
A
1672-0946(2015)05-0527-03

