补肾健骨方治疗慢性肾脏病-矿物质和骨异常35例临床观察
于思明,裴春鹏,代丽娟,郭丹丹
(1.黑龙江中医药大学附属第一医院,黑龙江 哈尔滨 150040;2.黑龙江中医药大学附属第二医院,黑龙江 哈尔滨 150001)
随着现代医学的不断进步,慢性肾脏病(chronic kidney disease,CKD)患者的生存时间逐渐延长,其矿物质和骨代谢紊乱变得十分常见,这一代谢紊乱综合征以往曾被称为肾性骨营养不良(renal osteodystrophy)或肾性骨病(renal osteopathy)。鉴于这些名词已不能准确反映这一组代谢紊乱综合征的特点,2009年,改善全球肾脏病预后组织(KDIGO)将其重新命名为慢性肾脏病-矿物质和骨异常(CKD-MBD),以期加强医务工作者对慢性肾脏病患者矿物质代谢异常、骨异常和异位钙化三方面的整体认识和把握。我国目前对CKD-MBD的控制形势不容乐观[1],中医药治疗CKD的作用已得到广泛认可,但防治CKD-MBD的研究尚处于起步阶段。本课题组以中医学“肾主骨”理论为指导,观察补肾健骨方加减对CKD-MBD的治疗作用,现报道如下。
1 资料与方法
1.1 一般资料
70例患者来自黑龙江中医药大学附属第一医院肾病科2014年1月~2015年3月门诊及住院患者,按随机数字表法分为治疗组与对照组、各35例。治疗组中男性15例,女性20例;年龄32~74岁,平均年龄(52.1±11.4)岁;病程5~17年,平均病程(10.3±3.2)年;原发病为慢性肾炎17例,糖尿病肾病10例,高血压肾病5例,慢性间质性肾炎2例,多囊肾1例。对照组中男性16例,女性19例;年龄30~71岁,平均年龄(51.6±12.3)岁;病程4~18年,平均病程(9.3±3.8)年;原发病为慢性肾炎15例,糖尿病肾病9例,高血压肾病6例,慢性间质性肾炎3例,慢性肾盂肾炎1例,多囊肾1例。两组患者在性别、年龄、病程、基础疾病等方面比较,差异无统计学意义(P>0.05),具有可比性。
1.2 西医诊断标准
慢性肾脏病诊断标准参照美国肾脏基金会的CKD诊断和分期标准,选取CKD分期在3~4期,GFR 44~15ml/(min·1.73m2);具有肾性骨病症状:全身骨痛和(或)压痛、叩击痛;骨骼畸形及其相应体征;病理性骨折及相应体征。
1.3 中医辨证标准
中医辨证属肾精不足证者,参照《中药新药临床研究指导原则》。主症:腰膝酸软,下肢痿弱,耳鸣耳聋,心烦失眠,手足抽搐,骨痛。次症:畏寒喜暖,夜尿清长,大便稀溏。舌脉:舌红苔薄,脉细弱。
1.4 排除标准
排除原发性甲状旁腺功能亢进、原发性骨质疏松、其他原因引起的骨质疏松、其他原因引起的代谢性骨病者;合并心、脑、肝、血液系统等严重原发性疾病者;透析及肾移植患者;近期存在难以控制的感染者;行甲状腺全切术或次全切术者。
1.5 治疗方法
所有患者均接受常规治疗,包括低盐、低磷、低蛋白饮食,降压,纠正贫血、纠正酸碱失衡及离子紊乱等,并口服骨化三醇0.5μg/d。治疗组在常规治疗基础上,给予补肾健骨方加减治疗。处方:盐杜仲15g,怀牛膝15g,熟大黄15g,生牡蛎30g。气虚者加黄芪20g,党参20g;血瘀者加三七粉5g,丹参15g;水肿者加茯苓30g,猪苓15g;湿热者加积雪草20g,蒲公英30g;痰饮者加姜半夏15g,陈皮15g;湿浊中阻者加藿香15g,佩兰15g。由黑龙江中医药大学附属第一医院制剂室进行统一煎煮,每日1剂,早晚餐后15~30min内温服,连续治疗4周。
1.6 观察指标
1.6.1 疗效判定标准
疗效判定标准参照《中药新药临床研究指导原则》[4]制定。显效:临床症状积分减少≥60%,Scr降低≥20%;有效:临床症状积分减少≥30%,Scr降低≥10%;稳定:临床症状有所改善,积分减少<30%,Scr无增加或降低<10%;无效:临床症状无改善或加重,Scr增加。
1.6.2 生化指标与全段甲状旁腺激素
观察两组患者治疗前后血清肌酐(Scr)、尿素氮(BUN)、尿酸(UA)、内生肌酐清除率(CCr)、Ca、P、全段甲状旁腺激素(iPTH)的变化。
1.7 统计学处理
采用SPSS 17.0统计学软件进行统计学分析,计量资料以()表示。组内比较用配对t检验,组间比较用两样本t检验,计数资料用χ2检验。
2 结果
2.1 两组患者疗效比较
治疗组总有效率为82.9%,对照组总有效率为65.7%,两组疗效比较差异具有统计学意义(P<0.05),见表1。
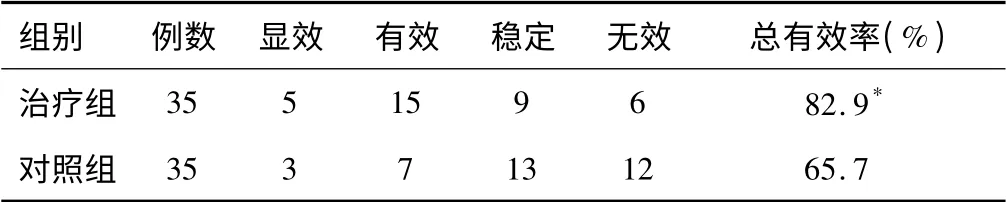
表1 两组患者疗效比较
2.2 两组患者治疗前后肾功能指标比较
治疗后,两组患者BUN、Scr、UA水平均低于治疗前,差异具有统计学意义(P<0.05或P<0.01),治疗组BUN水平低于对照组(P<0.05),两组患者Scr、UA水平比较差异无统计学意义(P>0.05)。两组治疗后GFR水平均上升,与同组治疗前比较差异具有统计学意义(P<0.05),组间比较差异无统计学意义(P>0.05),见表2。
2.3 两组患者治疗前后血清Ca、P、iPTH水平比较
两组患者治疗后血清Ca水平较治疗前升高(P<0.01),组间比较差异无统计学意义(P>0.05);两组患者血清P、iPTH水平低于治疗前,差异具有统计学意义(P<0.05,P<0.01),治疗组优于对照组(P<0.05),见表3。
表2 两组患者治疗前后肾功指标变化比较()

表2 两组患者治疗前后肾功指标变化比较()
注:与同组治疗前比较,*P<0.05,**P<0.01;与对照组比较,△P<0.05。
组别 例数 BUN(mmol/L) Scr(μmol/L) UA(mmol/L) CCr(ml/min·1.73m2)治疗组 35 治疗前 17.85±3.07 466.22±57.10 529.76±67.21 23.15±4.26治疗后 10.37±2.55**△ 370.65±44.97** 438.33±31.30** 30.09±5.43*对照组 35 治疗前 18.32±2.84 469.30±50.12 540.40±61.83 22.23±4.90治疗后 14.78±3.42* 384.12±52.49** 444.56±50.07** 28.12±5.61*
表3 两组患者治疗前后血清Ca、P、iPTH变化比较()

表3 两组患者治疗前后血清Ca、P、iPTH变化比较()
注:与同组治疗前比较,*P<0.05,**P<0.01;与对照组比较,△P<0.05。
组别 例数 Ca(mmol/L) P(mmol/L) iPTH(pg/ml)治疗组 30 治疗前1.81±0.33 1.91±0.26 215.20±27.33治疗后 2.18±0.25** 1.46±0.28**△ 92.08±25.41**△对照组 30 治疗前 1.84±0.27 1.93±0.34 211.54±31.36治疗后 2.12±0.23** 1.75±0.25* 145.20±7.32**
3 讨论
从肾性骨病的概念发展到慢性肾脏病-矿物质和骨异常是近年肾脏病领域的一个重要进展,其意义在于不再把肾性骨病仅仅视为慢性肾脏病的并发症之一,而是把慢性肾脏病的矿物质代谢异常、骨异常和血管、软组织钙化作为一个整体来把握,这一理念与中医学的整体观念不谋而合。CKD-MBD是CKD患者常见而严重的并发症,包括钙、磷、甲状旁腺激素和维生素D代谢异常;骨的转化、矿化、体积、线性生长和强度异常;血管或其他软组织钙化[2]。目前对这一疾病的干预方法有限,如采用饮食控制、磷结合剂和活性维生素D制剂等,但其疗效有限,在缓解患者的临床症状方面常不能获得满意疗效。
“肾主骨”是中医学的重要理论。肾藏精,精生髓,髓滋养骨骼。现代医学研究结果也提示,肾与骨之间存在着密切的联系,其联系是通过肾细胞与骨细胞的“通讯”来实现的[3]。骨形态形成蛋白(BMP)在骨骼生成和肾脏发育中均发挥重要作用,慢性肾脏病时BMP减少并出现骨骼病变,而BMP对慢性肾脏病及其骨病可发挥显著的治疗作用,这与中医学“肾主骨”的理论基本一致,进一步证实了从肾论治CKD-MBD的可行性。CKD-MBD的临床表现与中医学对“骨痿”的论述相符合,其基本病机为肾精不足,骨髓不充,骨失所养。如《素问·痿论》所言的“骨枯而髓减,发为骨痿”。此外,肝肾同源,肝主筋、肾主骨、二者直接相关且相互滋生,亦不应忽视。因慢性肾脏病患者多兼有湿浊、瘀血、痰饮、湿热等病理因素,故以单纯的补益肝肾、强壮筋骨法治疗CKD-MBD常疗效欠佳,还需针对上述病理因素辅以通腑泄浊、清利湿热、活血化瘀、芳化湿浊等治疗方法,才能取得较好的治疗效果。
本研究采用的补肾健骨基本方,是我院肾病科治疗肾性骨病和钙磷代谢紊乱的经验方,方中以杜仲、牛膝药对补肝肾、强筋骨以治本,熟大黄排毒泄浊以治标;生牡蛎滋阴潜阳,且可提供钙盐、直接促进骨形成。在此基础上再视湿浊、瘀血、痰饮、湿热等病理因素情况进行加减,全方标本兼治,共奏补肾健骨之功。本研究对补肾健骨方进行了为期4周的临床观察,其结果显示,补肾健骨方对缓解CKD-MBD患者的临床症状具有一定作用,在降低患者BUN水平方面优于对照组,可能与其排毒泄浊作用有关。在钙磷代谢方面,治疗组与对照组疗后的血钙水平无明显差异,但治疗组能更好的控制CKD患者的血磷水平,同时降低iPTH,展现了其调节钙磷代谢的优势,值得进一步研究。
[1]刘志红,李贵森.重视慢性肾脏病-矿物质和骨异常的诊断和治疗[J].肾脏病与透析移植杂志,2013,22(6):501-503.
[2]陈孜瑾,陈楠.从KDOQI到KDIGO指南解读慢性肾脏病矿物质和骨异常[J].中国实用内科杂志,2011,31(12):927-929.
[3]郑法雷,袁群生.肾-骨对话和肾性骨病:机制与治疗进展[J].中国中西医结合肾病杂志,2008,9(2):95-97.

