利伐沙班片的制备及处方优化
钟益玮,胡 翔,陆 阳
(1.同济大学附属第一妇婴保健院药剂科,上海 200040;2.上海众胜医药科技有限公司,上海 201203)
利伐沙班片的制备及处方优化
钟益玮1,胡翔2,陆阳2
(1.同济大学附属第一妇婴保健院药剂科,上海200040;2.上海众胜医药科技有限公司,上海201203)
摘要:目的制备利伐沙班片剂,优选适合中试生产的最佳处方。 方法通过设计不同处方,对增溶剂、崩解剂、黏合剂、填充剂的用量及工艺进行考察,并进行了中试三批放大,测定在四种溶出介质中的溶出曲线、含量均匀度和有关物质等指标。结果用利伐沙班为主药,以乳糖、微晶纤维素为填充剂,以十二烷基硫酸钠为增溶剂,以交联羧甲基纤维素钠为崩解剂,以羟丙基甲基纤维素为黏合剂、以硬脂酸镁为润滑剂,以胃溶型薄膜包衣预混剂为包衣材料,制得利伐沙班片。 结论该制剂工艺稳定,制得利伐沙班片(10 mg)与原研市售品溶出行为相似,质量符合规定。
关键词:利伐沙班片;处方优化
利伐沙班(Rivaroxaban)是全球第一个口服的直接Xa因子抑制剂,由拜耳/强生公司研制开发。2008年10月,在加拿大和欧盟获得批准上市,商品名为Xarelto。2009年3月,美国食品药品监督管理局(FDA)批准在美国上市,2009年6月18日中国食品药品监督管理局(SFDA)批准进口中国,商品名为拜瑞妥[1-2]。
利伐沙班的适应证为用于择期髋关节或膝关节置换手术成年患者,以预防静脉血栓形成(VTE),也可用于预防非瓣膜性心房纤颤患者脑卒中和非中枢神经系统性栓塞,降低冠状动脉综合征复发的风险等。和传统的抗凝药肝素和华法林相比,利伐沙班作为口服制剂,只需每日服用一次即可达到治疗效果,服用方便,起效迅速,无需调整剂量,无需常规监测,可显著减少静脉血栓的发生,且不增加出血发生率,安全性较高[1,3-4]。
一项前瞻性、随机、双盲、双模拟、平行组对照、多中心临床试验,纳入受试者14 264例,利伐沙班组受试者每日1次口服利伐沙班和安慰剂量的华法林,阳性对照组受试者每日1次口服标准剂量华法林和安慰剂量的利伐沙班,结果显示,与阳性对照组相比,利伐沙班组受试者的中风和非中枢神经系统的全身性栓塞发生率降低21%,而临床重大出血事件发生率相当,但颅内出血发生率、重要器官出血发生率以及出血相关病死率均显著降低[5]。
本品国内至今为止尚无厂家生产,因此研发利伐沙班片剂具有广阔的市场前景,对于填补国内市场,丰富临床用药,降低医疗成本具有重要意义,必将产生巨大的社会效益和经济效益。
1试剂与仪器
1.1试药利伐沙班(批号:140201,上海众胜医药科技有限公司提供),乳糖(批号:8511112810,北京凤礼精求商贸有限责任公司提供),微晶纤维素(批号:130902)、羟丙甲纤维素(批号:130211)、十二烷基硫酸钠(批号:131101)、交联羧甲基纤维素钠(批号:131201)、硬脂酸镁(批号:131129)均由安徽山河药用辅料股份有限公司提供,欧巴代20A17431(批号:THL25570,上海卡乐康包衣技术有限公司) ,利伐沙班对照品(上海众胜医药科技有限公司自制),乙腈为色谱纯,其他试剂均为试剂纯。
1.2仪器智能溶出仪(天津大学无线电厂 D- 800LS),分析天平(赛多利斯科学仪器(北京)有限公司 BS124S),pH计(梅特勒-托利多国际股份有限公司 SG8),高效液相色谱仪(戴安中国公司 UItiMate 3000)。
2处方筛选及制备工艺
2.1溶出度测定方法的建立[6]取本品,按照溶出度测定法(中国药典2010版二部附录XC第二法)测定,以pH 4.5醋酸盐缓冲液900 mL为溶剂,转速为每分钟75转,依法操作,分别在5, 10, 15, 30, 45 min,取溶液10 mL,滤过,并即时在操作容器中补充等量溶剂。取续滤液,照高效液相色谱法(中国药典2010年版二部附录VD)记录色谱图,按外标法计算出每片的溶出量。
色谱条件:戴安高效液相色谱仪:UItiMate 3000。色谱柱:Gemini-NX C18250 mm×4.6 mm 菲罗门科学仪器有限公司。流动相:乙腈-水(50∶50)。检测波长:250 nm。流速:1.0 mL·min-1。柱温:40℃。进样体积:10 μL。
2.2市售制剂溶出度的测定取利伐沙班片市售制剂“拜瑞妥” 6片,分别称重。照溶出度测定方法测定溶出度,作为自制片剂的参考。溶出度数据见表1,溶出度曲线见图1。

表1 市售制剂溶出度数据
从图1可以看出,市售制剂在15 min内即释放完全,且释放平稳。
2.3处方设计利伐沙班为白色至淡黄色粉末;无臭,无味。利伐沙班微溶于有机溶剂(比如丙酮、聚乙二醇400),几乎不溶于水。
“拜瑞妥”使用说明书表明其处方中辅料有乳糖、微晶纤维素、交联羧甲基纤维素钠、羟丙基甲基纤维素、十二烷基硫酸钠、硬脂酸镁。薄膜包衣材料包括红色三氧化二铁,羟丙甲纤维素(15cp),聚乙二醇3350,二氧化钛。
2.4处方筛选通过查阅相关文献与资料[7-10],根据主药与辅料的性质,我们进行了利伐沙班片的处方筛选和工艺研究,测定的关键指标为溶出曲线、含量均匀度、含量。自制品与原研市售品在四种溶出介质中的溶出曲线需相似,即自制品在四种溶出介质中的溶出曲线15 min时的累积溶出量均大于85%;含量均匀度和含量符合规定。
我们设计出 4 个处方(表 2),分别制备 200 片利伐沙班片剂,考察不同的填充剂用量对片剂外观,硬度,脆碎度的影响。
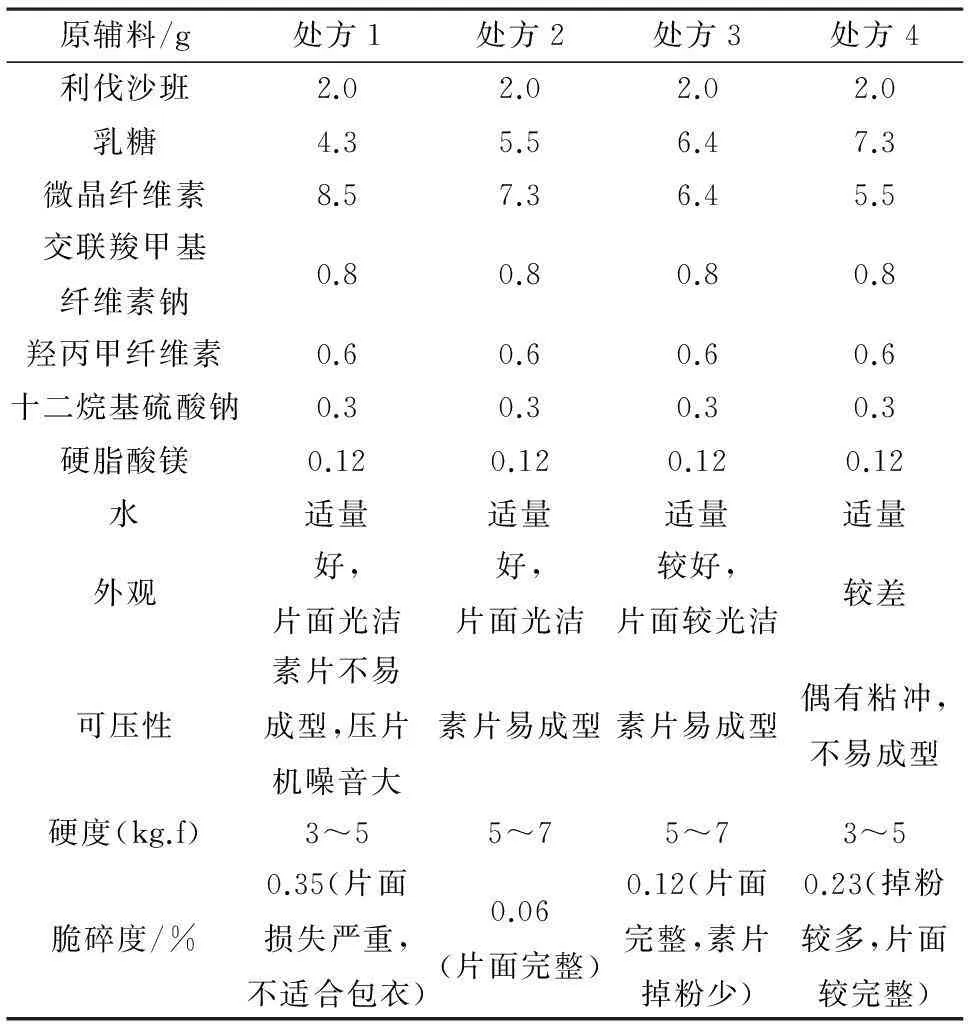
表2 填充剂用量的筛选
制备工艺:将主药过200目筛,各辅料过100目筛备用,称取处方量主药和处方量辅料,采用等量递增方法混合均匀。用水做润湿剂进行湿法制粒,60℃干燥,24目整粒,加入处方量的硬脂酸镁,混匀压片即得。
结果显示:处方2制得的素片外观好,片面光洁,可压性好,硬度和脆碎度都好,因此选择处方2作为进一步研究的处方。
在处方2的基础上我们又设计出 4 个处方(表 3),分别制备 200 片利伐沙班片剂,考察不同的崩解剂和不同的黏合剂对片剂外观及溶出行为的影响。
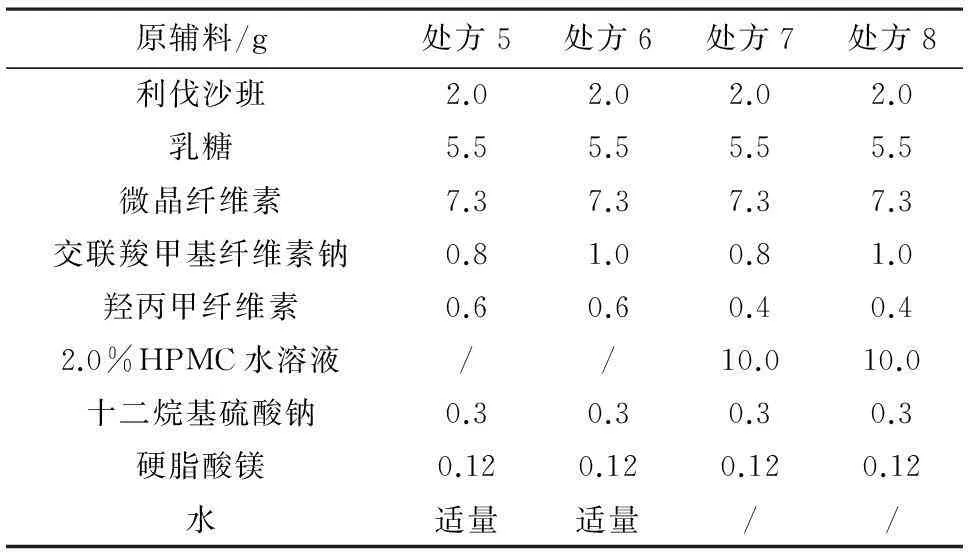
表3 崩解剂和黏合剂用量的筛选
制备工艺:将主药过200目筛,各辅料过100目筛备用,称取处方量主药和处方量辅料,采用等量递增方法混合均匀。处方7和处方8中部分羟丙甲纤维素溶于适量水中做黏合剂,湿法制粒后60℃干燥,24目整粒,加入处方量的硬脂酸镁,混匀压片即得。
分别对所制备的颗粒的流动性、水分及素片的外观、脆碎度、崩解时限、溶出度等基本指标进行重点评价,以筛选出较好的处方,结果见表4。

表4 利伐沙班崩解剂与黏合剂用量的处方评价结果
以上结果显示:四个处方比较外观、流动性、脆碎度、溶出度等指标,处方6的颗粒较散,素片可压性差。处方7的溶出度较差,因此,选择处方5和处方8进行溶出曲线的比较,见表5和表6。
经在pH1.0盐酸溶液、pH4.5醋酸盐缓冲溶液、pH6.8磷酸盐缓冲溶液和水中测定溶出曲线,相似因子取5、10、15 min三个点进行比较。

表5 处方5溶出曲线检查结果

表6 处方8溶出曲线检查结果
结果表明:处方5在30 min基本溶出,15 min累积溶出度小于85%,处方8在15 min时基本溶出完全,且相似因子大于50%,因此综合考虑选择处方8作为进一步研究的处方。
在处方8 的基础上筛选助溶剂的用量对处方进行优化,设计了两个处方,见表7。

表7 助溶剂用量的优化
经在pH1.0盐酸溶液、pH4.5醋酸盐缓冲溶液、pH6.8磷酸盐缓冲溶液和水中测定两个处方的溶出曲线,相似因子取5、10、15 min三个点进行比较,并与处方8比较,结果见表8和比表9。

表8 处方9溶出曲线检查结果

表9 处方10溶出曲线检查结果
结果表明:处方9与处方10的 溶出曲线都较好,15 min内基本溶出完全,处方10的相似因子在各个溶出介质中都是最高的,溶出行为与市售制剂最相似。综合考虑选择处方10为最优处方。
将处方10制备成1 000片,并包衣,见表10。

表10 利伐沙班包衣片处方
注:欧巴代用量为素片重量的3%,包衣液浓度为10.0%。
包衣液配制方法:按处方量称取水溶液,在搅拌状态下缓缓加入处方量的胃溶型薄膜包衣预混剂,继续搅拌45 min以上,配成浓度约为10%的包衣液。
经在pH1.0盐酸溶液、pH4.5醋酸盐缓冲溶液、pH6.8磷酸盐缓冲溶液和水中测定溶出曲线,相似因子取5、10、15 min三个点进行比较,15 min累积溶出度均达到85%,含量均匀度符合规定。

表11 包衣片含量均匀度和有关物质

表12 包衣片溶出曲线检查结果

表13 利伐沙班片中试三批试验结果
从图2中可以看出利伐沙班片在不同pH值条件下15 min中的累积溶出度均达到85%以上,与市售药品四条溶出曲线相似,含量均匀度含量和有关物质符合规定,将处方10的包衣片进行影响因素试验,在高温(60℃)、高湿(75%)和光照条件(4500、500Lx)下进行实验,结果表明:5、10 d下的样品与0 d的样品相比,性状、有关物质、溶出度和含量均匀度无明显变化,因此确定处方10为利伐沙班片的处方。
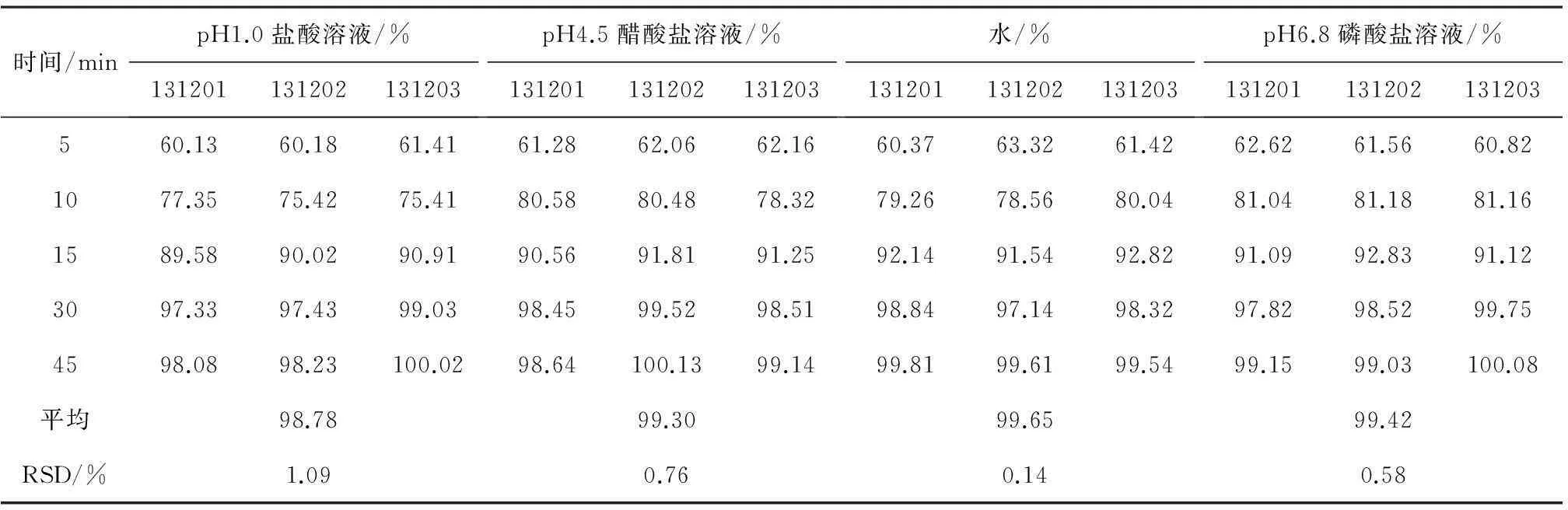
表14 利伐沙班片中试三批溶出试验结果
3处方的中试验证
对初步确定的处方按照每批1万片的规模进行中试放大,试制3批,进行性状、溶出度、有关物质和含量含量均匀度的考察。结果见表13~15。结论:该处方工艺重现性好,制成的成品符合要求。最终确定利伐沙班片的处方见表15。

表15 利伐沙班片处方
注:欧巴代用量为素片重量的3.0%,制成配制包衣液浓度为10.0% 。
4讨论
我们参照利伐沙班片的原研处方,通过设计不同处方,筛选了填充剂、崩解剂、黏合剂和增溶剂的用量,并通过在四种溶出介质中的溶出曲线对比,确定了最终的处方:以乳糖、微晶纤维素为填充剂,以十二烷基硫酸钠为增溶剂、以交联羧甲基纤维素钠为崩解剂,以羟丙甲纤维素为黏合剂、以硬脂酸镁为润滑剂,以胃溶型薄膜包衣预混剂为包衣材料。
通过三批中试工艺放大,验证了本品处方工艺重现性良好,制成的成品符合要求,自制品和原研市售品在四种溶出介质中的溶出曲线相似,表明了本品处方和制备工艺适合大生产。
参考文献:
[1]拜耳医药保健股份公司.利伐沙班片说明书,2013.
[2]符坚,朱小华,李强,等.利伐沙班合成工艺改进[J].安徽医药,2013,17(6):917-919.
[3]王秀,夏泉.抗凝血药物临床应用的现状及研究进展[J].安徽医药,2011,15(10):1189-1192.
[4]张石革.凝血Xa因子直接抑制剂的研究进展与临床应用评价[J].中国医院用药评价与分析,13(9):782-786.
[5]范鸣.新型口服抗凝药利伐沙班在欧美申报用于预防中风[J].药学进展,2011,35(4):191.
[6]国家食品药品监督管理局进口药品注册标准.利伐沙班片[S].JX20080077.
[7]K·本克.能够口服和活性成分快速释放的固体药物剂型. CN101321517[P].2006-09-21.
[8]蔡进,吉民,徐春涛,等.一种利伐沙班口服微球制剂. CN,103550166[P].2013-10-31.
[9]K·本克.用于制备可口腔给药的固态药物组合物的方法. CN,1886120[P].2004-11-13.
[10] K·本克,J 亨克.具改进的释放性且含有RIVAROXABAN的可口腔给药的固态药物给药剂型. CN101128205[P].2005-12-13.
Preparation and formulation optimization of Rivaroxaban tablets
ZHONG Yi-wei1,HU Xiang2,LU Yang2
(1.DepartmentofPharmacy,ShanghaiFirstMaternityandInfantHealthHospitalAffiliatedtoTongjiUniversity,
Shanghai200040,China;2.ShanghaiZingsumPharm-techCo.,Ltd,Shanghai201203,China)
Abstract:ObjectiveTo prepare Rivaroxaban tablets and choose the best prescription for pilot scale production.MethodsThrough the design of different prescriptions and the selection of the amount of solubilizers, disintegrants, fillers and formulation process, three batches of test product in pilot scale were prepared according to the optimized formulation. The dissolution curve, content uniformity, related substances and other indicators tested in four kinds of dissolution media were determined correspondingly.ResultsRivaroxaban tablets were formulated with Rivaroxaban as the main drug,lactose and microcrystallinecellulose as fillers, sodium lauryl sulfate as solubilizer, roscarmellose sodium as disintegrant, stearic magnesium as lubricant, film coating premixed adjuvant(gastric-dissolving type)as the coating material.ConclusionThe present formulation process of newly developed Rivaroxaban tablets(10 mg)was stable. The dissolution behavior of newly developed formulation was similar to that of the originally commercial product. The quality complies with the provisions.
Key words:Rivaroxaban tablets;formulation optimization
(收稿日期:2014-07-11,修回日期:2014-10-21)
通信作者:胡翔,男,工程师,研究方向:新药研发, E-mail:dmyykj@163.com
doi:10.3969/j.issn.1009-6469.2015.02.006

