多发性硬化的联合治疗进展
冯美娜(综述),陈玉华(审校)
(长江航运总医院神经内科,武汉 430015)
多发性硬化的联合治疗进展
冯美娜※(综述),陈玉华(审校)
(长江航运总医院神经内科,武汉 430015)
摘要:免疫调节药物在治疗多发性硬化上取得了很好的效果,降低了复发率,延缓了残疾进展,减少了磁共振成像病灶数量或缩小了其体积。但仅部分有效,许多患者在服药期间疾病仍快速进展,故有学者提出联合用药方案。许多临床试验用两种或两种以上不同机制的药物治疗多发性硬化患者,以此来评定其效果与安全性。该文就多发性硬化联合治疗的合理性及临床研究现状等进行综述。
关键词:多发性硬化;联合用药;免疫调节药;免疫抑制剂
多发性硬化是以中枢神经系统白质脱髓鞘病变为特点的自身免疫性疾病,遗传易患个体与环境因素共同作用,病理上以髓鞘的炎性损伤伴不同程度的轴索丢失为特点。目前尚无法治愈,治疗目标仅为通过改变疾病进程,减轻疾病症状而提高患者的生活质量。免疫调节药物(如一线药干扰素β-1α、干扰素β-1b、醋酸格拉默等;二线药那他珠单抗、米托葱醌等)的出现,使多发性硬化的治疗有了突破性进展。但这些药物仅部分有效,大多数患者在服药期间仍有病情进展,故有学者提出联合治疗方案。现就多发性硬化联合治疗的合理性及研究现状等进行综述。
1联合治疗的合理性
多年来,联合治疗已成功用于肿瘤、感染性疾病以及高血压、糖尿病等常见病的治疗,如3种药物联合应用治疗人类免疫缺陷病毒感染时,病毒的数量下降到可检测水平以下,并戏剧性地改变了疾病病程和患者的预后[1]。多发性硬化发病机制复杂,涉及遗传、环境因素、病毒感染等,病理过程包括炎症反应,T细胞、B细胞和自然杀伤细胞介导机制及脱髓鞘、轴突丢失、神经变性、髓鞘再生等。多发性硬化不是单一因素疾病,要注意临床、遗传学、影像学及病理学特征[2]。对大量活动的脱髓鞘损伤的研究分析,基于斑块形成的脱髓鞘、少突胶质细胞病理的范围和模式、免疫球蛋白沉积和补体激活的证据以及髓鞘脂蛋白丢失的模式,将损伤分为巨噬细胞联合性脱髓鞘、抗体/补体联合性脱髓鞘、末梢濒死的少突胶质细胞病和原发性少突胶质细胞变性[1],说明不同患者之间的发病机制存在不同质性,因而对药物治疗的反应亦存在差异。在疾病发展过程中也存在高度的变异,很多复发-缓解型多发性硬化(relapsing-remitting multiple sclerosis,RRMS)患者在数十年内最终发展为继发进展型多发性硬化(secondary progressive multiple sclerosis,SPMS),对同一患者一种有效的药物若干年后可能失效。此外,多发性硬化临床分型除RRMS、SPMS、原发进展型多发性硬化、进展复发型多发性硬化4种常见类型外,还有良性多发性硬化、爆发性多发性硬化(又称恶性型或变异型)等,说明对多发性硬化患者可以针对不同的发病机制联合用药。许多患者已使用过一种或多种药物治疗,有时药效并不理想,一线药物干扰素和醋酸格拉默也仅能降低30%的复发率[3-5]。目前的治疗方案受用药途径和局部或全身性不良反应的限制,因此迫切需要更有效且耐受良好的治疗方案。
2研究现状
治疗多发性硬化的药物很多,可选择两种或两种以上不同作用机制或有协同作用的药物联合治疗复发率较高、残疾进展较快、单药治疗不理想的多发性硬化。目前临床研究多以一线药物干扰素或醋酸格拉默联合其他药物,以复发率、磁共振成像(magnetic resonance imaging,MRI)增强像病灶数量、T2像新发病灶数量或体积变化及扩展残疾状况评分来评价联合用药的有效性。临床研究中合用的药物大致分为3类:①与糖皮质激素合用;②与免疫抑制剂合用(如硫唑嘌呤、环磷酰胺、米托葱醌、甲氨蝶呤、麦考酚酸莫酯等);③与那他珠单抗合用;此外,还有与阿托伐他汀、多西环素、米诺环素等合用,以及一种免疫调节药与一种神经保护药合用。有荟萃分析显示,他汀类药物与干扰素合用治疗RRMS并未显著降低复发率及残疾进展[6]。
2.1与糖皮质激素合用干扰素与激素合用效果理想,两者可能有协同作用。一项随机安慰剂对照的临床试验纳入130例 RRMS患者,治疗前这些患者1年内至少复发1次,皮下注射干扰素1α 44 μg,每周3次,口服甲泼尼龙200 mg/d,每月连续口服5 d,至少联合用药96周;服用甲泼尼龙组与安慰剂组相比复发率明显降低(82%比0.34%,P<0.0001),残疾进展两组无明显区别,T2像病灶体积甲泼尼龙组明显缩小,但由于激素的不良反应甲泼尼龙组有27%的患者中途退出,而安慰剂组仅3%中途退出[7]。在另一项研究中亦得到相似结果,甲泼尼龙组在复发率、MRI、多发性硬化功能复合量表证实两者合用的有效性,但由于激素的不良反应中途退出的患者也较多,给临床数据、长期风险评估带来困难[8]。
2.2与免疫抑制剂合用免疫抑制剂又叫细胞毒性药物,不良反应较大,对多发性硬化的治疗效果好,但不能长期应用。有学者提出诱导-维持治疗方案来控制疾病进展,即在多发性硬化的复发期病情恶化时可短时间应用免疫抑制药,随后用一线药维持[9-10]。一项随机对照试验评价米托葱醌短期治疗效果,诱导组55例患者每月接受米托葱醌治疗共6个月,随后用干扰素β-1b维持治疗;对照组54例患者每月接受干扰素β-1b和甲泼尼龙 1 g治疗6个月,之后干扰素β-1b维持治疗,观察3年。结果显示,残疾进展米托葱醌组相比对照组延长,年复发率明显降低[9]。此试验证明,米托葱醌可以控制疾病进展,在疾病恶化时可以短时间内加用,但没能证明维持治疗阶段是干扰素还是米托葱醌停药后的后续效应发挥作用。在与免疫抑制剂合用的试验中硫唑嘌呤是最常用的药物之一,试验结果较为乐观,显示了安全性和有效性[11-12]。Fernández等[11]观察了10例SPMS患者发现,硫唑嘌呤与干扰素β联用比单用干扰素β复发率降低了50%,T2病灶数也明显减少,唯一的不良反应是淋巴细胞数减少。另一项小型试验只观察了6例复发率很高的RRMS患者,观察6个月,硫唑嘌呤逐渐加量至2 mg/(kg·d),MRI增强像上新发病灶数量降低69%(P=0.002),但对复发率没有明显影响,且T2显示在联合用药期间仍不断有新发病灶,未观察到不良反应,且耐受性好[12]。此试验仅纳入6例患者没有说服力,为了更好地证明两药合用的有效性及安全性,需要大型的对照试验。另一项试验选取23例RRMS患者,之前以干扰素β-1α和硫唑嘌呤单药治疗效果不佳,然后两者合用观察2年,结果显示,T1、T2及增强像新发病灶数均明显低于之前的单药治疗,且无严重不良反应[13],表明两药合用可能有较高的安全性和有效性。
2.3与那他珠单抗合用在Rudick等[14]设计的Ⅲ期临床试验中,将1171例RRMS患者随机分为那他珠单抗组与安慰剂组,那他珠单抗组每周皮下注射干扰素β-1α,静脉注射那他珠单抗300 mg,每4周1次;安慰剂组每周皮下注射干扰素β-1α,静脉注射安慰剂300 mg,每4周1次,观察2年。结果显示,两者合用比单用干扰素在第1年和第2年复发率明显降低,其他临床评估、MRI结果亦支持合用效果优于单一用药,但在治疗过程中那他珠单抗组出现了2例进行性多灶性白质脑病患者。长期应用时应注意可能出现的不良反应,至今有超过数百例应用那他珠单抗并发进行性多灶性白质脑病的报道[15-18]。此试验证明了干扰素与那他珠单抗合用比单用干扰素有效,但未能回答有效性是仅来自那他珠单抗还是两者有协同作用。Polman等[19]的试验设计与之类似,也没有设计那他珠单抗单独用药组。Goodman等[20]设计了醋酸格拉默和那他珠单抗合用与单用醋酸格拉默疗效及安全性的评估,观察指标是新病灶的增加(MRI增强像与T2像上新发或原有病灶的扩大)、复发率、感染率等。结果显示,合用组新发病灶数量明显减少,复发率亦降低,且感染率、输液反应等两组无明显区别,没有发现多灶性白质脑病。此试验也同样没有设计那他珠单抗单独用药组。
此外,还有一线药合用的研究,如一项双盲、随机、安慰剂对照试验招募1008例RRMS患者评定干扰素β-1α与醋酸格拉默合用的有效性及安全性[21],实验结果较为乐观。各种联合用药试验详见表1和表2。
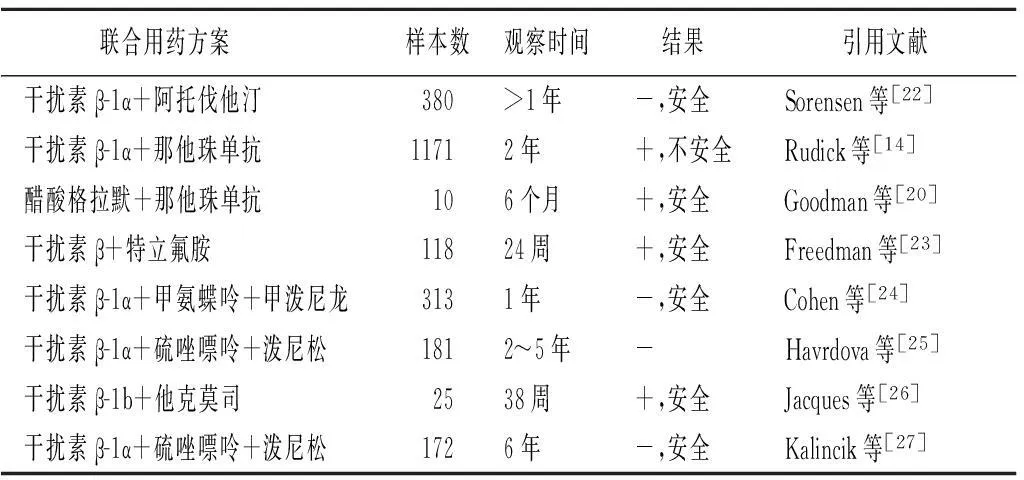
表1 联合用药小型临床试验
+:优于对照组,差异有统计学意义,有临床意义; -: 与对照组差异无统计学意义
+:优于对照组,差异有统计学意义,有临床意义; -: 与对照组差异无统计学意义

表2 一些大型的随机对照试验
SPMS:继发进展型多发性硬化;RRMS:复发-缓解型多发性硬化;+:优于对照组,差异有统计学意义,有临床意义; -:与对照组差异无统计学意义
3小结
近几年随着一些新药的上市,为联合治疗提供了条件,成为多发性硬化治疗领域的新亮点。联合用药是治疗顽固性疾病史上的必然过程,不仅可以更好地了解现存药物的机制,还可促进新药的研发。目前为止,大部分临床试验结果还是令人满意的。将来的临床试验应以多中心、随机双盲、安慰剂对照及患者治疗前基线大致平行来进行设计,尽快明确哪些药物联用有效、安全及耐受好。
参考文献
[1]王运良,娄季宇,谢鹏.多发性硬化的基础与临床[M].郑州:郑州大学出版社,2009:375-376.
[2]Hφglund RA,Maghazachi AA.Multiple sclerosis and the role of immune cells[J].World J Exp Med,2014,4(3):27-37.
[3]Milo R,Panitch H.Combination therapy in multiple sclerosis[J].J Neuroimmunol,2011,231(1/2):23-31.
[4]Rieckmann P.Concepts of induction and escalation therapy in multiple sclerosis[J].J Neurol Sci,2009,277 Suppl 1:S42-45.
[5]Costello K.Multiple sclerosis research:diagnostics,disease-modifying treatments,and emerging therapies[J].J Neurosci Nurs,2013,45 6 Suppl 1:S14-23.
[6]Bhardwaj S,Coleman CI,Sobieraj DM.Efficacy of statins in combination with interferon therapy in multiple sclerosis:a meta-analysis[J].Am J Health Syst Pharm,2012,69(17):1494-1499.
[7]Sorensen PS,Mellgren SI,Svenningsson A,etal.NORdic trial of oral Methylprednisolone as add-on therapy to Interferon beta-1a for treatment of relapsing-remitting Multiple Sclerosis (NORMIMS study):a randomised,placebo-controlled trial[J].Lancet Neurol,2009,8(6):519-529.
[8]Ravnborg M,Sφrensen PS,Andersson M,etal.Methylprednisolone in combination with interferon beta-1a for relapsing-remitting multiple sclerosis (MECOMBIN study):a multicentre,double-blind,randomised,placebo-controlled,parallel-group trial[J].Lancet Neurol,2010,9(7):672-680.
[9]Edan G,Comi G,Le Page E,etal.Mitoxantrone prior to interferon beta-1b in aggressive relapsing multiple sclerosis:a 3-year randomised trial[J].J Neurol Neurosurg Psychiatry,2011,82(12):1344-1350.
[10]Wingerchuk DM,Carter JL.Multiple sclerosis:current and emerging disease-modifying therapies and treatment strategies[J].Mayo Clin Proc,2014,89(2):225-240.
[11]Fernández O,Guerrero M,Mayorga C,etal.Combination therapy with interferon beta-1b and azathioprine in secondary progressive multiple sclerosis.A two-year pilot study[J].J Neurol,2002,249(8):1058-1062.
[12]Markovic-Plese S,Bielekova B,Kadom N,etal.Longitudinal MRI study:the effects of azathioprine in MS patients refractory to interferon beta-1b[J].Neurology,2003,60(11):1849-1851.
[13]Lus G,Romano F,Scuotto A,etal.Azathioprine and interferon beta(1a) in relapsing-remitting multiple sclerosis patients:increasing efficacy of combined treatment[J].Eur Neurol,2004,51(1):15-20.
[14]Rudick RA,Stuart WH,Calabresi PA,etal.Natalizumab plus interferon beta-1a for relapsing multiple sclerosis[J].N Engl J Med,2006,354(9):911-923.
[15]Stüve O,Morra CM,Cravens PD,etal.Potential risk of progressive multifocal leukoencephalopathy leukoencephalopathy with natalizumab therapy:possible interventions[J].Arch Neurol,2007,64(2):169-176.
[16]Peaureaux D,Pignolet B,Biotti D,etal.Fingolimod treatment after natalizumab-related progressive multifocal leukoencephalopathy:Three new cases[J].Mult Scler,2015,21(5):671-672.
[17]Hellwig K,Gold R.Progressive multifocal leukoencephalopathy and natalizumab[J].J Neurol,2011,258(11):1920-1928.
[18]Wattjes MP,Vennegoor A,Steenwijk MD,etal.MRI pattern in asymptomatic natalizumab-associated PML[J].J Neurol Neurosurg Psychiatry,2015,86(7):793-798.
[19]Polman CH,O′Connor PW,Havrdova E,etal.A randomized,placebo-controlled trial of natalizumab for relapsing multiple scle-rosis[J].N Engl J Med,2006,354(9):899-910.
[20]Goodman AD,Rossman H,Bar-Or A,etal.GLANCE:results of a phase 2,randomized,double-blind,placebo-controlled study[J].Neurology,2009,72(9):806-812.
[21]Lublin FD,Cofield SS,Cutter GR,etal.Randomized study combining interferon and glatiramer acetate in multiple sclerosis[J].Ann Neurol,2013,73(3):327-340.
[22]Sorensen PS,Lycke J,Erälinna JP,etal.Simvastatin as add-on therapy to interferonβ-1a for relapsing-remitting multiple sclerosis (SIMCOMBIN study):a placebo-controlled randomised phase 4 trial[J].Lancet Neurol,2011,10(8):691-701.
[23]Freedman MS,Wolinsky JS,Wamil B,etal.Teriflunomide added to interferon-βin relapsing multiple sclerosis:a randomized phase Ⅱ trial[J].Neurology,2012,78(23):1877-1885.
[24]Cohen JA,Imrey PB,Calabresi PA,etal.Results of the Avonex Combination Trial (ACT) in relapsing-remitting MS[J].Neurology,2009,72(6):535-541.
[25]Havrdova E,Zivadinov R,Krasensky J,etal.Randomized study of interferon beta-1a,low-dose azathioprine,and low-dose corticosteroids in multiple sclerosis[J].Mult Scler,2009,15(8):965-976.
[26]Jacques F,Gaboury I,Christie S,etal.Combination therapy of interferon Beta-1b and tacrolimus:a pilot safety study[J].Mult Scler Int,2012,2012:935921.
[27]Kalincik T,Horakova D,Dolezal O,etal.Interferon,azathioprine and corticosteroids in multiple sclerosis:6-year follow-up of the ASA cohort[J].Clin Neurol Neurosurg,2012,114(7):940-946.
[28]Pulicken M,Bash CN,Costello K,etal.Optimization of the safety and efficacy of interferon beta 1b and azathioprine combination therapy in multiple sclerosis[J].Mult Scler,2005,11(2):169-174.
[29]Lindsey J,Scott T,Lynch S,etal.The CombiRx trial of combined therapy with interferon and glatiramer cetate in relapsing remitting MS:Design and baseline characteristics[J].Mult Scler Relat Disord,2012,1(2):81-86.
[30]Reggio E,Nicoletti A,Fiorilla T,etal.The combination of cyclophosphamide plus interferon beta as rescue therapy could be used to treat relapsing-remitting multiple sclerosis patients-twenty-four months follow-up[J].J Neurol,2005,252(10):1255-1261.
[31]Smith DR,Weinstock-Guttman B,Cohen JA,etal.A randomized blinded trial of combination therapy with cyclophosphamide in patients-with active multiple sclerosis on interferon beta[J].Mult Scler,2005,11(5):573-582.
[32]Calabresi PA,Wilterdink JL,Rogg JM,etal.An open-label trial of combination therapy with interferon beta-1a and oral methotrexate in MS[J].Neurology,2002,58(2):314-317.
[33]Jeffery DR,Chepuri N,Durden D,etal.A pilot trial of combination therapy with mitoxantrone and interferon beta-1b using monthly gadolinium-enhanced magnetic resonance imaging[J].Mult Scler,2005,11(3):296-301.
[34]Vermersch P,Waucquier N,Michelin E,etal.Combination of IFN beta-1a (Avonex) and mycophenolate mofetil (Cellcept) in multiple sclerosis[J].Eur J Neurol,2007,14(1):85-89.
《医学综述》欢迎广大作者投稿
投稿地址:北京市通州区北苑通典铭居F座0806室(101100)电话:010-60551103
E-mail:yxzs@chinajournal.net.cnyxzs2005@163.comHttp://www.yxzszz.com
New Advancement in the Combination Therapy of Multiple SclersisFENGMei-na,CHENYu-hua.(DepartmentofNeurology,YangtzeRiverShippingGeneralHospital,Wuhan430015,China)
Abstract:Immunomodulating agents have beneficial effects in the treatment of multiple sclerosis,which decreases the frequency of relapses,delays the progression of disability,and reduces magnetic resonance imaging lesion quantity or shrinks the lesion volume.Despite the efficacy of these agents,many patients continue to show progression of the disease.Therefore,clinicians have proposed a variety of combinations of agents in an attempt to decrease disease activity. A number of clinical trials applying two or more drugs with different mechanisms for the treatment of multiple sclerosis have been done,in order to assess the effectiveness and safety.Here is to make a review of the rationale and clinical research of combination therapies for multiple sclerosis.
Key words:Multiple sclerosis; Combination therapy; Immunomodulators; Immunosupressants
收稿日期:2014-10-17修回日期:2015-02-17编辑:郑雪
doi:10.3969/j.issn.1006-2084.2015.18.036
中图分类号:R744.5
文献标识码:A
文章编号:1006-2084(2015)18-3361-03

