二尖瓣关闭不全合并巨大左心室外科治疗效果
尚 亮,姜胜利,任崇雷,王 瑶,王明岩,李伯君,高长青
·临床研究·
二尖瓣关闭不全合并巨大左心室外科治疗效果
尚 亮,姜胜利,任崇雷,王 瑶,王明岩,李伯君,高长青
目的报道原发性二尖瓣关闭不全合并巨大左心室患者外科术后随访结果。方法自2000年1月至2012年12月,本院共对55例慢性二尖瓣关闭不全合并巨大左心室患者进行了二尖瓣手术,其中男性35例,女性20例,年龄8~62(40.5±15.1)岁。病例入选标准:术前诊断为中、重度二尖瓣关闭不全合并左心室舒张末期内径(LVDD)≥65 mm者。该组患者中病因为风湿性19例(占34.5%),其中2例合并轻度二尖瓣狭窄,退行性变23例(占41.8%),先天性12例(占21.8%),感染性1例(占1.9%)。术前心功能分级:NYHAⅡ级17例,NYHAⅢ级34例,NYHAⅣ级4例。胸部X线片C/T示:(0.71±0.16)。病程0.3~38(19.5±11.3)年。心电图显示心房颤动者33例(占60%)。超声心动图(UCG)示患者均为中度或重度二尖瓣关闭不全合并巨大左心室,左室舒张末期内径(LVEDD)为65.0~91.0(71.6±5.5)mm,左室收缩末期内径(LVESD)为45.6~75.2(54.6±5.6)mm,左心室舒张末容积指数(LVEDDI)为28.8~68.3(42.5±7.5)mm/m2,左心室舒张末期容积(LVEDSI)为21.8~50.0(32.4±6.3)mm/m2;左心房内径(LAD)为43.0~110.0(67.9±15.7)mm;射血分数(EF)为30.0%~79.0%(59.5±10.1)%;室间隔厚度为6~13(10.0±1.5)mm。结果全组55例患者中,围术期死亡2例,病死率为3.63%,术后2周UCG示LVDD减小为(58.1±7.6)mm,与术前相比P<0.01。随访至2012年12月,38例患者得到随访,占总数的71.69%,平均随访时间为19~179(98.41±50.29)个月,至今存活患者33例(86.84%),其中10例患者心功能I级,20例患者心功能Ⅱ级,2例患者心脏功能Ⅲ级,1例心功能Ⅳ级。随访期间死亡5例,随访总病死率为13.15%,失访15例,失访率为28.3%。因心脏原因死亡者3例,占死亡人数的60.0%。死亡主要原因为慢性心功能不全。非心脏原因死亡的疾病为尿毒症及脑出血。存活患者LVDD进一步减小达(50.0±7.8)mm,与术后围术期LVDD相比有明显缩小(P<0.001)。结论对于二尖瓣关闭不全合并巨大左心室患者,二尖瓣手术是改善患者左心室功能并使左心室进一步缩小的有效治疗。
二尖瓣关闭不全;巨大左心室;心脏外科手术
合并巨大左心室是二尖瓣关闭不全行心脏瓣膜手术的主要危险因素之一,其术后中远期结果尚不清楚。本文回顾性地分析了解放军总医院心血管外科2000年1月至2012年1月55例巨大左心室患者行二尖瓣瓣膜手术的临床资料,旨在探讨二尖瓣手术后巨大左室的形态学变化规律及其对心脏收缩功能和预后的影响。
1 资料与方法
1.1 病例选自2000年1月至2012年12月在我院心血管外科接受二尖瓣置换术(mitral valve replacement,MVR)或二尖瓣成形术(mitral valve plasty,MVP)治疗的二尖瓣关闭不全合并巨大左心室患者,其中男性35例,女性20例,年龄8~62(40.5± 15.1)岁。入选标准:术前诊断为中、重度二尖瓣关闭不全合并左心室舒张末期内径(1eft ventricle end-diastole diameter,LVEDD)≥65 mm者。排除合并中、重度二尖瓣狭窄,中、重度主动脉瓣狭窄或关闭不全和冠状动脉粥样硬化性心脏病的患者。该组患者中病因为风湿性19例(占34.5%),其中2例合并轻度二尖瓣狭窄,退行性变23例(占41.8%),先天性12例(占21.8%),感染性1例(占1.9%)。术前心功能分级:NYHAⅡ级17例,NYHAⅢ级34例,NYHAⅣ级4例。胸部X线片C/T示:(0.71±0.16)。病程0.3~38(19.5±11.3)年。心电图显示心房颤动者33例(占60%)。超声心动图(echocardiogram,UCG)示患者均为中度或重度二尖瓣关闭不全合并巨大左心室,LVEDD为65.0~91.0(71.6±5.5)mm,左室收缩末期内径(left ventricular end-systolic dimension,LVESD)为45.6~75.2(54.6±5.6)mm,左心室舒张末期容积指数(left ventricular end-diastolic volume index,LVEDDI)为28.8~68.3(42.5±7.5)mm/m2,左心室舒张末期容积(left ventricular enddiastolic volume,LVEDSI)为21.8~50.0(32.4±6.3)mm/m2;左心房内径(left auricle dimension,LAD)为43.0~110.0(67.9±15.7)mm;左室射血分数(left ventricular ejection fraction,LVEF)为30.0%~79.0%(58.5±10.1)%,缩短分数(fractional shortening,FS)为15.0%~49.0%(31.0±6.5)%;室间隔厚度为6~13(10.0±1.5)mm。
1.2 全组患者手术均于中度低温全麻体外循环下进行。胸部正中切口,常规建立体外循环,心肌保护采用冷康斯特保护液(HTK液)经主动脉根部正向间断灌注,同时心包内放置冰屑降温。手术行MVR 46例,其中生物瓣置换2例,机械瓣置换44例,MVP 9例,三尖瓣成形术34例,左心房折叠术17例。主动脉阻断时间为32~153(66.2±21.4)min,体外循环时间为58~163(102.1±25.3)min,所有患者于术后7~14 d行心脏超声多普勒检查,术后早期6~12个月内继续应用洋地黄和/或利尿剂治疗以进一步改善心功能。
1.3 所有随访数据来自病历记录或患者访问医生或对患者电话采访。
1.4 应用SPSS 13.0软件包进行统计分析,数据结果均以均数±标准差(s)表示,手术前后比较采用配对t检验,以P<0.05为差异有统计学意义。
2 结 果
55例患者中有2例(3.63%)围手术期死亡(1例术后低心排综合征,1例严重肺部感染)。所有存活患者ICU时间为0.06~21.4(4.2±3.2)d,术后住院时间为1~25.7(12.6±4.7)d。术后并发症包括低心排量综合征3例(17.8%),术后延迟通气9例(16.4%),术后二次气管插管1例(1.8%),术后脑中风1例(1.8%),术后肾功能衰竭3例(17.8%),术后新发房颤4例(18.2%),30例(90.9%)患者术后仍然存在心房颤动。手术后2周内LVEDD显著降低(P<0.001)。LVESD显著降低(P<0.001)。术后LVEF有所降低(P<0.001)。术后FS亦较术前减低(P<0.001)。见表1。
至2014年12月,38例(71.69%)患者得到随访,随访时间为19~179(98.41±50.29)个月,至今存活患者33例(86.84%),其中10例患者心功能Ⅰ级,20例患者心功能Ⅱ级,2例患者心脏功能Ⅲ级,1例心功能Ⅳ级。随访期间死亡5例(13.15%),失访15例(28.3%)。因心脏原因死亡者3例,占死亡人数的60.0%。死亡主要原因为慢性心功能不全。非心脏原因死亡的疾病为尿毒症及脑出血。术后1年随访38例,存活37例,存活率97.4%,术后5年随访22例,存活20例,存活率达90.9%;术后10年随访11例,存活9例,存活率达81.8%。现存活患者LVEDD进一步减小达(50.0±7.8)mm,与术后围术期相比有明显缩小(P<0.001),其中16例患者(48.5%)LVEDD<50 mm。LVEF术后较术前水平无统计学差异,从术前(58.6±9.4)%到术后(58.3±12.2)%,P=0.93。术后缩短分数(32.2±8.0)%与术前相比亦无统计学差异(P=0.62)。无患者行二次手术。
表1 患者手术前后及随访的心功能对比(n=38,s)
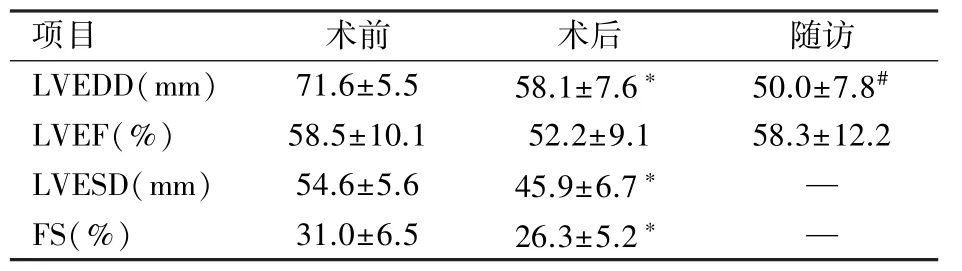
表1 患者手术前后及随访的心功能对比(n=38,s)
注:与术前比较*P<0.01;与术后比较#P<0.01。
项目 术前 术后 随访LVEDD(mm) 71.6±5.5 58.1±7.6*50.0±7.8#LVEF(%) 58.5±10.1 52.2±9.1 58.3±12.2 LVESD(mm) 54.6±5.6 45.9±6.7*—FS(%) 31.0±6.5 26.3±5.2*—
3 讨 论
3.1 慢性二尖瓣反流的病因分析 二尖瓣反流(mitral regurgitation,MR)是一种常见的心脏瓣膜病[1]。分为原发性MR和继发性MR,两者病因不同,本组研究对象均为原发性二尖瓣关闭不全。原发性MR的病理形态表现为瓣叶、瓣环、腱索、乳头肌病变致瓣叶对合不全进而导致收缩期血流从左心室反流入左心房。在发达国家中,二尖瓣脱垂是二尖瓣关闭不全的主要病因[2]。年轻患者因黏液样变性致瓣叶、腱索冗长,瓣叶对合不全,年老患者因纤维弹性丧失致腱索断裂,瓣叶不能对合。本组患者中,退行性变者23例(占41.8%),其它病因主要是风湿性瓣膜病,先天发育异常,感染性心内膜炎等。该组患者中病因为风湿性19例(34.5%),先天性12例(21.8%),感染性1例(1.9%)。以往风湿性瓣膜病是我国二尖瓣关闭不全最常见的原因,但近年来,随着我国经济社会的发展,退行性变致二尖瓣关闭不全患者逐渐增多,二尖瓣关闭不全的病因构成较前有所变化,在经济相对发达的城市尤为明显,此类患者往往发病隐匿,左心功能不全症状出现较晚,而不可逆性的左心室重构对患者的治疗及预后影响极大,这一点需引起重视。
3.2 随访结果分析 本组患者术后5年的存活率达90.9%,术后10年的存活率达81.8%,该结果接近上海张宝仁等[3]报道的5年存活率(89.46±1.35)%,10年存活率(86.5±1.9)%。本组患者LVEDD为(71.6±5.5)mm,LVESD为(54.6±5.6)mm,LAD为(67.9±15.7)mm,而室间隔厚度为(10.0±1.5)mm,可见二尖瓣关闭不全引起的巨大左室主要以离心性扩大为主,室间隔及左室后壁未见明显肥厚。巨大左室患者换瓣术后LVEDD和LVESD呈进行性缩小,与国内[4-6]及国外相关研究[7-9]相符,尤以术后早期内缩小程度最显著。但随访至术后10年以上,仍有部分患者未能恢复至正常范围内。提示二尖瓣关闭不全患者长期形成的巨大左室,在术后相当长的时间内不能完全恢复至正常范围。尽管术前患者LVEF(58.5±10.1)%,大部分在正常水平,但多已伴有左室功能的下降[10]。该组患者术后早期LVEF和FS反而较术前有所下降,术后6个月逐渐恢复至术前水平,直至术后1~2年以上才基本恢复至正常范围。分析可能原因包括[11-15]:术前瓣膜关闭不全引起左心室容量负荷增加,出现LVEF正常,但并不代表真实的左心功能,实际上由于长期过度前负荷及心肌做功和耗氧量增加,已经对左心室功能造成了一定的损害;体外循环手术本身对心肌的损伤;以重度二尖瓣关闭不全为主的病变,术后左心室后负荷突然增加,而前负荷变小,对左心室功能有负性影响。所以LVEF并不能作为术后左心功能改善的评价指标[16]。
3.3 巨大左心室的形成机制 术前患者因慢性二尖瓣关闭不全造成的左室、左房容量负荷增加,为适应不断升高的左室、左房内压力,进一步引起左心室扩大或同时伴有左心室肥厚以及左心室顺应性下降,舒张功能受损[17-18]。严重者会出现心肌结构的不可逆病理损害,导致心肌收缩和舒张功能的显著下降,表现为患者症状加重,左心室容积的长期严重超载导致巨大左心室的形成[19]。二尖瓣关闭不全一旦合并巨大左心室,往往提示左心室心肌已出现明显的病理损害,是外科手术的高危因素[20]。此前临床上一般将LVESD≥50 mm和/或LVEDD≥70 mm者认为是巨大左心室[21]。根据最新的美国心脏瓣膜指南[2],该组将LVEDD≥65 mm者认为是巨大左心室。细胞外基质的结构改变以及胶原交联的减少,使细胞外基质更容易退化。动物模型表明细胞外基质的逐步丧失伴随着心肌细胞的延长和心肌细胞与基质成分的黏附结构的损失[22]。这些变化有助于左室扩张和功能障碍的进展。慢性瓣膜关闭不全的患者左心室不断扩大,但由于左心室储备能力巨大,可在很长时间内无症状,直至出现左心功能失代偿。
3.4 外科治疗策略 手术是治疗二尖瓣关闭不全最好的方法。目前,手术方式主要为MVP、MVR。外科手术的目标是:降低长期死亡率,一定程度改善心室重塑,保留左心室功能。手术时机的选择应注意以下几点:① 巨大左心室患者术前积极强心、利尿、营养心肌等药物治疗改善心功能;② 左心室扩大不是手术的绝对禁忌,此类患者不同于继发性心肌梗死后的二尖瓣关闭不全,过长时间的术前准备对于扩大的左心室无明显受益,建议在适当准备后对手术持积极态度。术中的处理是术后早期心脏功能明显改善的保障,本组主要措施有:① 行二尖瓣成形或尽量保留二尖瓣瓣下结构,保证足够的牵拉作用对改善术后左心室的收缩功能,防止左心室后壁破裂具有重要作用[23]。② 纠正三尖瓣反流。对明确的三尖瓣反流或三尖瓣环扩大者,行Devega成形术或瓣环成形术,以利术后心功能的恢复。③合并巨大左心房者,同时行左心房折叠术,以使左心血流方向正常化,有利于降低术后低心排血量综合征和呼吸衰竭的发生[24]。④ 复跳后,继续辅助循环,一般为主动脉阻断时间的1/4~1/3,待心脏收缩有力,心率及心律稳定后,停止体外循环。围术期处理重点注意:①适量补充胶体液,提高胶体渗透压,适当利尿,严格限制晶体液人量。②在保证心脏的正常容量负荷同时,早期使用多巴胺、肾上腺素等正性肌力药物支持心脏功能,必要时尽早使用主动脉球囊反搏[25]或左室辅助装置辅助心功能[26-27],根据情况安装心外膜起搏导线,必要时可予心脏同步化治疗。③围术期根据血压水平适当给予血管紧张素转化酶抑制剂/肾上腺素能受体结合剂类药物口服,改善心脏形态[28-29]。④ 本组患者均在术后尽早给予营养支持,纠正低蛋白血症。术后早期6~12个月内继续应用洋地黄和/或利尿剂治疗以进一步改善心功能。
[1] Nkomo VT,Gardin JM,Skelton TN,et al.Burden of valvular heart diseases:a population-based study[J].Lancet,2006,368(9540):1005-1011.
[2] Nishimura RA,Otto CM,Bonow RO,et al.2014 AHA/ACC Guideline for the Management of Patients With Valvular Heart Disease:executive summary:a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines[J].Circulation,2014,129(23):2440-2492.
[3] 张宝仁,邹良建,徐志云,等.风湿性瓣膜病二尖瓣与主动脉瓣置换术1154例长期效果分析[J].中华外科杂志,2003,41(4):243-246.
[4] 于伟勇,张宝仁,侯明君,等.二尖瓣置换术后巨大左室的几何形态学变化及其与左室收缩功能的关系[J].中华胸心血管外科杂志,2002,18(5):267-270.
[5] Liu XM,Wu H,Zhang WK,et al.Long-term results of surgical treatment of aortic and mitral regurgitation with enlarged left ventricle[J].Int J Clin Exp Med,2014,7(3):709-713.
[6] 龚达,李温斌,陈宝田,等.二尖瓣关闭不全合并巨大左心室外科治疗及远期随访[J].心肺血管病杂志,2014,33(1):21-24.
[7] Shafii AE,Gillinov AM,Mihaljevic T,et al.Changes in left ventricular morphology and function after mitral valve surgery[J].Am J Cardiol,2012,110(3):403-408.
[8] Zile MR,Tomita M,Ishihara K,et al.Changes in diastolic function during development and correction of chronic LV volume overload produced by mitral regurgitation[J].Circulation,1993,87(4):1378-1388.
[9] Schuler G,Peterson KL,Johnson A,et al.Temporal response of left ventricular performance to mitral valve surgery[J].Circulation,1979,59(6):1218-1231.
[10] Krishnamoorthy A1,Brown T,Ayers CR,et al.Progression from normal to reduced left ventricular ejection fraction in patients with concentric left ventricular hypertrophy after long-term follow-up[J].Am J Cardiol,2011,108(7):997-1001.
[11] 姜胜利,高长青,李伯君,等.巨大左心室患者瓣膜术后早期心脏形态学及收缩功能的变化[J].解放军医学杂志,2007,32(4):333-334.
[12] 姜胜利,李伯君,高长青,等.合并巨大左心室心脏瓣膜手术的临床分析[J].中华医学杂志,2010,90(42):2999-3002.
[13] Hirasawa Y,Miyauchi T,Sawamura T,et al.Giant left ventricular pseudoaneurysm after mitral valve replacement and myocardial infarction[J].Ann Thorac Surg,2004,78(5):1823-1825.
[14] Zhang X,Xu Z,Xu YQ,et al.Surgical intervention for advanced valvular heart disease in 227 cases[J].Chin Med J(Eng1),2005,118(12):989-994.
[15] Dzemeshkevich S,Korolev S,Frolova J,et al.Isolated replacement of the mitral leaflets and"Mercedes"-plastics of the giant left atrium:surgery for patients with left ventricle dysfunction and left atrium enlargement[J].J Cardiovasc Surg(Torino),2001,42(4):505-508.
[16] Timmis SB1,Kirsh MM,Montgomery DG,et al.Evaluation of left ventricular ejection fraction as a measure of pump performance in patients with chronic mitral regurgitation[J].Catheter Cardiovasc Interv,2000,49(3):290-296.
[17] Haluska BA,Short L,Marwick TH.Relationship of ventricular longitudinal function to contractile reserve in patients with mitral regurgitation[J].Am Heart J,2003,146(1):183-188.
[18] Corin WJ,Murakami T,Monrad ES,et al.Left ventricular passive diastolic properties in chronic mitral regurgitation[J].Circulation,1991,83(3):797-807.
[19] Pandis D,Sengupta PP,Castillo JG,et al.Assessment of longitudinal myocardial mechanics in patients with degenerative mitral valve regurgitation predicts post-operative worsening of left ventricular systolic function[J].J Am Soc Echocardiogr,2014,27(6):627-638.
( )[20] Poelzing S,Rosenbaum DS.Nature,significance,and mechanisms of electrical heterogeneities in ventricle[J].Anat Rec A Discov Mol Cell Evol Biol,2004,;280(2):1010-1017.
[21] 胡盛寿,张国平,朱晓东,等.巨大心脏瓣膜置换手术后远期疗效的观察[J].中华外科杂志,1996,34(3):164-166.
[22] Segura AM,Frazier OH,Buja LM.Fibrosis and heart failure[J].Heart Fail Rev,2014,19(2):173-185.
[23] Borger MA,Yau TM,Rao V,et al.Reoperative mitral valve replacement:importance of preservation of the subvalvular apparatus[J].Ann Thorac Surg,2002,74(5):1482-1487.
[24] Rosenhek R,Rader F,Klaar U,et al.Outcome of watchful waiting in asymptomatic severe mitral regurgitation.[J].Circulation,2006,113(18):2238-2244.
[25] Thiele H,Zeymer U,Neumann FJ,et al.Intra-aortic balloon counterpulsation in acute myocardial infarction complicated by cardiogenic shock(IABP-SHOCK II):final 12 month results of a randomised,open-label trial[J].Lancet,2013,382(9905):1638-1645.
[26] Xydas S,Rosen RS,Ng C,et al.Mechanical unloading leads to echocardiographic, electrocardiographic, neurohormonal, and histologic recovery[J].J Heart Lung Transplant,2006,25(1):7-15.
[27] Levin HR,Oz MC,Chen JM,et al.Reversal of chronic ventricular dilation in patients with end-stage cardiomyopathy by prolonged mechanical unloading[J].Circulation,1995,91(11):2717-2120.
[28] Xu Y,Tang T,Ding Y,et al.Improved cardiac performance by rosuvastatin is associated with attenuations in both myocardial tumor necrosis factor-alpha and p38 MAP kinase activity in rats after myocardial infarction[J].Am J Med Sci,2010,340(2):121-127.
[29] Landmesser U1,Wollert KC,Drexler H.Potential novel pharmacological therapies for myocardial remodelling[J].Cardiovasc Res,2009,81(3):519-527.
Study of surgical treatment for mitral regurgitation associated with dilated left ventricle
Shang Liang,Jiang Sheng-li,Ren Chong-lei,Wang Ming-yan,Gao Chang-qing
Department of Cardiovascular Surgery of PLA General Hospital,Institute of Cardiac Surgery of PLA,Beijing 100853,China
Jiang Sheng-li,Email:Jiangsl301@sina.com
ObjectiveTo report the surgical outcome of mitral valve surgery for isolated chronic mitral insufficiency with severely dilated left ventricle(LV).MethodsBetween January 2000 and December 2012,55 patients(35 male and 20 female)with a mean age of(40.5±15.1)years,underwent MVR or MVP at PLA general Hospital.Rheumatic MR was found in 19 cases(34.5%),congenital MR in 12 cases(21.8%)and infectious MR in 1 cases(1.9%).17 patients were in NYHA functional class II,34 in classⅢand 4 in classⅣ.The C/T ratio was 0.71±0.16 on chest x-ray.The clinical course was 0.3-38(19.5±11.3)years.Electrocardiogram(ECG)showed 33 patients(60%)had atrial fibrillation.Echocardiogram(UCG)showed severe or moderate MR and LV hypertrophy in all patients.LVDD was:65.0-91.0(71.6±5.5)mm;Left ventricular end-systolic dimension(LVESD)was 45.6-75.2(54.6± 5.6)mm;Left ventricular end-diastolic volume index(LVEDDI)was 28.8-68.3(42.5±7.5)mm/m2;Left ventricular end-diastolic volume index(LVEDVI)was 21.8-50.0(32.4±6.3)mm/m2;Left atrial diameter was 43.0-110.0(67.9±15.7)mm;Ejective fraction was 30.0%-79.0%(59.5±10.1)%;Interventricular septum was 6-13(10.0±1.5)mm.ResultsTwo of 55 cases died in the peri-operative period(3.63%).Two weeks after surgery the UCG showed a reduction of left ventricle diastole diameter(LVEDD)from(71.6±5.5)to(58.1±7.6)mm(P<0.001).A total of 38 cases(71.69%)were successful followed.In themean follow-up of 19-179(98.41±50.29)months,33 patients(86.4%)survived,with 10 patients in NYHAclass I,20 in class II,2 in class III,and 1 in class IV.5 deaths(13.15%)were noted during the follow-up,including 3(60%)cardiac death.The non-cardiac deathsincludeduremia and cerebral hemorrhage.The LVEDD further decreased from(58.1±7.6)to(50.0±7.8)mm after discharge(P<0.001).ConclusionMitral valve replacement is indicated in patients with mitral insufficiency and severely dilated left ventricles,and the intervention has the potential to restore theLV volume.
Mitral valve regurgitation;Severely dilated left ventricle;Cardiac surgery.
2015-01-26)
2015-02-02)
10.13498/j.cnki.chin.j.ecc.2015.01.08
解放军总医院临床扶持基金(2012FC-TSYS-3043)
100853北京,中国人民解放军总医院心血管外科
姜胜利,Email:Jiangsl301@sina.com

