以壳聚糖为基质的盐酸利多卡因凝胶剂的研究*
吕 玥,李 晗,戴学文,房志仲
(1.天津市南开医院,天津 300100; 2.天津医科大学药学院,天津 300070)
药物制剂
以壳聚糖为基质的盐酸利多卡因凝胶剂的研究*
吕 玥1,李 晗2,戴学文2,房志仲2
(1.天津市南开医院,天津 300100; 2.天津医科大学药学院,天津 300070)
目的:以壳聚糖为基质制备盐酸利多卡因凝胶剂,并建立盐酸利多卡因的含量测定方法。方法:以壳聚糖为基质制备凝胶剂,以HPLC法测定利多卡因的含量;色谱条件为Kromasil C18色谱柱(200 mm×4.6 mm,5 μm,);流动相:甲醇-磷酸缓冲液(加磷酸调节pH=8.00)(75∶25),流速为0.8 ml/min,检测波长为254 nm,柱温:室温,进样量20 μl。结果:盐酸利多卡因在16.24~121.80 μg/ml范围内浓度与峰面积线性关系良好(r=0.999 9,n=7),平均回收率为100.59%,RSD为0.35%。 结论:以壳聚糖为基质制备的凝胶剂方法简便,HPLC法测定凝胶剂中的利多卡因方法准确、可靠,可用于对利多卡因凝胶剂进行质量控制、含量控制。
壳聚糖,利多卡因,凝胶剂,高效液相色谱法
国外对凝胶剂的研究较早,《英国药典》1993年版收载了外用凝胶剂。《美国药典》于1995 年版和《中国药典》2000年版首次收载凝胶剂[1]。国内外凝胶剂用的辅料主要有卡波姆、壳聚糖、海藻酸钙、羧甲基纤维素钠等。壳聚糖来源广泛,具有良好的组织相容性、生物可降解作用等,同时具有胶原质和植物纤维的功能,无抗原和致敏性,无不良反应,其成膜性、黏滞性良好。目前,壳聚糖在医学、药学等领域得到了深入的研究和临床应用[1]。
盐酸利多卡因注射剂用于表面浸润麻醉时患者有疼痛感,而胶浆剂仅适于黏膜用局部麻醉,且临床对无创伤性表面麻醉制剂需求较大。凝胶剂的给药途径除经皮给药外、还可以经口腔、眼部、鼻腔、阴道和直肠黏膜给药,不同的给药途径均能收到满意的临床效果。盐酸利多卡因凝胶剂在使用中患者无痛苦和损伤,给药方便,作用持久,增加了患者的顺应性,可替代局部浸润麻醉给药,且较为经济。本文以壳聚糖为基质,制备盐酸利多卡因凝胶剂,并建立质量控制方法。
1 仪器与试药
1.1 仪器 美国高效液相色谱仪(Spectra-physics),输液泵(SP8810 precision isocratic, BIO-RAD),检测器(Spectra SYSTEM UV2000,Thermo separation products),Anastar 色谱工作站,Kromasil C18色谱柱(200 mm×4.6 mm,5 μm);ALC-210.4电子分析天平(北京赛多利斯仪器系统有限公司);KQ-100B型超声波清洗器(昆山市超声仪器有限公司);pHS-25(数显)pH计(上海精密科学仪器有限公司),80-2B台式离心机(上海安亭科学仪器厂制造)。
1.2 试药 利多卡因对照品(中国药品生物制品检定所,批号110715-201016)。盐酸利多卡因样品(湖北远成药业有限公司提供),壳聚糖(南通兴成生物制品厂提供),甲醇(天津市风船化学试剂有限公司,色谱纯),盐酸利多卡因凝胶剂(本院自制,批号20140505、20140510、20140512),其他试剂均为市售分析纯;重蒸水(天津医科大学自制)。
2 方法与结果
2.1 盐酸利多卡因凝胶剂的制备
2.1.1 处方 0.625 g盐酸利多卡因(利多卡因0.5 g),壳聚糖4 g,冰醋酸0.5 ml,丙二醇20 ml,氮酮1.5 ml,薄荷脑0.1 g,加蒸馏水至100 g。
2.1.2 制备 ①将冰醋酸加蒸馏水配成2%的醋酸水溶液,加入壳聚糖使其溶胀;②将盐酸利多卡因溶于少量蒸馏水;③将薄荷脑、氮酮溶于丙二醇中,④将②和③分别加入①中,加蒸馏水至100 g,搅拌均匀,即得凝胶剂。
2.2 含量测定
2.2.1 色谱条件 TIANHE Kromasil C18色谱柱(200 mm×4.6 mm,5 μm);流动相:甲醇-磷酸盐缓冲液(25∶75,pH 8.0);检测波长为254 nm;流速:0.8 ml/min;柱温:室温,进样量20 μl[1]。
2.2.2 溶液的配制
2.2.2.1 对照品溶液的配制 精密称取盐酸利多卡因对照品40 mg,置于50 ml量瓶中,加甲醇溶解并至刻度,摇匀。
2.2.2.2 样品溶液的配制 精密称取凝胶剂4 g,置50 ml烧杯中,加适量的流动相超声使其溶解后,定量转移至25 ml量瓶中,定容,摇匀;再取样品溶液置于离心管,置入离心机中,离心10 min,转速2 000 r/min;取上清液0.2 ml置于10 ml量瓶,定容至刻度。摇匀即得。
2.2.2.3 阴性对照溶液的配制 依处方制备不含盐酸利多卡因的空白凝胶剂,依“2.2.2”项下样品溶液的配制方法操做,得阴性对照溶液,备用。
2.2.3 专属性试验 分别取对照品溶液、样品溶液和阴性对照溶液各取20 μl,按照“2.2.1”项下色谱条件进样分析,结果显示阴性对照液在利多卡因相同保留时间处无干扰,见图1。
2.2.4 线性范围 分别量取盐酸利多卡因对照品溶液0.2、0.4、0.6、0.8、1.0、1.2和1.5 ml于10 ml量瓶中,加甲醇至刻度,摇匀。按“2.2.1”项下色谱条件,进样20 μl。以盐酸利多卡因浓度为横坐标,峰面积为纵坐标,绘制标准曲线,结果回归方程为Y=2 189.2X+5 336.4(r=0.999 9,n=7),盐酸利多卡因在16.24~121.80 μg/ml范围内呈良好的线性关系。
2.2.5 精密度的测定 按“2.2.1”项下色谱条件,取对照品溶液进样20 μl,以峰面积计算相对标准偏差,结果RSD为 0.85%(n=6),说明日内精密度良好。按“2.2.1”项下色谱条件于第1、2、3、4、5和6 d分别进行精密度测定,以峰面积计算相对标准偏差,RSD为0.79%(n=6),说明日间精密度良好。
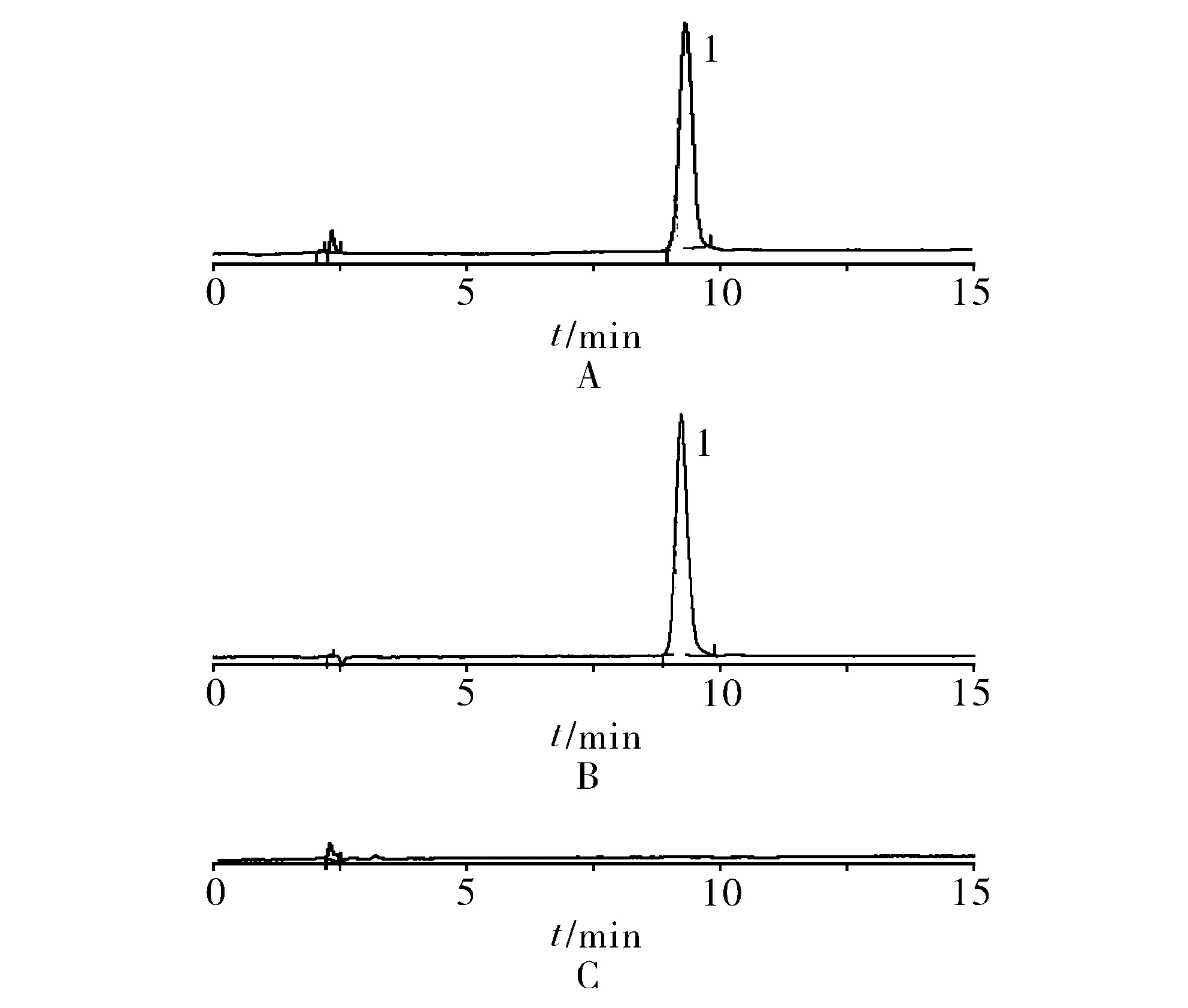
1.盐酸利多卡因
2.2.6 重现性实验 取同一盐酸利多卡因样品溶液,按“2.2.1”项下色谱条件,连续进样6次,进样量20 μl,以峰面积计算相对标准偏差RSD为0.60% (n=6),说明该法重现性良好。
2.2.7 稳定性的测定 按“2.2.1”项下色谱条件,取同一对照品溶液,分别在制备后0、3、6、9、12和24 h,进样20 μl,记录峰面积,以峰面积计算相对标准偏差RSD为0.81%,说明该溶液在24 h内稳定。
2.2.8 回收率的测定 精密称取凝胶剂4 g置50 ml烧杯中,共9份,分别精密称定0.8、1.0和1.2 g 盐酸利多卡因于烧杯中,依“2.2.2.2”项下方法操作,配成80%、100%和120%的加样溶液。按“2.2.1”项下色谱条件,进样量20 μl,计算回收率,结果平均回收率为100.59%,RSD为0.35%,见表1。
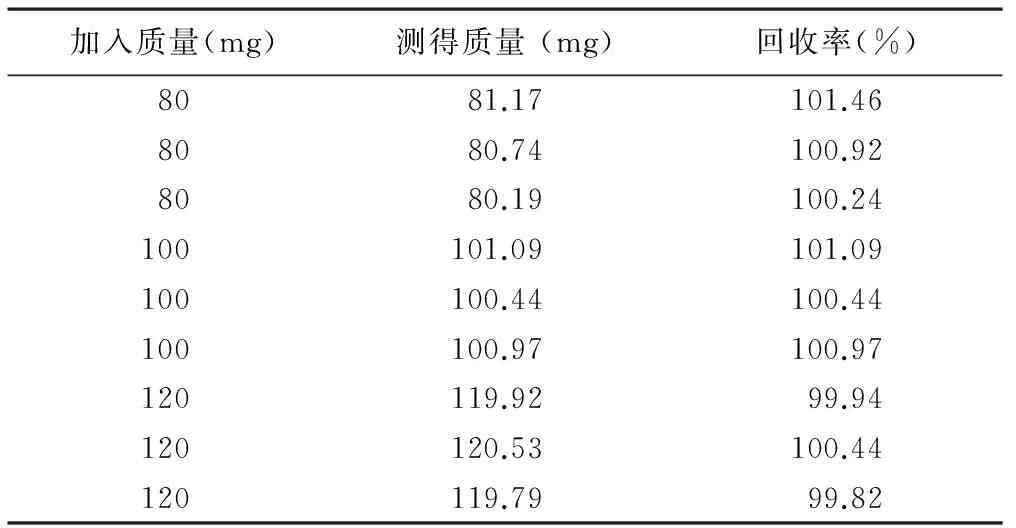
表1 回收率试验结果(n=9)
2.4.9 样品含量测定 取供试品3批,分别按“2.2.2.2”项下方法配制供试品溶液,精密吸取供试品溶液20 μl,按“2.2.1”项下色谱条件分析,根据供试品和对照品的峰面积,按照外标法计算样品的含量,结果3批样品的含量分别为标示量的99.15%、104.09%和105.93%。
3 讨论
3.1 壳聚糖用量 壳聚糖本身为一种多糖类纤维素,在醋酸溶液中溶解,壳聚糖溶液呈较好的凝胶剂,壳聚糖用量从1%~6%,凝胶剂的黄色逐渐加深,而且凝胶剂的黏性也会随之增加。当壳聚糖用量在4%时,与氮酮、丙二醇能充分混合,制备过程简单、易行[3,4]。
3.2 系统适应性 在试验中用甲醇代替乙腈,用甲醇-磷酸缓冲液(50∶50)为流动相,结果发现利多卡因的峰型不对称,当调整甲醇与磷酸缓冲液的比例为25∶75时, 利多卡因的峰型对称,保留时间在11 min左右,塔板数大于2 500,分离度大于1.5,符合分析要求[3,5]。
3.3 盐酸利多卡因加入方式 分别考查了直接将盐酸利多卡因粉末加入制备好的凝胶基质中和先配成盐酸利多卡因溶液再加到凝胶基质中,经试验发现,先将盐酸利多卡因配成溶液,再加到凝胶基质中,盐酸利多卡因溶液与凝胶基质能均匀混合,而且凝胶剂黏性更好。
1 中国药典[S]. 二部.2010:709-701,2371
2 王署东,刘文雅.凝胶剂的研究进展及应用概况[J].中国药业,2010,19(21):1-3
3 孙庆申,车小琼,赵凯.壳聚糖基质与蛋白质药物的释放[J].高分子通报,2008,21(6):46-48
4 董煜.高效液相色谱法测定盐酸利多卡因胶浆的含量[J].中国药业,2010,10(2):36-38
5 吴洪应,龚纯.HPLC法同时测定林可霉素利多卡因凝胶中林可霉素和盐酸利多卡因的含量[J].中国药品标准,2005,6(2):26-28
Research on lidocaine hydrochloride gels with chitosan as the matrix
Lv Yue1,Li Han2,Dai Xuewen2,Fang Zhizhong2
(Tianjin Nankai Hospital,Tianjin 300100;2.College of Pharmacy, Tianjin Medical University,Tianjin 300070)
Objectives:Preparation of chitosan as the matrix of lidocaine hydrochloride gels,to establish content determination and methodology of the method.Methods:Design the prescription, according to the prescription preparation gels. To establish HPLC method for determining the content of lidocaine,the chromatographic conditions is Kromasil C18chromatographic column(200 mm×4.6 mm, 5 μm); mobile phase: methanol - phosphate buffer(75∶25); add phosphoric acid to adjust pH 8.0, flow rate of 0.8 ml/min,λmax=254 nm;column temperature: room temperat ure, injection amount 20 μl .Results:The calibration curves of lidocaine were linear in the ran ges of 16.24~121.8 μg/ml (r=0.999 9,n=7).The recoveries were 100.59%,and RSD were 0.35%(n=3).Conclusions:The methods of HPLC is specific, effective, sensitive and accurate. It can be used to lidocaine hydrochloride gel agent for quality control,content control.
chitosan,lidocaine,hydrochloride gels,HPLC
2014-11-13
TQ460.6 R927.2
A
1006-5687(2015)02-0029-03

