邻菲罗啉分光光度法测定微量铁实验条件的探讨
姚雪霞, 戴存礼, 李晓林, 刘玉涛
(南京农业大学 工学院, 江苏 南京 210031)
邻菲罗啉分光光度法测定微量铁实验条件的探讨
姚雪霞, 戴存礼, 李晓林, 刘玉涛
(南京农业大学 工学院, 江苏 南京 210031)
在实验教学中,一般采用邻菲罗啉分光光度法测定微量铁的含量,因为该方法具有取样少、简便和灵敏度高等特点。但在实际教学过程中,发现该实验的影响因素较多,如波长的选择、缓冲溶液的用量、显色时间、显色剂的用量,以及还原剂的选择等都对最终的实验结果产生一定的影响。并且不同的教材版本介绍的操作方法也不尽相同。为了更好地开展实验教学,探讨了以上各种影响因素对吸光度的影响,并得出最佳的实验条件。和以往传统的实验教学相比,改进后的实验不仅可以节省很多化学试剂,也减少了一定的环境污染。
分光光度法; 邻菲罗啉; 盐酸羟胺; 维生素C
0 引 言
溶液中微量铁离子的测定方法很多,有原子吸收法、重铬酸钾法、分光光度法等[1-2]。其中采用分光光度法测定微量铁的方法较多,如用双波长法测定微量铁的含量,用不同显色剂测定微量铁的含量[3-4],并对电镀废液、循环水,脱盐水,自来水等溶液中铁离子含量进行了相应的测定[5-9]。目前,在实验教学中,一般采用邻菲罗啉(又名邻二氮菲)分光光度法测定微量铁的含量,因为该方法具有取样少、分析快、简便、准确和灵敏度高等优点。但是采用该方法进行实验教学时,发现实验过程中的影响因素较多,如波长的选择、缓冲溶液的选择和用量、显色的时间、显色剂的用量以及还原剂的选择等都会对最终的实验结果产生一定的影响。以往的文献也对该实验进行了一些改进[10-13],但是对以上这些影响因素进行全面系统分析却不是很多,并且不同的教材版本介绍的操作方法也不尽相同[14-16]。为了更好地进行实验教学,很有必要对这些影响因素进行系统分析,选择出最佳的实验条件,用以测定未知液的含铁量。
1 实验部分
1.1 分光光度计的光学原理
分光光度计采用的光学原理为朗伯-比尔定律。即当一束单色光通过一定浓度的稀有色溶液时,溶液对光的选择吸收程度A与溶液的浓度或液层成正比,具体的数学表达式为
A=kcL=log(I0/I)
式中:A为吸光度,即光通过溶液时被吸收的强度;c为有色溶液的浓度;I0为入射光的光强;I为透射光的光强;L为液层的厚度;k为吸光系数。式中,k为常数,且待测溶液被装在标准比色皿中,可认为溶液的厚度L也是常数。因此溶液的吸光度A只和溶液的浓度c成正比。在实验中,可通过测定一组标准铁溶液的吸光度A,绘制标准曲线,反过来求未知溶液的溶度c。
1.2 主要仪器和试剂
V-1200型紫外-可见分光光度计,0.1 mg的电子分析天平,PHS-3CT型酸度计。
0.1 g/L铁标准溶液的配置:用电子分析天平准确称取0.702 0 g分析纯的NH4Fe(SO4)2·6H2O,置于一烧杯中,用30 mL, 2 mol/L HCl 溶液溶解后移入1 000 mL容量瓶中,用去离子水稀释至刻度,摇匀。
0.01 g/L铁标准溶液的配置:将0.1 g/L的铁标准溶液准确移取稀释10倍而成;1% 盐酸羟胺溶液(因其不稳定,需临时用配);0.1 % 邻菲罗啉(新配制)。
HAc-NaAc缓冲溶液的配置:136 g NaAc和120 mL 纯HAc混合稀释至500 mL容量瓶;1%的Vc溶液(新配置)。
2 结果与讨论
2.1 波长对吸光度的影响
移取3 mL铁的标准液 (0.01 g/L)于50 mL的容量瓶中,依次加入5.0 mL缓冲溶液,2.5 mL盐酸羟胺,5.0 mL邻菲罗啉,并用去离子水稀释至刻度线。以去离子水为参比液,在波长460~550 nm范围内测量该标准铁溶液的吸光度。以波长为横坐标,吸收度A为纵坐标,绘制吸收曲线。
由图1可知,在波长为510 nm处有最大的吸收度,因此后面实验所采用的波长均为510 nm。

图1 波长对吸光度的影响
2.2 缓冲溶液的用量对吸光度的影响
按照标准缓冲溶液的配置方法,应该是136 g NaAc和120 mL 纯HAc混合稀释至500 mL容量瓶,在配置标准溶液和待测液时,每次加入5 mL 的缓冲溶液。但是根据缓冲溶液的特性,只要加入的试剂不是强酸、强碱,则几乎不改变弱酸 (HAc) 和其共轭碱 (NaAc) 的配比,即使加入较少的缓冲溶液,也可以很好地控制溶液的pH值。为了验证缓冲溶液用量对于吸光度的影响,取6个编号为1~6的50 mL的容量瓶,分别加入1~6 mL的缓冲溶液,然后在每个容量瓶里面分别加入3 mL, 0.01 g/L标准铁溶液, 2.5 mL 盐酸羟胺,5 mL邻菲罗啉,测量相应的pH值和吸光度。测量结果如表1所示。
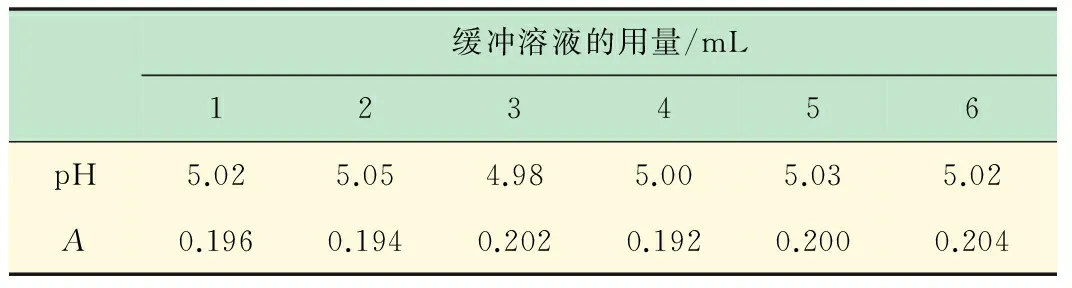
表1 缓冲溶液用量对吸光度的影响
根据表1的测量结果,发现减少缓冲溶液试剂的用量对于溶液的pH值影响很小,对于溶液的吸光度也基本没有影响。因此为了节约教学成本,减少实验试剂的使用量,在配置标准铁溶液时,均采用1 mL缓冲溶液控制溶液的pH值。
2.3 显色时间对吸光度的影响
为了研究显色时间对于吸光度的影响,移取3 mL铁的标准液 (0.01 g/L)于50 mL的容量瓶中,依次加入1.0 mL缓冲溶液,2.5 mL盐酸羟胺,5.0 mL邻菲罗啉,并用去离子水稀释至刻度线。以去离子水为参比液,开始每隔10 min测量1次该溶液的吸光度,到达1 h后,每隔1 h测量1次溶液的吸光度。
由图2发现,显色时间对吸光度存在一定影响。当显色时间到达50 min后,吸光度的值已经非常稳定,不再变化。表明在50 min内,亚铁离子和邻菲罗啉的显色反应已经完成。在以往实验教材里面,一般要求显色时间为10 min左右。图2实验数据表明,10 min后测定的吸光度和50 min后测定的吸光度差别已经很小。对于一般的教学实验,由于上课实验时间的限制,在充分摇匀基础上,采用10 min后测A也是可行的。但是对于工业废液等微量铁离子含量的测定,最好在1 h以后进行,这样可以减少一定的误差。

图2 显色时间对吸光度的影响
2.4 显色剂用量对吸光度的影响
作为显色剂,邻菲罗啉的用量既要保证亚铁离子的显色,但也要避免试剂浪费。理论上,1 mol的亚铁离子需要3 mol的邻菲罗啉,以形成稳定的橘红色络合物。以往的实验教材里面规定0.1% 的邻菲罗啉显色剂用量为5 mL。但是一般情况下,标准的显色剂用量往往都超过实际需要的量。为了研究显色剂用量对吸光度的影响,分别取6个编号为1~6的50 mL容量瓶,然后在每个容量瓶里面分别加入5 mL, 0.01g/L标准铁溶液,1 mL 缓冲溶液,2.5 mL 盐酸羟胺,再分别加入1~6 mL的邻菲罗啉显色剂,测量相应的吸光度。测量结果如表2所示。

表2 显色剂的用量对吸光度的影响
根据表2的测定结果,发现2 mL显色剂的用量已足够使用。这主要是因为以往教材里面所使用的邻菲罗啉显色剂用量已经大大超过实际所需要的量。因此,为了节省实验成本,减少实验试剂的用量,在大规模的教学实验过程中,采用2 mL邻菲罗啉溶液配置铁的标准溶液。
2.5 还原剂的选择及标准曲线的绘制
对于该实验,一般都是采用盐酸羟胺作为还原剂,将三价铁还原为二价铁。但是盐酸羟胺作为一种有毒试剂,并且在使用过程很不稳定,每次实验均需要临时配置。为了减少实验过程中带来的环境污染,实现绿色化学实验改革的目的,本实验拟采用维生素C作为还原剂,测试标准溶液的吸光度,并和盐酸羟胺的测试结果进行比较。下面为两组标准铁溶液的配置。
第一组采用盐酸羟胺配置的标准铁溶液:分别移取铁的标准液 (0.01 g/L) 1.0~5.0 mL于编号1~5的5只50 mL容量瓶中,依次加入1.0 mL 缓冲溶液,2.5 mL盐酸羟胺,2.0 mL邻菲罗啉溶液,并用去离子水稀释至刻度线,摇匀,放置50 min。
第二组为采用维生素C配置的铁标准溶液,将盐酸羟胺换成了具有同样还原功能的维生素C 2.5 mL,其余步骤同上。
在510 nm波长处,测得编号1~5的3组含铁溶液的吸光度,分别以1~5号标准铁溶液的含铁量为横坐标,吸光度为纵坐标,通过Origin作图软件,进行线性回归,得到两条拟合的标准曲线(见图3)。
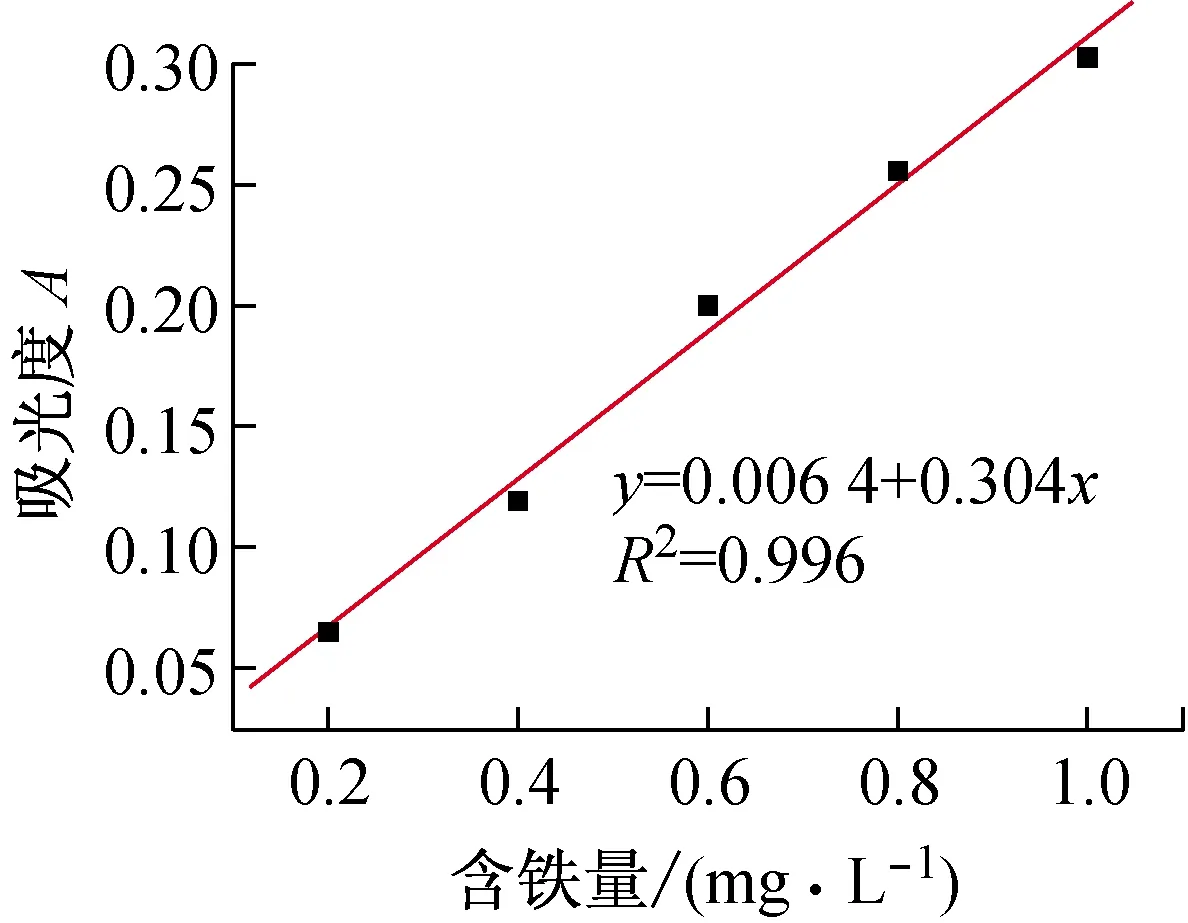
(a) 添加盐酸羟胺

(b) 添加维生素C
分析图3可知,不论是添加还原剂盐酸羟胺或是还原剂维生素C,都能得到相关性很好的标准曲线。并且对于含铁量相同的标准铁溶液,所测得的吸光度差别非常小。因此,对于邻菲罗啉分光光度法测定微量铁的实验,采用无毒和更加环保的维生素C做还原剂是完全可行的。
2.6 未知液含铁量的测定
以上标准曲线的绘制,采用了两种还原剂,并对结果进行了比较分析。对于未知待测液,同样采用两种还原剂进行配置。首先,移取未知待测液3 mL 于编号为6的50 mL容量瓶中,然后分别添加1 mL的缓冲溶液,2.5 mL的盐酸羟胺,2 mL的邻菲罗啉,最后加去离子水至刻度线,摇匀,放置 50 min。
另外移取相同的未知待测液3 mL于另一个编号为6的50 mL容量瓶中,然后分别添加1 mL 的缓冲溶液,2.5 mL的维生素C,2 mL的邻菲罗啉,最后加去离子水至刻度线,摇匀,放置50 min。
以上配置的两组未知待测液,理论上含铁量是完全相同的。下面对以上两组未知待测液分别测试它们的吸光度。第一组加盐酸羟胺的吸光度为0.166;第二组加维生素C的吸光度为0.168。根据上一节所得到的两组标准曲线,带入相应的线性回归公式,分别得到第一组的含铁量为0.525 mg/L,第二组的含铁量为0.532 mg/L。由于本实验在操作过程中,所需量取的溶液较多,难免会引入一定的误差,因此可以认为以上两种方法所测得的含铁量基本一致。故采用维生素C代替传统的还原剂盐酸羟胺是完全可行的。
2.7 实验数据的不确定分析
尽管该实验具有取样少,分析快、简便、准确和灵敏度高等优点,但是在配置溶液时,由于量取的化学试剂较多,这些步骤都会或多或少的引入一些误差。此外,在使用分光光度计时,也要严格按照实验的规定进行,否则也会给实验带来一定的不确定度。比如,仪器预热20 min后,开始测量前需要反复调透光率0%和透光率100%。比色皿必须用去离子水洗涤干净,拿取比色皿时,只能用手捏住比色皿的毛玻璃面,装待测液时,应先用待测液润洗2或3次,保证待测液浓度不变,倒入的溶液应在2/3左右而不要太满,放时应将透光面对着光路。此外,实验完毕后用专用的洗涤液以及去离子水清洗比色皿,晾干后存放在比色皿盒内,不能用强碱溶液和强氧化剂洗涤,以免腐蚀玻璃,测量时最好从低浓度到高浓度进行,这样可减少实验的误差。
3 结 语
在邻菲罗啉分光光度法测定微量铁的实验教学过程中,发现该实验的影响因素较多,各种教材的版本也不统一。为此,本文探讨了吸收波长、缓冲溶液的用量、显色时间、显色剂的用量以及还原剂的选择对吸光度的影响,并找到最佳的实验条件。和以往传统的实验教学相比,在不影响实验教学效果的同时,改进后的实验不仅可以节省很多化学试剂,也减少了一定的环境污染。
[1] 张 琨. 铁元素分析方法的进展 [J]. 化学分析计量, 2011, 20(3) : 95-98.
[2] 李国强, 杨建君, 何家洪, 等. 分光光度法测定铁(Ⅲ)的研究进展 [J]. 冶金分析, 2014,34(1) : 34-44.
[3] 常西亮, 赵金安. 双波长分光光度法测定自来水中Fe(Ⅱ)和Fe(Ⅲ)的含量 [J]. 山西化工, 2003, 23(3) : 27-29.
[4] 陆娜萍, 年季强, 朱春要, 等. 微波消解-邻二氮菲分光光度法测定高炉渣中的全铁 [J]. 光谱实验室, 2012, 29(5) : 3042-3046.
[5] 宣亚文, 武 文. 分光光度法测定工业废水中的铁 [J]. 光谱实验室, 2011, 28(3) : 1560-1563.
[6] 李建雄. 自来水中铁含量测定的实验研究 [J]. 内蒙古石油化工, 2011(6) : 4-6.
[7] 郭小群, 谯康全, 蔡述兰, 等. 邻菲罗啉分光光度法测定自来水中的铁(Ⅲ)含量 [J]. 四川理工学院学报(自然科学版), 2008, 21(4) : 72-73, 79.
[8] 徐彦芹, 张 雪, 曹 渊, 等. 分光光度法测定全铁和亚铁的改进 [J]. 实验室研究与探索, 2013, 32(5) : 29-31.
[9] 姜 健. 分光光度法测定自来水中的铁含量 [J]. 辽宁化工, 2005, 34(4) : 183-184.
[10] 黄志中, 罗六保, 张世誉, 等. 邻二氮菲分光光度法测定铁条件选择实验的改进 [J]. 化工科技, 2008, 16 (6) : 50-53.
[11] 李丝红, 郭幼红. 邻二氮菲分光光度法测定微量铁实验探讨 [J]. 海峡药学, 2013, 25(8) : 82-85.
[12] 朱庆珍, 夏 红. 分光光度法测定微量铁实验方法的改进 [J]. 实验科学与技术, 2009, 7(6) : 25-27.
[13] 金 瑜. 邻菲啰啉分光光度法测定水中总铁的改进 [J]. 污染防治技术, 2010, 23(2) : 75-76.
[14] 雷丽红. 分析化学实验 [M]. 2版. 北京: 中国医药科技出版社, 2006: 138-140.
[15] 李吉学. 仪器分析 [M]. 北京: 中国医药科技出版社, 1999: 178-179.
[16] 张 威,张 斌. 仪器分析实训 [M]. 北京: 化学工业出版社, 2010: 25-27.
Investigating the Experimental Condition for Determination of Trace Iron by Phenanthroline Spectrophotometry
YAOXue-xia,DAICun-li,LIXiao-lin,LIUYu-tao
(College of Engineering, Nanjing Agricultural University, Nanjing 210031, China)
In the experimental teaching, phenanthroline spectrophotometry has been generally used to determinate the content of trace iron, because this method has less sampling, simple and high sensitivity. But in the course of the experimental teaching, it was found that many factors, such as the choice of the wavelength, the amount of buffer solution, the color time of color-developing agent, the amount of color-developing agent, and the selection of reductants and so on, had a certain impact on the final results. In addition, the different edition teaching materials have different operating methods. In order to better carry out the experimental teaching, the various factors effect on the absorbance were systematically analyzed. And the optimal experimental conditions were determined. Compared with traditional experimental teaching, the improved experiment can not only save many chemical reagents, but also reduce certain environmental pollution.
spectrophotometry; phenanthroline; hydroxylamine hydrochloride; vitamin C
2014-05-26
国家自然科学基金(No.41301261); 江苏省自然科学基金(No.BK20130680); 南京农业大学工学院实验教学改革研究项目(No.051010)
姚雪霞(1975-),女,安徽黄山人,讲师,现主要从事理论计算化学方向的研究。
Tel.:13770652672; E-mail:yaoxuexia@njau.edu.cn
O 6-339
A
1006-7167(2015)03-0016-04

