活性艳蓝KN-R溶液电化学脱色工艺研究
陈 镇,周 辉,钟 翔,聂国勇
(1. 湖南工程学院 化学化工学院, 湖南 湘潭 411104; 2. 湖南大学 环境科学与工程学院, 湖南 长沙 410082;3. 长沙天维环保设备有限公司,湖南 长沙 410013)
活性艳蓝KN-R溶液电化学脱色工艺研究
陈 镇1,2,周 辉1,钟 翔1,聂国勇3
(1. 湖南工程学院 化学化工学院, 湖南 湘潭 411104; 2. 湖南大学 环境科学与工程学院, 湖南 长沙 410082;3. 长沙天维环保设备有限公司,湖南 长沙 410013)
采用电化学法对活性艳蓝KN-R溶液进行脱色研究,考察了主要影响因素电流密度、脱色时间、电解质浓度、电极间距、染液温度、pH、搅拌转速等对脱色效果的影响,并采用正交实验对脱色工艺进行了优化。结果表明,活性艳蓝KN-R溶液电化学脱色最佳工艺为:电流密度55 A/m²、脱色时间25 min、电解质浓度30 g/L、极距7 cm、室温、染液初始pH值6、转速60 r/min,该工艺下,能实现染料的100%脱色。同时,整个脱色过程简单、能耗低、效果好。
活性艳蓝KN-R;电化学;脱色;电能消耗
活性染料染色牢度好、色谱全、色泽艳、价格低,是纤维素纤维(棉、麻)、聚酰胺纤维(尼龙)、蛋白质纤维(羊毛、丝绸)染色的首选染料,产、销量居所有染料前列[1,2]。但活性染料存在固色率低(50%~80%)、需高盐(NaCl,30~50 g/L)助染等问题[3],经水洗后,约含有20%~50%的染料及大量的促染盐(20~40 g/L)随残液排入环境,形成色度高、盐度高、污染高的染色废水,是公认的难处理的废水[4,5]。
目前有关染液脱色的方法主要有物理吸附法:简单,但在处理效率及吸附剂再生方面有待改善[6,7];化学反应法:快速,但存在二次污染问题[8,9];生物降解法:环保,但其脱色效率还有待进一步提高[10,11]。电化学法具有其处理能力强、脱色效果好、不发生相变、无二次污染、操作连续、设备简单、占地小且易与其它方法联用等诸多优点[12-14]而在难处理有机废水领域受到极大关注。本文拟采用电化学法对活性艳蓝溶液进行脱色研究,为处理活性染料染色废液提供参考和支持。
1 实验部分
1.1 药品与仪器
1.1.1 药品
染料:活性艳蓝KN-R(广东得宝化工);电解质:食盐(市售);pH调节剂:氢氧化钠、盐酸(市售)。
1.1.2 仪器
(1)电化学实验装置如图1。

图1 电化学脱色实验装置Fig.1 Device of decolorization by electrochemical method
极板:石墨阳极,尺寸:8 cm(宽)×12 cm(高)×1 cm(厚);铜板阴极,极板尺寸:8 cm(宽)× 12 cm(高)×0.2 cm(厚),无色透明有机玻璃电解槽,尺寸:10 cm(长)×10 cm(宽)×10 cm(高),(以上材料由长沙天维环保设备有限公司提供)。PS-305DM直流稳压电流(东莞市龙威电子科技有限公司)。
(2)其他主要仪器:V-1200紫外/可见分光光度计(上海美谱达仪器有限公司),SZCL-4数显智能控温磁力搅拌器(巩义市予华仪器有限责任公司),电子天平(常州市宏衡电子仪器厂),烘箱(苏州台华烘箱设备有限公司)等。
1.2 实验内容
1.2.1 染液配置
以蒸馏水溶解活性艳蓝KN-R来配制染液。
浓度选择:活性染料上染棉织物饱和浓度一般为2%o·w·f(染料对织物重),染色浴比一般为1∶50(织物对染液重),以单位质量1 g计织物重,所需染料为0.02 g,所需染液体积为50 mL,则初始染液浓度为0.4 g/L,以染料最低上染率50%计,则染色后形成的废液中所含的染料浓度为 0.2 g/L。故,本实验所选择活性艳蓝KN-R染液的初始浓度为0.2 g/L。
1.2.2 脱色实验
(1)单因素实验:取活性艳蓝KN-R初始液于电解槽中,插入电极,连接电源,考察各单因素对脱色效果的影响,各单因素及其数值范围的选择如表1。
初始实验条件:活性艳蓝0.2 g/L,体积700 mL,电流密度50 A/m2、电解时间15 min、电解质浓度30 g/L、极距5 cm、溶液温度为室温23 ℃、pH为染液初始值6、搅拌转速60 r/min。
(2)正交实验:通过单因素实验得出主要影响因素,做三水平正交实验,优化脱色工艺。
(3)最佳工艺实验:通过正交实验得出因素影响顺次及最佳工艺,并进行电能消耗、极板损耗评估。
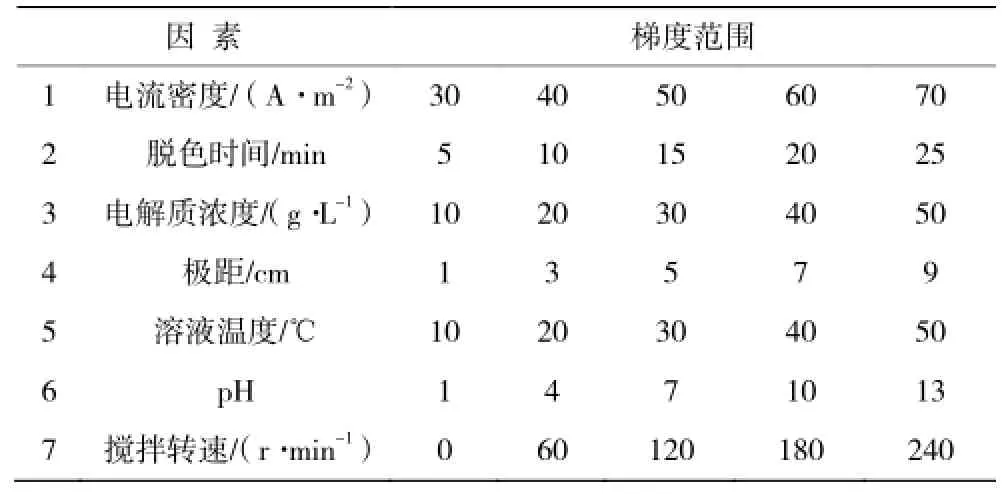
表1 单因素及梯度范围选择Table 1 Gradient of range of each factor
1.3 分析与测试
1.3.1 脱色率测定
紫外分光光度法:采用V-1200紫外/可见分光光度计在活性艳蓝KN-R592 nm最大吸收波长处对染液样品进行扫描,得到吸光度曲线,再对染色前后溶液进行吸光度测定,通过吸光度曲线来计算染液脱色前后的浓度,计算脱色率η。
染液浓度与吸光度的关系曲线:

其中:C—测试样品浓度,mg/L;A—测试样品吸光度;
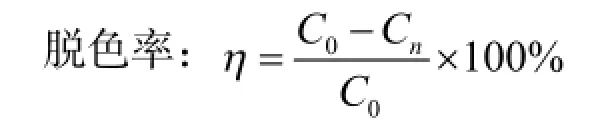
其中:η—染液脱色率,%;
C0—染液初始浓度,mg/L;
Cn—脱色后染液浓度,mg/L。
1.3.2 电能消耗
根据脱色实验时间设计,直流稳定电源上显示的电压、电流读数,按焦耳定律计算电能消耗W:
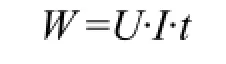
其中:W —电能消耗,J;
U —电压,V;
I —电流,A;
t —时间,s。
1.3.3 电极损耗
脱色实验前,将极板在乙醇溶液中浸泡15 min,然后用蒸馏水冲洗,软毛刷轻刷,毛巾擦干,放入65 ℃烘箱15 min,烘干称重,计M0;脱色实验结束后,将极板取出,冷水清洗,然后重复上述步骤,计Mn。则,电极损耗λ:
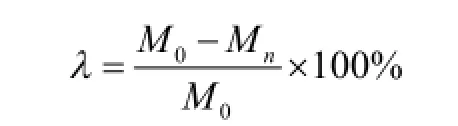
其中:λ—电极损耗率,%;
M0—脱色实验前电极质量,g;
Mn—脱色实验后电极质量,g。
2 结果与讨论
2.1 单因素实验
2.1.1 电流密度对染液脱色效果的影响
保持初始实验条件其它因素不变,根据表1单因素实验所设计的电流密度梯度及范围,考察电流密度在30、40、50、60、70 A/m2时对染液脱色效果的影响,结果如图2。

图2 电流密度对染液脱色效果的影响Fig.2 Effect of current density on the decolorization
从图2可以看出,电流密度对染液脱色效果有重要影响。随着电流密度的增加,活性艳蓝的脱色率呈不断增加趋势,在50 A/m2时达到94.1%,而后增速减缓,到60 A/m2时,脱色率达到99%以上。可见,电流密度对活性艳蓝的电化学脱色有着重要影响,电流密度大,同等条件下,阳极上释放的电子数量多,产生的能氧化染料分子的活性基或中间态物质多,则参与降解染料分子或破坏染料发色基团的物质数量就多,因此,溶液中染料被电化学氧化的数量就大,脱色率就越高。
2.1.2 脱色时间对染液脱色效果的影响
保持初始实验条件其它因素不变,根据表1单因素实验所设计的脱色时间梯度及范围,考察脱色时间为5、10、15、20、25 min时对染液脱色效果的影响,结果如图3。

图3 脱色时间对染液脱色效果的影响Fig.3 Effect of holding time on the decolorization
从图3可以看出,脱色时间对染液脱色效果有很大影响。随着脱色时间的增加,活性艳蓝的脱色率呈急剧上升趋势,在15 min时达到93.9%,而后脱色率提升缓慢,在25 min时脱色率95.4%。可见,在一定反应时间内,脱色时间对活性艳蓝的电化学脱色有着重要影响,在反应初期,染料被快速、大量氧化降解,但随着作用累积到一定时间后,剩余未被氧化降解染料数量减少,脱色率增加变得缓慢。
2.1.3 电解质浓度对染料脱色效果的影响
保持初始实验条件其它因素不变,根据表1单因素实验所设计的电解质浓度梯度及范围,考察电解质浓度在10、20、30、40、50 g/L时对染液脱色效果的影响,结果如图4。
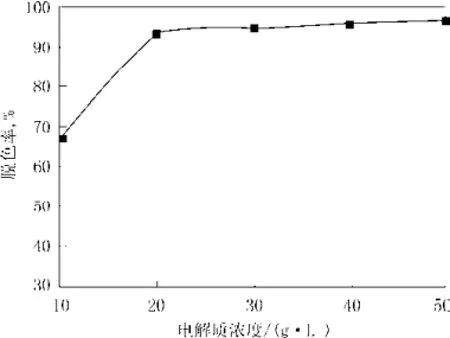
图4 电解质浓度对染液脱色效果的影响Fig.4 Effect of electrolyte concentration on the decolorization
从图4可以看出,电解质浓度对染液脱色效果有较大影响。活性艳蓝的脱色率在电解质浓度 10到20 g/L呈明显增加趋势,从67.2%增加到93.3%,在20 g/L后增速不明显。电解质在电化学反应过程中的主要作用是电荷迁移,使电路连通,它能将电极上所产生的电子输送到相对应电极上,在一定范围内,电解质浓度高,输送能力大,电子迁移数量多且转化快,氧化降解染料分子的数量多;但由于电流密度恒定,即单位时间内所产生的电荷数量是恒定的,因此,当溶液中的电解质数量超过一定值(电极上所产生电荷数量)时,多余的电解质离子无法有效做功,因此,脱色率增加不显著。
2.1.4 电极间距对染液脱色效果的影响
保持初始实验条件其它因素不变,根据表1单因素实验所设计的极距梯度及范围,考察电极间距在1、3、5、7、9 cm时对染液脱色效果的影响,结果如图5。
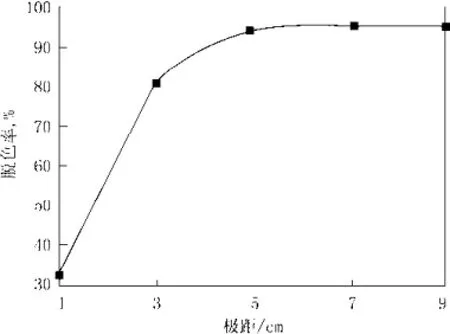
图5 电极间距对染液脱色效果的影响Fig.5 Effect of electrode spacing on the decolorization
从图5可以看出,电极间距对染液脱色效果有重大影响。染液脱色率随着极距的增加先快速增加,从1 cm时的33.6%上升到到5 cm 时的93.8%,随后增势减缓。在极距很短时,虽然阴、阳极板间电子交换频率很快,但由于在两极板间参与反应的有效溶液相对较少,而在两极板外侧的溶液占大多数,虽有搅拌,但两极板较小的间距还是限制了有效参与反应的溶液体积,随着极距的增加,两极板间的溶液体积越来越大,在有效反应区内的染料数量越来越多,染料被电化学氧化的数量越来越多,脱色率则越高,极距超过一定数值时,有效反应区内的染料分子数量与溶液中染料分子总数接近,因此,同等条件下,脱色率的增加不再明显。
2.1.5 染液温度对脱色效果的影响
保持初始实验条件其它因素不变,根据表1单因素实验所设计的染液温度梯度及范围,考察染液温度在 10、20、30、40、50 ℃时对脱色效果的影响,结果如图6。
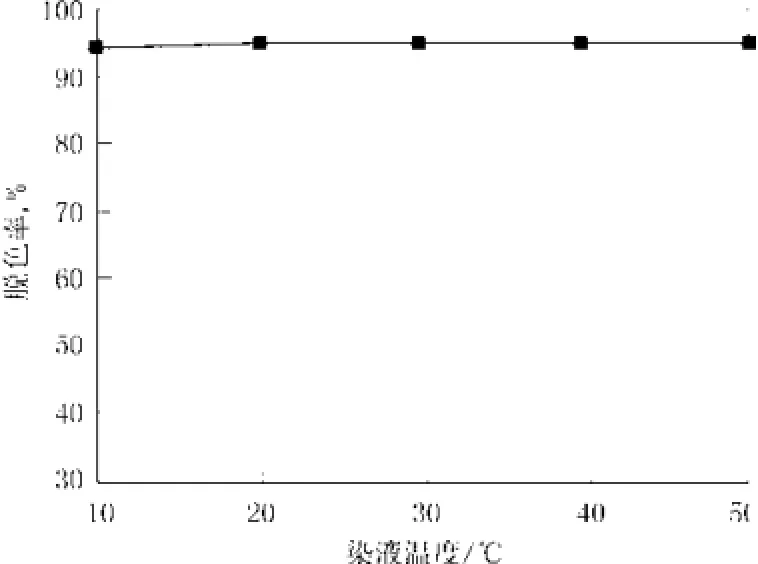
图6 染液温度对脱色效果的影响Fig.6 Effect of solution temperature on the decolorization
从图6可以看出,溶液体系温度对活性艳蓝的电化学脱色几乎没有影响。根据布朗运动定律,升高温度会使溶液体系内的分子活性提高,运动速率加大;但在本实验中,首先,活性艳蓝是完全均匀溶解在水溶液中的,所形成的相态是非常稳定的体系,其次,在电化学反应中,外加电场力和场能远远高于分子内部热运动的作用力及能量,因此,在常规条件下,染液温度的改变对脱色率并没有明显的影响。
2.1.6 染液pH值对脱色效果的影响
保持初始实验条件其它因素不变,根据表1单因素实验所设计的pH值梯度及范围,考察染液pH值在1、4、7、10、13时对染液脱色效果的影响,结果如图7。
从图7可以看出,在酸性、中性及弱碱性条件下(pH=1~10),染液的pH值对活性艳蓝的电化学效果脱色影响不大,但随着染液碱性继续加强,脱色率下降明显。
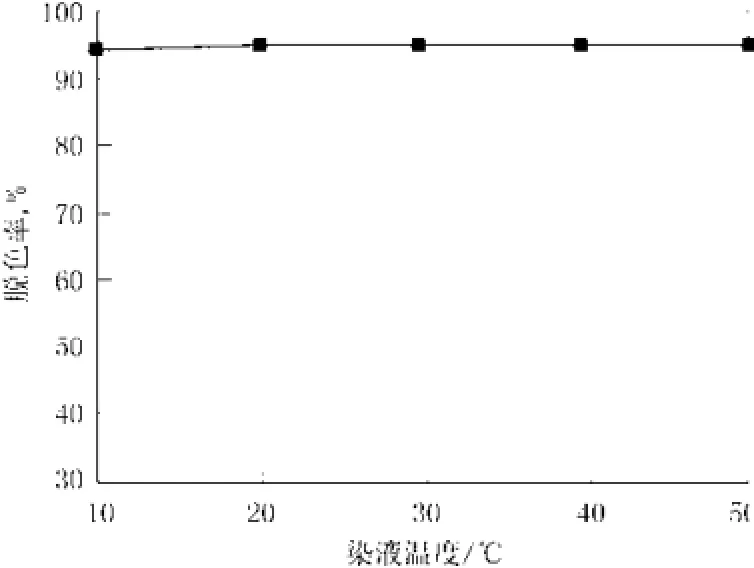
图7 染液pH值对脱色效果的影响Fig.7 Effect of solution pH on the decolorization
在电化学反应中,阳极反应为:OH-—e→O2,在电化学氧化中,阳极是产生中间态活性物质羟基自由基OH-→OH·,因此,随着pH值的继续增大,意味着染液中氢氧根离子浓度增加,则会抑制阳极反应,即同时抑制具有强氧化性的羟基自由基的生成,降低了氧化降解染料的有效物质的数量,因此脱色率降低。
2.1.7 搅拌转速对染液脱色效果的影响
保持初始实验条件其它因素不变,根据表1单因素实验所设计的磁力搅拌的转速梯度及范围,考察搅拌转速在0、60、120、180、240 r/min时对染液脱色效果的影响,结果如图8。

图8 搅拌转速对染液脱色效果的影响Fig.8 Effect of stirring speed on the decolorization
从图8可以看出,搅拌与否对染液脱色率还是有一定影响,不搅拌时,同等条件下,脱色率只有74%,而搅拌情况下,脱色率均高于90%,原因是通过搅拌作用,能加速两极板区域内溶液与两极板区域外溶液的交换,使反应过程中溶液中的染料分布均匀;但转速的过高对脱色率的提升并无积极影响,原因是在较高转速下,溶液具向外的离心力,其作用方向并不与电场力方向一致,因此,反而不利于阳极板所产生的活性基团与溶液中的染料分子快速结合、反应,因此脱色率不升反略有下降。
2.2 正交实验设计及结果分析
综合上述单因素实验,选择电流密度、脱色时间、电解质浓度、极距作为本次活性艳蓝KN-R电化学脱色的主要影响因素,在室温(23 ℃)、溶液初始pH值(pH=6)、低转速(60 r/min)下,作4因素3水平L9(34)正交实验,进一步优化活性艳蓝的电化学脱色工艺,其水平选择、实验结果及正交分析的k值、R值见表2。

表2 电化学脱色正交实验设计及结果分析Table 2 Results and analysis of orthogonally designed tests of electrochemical decolorization
根据表 2,按照极差大小得到了主次因素,可以看出,对于活性艳蓝电化学的脱色效果,电流密度是最重要的影响因素,脱色时间、电解质浓度、极距三者影响接近,但比电流密度的影响要小得多,根据正交实验结果,确定主要影响因素的最佳条件范围为电流密度55 A/m²、脱色时间25 min、电解质浓度30 g/L、极距7 cm。
2.3 最佳工艺下的脱色效果及能耗分析
在最佳工艺条件:电流密度55 A/m²、脱色时间25 min、电解质浓度30 g/L、极距7 cm、室温、染液初始 pH值 6、60 r/min转速下进行活性艳蓝KN-R电化学脱色实验,测定脱色率、电能消耗及极板损耗,结果如表3。

表3 最佳工艺下的脱色效果及能耗Table 3 Decolorization effect and energy consumption under the optimum process conditions
从表3可以看出,在最佳工艺条件下,在实验测定条件下,活性艳蓝脱色率 100%,其电能消耗为1 785 J,由于实验所用电流较低(0.31 A)且单次实验时间较短(25 min),极板损耗在常规测试条件下无法检出,几乎没有损耗。
3 结 论
(1)活性艳蓝KN-R溶液电化学脱色最佳工艺为:电流密度55 A/m²、脱色时间25 min、电解质浓度30 g/L、极距7 cm、室温、溶液初始pH值6、60 r/min转速,在该条件下,能实现染液的100%脱色。
(2)采用上述脱色工艺,电能消耗1 785 J,极板几乎没有损耗,同时,整个处理过程工艺简单、脱色效果好、节能环保。
[1]陈镇,胡灿辉,王世豪,许海龙.活性染料电化学氧化降解反应机理分析[J].哈尔滨师范大学自然科学学报,2012,28(5):73-74.
[2]王利平,葛川,王子鹤,高建云.活性染料羊绒绞纱染色技术[J].纺织学报,2011,32(9):84-88.
[3]何瑾馨. 染料化学[M]. 北京:中国纺织出版社, 2009: 195-196.
[4]刘辉,赵翠,李萍.印染废水集成处理技术研究发展[J].当代化工,2014,43(5):806-808.
[5]AE Ghaly, R Ananthashankar, M Alhattab and VV Ramakrishnan. Production, Characterization and Treatment of Textile Effluents: A Critical Review[J]. Journal of Chemical Engineering & Process Technology, 2014, 5(1):1000182.
[6]Mohammed M.A., Shitu A. , Ibrahim A. Removal of Methylene Blue Using Low Cost Adsorbent: A Review[J]. Research Journal of Chemical Sciences,2014,4(1):91-102.
[7]T. Lakdioui; M. Berradi; J. El Azzaoui. Kinetic Studies of the Adsorption of Two Major Textile Dyes Dyeing Indigo and Red Cibacrone on Activated Carbon and Anion Resin in an Aqueous[J]. International Journal of Engineering Research and Technology, 2014,3(3): 2412-2416.
[8]Zahra Monsef Khoshhesab; Katayon Gonbadi; Gholamreza Rezaei Behbehani. Removal of Reactive Red 74 Dye from Textile Industrial Waste using Zinc Oxide Nanoparticle [J].Journal of Advances in Chemistry,2014(1):1077-1084.
[9]任南琪,周显娇,郭婉茜,杨珊珊. 染料废水处理技术研究进展[J].化工学报,2013,64(1): 84-94.
[10]Hong-Wen Sun; Hong-Wei Hu; Lei Wang. The Bioconcentration and Degradation of Nonylphenol and Nonylphenol Polyethoxylates by Chlorella vulgaris[J]. 2014, 15(1): 1255-1270.
[11]Beenish Saba; Madeeha Jabeen; Tariq Mahmood. Treatment Comparison Efficiency of Microbial Amended Agro-waste Biochar Constructed Wetlands for Reactive Black Textile Dye[J]. International Proceedings of Chemical, Biological and Environmental Engineering, 2014,65: 13-16.
[12]Zhen Chen, Xinliang Yu, Xianwei Huang ,,Shihua Zhang. Prediction of reaction rate constants of hydroxyl radical with organic compounds[J]. Journal of the Chilean Chemical Society, 2014,58(1):1986-1993.
[13]陈镇,汪南方,刘日平,聂国勇.离子膜电解处理活性染料染色废水工艺研究[J].湖南工程学院学报(自科版),2013(2):101-104.
[14]Gamal O. El-Sayed, Mohamed S. Awad , Zahraa A.Ayad. Electrochemical Decolorization of Maxilon Red GRL Textile Dye[J].International Research Journal of Pure & Applied Chemistry, 2014, 4(4): 402-416.
Study on Electrochemical Decolorization Process of Reactive Brilliant Blue KN-R Solution
CHEN Zhen1,2, ZHOU Hui1, ZHONG Xiang1, NIE Guo-yong3
(1. School of Chemical & Chemistry Engineering, Hunan Institute of Engineering, Hunan Xiangtan 411104,China; 2. College of Environmental Science & Engineering, Hunan University, Hunan Changsha 410082,China; 3. Changsha Tianwei Environmental Protection Equipment Co., Ltd., Hunan Changsha 410013,China)
The reactive brilliant blue KN-R solution was decolorized by electrochemical method. The influence of some factors on the decoloration was discussed, including current density, decolorization time, electrolyte concentration, solution temperature, distance of electrodes, pH of solution, stirring speed. And the decolorization process was optimized by orthogonal experiment. The results show that, the optimum decolorization process conditions of reactive brilliant blue KN-R solution by electrochemical method are as follows: current density 55 A/m², decolorization time 25 min, electrolyte concentration 30 g/L, electrodes distance 7 cm, room temperature, dye solution original pH value 6, stirring speed 60 r/min. The reactive brilliant blue KN-R solution can thoroughly be decolorized under above conditions. On the other hand, the decolorization process is simple, perfect effect, energy saving and environmental protection.
Reactive brilliant blue KN-R; Electrochemical method; Decolorization; Electricity consumption
X703.1
A
1671-0460(2015)08-1762-05
湖南省高校重点实验室开放基金项目(20130101)。
2015-02-01
陈镇(1981-),男,湖南降回人,讲师,硕士,2007年毕业于中南林业科技大学环境科学专业,研究方向:主要从事环境友好型染整技术及印染废水处理研究。E-mail:chenzhen0732@163.com。

