3,4-二氨基苯甲酸水杨醛席夫碱合钴的制备
杨 云,霍宇辰,赵美娇,任 康,赵中雪
(1. 天津商业大学理学院化学系,天津 300134; 2. 中国人民武装警察部队后勤学院,天津市职业与环境危害防制重点实验室,天津 300162)
3,4-二氨基苯甲酸水杨醛席夫碱合钴的制备
杨 云1,2,霍宇辰1,赵美娇1,任 康1,赵中雪1
(1. 天津商业大学理学院化学系,天津 300134; 2. 中国人民武装警察部队后勤学院,天津市职业与环境危害防制重点实验室,天津 300162)
采用模板法,将3,4-二氨基苯甲酸、水杨醛和钴盐以1:2:1比例混合制备席夫碱合钴配合物,并对其进行了红外表征紫外及、摩尔电导和磁性等性质测定。数据分析结果表明:通过席夫碱合钴红外谱图和摩尔电导结果的对比和分析,表明金属与N原子进行了配位,钴盐中的阴离子并未参与配位;通过磁化率的测定,得出席夫碱合钴配合物中钴的单电子数为1,进而可以推测该配合物的分子构型是平面四边形。
水杨醛;席夫碱;钴配合物;表征
席夫碱类化合物及其金属配合物在生物活性、催化性能、分析化学、腐蚀以及光致变色领域的重要应用[1-3]。早在100多年前,Werner等就发现Co(II)的配合物具有键合氧原子的能力,并且过程是可逆的,所以人们不仅仅局限于研究席夫碱,更把重点延伸到了席夫碱的钴的配合物上来[4]。
本文以3,4-二氨基苯甲酸、水杨醛和钴盐为原料,设计并制备席夫碱合钴配合物,对其进行了红外表征及紫外、摩尔电导和磁性等性质测定。
1 实验部分
1.1 仪器和药品
水杨醛:天津市光复精细化工研究所;3,4-二氨基苯甲酸:上海迈瑞尔化学技术有限公司;电化学工作站(CHI660D北京华科普天科技有限责任公司);紫外-可见分光光度计(Lambda-25美国PE公司);傅里叶变换红外光谱仪(IR Affinity-1日本岛津公司) ; DPS-307A电导率仪(上海盛磁)。
1.2 3,4-二氨基苯甲酸水杨醛席夫碱合钴的制备
将0.152 1 g(1 mmol)3,4-二氨基苯甲酸溶于装有 10 mL无水甲醇三口瓶中,在氮气保护下将0.2442 g(2 mmol)水杨醛滴加到上述溶液中并加入0.12 g氢氧化钠固体调节pH约到7~8,向其中加入1 mmol的CoCl2·6H2O 在40 ℃条件下搅拌反应3 h。冷却,过滤,乙醇重结晶,产物(Co1L)产率为80%。重复上述操作将 CoCl2·6H2O改为 Co(NO3)2·6H2O和Co(CH3COO)2·6H2O产率分别为(Co2L)81%,(Co3L)78%。
2 结果与讨论
2.1 红外光谱分析
在3 300 cm-1左右的宽峰为羟基的吸收峰,表明苯环上的酚羟基参与了配位,配合物1 600~1 350 cm-1出现苯环骨架振动峰,发生了一定的红移,说明苯环的共轭在配位完成后变弱;配合物在 1 598 cm-1处的C=N的伸缩振动发生了红移,说明N原子参与了配位,并且在750 cm-1左右一个特别尖锐的峰,进一步证明了金属与N原子发生了配位[5]。从图1中发现在由不同原料的钴盐制备的产物的红外谱图中,波峰位置基本上完全一致,同时也并未发现钴盐阴离子产生的峰,由此可以推断在制备席夫碱钴配合物的过程中钴盐中的阴离子并未参加配位。
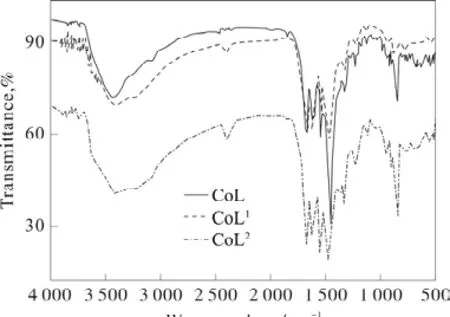
图1 配合物的红外光谱图Fig.1 IR spectra of Schiff base complexes
2.2 紫外光谱分析
从图 2中可以发现与钴的金属盐形成配合物后,225 nm,297 nm为苯环的特征吸收带;341 nm处为亚胺基C=N的π-π*跃迁特征吸收带,都不同程度的发生一定的蓝移[6]。
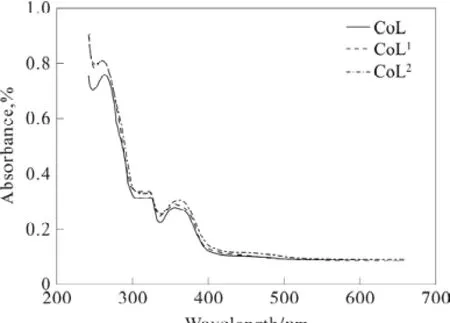
图2 配合物的紫外光谱图Fig.2 UV spectra of Schiff base complexes
2.3 磁化率数据分析
利用古埃法测定了配合物的摩尔磁化率[7]。经过计算发现三种不同原料制备的席夫碱钴配合物的单电子数都在1~2的范围内。考虑到实验过程中产生的误差及钴元素本身具有的轨道角动量,会使算出来的单电子比实际的单电子数偏大;所以可以推断合成的席夫碱钴的配合物中的钴离子所含有的单电子数是一个,钴离子是以二价的形式存在的,配合物是dsp2方式杂化结合成键的,具体的电子排最终产物可能以平面四边形的构型存在(表1)。
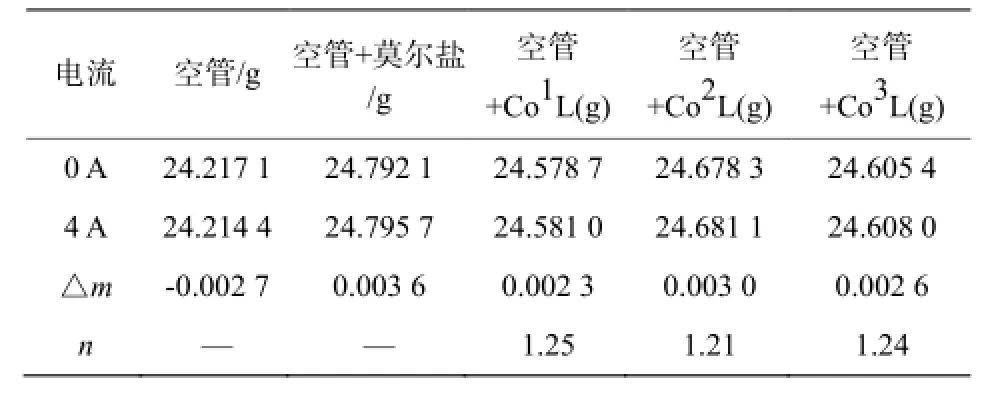
表1 配合物的摩尔磁化率测定Table 1 Moore susceptibility determination of Schiff base complexes
2.4 摩尔电导的测定
3种不同金属盐制备的席夫碱合钴配合物在无水甲醇中摩尔电导值都小于20 S·cm-1·mol-1,属于非电解质[8,9]。
3 结 论
从由3种原料制备的配合物的叠加红外谱图及后续的电导的测定,可以证明原料中的阴离子并未参与配位; 通过配合物磁化率的测定数据的计算,可以得出配合物的单电子数为 1,进一步推断配合物的分子构型为平面四边形。
[1] 江银枝,时永强,等.水杨醛缩环己二胺席夫碱配合物的合成及生物活性[J].浙江理工大学学报,2013,30(4):564-568.
[2] 闰小宁,王博,等.不对称席夫碱过渡金属配合物的合成和催化性能[J].化学研究与应用,2006,18(6):621-624.
[3] 陈玉红,丁克强,等.席夫碱研究应用新进展[J].河北师范大学学报(自然科学版),2003,27(1):71-74.
[4] 马继龙,武海,等. [CoL2]NO3的合成、晶体结构和红外光谱[J]. 阜阳师范学院学报(自然科学版),2005,22(2):4-6.
[5] 梅艳,钟昀. 双水杨醛缩邻苯二胺双希夫碱过渡金属(Ni,Cu,Cd)配合物的合成、结构及其荧光性质研究[J]. 江西化工,2010(4):64
68.
[6] 秦大斌,杨海英,雷刚.水杨醛缩邻苯二胺Schiff碱及其配合物的合成与催化性能[J].西华师范大学学报(自然科学版),2003,24(4):423-425.
[7] 王建华. 铜、钴、镍希夫碱配合物的合成及其性质的研究[J].淮北煤师报,1996,17(3): 46-49.
[8] 刘志昌,刘凡,等. 金属(Ni、Co、Zn)-Salen 配合物的合成及性质研究[J]. 乐山师范学院学报,2002,17(4): 30-33.
[9] W J Geary. The use of conductivity measurement in organic solvents for the characterisation of coordination compounds[J]. Coordination Chemistry Reviews,1971,7(1): 81-122.
Preparation of Cobalt(II) Schiff Base Complexes With 3,4-(Bis(salicylaldehyde)amino)benzoic Acid
YANG Yun1,2,HUO Yu-chen1,ZHAO Mei-jiao1,REN Kang1,ZHAO ZHong-xue1
(1. Department of Application Chemistry, College of Science, Tianjin University of Commerce, Tianjin 300134, China;2. Tianjin Key Laboratory for Prevention and Control of Occupational and Environmental Hazards,Logistics University of PAPF ,Tianjin 300162, China)
Cobalt(II) schiff base complexes with 3,4-(bis(salicylaldehyde)amino)benzoic acid were synthesized by template method. The complexes were characterized by IR, UV-Vis, molar conductivity and magnetic properties. The results show that, cobalt salt anion is not involved in the complexes; it is found that there is only one unpaired electron in the complex, so it is proved the structure of the complex is square planar.
Salicylaldehyde; Schiff base; Cobalt(ii) complex; Characterization
TQ 028
A
1671-0460(2015)08-1743-02
中国人民武装警察部队后勤学院,天津市职业与环境危害防制重点实验室开放基金,项目号:2015WHKF04;天津商业大学校级“大创计划”资助项目,项目号:2015071。
2015-02-04
杨云(1976-),女,天津人,讲师,硕士研究生,研究方向:功能配合物及生物无机。E-mail:yyun@tjcu.edu.cn。

