新型耐酸钢在硫酸盐酸混合溶液中的腐蚀行为
张 聪,周 成,叶先祥
(北京科技大学 材料科学与工程学院,北京100083)
在冶金、电力、石化等工业领域,以重油或燃煤为主要燃料的烟气处理系统,如锅炉低温部位的空气预热器、省煤器、烟道、烟囱以及脱硫装置等,普遍会遇到燃料中含硫量偏高的情况。重油燃料中通常含有2%~3%的硫及硫化物,燃烧中绝大部分形成二氧化硫。二氧化硫中约有1%~5%在一定条件下与氧化合成三氧化硫。当它与烟气中水蒸汽(5%~18%)结合形成硫酸蒸汽时,会大幅度提高烟气的露点。当接触烟气的装置表面温度低于露点时,即发生酸液的凝结并强烈的腐蚀金属。这种现象称之为硫酸露点腐蚀[1-2]。同理,煤燃料中98%以上的氯转化成HCl留于废气中。比较低碳钢在燃烧废气中含HCl与不含HCl时的腐蚀量,当60℃以上时无差异,在60℃以下含有HCl的低碳钢腐蚀量明显增加[3]。因为在此温度下有HCl结露,称之为盐酸露点腐蚀。随着硫含量越来越高,导致燃烧或热交换系统设备遭受冷却过程中发生的露点腐蚀。在这种环境中不锈钢的腐蚀速率比低碳钢还高,因此也不易使用不锈钢。为解决这一难题,人们采用提高排烟温度的方法,或采用玻璃管等非金属材料管代替钢管,然而这样影响了热效率,也增加了技术上的难度[4]。
出于节能、降耗、减排的国家战略思路,发电、石化等行业要求排出气体的低温化(要求低于130℃)。低温化后低温段的硫酸露点腐蚀(60~70℃腐蚀最严重)更为严重,同时在低温段还产生盐酸露点腐蚀(露点温度60~70℃)。传统耐硫酸露点腐蚀钢服役温度高于130℃,该服役环境下仅需满足高温段硫酸露点腐蚀性能,不存在盐酸露点腐蚀现象[5]。因此传统的耐硫酸露点腐蚀钢已不适应于排烟低温化后的服役环境,因此,开发使用一种能够在硫酸和盐酸露点腐蚀环境下长期使用的新型耐酸钢,对于提高锅炉、省煤器、空气预热器、烟囱等部件的使用寿命,减少能耗和环境保护,都具有重要意义[6]。
本工作以16.9%H2SO4+0.35%HCl的混合溶液为腐蚀介质,在60℃的温度条件下进行试验,这是韩国一种烟气脱硫装置最具代表性的腐蚀环境[7]。实验室研制了一种新型耐硫酸盐酸露点腐蚀钢,这是一种添加了合金元素的低合金钢。在铁碳合金中,为了改进钢的某一种或几种性能,特意向钢中加入一定量的一种或几种合金元素。钼能有效地提高钢的抗大气腐蚀能力。当钢中含0.4%~0.5%钼时,在大气环境(尤其是工业大气)条件下钢的腐蚀速率可能降低1/2以上。钼的作用在于改善了锈层的性质,并能促使生成非晶态的氧化膜[8]。因此可以模拟在这种硫酸盐酸混合条件下,研究新型耐酸钢的耐硫酸盐酸露点腐蚀性能。
1 试验
1.1 腐蚀失重试验
试验材料为新型耐酸钢(称为1号钢)和Q235钢,其化学成分见表1。样品经机械加工后,再用800号到2000号砂纸逐级打磨,最后用丙酮和酒精清洗试样表面,放入干燥皿24h后称量,精确度为0.1mg,试样尺寸为50mm×25mm×4mm,取三个平行试样。腐蚀溶液为16.9%H2SO4+0.35%HCl的混合溶液,试验温度为60℃。在试样上方打一个φ2mm的孔,将1号试样和Q235试样分别悬挂浸泡在1 000mL的腐蚀溶液中6h。对于浸泡腐蚀后的试样,首先采用500mL盐酸+500mL去离子水+10g六次甲基四胺去除腐蚀产物,在室温下进行。疏松的外锈层除去后再用毛刷刷洗残留的锈层。锈层被除尽后的试样用蒸馏水冲洗,用酒精清洗,吹干后放入干燥器中,24h后称量。
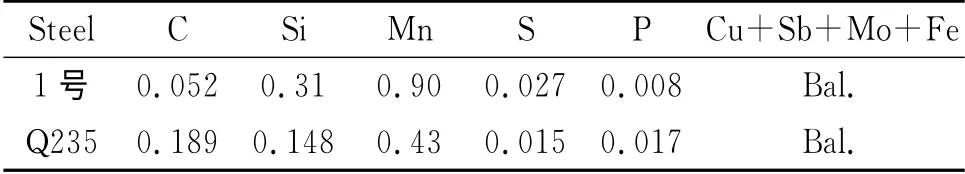
表1 1号钢和Q235钢的主要化学成分Tab.1 Chemical composition of 1#steel and Q235steelmass fraction/%
腐蚀速率采用下式计算:

式中:v是腐蚀速率,g·(m-2·h-1);W0是试样原始质量,g;Wt是试样除去产物后的质量,g;S是试样表面积,m2;t为浸泡时间,h。
1.2 电化学极化曲线和电化学阻抗谱测试
电化学测试在Princeton VMP3电化学工作站上进行,使用铂片作为辅助电极,饱和甘汞电极(SCE)作为参比电极,工作电极尺寸10mm×10mm×4mm,用铜导线点焊留出引线,用环氧树脂封住并留出10mm×10mm的工作面积,用砂纸打磨到2000号。腐蚀介质为16.9%H2SO4+0.35%HCl的混合溶液,由于在高温下测试开路电位(OCP)难以达到稳定状态,参考国内外研究方法降低试验溶液温度而不改变浓度,在室温条件下(20℃)进行电化学测试。动电位极化曲线和电化学阻抗谱(EIS)均在开路电位(OCP)达到稳定后进行,极化曲线测试电压扫描范围为-0.3~0.3V,扫描速率0.5mV/s。EIS测试频率范围为100mHz~10kHz,正弦电压振幅为10mV。
1.3 锈层微观形貌分析
将1号钢和Q235钢加工成15mm×15mm×4mm尺寸,置于16.9%H2SO4+0.35%HCl的混合溶液中,在60℃条件下全浸6h,取出试样吹干,置于干燥皿24h。采用ZEISS S-360型扫描电镜(SEM)观察试样表面锈层的致密度和连续性。
2 结果与讨论
2.1 腐蚀失重试验
试样在60℃的16.9%H2SO4+0.35%HCl的混合溶液中浸泡6h后,按照腐蚀速率计算公式,算出1号钢的Q235钢的腐蚀速率如表2所示。

表2 60℃的试样在16.9%H2SO4+0.35%HCl的混合溶液中的腐蚀速率Tab.2 The corrosion rate for specimens in 16.9%H2SO4+0.35%HCl solution at 60℃
从表2可以看出混合溶液中:1号钢的腐蚀速率为7.17g·m-2·h-1,Q235钢的腐蚀速率为225.01g·m-2·h-1,是1号钢的31倍,说明1号钢的耐硫酸盐酸露点腐蚀性能远优于Q235钢,含有铜,锑,钼的低合金钢适合于硫酸盐酸腐蚀环境。新型耐酸钢在Q235成分的基础上,适当减小碳含量,添加适量的合金元素铜,锑,钼可以使试样在腐蚀溶液中表面生成了一层致密的腐蚀产物,它有效地阻碍了腐蚀溶液对金属基体的进一步侵蚀,提高钢种的耐硫酸盐酸露点腐蚀性能。
2.2 动电位极化曲线
可以通过对1号和Q235试样进行极化曲线测试分析比较两个钢种的耐硫酸盐酸腐蚀性能。图1显示出两种试样在20℃的16.9%H2SO4+0.35%HCl的混合溶液中测得的极化曲线,极化曲线电化学参数拟合结果见表3。

表3 20℃时试样在16.9%H2SO4+0.35%HCl的混合溶液极化曲线测试的电化学参数Tab.3 Electrochemical parameters of potentiodynamic polarization measurements for specimens in 16.9%H2SO4+0.35%HCl solution at 20℃
从图1可以看出,在这种溶液条件下,刚开始时1号钢和对比钢Q235钢的阳极腐蚀电流密度均随着电位的升高而增大,呈活性溶解状态,没有明显的钝化区。但是随着电位的升高,1号钢的阳极腐蚀电流密度出现减小的趋势,这可能是由于合金元素铜,锑,钼的添加使试样表面生成了一层保护膜,可以抑制金属阳极活性溶解,同时抑制阴极析氢反应的发生,降低腐蚀电流密度,有效的阻碍腐蚀的进一步发生。而Q235钢由于没有添加合金元素,没有生成致密的保护膜,不能有效抑制金属阳极的活性溶解和阴极析氢反应的发生,阳极腐蚀电流密度继续增大,腐蚀更加严重。从表3可知1号钢的自腐蚀电流密度Jcorr比Q235的小很多,进一步说明添加了铜,锑,钼等合金元素的低合金钢1号较普通碳钢Q235具有优异的耐硫酸盐酸腐蚀性能。
其中年腐蚀速率根据Faraday定律及腐蚀电流密度按照公式推算出[9]:
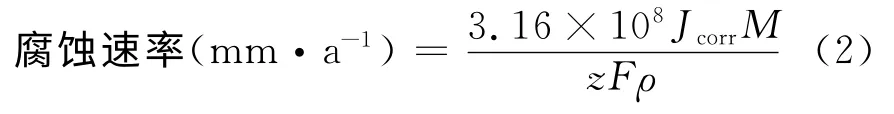
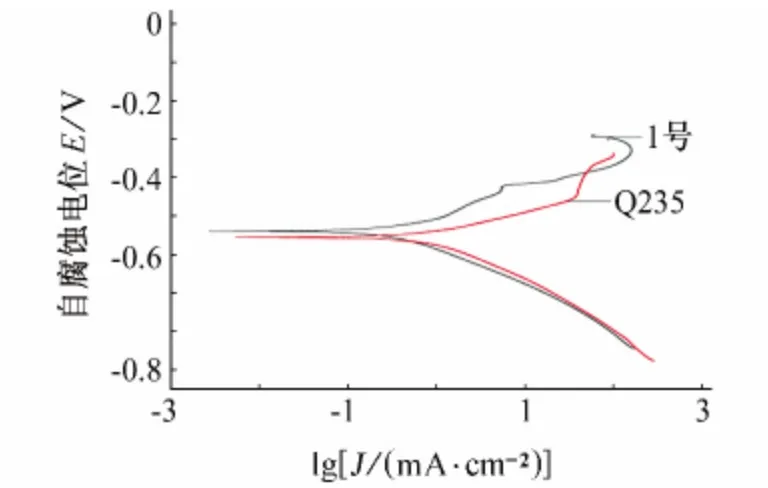
图1 20℃时试样在16.9%H2SO4+0.35%HCl的混合溶液极化曲线Fig.1 Potentiodynamic polarization curves for specimens in 16.9%H2SO4+0.35%HCl solution at 20℃
式中:Jcorr是自腐蚀电流密度(A·cm-2);M是金属的摩尔质量(g·mol-1);z是每个金属原子转移的电子数;F是Faraday常数;ρ是金属的密度(g·cm-3)。推算出的年腐蚀速率(表3),反映出1号钢相比Q235钢具有优异的耐硫酸盐酸腐蚀性能。
2.3 电化学阻抗谱
电化学阻抗谱测试能反映腐蚀速率的大小,校准溶液的电阻。图2是两种试样在20℃的16.9%H2SO4+0.35%HCl的混合溶液中测得的Nyquist图,Nyquist图中的高频容抗弧与试样表面生成的锈层相关,低频容抗弧与电荷转移过程相关,电化学阻抗谱显示的是一个半圆弧,如图3所示。
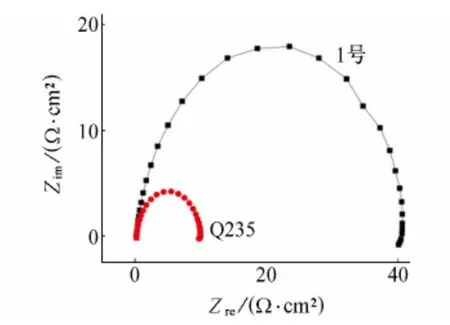
图2 20℃时试样在16.9%H2SO4+0.35%HCl的混合溶液中的Nyquist图Fig.2 Nyquist plot of specimens in 16.9%H2SO4+0.35%HCl solution at 20℃
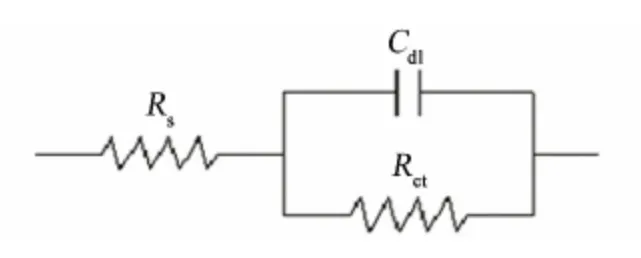
图3 电化学阻抗谱的等效电路图Fig.3 Equivalent circuit used to fit EIS data
将试样在16.9%H2SO4+0.35%HCl的混合溶液中的电化学阻抗谱进行等效电路拟合,如图3所示,等效电路图由溶液电阻Rs、双电层电容Cdl和电荷转移电阻Rct组成[10]。通过Zsimpwin软件拟合出电荷转移电阻Rct如表4所示。

表4 20℃时试样在16.9%H2SO4+0.35%HCl的混合溶液中的电荷转移电阻Tab.4 The charge transfer resistance for specimens in 16.9%H2SO4+0.35%HCl solution at 20℃
从电化学阻抗谱测试可以看出1号钢的电荷转移电阻为40.35Ω·cm2,Q235钢为9.62Ω·cm2,这说明在16.9%H2SO4+0.35%HCl的混合溶液中1号钢具有远比普通碳钢Q235优异的耐蚀性。说明合金元素铜,锑,钼的添加有利于增大金属的电荷转移电阻Rct,从而抑制金属的溶解反应。
2.4 锈层微观形貌分析
图4是1号钢和Q235钢在16.9%H2SO4+0.35%HCl的混合溶液中浸泡6h后的腐蚀产物微观形貌。从图4可以看出经过腐蚀浸泡后,1号钢发生均匀腐蚀,腐蚀产物很致密,腐蚀产物紧紧的粘附在金属基体表面,没有明显的裂纹和孔洞。进一步放大后发现1号钢的腐蚀产物由团簇状细小颗粒组成,这种腐蚀产物比较致密,对基体有更好的保护作用[11],能够减小腐蚀溶液对金属基体的腐蚀。而Q235发生沟槽状腐蚀,腐蚀产物有明显分层现象,局部腐蚀产物已经脱落,进一步放大后发现蚀孔和大量裂纹,这当然不能有效的抑制溶液对基体的进一步腐蚀。相反当孔洞和裂纹充满溶液时,会产生较大的腐蚀电流密度,加剧腐蚀的进行。因此添加合金元素铜,锑,钼可以使金属表面生成致密的保护膜,这样就能有效抑制腐蚀溶液对金属基体的进一步腐蚀,提升钢种的耐硫酸盐酸露点腐蚀性能。
3 结论
(1)新型耐酸钢在Q235成分的基础上,适当减小碳含量,添加适量的合金元素铜,锑,钼,可以大幅提高钢种的耐硫酸盐酸露点腐蚀性能。
(2)合金元素铜,锑,钼的添加可以同时抑制金属的阳极溶解反应和阴极析氢反应,降低腐蚀电流密度,增大金属的电荷转移电阻。
(3)合金元素铜,锑,钼的添加使钢在浸泡条件下生成了一层致密的保护膜,从而抑制了金属基体的进一步腐蚀。

图4 经过6h浸泡后试样表面的SEMFig.4 SEM images of specimens after 6himmersion(a) 1# (b) Q235
[1]王钧.耐硫酸露点腐蚀JNS钢板的研制[J].山东冶金,2007,29(3):31-32.
[2]王维宗.硫酸露点腐蚀机理与防护[J].石油化工腐蚀与防护,1992(4):16-22.
[3]许适群.关于露点腐蚀及用钢的综述[J].石油化工腐蚀与防护,2000,17(1):1-6.
[4]朱忠亚.耐硫酸露点腐蚀无缝钢管用低合金钢——09CrCuSb(ND钢):中华人民共和国,CN1490427A[P].2004-04-21.
[5]钱余海,李自刚,杨阿娜.低合金耐硫酸露点腐蚀钢的性能和应用[J].特殊钢,2005,26(5):30-34.
[6]RYUJI U,YASUSHI H,TAKUYA H,et al.Steels for energy production and transport[J].Nippon Steel Technical Report,2012(101):68-78.
[7]LE D P,JI W S,KIM J G,et al.Effect of antimony on the corrosion behavior of low-alloy steel for flue gas desulfurization system[J].Corrosion Science,2008,50:1195-1204.
[8]徐增华.金属耐蚀材料 第三讲 耐蚀低合金钢[J].腐蚀与防护,2001,22(3):135-138.
[9]SUN-AH P,SEUNG-HWAN L,JUNG-GU K.Effect of chromium on the corrosion behavior of low alloy steel in sulfuric acid[J].Met Mater Int,2012,18(6):975-987.
[10]PARK S A,WOO S J,JUNG G K.Effect of chromium on the corrosion behavior of low-alloy steels containing copper in FGD environment[J].Int J Electrochem Sci,2013,8:7498-7509.
[11]CHENG X Q,SUN F L,LÜS J,et al.A new steel with good low-temperature sulfuric acid dew point corrosion resistance[J].Materials and Corrosion,2012,63(7):598-606.

