华蟾素片辅助治疗癌痛的疗效观察
于 滨,于 慧,苏智祥,袁 彬,袁 媛
(1. 陕西省肿瘤医院,陕西 西安710061;2. 河北大学基础医学院,河北 保定 071000)
华蟾素片辅助治疗癌痛的疗效观察
于 滨1,于 慧2,苏智祥1,袁 彬1,袁 媛1
(1. 陕西省肿瘤医院,陕西 西安710061;2. 河北大学基础医学院,河北 保定 071000)

目的观察华蟾素片干预对规范癌痛治疗患者疼痛、生活质量和不良反应的影响。方法将160例癌痛患者按诊疗次序随机分成2组,对照组给予规范癌痛治疗,观察组给予蟾素片联合规范癌痛治疗。治疗2周后观察2组镇痛疗效、生活质量改善情况及不良反应发生情况。结果观察组癌痛缓解率及疼痛控制良好率均明显高于对照组(P均<0.05)。观察组治疗后除便秘、经济困难得分较治疗前升高外(P均<0.05 ),其余各指标得分均较治疗前明显降低(P均<0.05 );治疗后除经济困难得分2组比较差异无统计学意义外,其余指标2组比较差异均有统计学意义(P均<0.05 )。观察组便秘、恶心发生率明显低于对照组(P均<0.05 )。结论华蟾素片联合规范癌痛治疗可提高癌痛镇痛疗效,改善患者生活质量,减轻不良反应。
华蟾素片;规范化癌痛治疗;生活质量
自1995年美国疼痛学会将疼痛作为与血压、呼吸、体温、脉搏并列的生命体征后,癌痛在癌症患者的治疗中被逐渐关注。临床研究显示,初期癌症患者疼痛发生率在25%左右,而晚期癌症患者疼痛发生率为60%~80%,严重影响患者的生命质量[1]。目前恶性肿瘤患者人数逐年提高,预计到2020年这一数字将达到1 500万[2],癌痛患者数也将呈明显上升趋势,慢性癌痛的规范化治疗作为肿瘤姑息治疗的重要组成部分将越来越受到重视。笔者临床中发现,经过癌痛规范化治疗后,多数患者疼痛减轻,生活质量改善,但有部分患者镇痛疗效不佳,癌痛未良好控制,癌痛治疗中出现不良反应,影响患者生活质量及癌痛治疗。2012年9月—2014年7月,陕西省肿瘤医院采用华蟾素片辅助治疗癌痛患者,取得较好疗效,现报道如下。
1 临床资料
1.1一般资料 选择上述时期陕西省肿瘤医院收治的癌痛患者160例,均经病理组织学或细胞学确诊为恶性肿瘤中晚期,伴有癌痛,年龄>18岁,治疗前1个月内未行放化疗,预计生存期>3个月,无精神病史、吸毒史及麻醉药物滥用史,意识清楚,依从性较好。排除意识不清、严重心脑血管疾病及肝肾功能障碍、严重精神性疾病者,不能口服用药者。所有患者入组前均提前告知治疗方案,同意后签署相关知情文件。将患者按诊疗次序随机分成2组:观察组80例,男42例,女38例;中位年龄62岁;轻度疼痛(NRS评分1~3分)9例,中度疼痛(NRS评分4~6分)28例,重度疼痛(NRS评分7~10分)43例;对照组80例,男43例,女37例;中位年龄61岁;轻度疼痛7例,中度疼痛28例,重度疼痛45例。2组患者性别、年龄、疼痛程度及QLQ-C30比较差异均无统计学意义(P均>0.05),具有可比性。
1.2治疗方法 2组患者均给予规范癌痛治疗及支持治疗。疼痛评估根据癌痛评估应遵循的常规、量化、全面及动态评估的原则进行,按照全国癌痛规范化示范病房要求,参照《NCCN成人癌性疼痛控制指南(2012版)》、《2012 EAPC阿片类药物治疗癌痛指南》及相关专家共识,由医护人员共同完成。轻度疼痛者给予对乙酰氨基酚0.5 g/片,3次/d口服,中重度疼痛者给予阿片类药物进行镇痛。阿片类药物未耐受患者给予盐酸吗啡片起始剂量5~10mg口服,口服滴定阶段1 h评估,滴定稳定后按血药动力学原理4 h 1次。对阿片类药物耐受者,则根据前24 h吗啡用量转换:参照药代动力学原理,血药浓度预计达到高峰时进行疼痛评估(口服即释吗啡片1 h评估),疼痛评分≥7分者剂量增加50%~100%,疼痛评分4~6分者剂量增加 25%~50%,疼痛评分≤3分者剂量增加25%,若疼痛评分持续≤3分则不继续加量。2~3个剂量周期确定吗啡每4 h用量(参照即释吗啡在人体代谢半衰期),在滴定过程中出现吗啡严重不良反应或患者疼痛控制良好减量25%~50%。观察24 h,疼痛控制稳定换算成缓释制剂盐酸羟考酮相应剂量。骨转移癌痛者加用塞来昔布,神经病理性疼痛者加用普瑞巴林。同时给予患者癌痛教育及心理疏导。治疗过程中出现镇静过度,观察2~3 d,未见好转予纳洛酮解救治疗;对爆发痛者,给予前24 h吗啡剂量的10%~20%;对疼痛难以控制或出现严重不良反应者改用芬太尼透皮贴(西安杨森);对出现烦躁、失眠等焦虑症状者给予艾司唑仑片治疗;中重度癌痛者治疗过程中给予缓泻剂。在上述治疗措施基础上,观察组给予华蟾素片(安徽金蝉生化股份有限公司,0.3 g/片)2片饭后口服,3次/d。
1.3观察项目 治疗2周后评定镇痛疗效、生活质量改善情况及药物相关不良反应发生情况。
1.3.1镇痛疗效 ①疼痛控制情况评估。控制良好:疼痛强度NRS评分≤3分,爆发痛次数≤3次/d,解救治疗次数≤3次/d;控制不佳:疼痛强度NRS评分>3分或未降低,爆发痛次数>3次/d,解救治疗次数>3次/d。②疼痛缓解度评估。疼痛未减轻为未缓解,疼痛减轻1/4为轻度缓解,疼痛减轻1/2为中度缓解,疼痛减轻3/4为明显缓解,疼痛消失为完全缓解。中度缓解+明显缓解+完全缓解为疼痛缓解。
1.3.2生活质量 应用欧洲癌症研究与治疗组织(EORTC)生活质量核心量表QLQ-C30 (V3.0)中文版[3]进行问卷及评定,功能领域和总体健康领域得分越高说明功能状况和生命质量越高,症状领域得分越高表明症状或问题越多(生命质量越差)。
1.4统计学方法 采用SPSS 19.0软件进行数据分析。计数资料采用2检验;计量资料以表示,采用t检验,P<0.05为差异有统计学意义。
2 结 果
2.12组镇痛疗效比较 2组患者均完成治疗,观察组疼痛控制良好62例(78%),对照组疼痛控制良好47例(59%);观察组疼痛控制良好率及疼痛缓解率均明显高于对照组(P均<0.05)。见表1。

表1 2组疼痛缓解情况比较
注:①与对照组比较,P<0.05。
2.22组治疗前后QLQ-C30(V3.0)量表评分比较 观察组治疗后除便秘、经济困难得分较治疗前升高外(P均<0.05),其余各指标得分均较治疗前明显降低(P均<0.05 );治疗后除经济困难得分外,其余指标2组比较差异均有统计学意义(P均<0.05 )。见表2。
2.32组不良反应发生情况 2组患者均发生止痛药物常见不良反应,多出现在治疗开始后1周之内。2组患者均未出现吗啡中毒症状及嗜睡3d以上情况。观察组便秘、恶心发生率明显低于对照组(P均<0.05),其他不良反应发生率2组比较差异无统计学意义(P均>0.05)。见表3。
3 讨 论
癌痛是21世纪公共健康的大敌,控制癌痛已成为肿瘤康复与姑息治疗需首要解决的问题,缓解疼痛是基本人权,然而时至今日即使在许多发达国家离此目标仍有差距。欧洲肿瘤内科学会2008年7月公布的一项有关癌痛治疗情况的调查结果显示,平均约43%的癌痛患者没有得到有效的止痛治疗[1]。且迄今仍没有一个成熟有效的体系去对癌痛的规范化诊疗做出科学评估。虽然美国疼痛协会(AmericanPainSociety,APS)曾致力于评估和改善疼痛诊疗水平并设置相应推荐指南,但始终没有统一标准去评估癌痛诊疗的好坏[4]。随着各学术团体及政府组织癌痛指南制定,临床疗效有所提高,但距离癌痛患者无痛睡眠、无痛休息、无痛活动的目标还有较大差距。
癌痛治疗对中晚期肿瘤患者实际获益主要体现在疼痛控制及生命质量改善。阿片类药物随着剂量增加镇痛效果加强,但不良反应也随之增加或加重。在镇痛治疗及药物不良反应之间很难取得平衡是癌痛治疗效果并不理想的原因之一。目前癌痛治疗注重全程管控,综合治疗,治疗手段包括放化疗、靶向治疗、生物治疗、微波、介入、神经毁损、手术等。中晚期癌痛患者由于肿瘤消耗,体质较差,大部分患者不能耐受细胞毒药物不良反应,并不能从抗肿瘤治疗中获益。随着靶向药物开发及靶向药物应用范围扩大,小部分肿瘤患者可以从靶向治疗中获益,患者易耐受,但大部分肿瘤患者通过基因及蛋白相关检测并未发现靶向药物作用的靶点,不适于靶向治疗。经济原因也限制靶向药物的应用。故中医药治疗癌痛越来越受到重视。目前研究显示,中医药治疗癌痛疗效确切,可显著改善患者症状,提高患者生活质量,且不良反应少[5]。华蟾素是以中药蟾皮为主要原料制成的抗癌药物,具有清热解毒、活血化瘀、软坚散结之功效[6]。现代研究认为,华蟾素具有抗肿瘤、免疫促进、抗病毒作用,广泛用于消化道肿瘤、肺癌等肿瘤治疗中,与化疗及靶向治疗联合应用临床疗效较好,可减轻细胞毒治疗及靶向治疗不良反应。胡卫等[7]研究发现华蟾素可提高癌痛模型小鼠热痛和机械痛阈值,认为该药物的止痛机制可能与提高肿瘤局部病变组织β-END的含量有关。余雪琴[8]发现华蟾素镇痛作用可以被阿片受体拮抗剂所阻断,推测其可能是通过阿片受体来达到镇痛作用。巩仔鹏[9]研究认为华蟾素镇痛的机制可能与其所含生物碱提高了机体痛阈有关。杨新波[10]报道华蟾素胶囊与硫酸吗啡控释片对癌痛的缓解程度相当,但华蟾素组不良反应少。
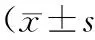
表2 2组QLQ-C30(V3.0)量表评分比较,分)
注:①与治疗前比较,P<0.05;②与对照组比较,P<0.05。
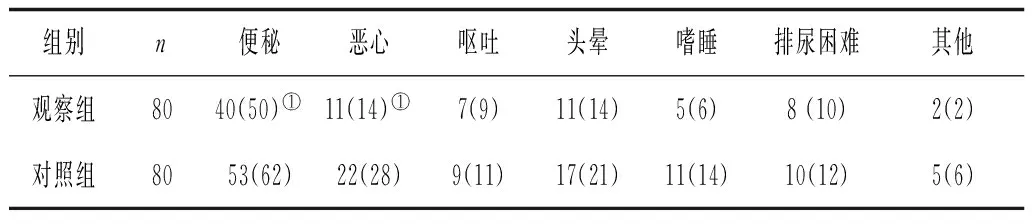
表3 2组不良反应发生情况比较 例(%)
注:①与对照组比较,P<0.05。
本研究结果显示,观察组癌痛缓解率及疼痛控制良好率均明显高于对照组;治疗后2组患者生活质量均较治疗前明显改善,治疗后除经济困难得分2组比较差异无统计学意义外,其余指标观察组改善情况均明显优于对照组;观察组恶心、便秘发生率明显低于对照组。提示华蟾素联合规范癌痛治疗可提高患者癌痛缓解率,改善患者生活质量,减轻不良反应,值得临床推广应用。
[1] Yost KJ,Hahn EA,Zaslavsky AM,et al. Predictors of health-related quality of life in patients with colorectal cancer[J]. Health Qual Life Outcomes,2008,6:66
[2] Frankish H. 15 million new cancer cases per year by 2020,says WHO[J]. Lancet,2003,361(9365):1278
[3] 万崇华,陈明清,张灿珍,等. 癌症患者生命质量测定量表EORCT QLQ-C30中文版评介[J]. 实用肿瘤杂志,2005,20(4):353-355
[4] 于洋,于世英. 癌痛规范化诊疗评估指标体系的构建研究[J]. 中国疼痛医学杂志,2012 ,20(18):225-230
[5] 赵志正,刘杰,林洪生. 中医药治疗癌性疼痛研究进展[J]. 世界中医药,2014,9(7):851-856
[6] 李杨. 华蟾素治疗晚期癌症19例疗效分析[J]. 山东医药,2011,51(13):97-98
[7] 胡卫,万信念,王晶,等. 华蟾素瘤周注射对癌痛模型小鼠癌痛行为的影响及外周机制研究[C]. 第九次全国中西医结合基础理论研究学术研讨会论文汇编,2013:267-275
[8] 余雪琴. 局部给予华蟾素对H22足部荷瘤小鼠癌痛行为的影响及其外周机制研究田[D]. 宜昌:三峡大学,2012
[9] 巩仔鹏. 从β-啡肽的表达探讨华蟾素治疗癌痛的外周机制研究[D]. 宜昌:三峡大学,2011
[10] 杨新波. 华蟾素胶囊治疗癌性疼痛的临床疗效观察[J]. 中国医药导刊,2014,16(3):478-479
Observe on the clinical curative effect of cinobufotalin tablets in the standardized treatment of cancer pain
YU Bin1, YU Hui2, SU Zhixiang1, YUAN Bin1, YUAN Yuan1
Objective It is to observe the influence of cinobufagin tablets intervention on analgesic effect, quality of life and adverse reaction for patients with standard treatment of cancer pain. Methods 160 patients with cancer pain were randomly divided into 2 groups according to the order of diagnosis and treatment, the patietns were treated with standard treatment of cancer pain in the control group, and with cinobufotalin tablets combined with standard treatment of cancer pain in the observation group. The analgesic effect, adverse reactions and quality of life of the both groups were observed. Results The remission rate and control rate of cancer pain in the observation group were significantly higher than that in the control group (allP<0.05). Except for the score of constipation and economic difficulties with significantly increased after treatment in the observation group (allP<0.05), the scores of the other indexes were significantly lower (allP<0.05); and there were significant differecent in all indexes except for the economic difficulties between the both groups (allP<0.05). The incidence of constipation and nausea in the observation group was significantly lower than that in the control group (allP<0.05).Conclusion cinobufotalin tablets combined with standard treatment of cancer pain can develop analgesic efficacy, improve the quality of life, reduce the adverse reaction
cinobufotalin tablets; standardized treatment of cancer pain; quality of life
于滨,男,硕士,主治医师,研究方向为中西医临床肿瘤的姑息治疗。
陕西省中医药管理局课题(LC63)
10.3969/j.issn.1008-8849.2015.36.003
R73
A
1008-8849(2015)36-3997-03
2015-07-20
(1. Shaanxi Provincial Tumor Hospital, Xi’an 710061, Shaanxi, China; 2. Basic Medical School of Hebei University, Baoding 071000, Hebei, China)

