复方苦参注射液联合GP方案治疗晚期非小细胞肺癌的Meta分析
丰育来,潘守杰,杨宁娟,殷长春
(江苏省连云港市中医院,江苏 连云港 222004)
复方苦参注射液联合GP方案治疗晚期非小细胞肺癌的Meta分析
丰育来,潘守杰,杨宁娟,殷长春
(江苏省连云港市中医院,江苏 连云港 222004)

目的 系统评价复方苦参注射液联合GP方案治疗晚期非小细胞肺癌的有效性及安全性。方法 计算机检索Cochrane Library、PubMed、中国生物医学文献数据库、中国期刊全文数据库、万方数据库、中文科技期刊全文数据库,检索时限为各数据库建库时间至2012年9月,搜索复方苦参注射液联合GP方案化疗对比单纯GP方案治疗晚期非小细胞肺癌的临床随机对照试验,任何语言的文献都在检索范围之内,由2名评价者独立评价并交叉核对纳入研究质量后,采用RevMan 5.2软件进行Meta分析。结果 共纳入12篇随机对照试验。Meta分析结果显示:与单纯GP方案化疗相比,复方苦参注射液联合GP方案治疗晚期非小细胞肺癌能提高近期疗效[OR=1.39,95%CI(1.08,1.79),P=0.01],改善患者的生活质量[OR=3.29,95%CI(2.30,4.71),P<0.000 01],减少白细胞下降[RR=0.45,95%CI(0.31,0.65),P<0.000 1],减轻呕吐反应[RR=0.38,95%CI(0.26,0.56),P<0.000 01]。结论 复方苦参注射液联合GP方案治疗晚期非小细胞肺癌能提高近期疗效,改善患者的生活质量,减少严重的化疗毒副反应。但需要更大样本的临床随机对照试验来进一步证实。
复方苦参注射液;非小细胞肺癌;化疗;Meta分析
美国癌症协会(American Cancer Society)统计数据显示,2014年预计将新出现224 210例肺癌患者,将会有86 930例男性、72 330例女性肺癌患者死亡,其病死率居所有肿瘤的首位[1]。在中国,2010年肺癌以46.08/10万人的发病率和37/10万人的病死率高居所有恶性肿瘤的首位[2]。肺癌正日益成为国内外对人类健康危害最大的疾病之一。肺癌可以分成小细胞肺癌(SCLC)和非小细胞肺癌(NSCLC),其中NSCLC约占所有肺癌患者的85%[1]。对于晚期NSCLC,以铂类为基础的两药联合化疗仍然是目前美国国立综合癌症网络(NCCN)制定的“NSCLC临床实践指南”所推荐的主要一线治疗方案,并且吉西他滨联合顺铂(GP)方案对于肺鳞癌患者具有更好的疗效。然而,尽管GP方案化疗能够提高晚期NSCLC患者的生存率,但是化疗的效果仍不甚理想且毒副作用较大,这些毒副作用严重影响了患者的生存质量,甚至很多患者因为不能耐受严重的不良反应而无法继续治疗。复方苦参注射液是一种由苦参、白土苓提取物组成的纯中药制剂,以苦参碱、氧化苦参碱等为主要有效成分[3]。苦参碱可通过抑制端粒酶活性、诱导细胞凋亡、抑制细胞增殖等途径作用于肺癌细胞而发挥抗肿瘤作用[4-5]。很多文献报道复方苦参注射液联合GP方案治疗NSCLC能够提高疗效,并降低不良反应。然而目前所进行的大多是小样本试验,缺乏一定的说服力。本研究旨在通过收集所有有关复方苦参注射液联合GP方案治疗晚期NSCLC的试验,采用Cochrane系统评价的方法,客观地评价复方苦参注射液的安全性和有效性,以期为晚期NSCLC的临床用药提供真实可靠的依据。
1 临床资料
1.1纳入标准
1.1.1 研究类型 随机对照试验(RCT),语言不限,无论是否采用盲法。
1.1.2 研究对象 纳入病例均经病理、细胞学检查证实为晚期NSCLC患者,年龄、性别不限;之前未接受化学治疗;治疗前无化疗禁忌证,肝肾功能、血液学、心电图无明显异常。
1.1.3 干预措施 试验组的干预措施为复方苦参注射液注射液静滴联合GP方案化疗,对照组的干预措施为单纯GP方案化疗。
1.1.4 结局指标 ①近期疗效:按照WHO抗肿瘤药物客观疗效标准[6]评价疗效,分为完全缓解(CR)、部分缓解(PR)、无变化(SD)和进展(PD),有效率=(CR+PR)/总例数×100%。②生活质量:以KPS评分(the Karnofsky performance scale)[7]为指标。治疗后KPS评分提高10分或以上为改善,下降10分或以上为恶化,提高或下降不足10分为稳定。③化疗毒副反应:根据WHO毒性反应分级标准[6]分为0~Ⅳ度,包括白细胞的降低及消化道不良反应。纳入研究的结局指标至少包含一项以上指标。
1.2 排除标准 ①非随机对照试验;②研究对象基线资料不一致,无可比性;③未使用GP方案化疗或联合其他化疗方案;④联合手术、放疗或其他治疗方法;⑤无本研究关注的结局指标。
1.3 资料来源和检索策略 检索PubMed(1966—2012年9月)、Cochrane Library(1988—2012年9月)、中国生物医学文献数据库(CBM,1978—2012年9月)、中国期刊全文数据库(CNKI,1984—2012年9月)、中文科技期刊数据库(VIP,1989—2012年9月)、万方数据库(1980—2012年9月)。检索词包括non-small cell lung cancer,non small cell lung carcinoma,nsclc,compound matrine injection,gemcitabine,chemotherapy,非小细胞肺癌,复方苦参注射液,岩舒注射液,吉西他滨,健泽,化疗等。RCT检索策略遵循Cochrane系统评价手册5.1.0[8],其他检索采用主题词与自由词相结合的方式,并根据具体数据库调整,所有检索策略通过多次预检索后确定。另外,追查已纳入文献的参考文献,与本领域的专家、通信作者等联系,以获取以上检索未发现的相关信息。
1.4 纳入研究的方法学质量评价和资料提取 按照Cochrane 5.1.0手册推荐的随机对照试验的质量评价标准进行。评价指标包括随机序列的产生、分配隐藏、盲法、数据缺失、选择性报道结果、其他可能的偏倚。质量评价由2位研究者独立进行并交叉核对,如遇分歧则通过讨论或请第3位研究者协助解决。2位研究者独立阅读所获文献题目和摘要,对可能符合纳入标准的试验阅读全文,以确定是否真正符合纳入标准,而后交叉核对,对有分歧的文献通过讨论或由第3位研究者决定其是否纳入。提取数据主要内容: ①一般资料,包括题目、作者姓名、发表日期和文献来源;②研究特征,包括研究对象的一般情况、各组患者的基线可比性及干预措施;③结局指标。如遇分歧通过讨论或根据第3位研究人员的意见协商解决。如试验报告不详或资料缺乏,通过信件与作者进行联系获取。
1.5 统计学方法 采用Cochrane协作网提供的RevMan 5.2.0软件进行Meta分析。计数资料采用相对危险度(relative risk,RR)或比值比(odds ratio,OR),计量资料则采用均数差(mean difference,MD) 分析统计,显著性水准设计为α=0.05,两者都取95%可信区间(95%CI)。采用I2对异质性进行定量分析,若I2>50%,则认为存在异质性。在各试验之间无临床异质性的前提下,存在统计学异质性时,则采用随机效应模式,反之,则采用固定效应模式,若存在临床异质性时,则放弃合并分析。必要时通过漏斗图来检验潜在的发表偏倚,同时为了确保Meta分析结果的可靠性,可采用不同的统计模型或取除低质量文献进行敏感性分析。
2 结 果
2.1检索结果 检索数据库共获得中文文献294篇,去重后阅读题目和摘要初步纳入29篇文献,再通过阅读全文排除不符合要求的文献,最后共纳入12篇文献[9-20],共包括1 022例患者。文献纳入流程见图1。
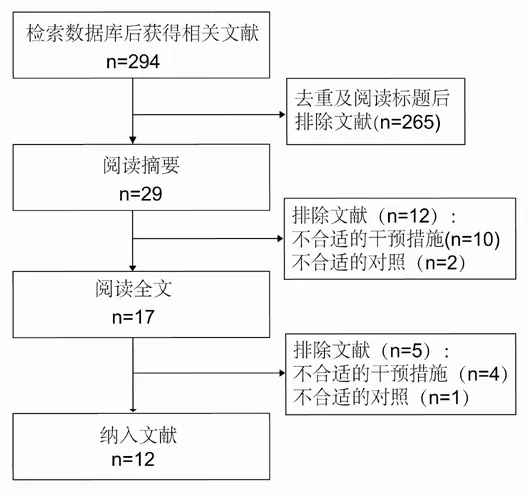
图1 文献纳入流程
2.2 纳入研究的基本特征 主要包括作者、发表年限、研究病例数、性别和年龄、治疗方案以及药物剂量等,在所有纳入的研究中均采用GP(吉西他滨 + 顺铂)化疗方案,至少化疗2个周期。复方苦参注射液均为静脉滴注,其中1篇文献[18]报道了复方苦参注射液用量为50~100 mL,1篇文献[19]用量为12 mL,1篇[10]为15 mL,其余[9,11-17,20]均为20~40 mL;除了有1篇[14]文献未报道Krnofsky评分或PS评分外,7篇文献[9-10,15-17,19-20]报道了Krnofsky评分≥60分,2篇文献[11,18]报道了Krnofsky评分≥70分,2篇文献[12-13]报道了PS评分≤2分。见表1。
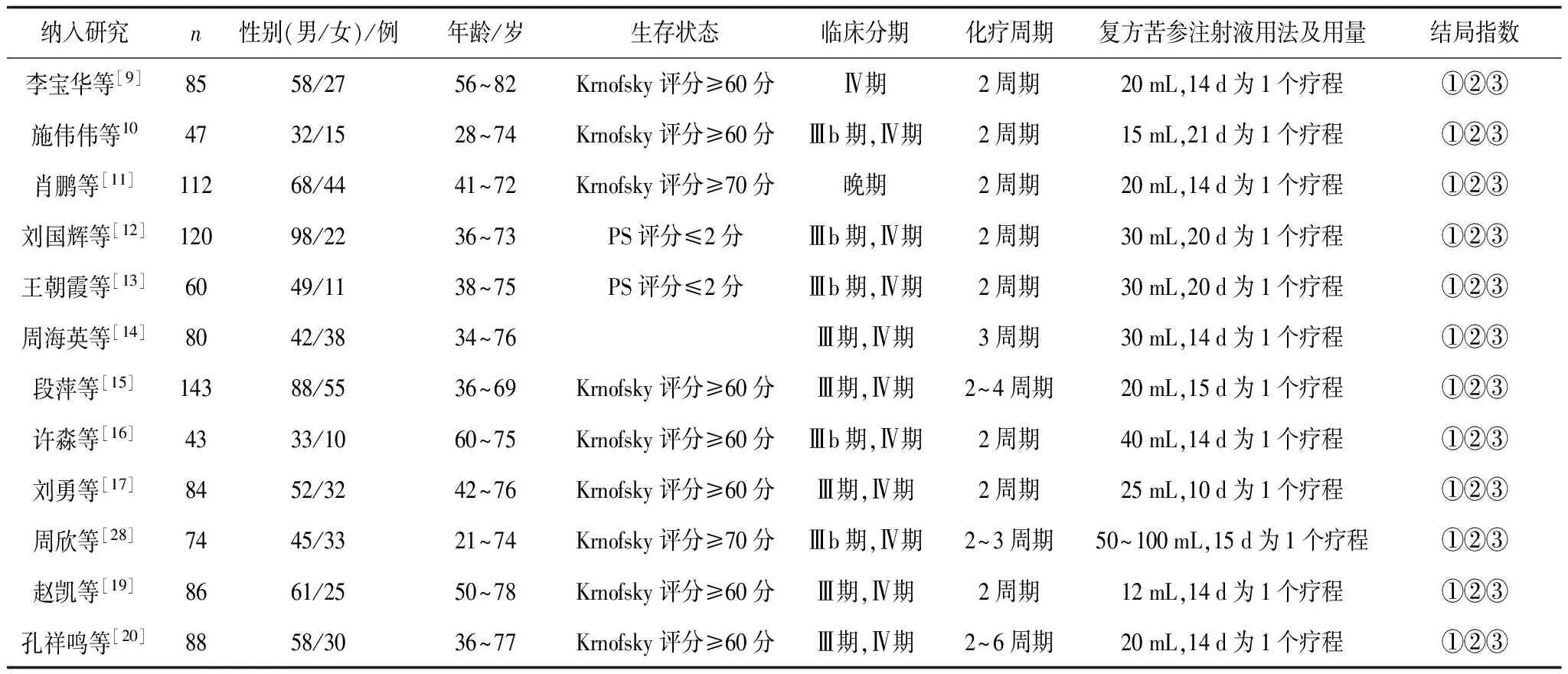
表1 纳入文献基线资料
2.3 纳入研究的质量评价 纳入的研究均提及了“随机”字样,其中1篇文献[19]采用随机数字表法分组,1篇[16]通过信封法分组,其余文献均未提及具体采用的随机方法;纳入的试验研究均未提及分配隐藏和盲法;仅有1篇文献[11]提及病例脱落,但并未采用意向性分析,其余文献均无不完整数据报告和数据缺失。
2.4 Meta分析结果
2.4.1 近期疗效 所纳入的研究[9-20]均报道了近期疗效,共1 013例患者,其中试验组516例,对照组497例,各研究之间无统计学异质性(P=0.89,I2=0%),故采用固定效应模型。Meta分析结果显示,试验组患者的近期疗效高于对照组[OR=1.39,95%CI(1.08,1.79),P=0.01]。见图2。
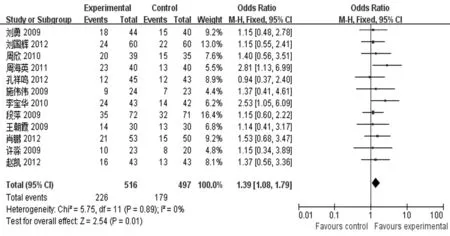
图2 试验组与对照近期疗效比较森林图
2.4.2 生活质量 所纳入的研究中有7篇文献[10-13,16-18]报道了KPS评分的改善率,共531例患者,其中试验组273例,对照组258例,各研究之间无统计学异质性(P=0.88,I2=0%),故采用固定效应模型。Meta分析结果显示,试验组患者生活质量优于对照组[OR=3.29,95%CI(2.30,4.71),P<0.000 01]。见图3。
2.4.3 毒副反应
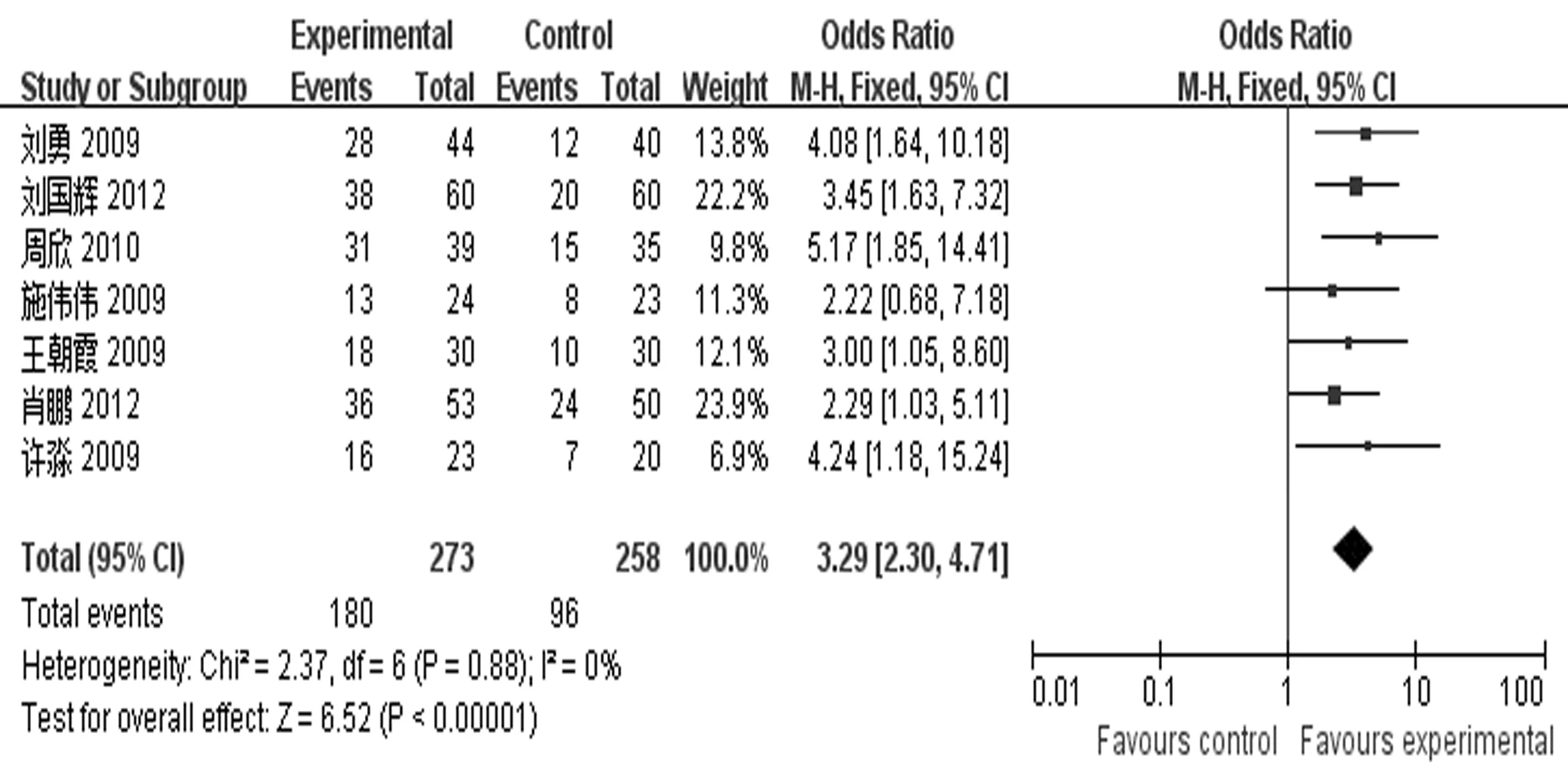
图3 试验组与对照组生活质量比较森林图
2.4.3.1 白细胞下降 所纳入的研究中有8篇文献[9,11-16,18]报道了白细胞的下降情况,共708 例患者,其中试验组360例,对照组348例,各研究之间无统计学异质性(P=0.40,I2=4%),故采用固定效应模型。Meta分析结果显示,引起 WBC下降Ⅲ度以上的病例数试验组少于对照组[RR=0.45,95%CI(0.31,0.65),P<0.000 1]。见图4。
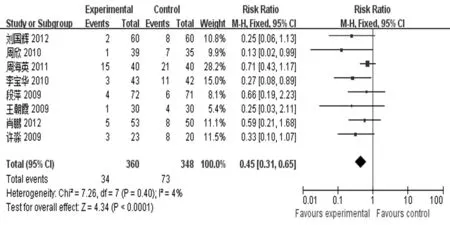
图4 试验组与对照组白细胞下降情况比较林林图
2.4.3.2 呕吐 所纳入的研究中有8篇文献[9,11-15,18,20]报道了呕吐的不良反应,共753例患者,其中试验组382例,对照组371例,各研究之间无统计学异质性(P=0.64,I2=0%),故采用固定效应模型。Meta分析结果显示,引起呕吐Ⅲ度以上的病例数试验组少于对照组[RR=0.38,95%CI(0.26,0.56),P<0.000 01]。见图5。
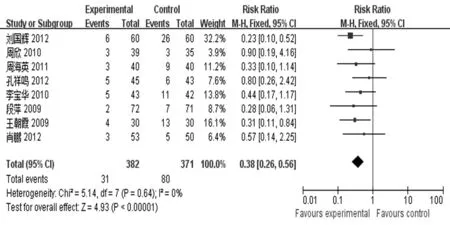
图5 试验组与对照组呕吐反应情况比较林林图
3 讨 论
本研究结果表明,复方苦参注射液联合GP方案治疗晚期NSCLC能够提高患者的近期疗效,改善患者的生活质量,并减少严重的化疗毒副反应。然而,本研究尚存在以下不足:①纳入的RCT 研究质量普遍偏低。纳入的所有研究均提及随机字样,但仅有2篇描述了具体的随机方法,其中1项研究[19]为随机数字表法,另1个研究[16]采用了信封法,其余文献均未提及具体随机方法;所有纳入试验均未提及分配隐藏,不清楚研究者是否进行了分配隐藏方案的设计,可能造成选择偏倚;本研究观察的结局指标部分具有主观性,如生活质量指标,而所有纳入的试验均未采取设盲的措施,这样很容易造成实施偏倚和测量偏倚;仅有1篇文献[11]提及病例脱落,并且未进行意向性分析,也可能造成最终数据的偏倚;所有纳入的研究均未提及样本量估算的依据,很多研究样本量都较小,这将导致检验效能低。②纳入研究在复方苦参注射液使用疗程和用量以及各研究之间的化疗周期存在差异,可能影响综合分析结果。③纳入研究均为已发表的中文文献,可能存在发表偏倚。
对于以后的临床研究,应进行严谨正确的随机设计,并注意分配隐藏,采取设盲的措施,尽量减少研究的偏倚,可考虑进行复方苦参注射液提高化疗疗效及降低化疗毒副反应机制方面的研究。另外,本研究提示复方苦参注射液与吉西他滨及铂类化疗药物之间可能存在相互的协同作用,这也是值得进一步研究的方向之一。
综上所述,复方苦参注射液联合GP方案治疗晚期NSCLC能够提高近期疗效,改善患者的生活质量,并减少严重的化疗毒副反应。这些结果需要大样本的随机对照试验来进一步证明。
[1] Siegel R,Ma JM,Zou ZH,et al. Cancer Statistics,2014[J]. Ca Cancer J Clin,2014,64(1):9-29
[2] Chen W,Zheng R,Zhang S,et al. Annual report on status of cancer in China,2010[J]. Chin J Cancer Res,2014,26(1):48-58
[3] 马悦. 复方苦参注射液化学成分和质量控制研究[D]. 北京:中国中医科学院,2012
[4] 雷怀定,刘先军,涂明利,等. 苦参碱对体外人肺癌A549细胞的抑制作用[J]. 实用医学杂志,2006,22(15):1717-1719
[5] 王锐,姜小军,郑婕,等. 苦参碱增强环磷酰胺抑制小鼠Lewis肺癌的生长作用[J]. 第四军医大学学报,2008,29(24): 2260-2262
[6] WHO. WHO handbook for reporting results of cancer treatment[M]. Geneva,Switzerland:World Health Orgnaization,1979
[7] Yates JW,Chalmer B,Mc-Kegney FP. Evaluation of patients with advanced cancer using the Karnofsky performance status[J]. Cancer,1980,45:2220
[8] Higgins JPT,Green S. Cochrane handbook for systematic reviews of interventions Version 5.1.0.The Cochrane Collaboration,2011[WEB].http//www.cochrane-handbook.org
[9] 李宝华,李红. 复方苦参注射液合GP方案治疗老年非小细胞肺癌临床观察[J]. 山西中医,2010,26(9):27-40
[10] 施伟伟,李方,胡毅,等. 复方苦参注射液联合GP方案化疗治疗晚期非小细胞肺癌47例临床观察[J]. 中国医院用药评价与分析,2009,9(4):306-307
[11] 肖鹏,孟晶茜,孟祥瑞,等. 复方苦参注射液联合吉西他滨+顺铂方案治疗晚期非小细胞肺癌56例临床观察[J]. 中国医院用药评价与分析, 2012,12(2):155-157
[12] 刘国辉,李婷. 复方苦参注射液联合吉西他滨和顺铂治疗非小细胞肺癌的疗效观察[J]. 中国新药杂志,2012,21(6):658-665
[13] 王朝霞,李娟,陆彬彬,等. 复方苦参注射液联合吉西他滨和顺铂治疗非小细胞肺癌的疗效及减毒作用观察[J]. 中国医院用药评价与分析,2009,9(12):932-933
[14] 周海英,胡志雄. 复方苦参注射液联合吉西他滨和顺铂治疗晚期非小细胞肺癌[J]. 中国临床医学,2011,18(4):489-491
[15] 段萍,肖敏伟,肖文,等. 复方苦参注射液在晚期非小细胞肺癌化疗中的增效减毒作用[J]. 中国新药杂志,2009,18(18):1760-1763
[16] 许淼,张丽萍. 复方苦参注射液联合化疗治疗老年中晚期非小细胞肺癌的疗效观察[J]. 中国老年学杂志,2009,5(29):1161-1162
[17] 刘勇,魏知,孟令占,等. 岩舒注射液结合化疗治疗中晚期非小细胞肺癌临床观察[J]. 山西中医,2009,25(8):24-25
[18] 周欣,刘春玲. GP方案联合岩舒治疗41例晚期非小细胞肺癌临床观察[J]. 中国肿瘤临床,2010,37(9):531-532
[19] 赵凯,杨俊泉,王建华,等. 复方苦参注射液联合GP方案治疗晚期非小细胞肺癌临床疗效及生存质量影响[J]. 实用预防医学,2012,19(12):1853-1854
[20] 孔祥鸣,龚黎燕,孙燕,等. 复方苦参注射液联合化疗治疗Ⅲ~Ⅳ期非小细胞肺癌的临床观察[J]. 中国新药杂志,2012,21(5):537-539
Meta-analysis on treatment of advanced non-small cell lung cancer with compound matrine injection in combination with Gemcitabine and Cisplatin chemotherapy
FENG Yulai, PAN Shoujie, YANG Ningjuan, YIN Changchun
(1.Lianyungang Hospital of TCM, Lianyungang 222004, Jiangsu, China)
Objective It is to systematically evaluate the effectiveness and safety in the treatment of advanced non-small cell lung cancer (NSCLC). Methods Cochrane library, PubMed, CBM, CNKI, VIP, WANFANG DATA and Traditional Chinese Medicine Database System were searched through computers. The search was finished in September 2012. Randomized controlled trials (RCTs) of CMI combining Gemcitabine and Cisplatin chemotherapy (versus chemotherapy alone) in any language were included. Two researchers extracted data and assess literature quality separately, and made meta-analysis by RevMan 5.2 software. Results Totally 12 RCTs were included. The Meta-analysis showed that compared with the Gemcitabine and Cisplatin chemotherapy alone, the combination of CMI and chemotherapy could enhance the near-term curative effect [OR=1.39, 95%CI(1.08, 1.79),P=0.01], improve the quality of life [OR=3.29, 95%CI(2.30, 4.71),P<0.000 01] and reduced WBC toxicity [RR=0.45, 95%CI(0.31, 0.65),P<0.000 1]and the gastrointestinal reactions [RR=0.38, 95%CI(0.26, 0.56),P<0.000 01]. Conclusion Compound matrine injection combined with GP regimen in the treatment of advanced non small cell lung cancer can improve the short-term effect, improve the quality of life of patients, reduction of serious adverse drug reactions, but a large sample of randomized controlled studies are needed.
compound matrine injection; non-small cell lung cancer; chemotherapy; Meta-analysis
丰育来,男,主治医师,研究方向为中西医结合治疗肿瘤疾病。
10.3969/j.issn.1008-8849.2015.21.008
R734.2
A
1008-8849(2015)21-2303-04
2014-12-15

