锂硫电池用S/KB复合材料的制备及性能
王 振,魏俊华,王庆杰,王雪丽
(贵州梅岭电源有限公司,贵州遵义 563003)
硫在常温下是电子和离子的绝缘体,导致锂硫电池的活性物质利用率偏低;充放电过程中硫正极的体积变化,导致结构的破坏;放电中间产物聚硫锂在电解液中的溶解,会导致“穿梭效应”[1-2]。将单质硫与活性炭、介孔碳、碳纳米管或科琴碳黑(KB)等复合作为锂硫电池的正极材料,可缓解上述问题[3]。杜锐等[4]用热处理法制备硫-活性炭复合材料,在1.5~2.8 V充放电,0.1 C首次放电比容量为650 mAh/g,循环40次,放电比容量降为480 mAh/g,活性物质利用率较低。X.Y.Geng等[5]用球磨法制备硫-碳纳米管复合材料,0.02 C首次放电到1.5 V的比容量为839 mAh/g,由于复合效果较差,放电性能不理想;以0.05 C在1.5~3.0 V循环50次,放电比容量降为620 mAh/g。
鉴于KB导电性能好、比表面积高,具有独特支链结构等特点,本文作者将KB作为单质硫的载体,分别用球磨法和热处理法制备含硫量60%的S/KB复合材料,并制备硫电极,研究正极复合材料对锂硫电池放电性能的影响。
1 实验
1.1 S/KB复合材料的制备
球磨法:将质量比3∶2的升华硫(上海产,≥99.5%)与KB(日本产,电池级)混合均匀,置于球磨罐中,在XQM-4L变频行星式球磨机(南京产)上以300 r/min的转速球磨(球料比2∶1)约8 h,然后过100目筛,将样品记为S/KB-1。
热处理法:将相同比例的升华硫和KB混合均匀,过100目筛,装入特制密封罐中,在氮气保护的电阻炉内先升温至155℃,保温5~6 h,以降低硫的黏度,使单质硫更好地扩散到碳结构内部;再升温至320℃,保持2~3 h,使剩余的硫进一步蒸发到碳材料的微孔中。自然冷却后,研磨、过100目筛,将样品记为S/KB-2。
1.2 极片的制备
以去离子水为溶剂,质量比8∶5的乙炔黑(AB,福建产,电池级)和碳纳米管(CNT,深圳产,电池级)混合物为导电剂,质量比5∶2的丁苯橡胶(SBR,山东产,电池级)和羧甲基纤维素钠(CMC,广东产,电池级)的混合物为粘结剂,按质量比80∶13∶7将制得的S/KB复合材料与导电剂、粘结剂搅拌成浆料,再涂覆到18 μm厚的铝箔(上海产,≥99.9%)集流体上,在60℃下预干燥1 h,再在60℃下真空(-0.1 MPa)干燥20 h以上,裁切成40 cm长×4.7 cm宽。极片中,活性物质含量约为4 mg/cm2。
在干燥房(RH<3.0%,下同)中将1.1 mm厚的泡沫镍(上海产,工业级)以10 MPa的压力压制到金属锂带(重庆产,≥99.99%)上,作为负极片,裁切成42 cm长×4.8 cm宽。
1.3 电池的装配
采用卷绕的方式,在干燥房中装配054055型软包装Li/S电池。隔膜为Celgard 2325膜(美国产),电解液为1 mol/L LiTFSI/DME+DOL(体积比1∶1,张家港产,电池级),所用添加剂为0.2 mol/L LiNO3(张家港产,电池级)。
1.4 性能测试
用DX-2000型X射线衍射仪(丹东产)对正极材料进行物相分析,CuKα,λ =0.154 056 nm,管压40 kV、管流25 mA,步长为0.03°,扫描速度为2(°)/min。
用CT-3008W-5 V 500 mA/3 A高精度电池性能测试系统(深圳产)在常温下进行恒流放电测试,放电终止电压为1.5 V,电流为0.1 C、0.5 C、1.0 C 及2.0 C;以0.5 C 进行恒流充放电测试,电压为1.5~2.5 V。1.0 C=1 672 mA/g。
用M-273A型电化学工作站(美国产)进行交流阻抗谱(EIS)和循环伏安测试。采用三电极体系,硫正极为工作电极,金属锂作为参比电极和辅助电极。EIS测试的频率为10-2~105Hz,交流幅值为±5 mV/s;循环伏安测试的电压为1.0~3.0 V,扫描速率为0.2 mV/s。
2 结果与讨论
2.1 XRD分析
图1为单质硫、KB和S/KB复合材料的XRD图。
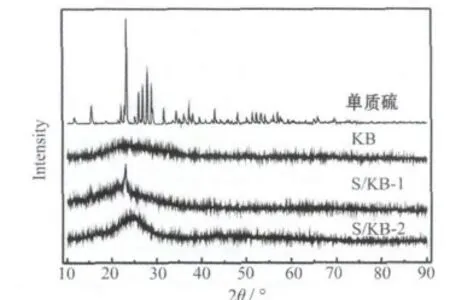
图1 单质硫、KB和S/KB复合材料的XRD图Fig.1 XRD patterns of element sulfur,KB and S/KB composites
从图1可知,单质硫出现了多个衍射峰,其中在23°和28°附近的特征峰,位置和强度都与硫(S8)的标准谱(JCP DS:74-1465)吻合,表明单质硫以晶态形式存在,结晶度很高。S/KB-1和S/KB-2都在23°附近出现了较宽的衍射峰,是单质硫与KB的特征峰重合所致,并未出现明显的硫元素特征峰,表明单质硫与KB复合后,较均匀地分散在KB的微结构中,主要形式为非晶态。球磨法制备的S/KB-1在23°处出现了较尖锐的衍射峰,半峰宽较窄;热处理法制备的S/KB-2的特征峰较弱,半峰宽较宽。这表明:S/KB-1的粒径更大。
2.2 EIS分析
S/KB复合材料的EIS见图2。
图2中的曲线均由1个半圆和1条直线组成,高频区的半圆代表电解质-电极界面的电荷传递阻抗(Rct),低频区的直线代表Li+在电极材料中扩散所引起的 Warburg阻抗(Rw)。从图2可知,与S/KB-1相比,S/KB-2的Rct更小,可能是由于热处理法制备的S/KB-2复合材料的粒径更小,单质硫与导电碳结构的接触更密切,具有更好的导电网络。
2.3 电化学性能分析
S/KB复合材料的循环伏安曲线见图3。
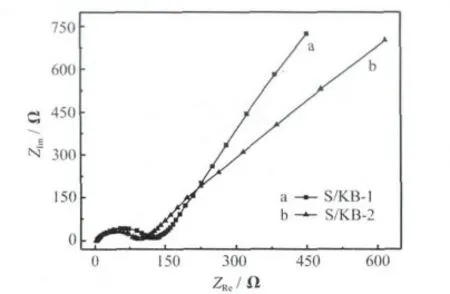
图2 S/KB复合材料的EISFig.2 Electrochemical impedance spectroscopy(EIS)of S/KB composites
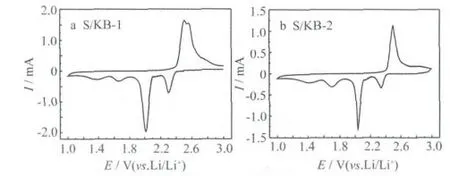
图3 S/KB复合材料的循环伏安曲线Fig.3 CV curves of S/KB composites
从图3可知,循环伏安曲线中均有两个明显的还原峰(2.3 V和2.0 V附近)和一个明显的氧化峰(2.5 V附近)。2.3 V附近的还原峰对应电解液中的S8逐步被还原为中间产物S2-n(4≤n≤8)的过程,2.0 V附近的还原峰对应长链聚硫离子进一步被还原为低价态聚硫离子S2-2和S2-,并与Li+结合成难溶Li2S2和Li2S的过程;此外,在1.7 V附近出现了一个不太明显的还原峰,可能是部分残留的S2-2和S2-离子进一步与Li+发生反应产生的;2.5 V附近的氧化峰对应Li2S2和Li2S逐步被氧化,生成长链聚硫锂的过程[1]。
制备的Li/S电池在不同倍率下的首次放电曲线见图4。
从图4可知,S/KB-1、S/KB-2复合材料制备的 Li/S电池,在放电过程中有两个电压平台,分别位于2.2~2.4 V及1.9~2.1 V,与循环伏安曲线的两个还原峰对应。放电平台电压的差别,是放电倍率不同造成的。电压平台的出现,表示在放电过程中发生反应,生成了聚硫锂Li2Sn,其中较高电压平台的出现,是由于放电过程中单质硫S8被还原生成长链聚硫锂Li2Sn(4≤n≤8),易溶解于电解液;较低电压平台的出现,是由于短链聚硫锂Li2Sn(n<4)的形成,难溶于电解液[6]。高、低电压平台的反应机理分别见式(1)、式(2)。
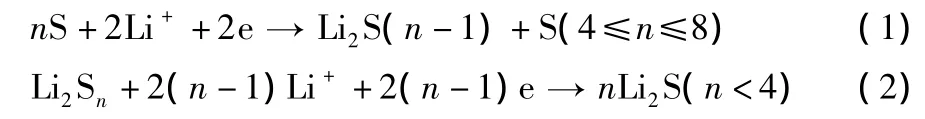
从图4可知,在0.1 C、0.5 C、1.0 C和2.0 C 时,S/KB-1复合材料的首次放电比容量分别为1 537 mAh/g、1 447 mAh/g、1 670 mAh/g和1 515 mAh/g;S/KB-2复合材料对应的首次放电比容量分别为 1 330 mAh/g、1 275 mAh/g、1 244 mAh/g 和1 166 mAh/g。S/KB-1复合材料的首次放电性能比S/KB-2复合材料好,原因是S/KB-1复合材料在球磨过程中,硫能够均匀地分散到KB的空隙中,导电碳结构对硫的包覆良好。
制备的Li/S电池在0.5 C时的循环性能见图5。
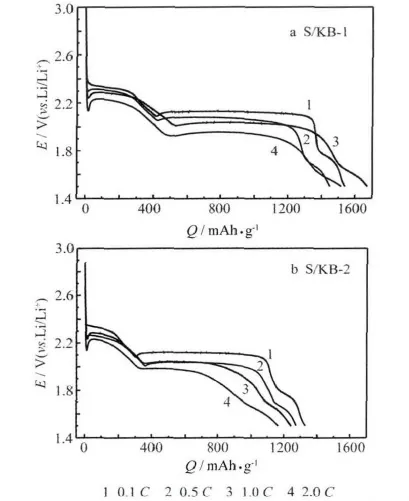
图4 Li/S电池在不同倍率下的首次放电曲线Fig.4 Initial discharge curves of Li/S cells at different rate
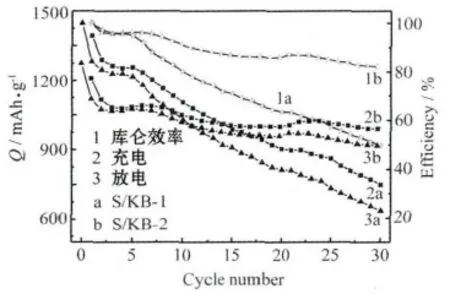
图5 Li/S电池的循环性能Fig.5 Cycle performance of Li/S cells
从图5可知,S/KB-1复合材料具有更高的首次放电比容量,而S/KB-2复合材料的循环性能更好,与图4的结果一致。S/KB-1复合材料在循环过程中,充、放电比容量都不断下降,第30次循环的放电比容量仅为637 mAh/g,库仑效率降低到50%左右;S/KB-2复合材料在循环3次以后,充、放电比容量下降的幅度减小,第30次循环的放电比容量仍有920 mAh/g,库仑效率为82%,好于S/KB-1复合材料。这可能是由于热处理制备的S/KB-2复合材料具有更小的粒径,单质硫熔化、蒸发后进入导电碳结构,与碳微粒有更密切的接触,在电池循环过程中产生的极化较轻,循环效率更高;另外,电池充放电过程中生成的聚硫化物能够更好地被限制在导电碳结构中,阻止了聚硫化物在电解液中的溶解,进而提高了电池的充放电效率[7]。
3 结论
采用超导科琴碳黑(KB)作为单质硫材料的复合载体,分别用球磨法和热处理法制备了硫含量为60%的S/KB复合材料,研究了两种方法制备的S/KB复合材料的性能。球磨法制备的S/KB-1复合材料具有较高的首次放电比容量,最高达到1 670 mAh/g;而热处理法制备的S/KB-2复合材料具有更好的循环性能,在1.5~2.5 V以0.5 C充放电,30次循环的放电容量保持率约为82%。
[1]DIAO Yan(刁岩),XIE Kai(谢凯),HONG Xiao-bin(洪晓斌),et al.Li-S电池硫正极性能衰减机理分析及研究现状概述[J].Acta Chimica Sinica(化学学报),2013,71(4):508 -518.
[2]Zhu X J,Wen Z Y,Gu Z H,et al.Electrochemical characterization and performance improvement of lithium/sulfur polymer batteries[J].J Power Sources,2005,139:269 -273.
[3]WANG Xue-li(王雪丽),WEI Jun-hua(魏俊华),WANG Qing-jie(王庆杰),et al.硫含量和集流体类型对锂硫电池性能的影响[J].Battery Bimonthly(电池),2013,43(3):151 -154.
[4]DU Rui(杜锐),YUAN Zhong-zhi(袁中直),ZHONG Qing-hua(钟清华),et al.锂硫二次电池正极复合材料的合成和性能研究[J].Dianyuan Jishu(电源技术),2008,32(12):845 -847.
[5]Geng X Y,Rao M M,Li X P,et al.Highly dispersed sulfur in multi-walled carbon nanotubes for lithium/sulfur battery[J].J Solid States Electrochem,2013,17(4):987 -992.
[6]Ahn W,Kim K B,Jung K N,et al.Synthesis and electrochemical properties of a sulfur-multi walled carbon nanotubes composite as a cathode material for lithium sulfur batteries[J].J Power Sources,2012,202:394 -399.
[7]Liang X,Wen Z Y,Liu Y,et al.Preparation and characterization of sulfur-polypyrrole composites with controlled morphology as high capacity cathode for lithium batteries[J].Solid State Ionics,2011,192(1):347-350.

